新型基于二氟苯并噻二唑和双噻吩丙烯腈共轭聚合物的设计、合成及光伏性能
2017-12-18郑江波陈智明胡志诚
郑江波 陈智明 胡志诚 张 杰 黄 飞
新型基于二氟苯并噻二唑和双噻吩丙烯腈共轭聚合物的设计、合成及光伏性能
郑江波 陈智明 胡志诚 张 杰*黄 飞*
(华南理工大学高分子光电材料与器件研究所,发光材料与器件国家重点实验室,广州 510640)
设计并合成了两种基于5,6-二氟苯并噻二唑和双噻吩丙烯腈单元的D-A型共轭聚合物,聚[(5,6-二氟-苯[c][1,2,5]噻二唑-4,7-基)-交替-(()-2,3-双(3'-(2-辛基十二烷基)-(2,2'-双噻吩)-5,5'-基)丙烯腈)] (DFBT812)和聚[(5,6-二氟-苯[c][1,2,5]噻二唑-4,7-基)-交替-(()-2,3-双(3'-(2-癸基十四烷基)-(2,2'-双噻吩)-5,5'-基)丙烯腈)](DFBT1014)作为聚合物太阳电池的给体材料。通过侧链工程,引入了2-辛基十二烷基和2-癸基十四烷基侧链实现对聚合物的溶解性,结晶性以及共混膜形貌的调节。研究结果表明,共轭聚合物DFBT812与PC61BM的共混膜表现出更好的相分离尺度,能够促进载流子的传输和抽取。基于共轭聚合物DFBT812的太阳电池器件取得了0.87 V的开路电压和6.25%的能量转换效率。除此之外,基于DFBT812的聚合物太阳电池器件在活性层厚度为220 nm时仍然表现出6%的能量转换效率。
二氟苯并噻二唑;双噻吩丙烯腈;侧链工程;聚合物给体;聚合物太阳电池
1 引言
聚合物太阳电池由于具有质轻,低成本,能够实现大面积印刷加工等优点,近年来已经吸引了广泛的关注1,2。在过去的二十年中,为了提高聚合物太阳电池的光电转换效率,科学家在给受体材料3−6、界面工程7−10、器件结构11−13、形貌优化14−16等做了大量的研究工作,并取得重大进步。迄今为止,单层本体异质结聚合物太阳电池的器件的转化效率已经超过12%17,18。
聚合物给体材料的创新一直是聚合物太阳电池研究的核心,而其中给体(D)-受体(A)型共轭聚合物给体材料是目前给体材料研究的重要方向之一,其中D是指给电子单元,而A指的是吸电子单元。由于给电子单元和吸电子单元间的推拉电子作用,产生了分子内的电荷转移作用,能够有效的降低聚合物的带隙,从而能够拓宽聚合物的吸收光谱19,20。同时选择合适的给电子单元和吸电子单元能够对聚合物的能级进行有效地调控,这有利于得到比较高的开路电压(oc)。
近年来,很多D-A型共轭共聚物作为给体材料应用于太阳电池中,光电转换效率都超过了10%17,21−24,而其中一个高效率聚合物体系就是基于二氟苯并噻二唑衍生物作为吸电子单元的聚合物给体材料25−27。Yan等23报道了一系列基于二氟苯并噻二唑(DFBT)和联噻吩类衍生物的聚合物给体材料,通过对烷基链支化位点和烷基链长度的优化,能量转换效率(PCE)超过10%。但基于此类聚合物的太阳电池器件的的开路电压(oc)比较低,大部分都没有超过0.8 V。为了进一步得到高oc的高效太阳电池器件,通过聚合物主链设计来降低聚合物给体的最高占有分子轨道能级(HOMO能级)是一种行之有效的方法。
相比于联噻吩来说,反式噻吩乙烯基噻吩(TVT)单元是一个分子平面性更好的给电子单元,其能够有效的促进聚合物主链间的堆积,从而提高聚合物的载流子迁移率28−32。但是,基于TVT的给体聚合物的HOMO能级并不深33,34,这不利于聚合物太阳电池器件获得高oc。在TVT单元的双键上引入吸电子基团是降低聚合物的HOMO能级的一种有效的办法。Yun等35报道了一种基于双噻吩丙烯腈(CNTVT)单元和并吡咯二酮(DPP)的共聚物。研究发现在TVT单元引入氰基基团可以显著降低聚合物的HOMO能级,并且不会破坏聚合物主链的平面性。此外,氰基基团也能够促进分子间的聚集,提高聚合物分子的结晶性36−38。
基于以上考虑,本文设计并合成两个新型基于DFBT与CNTVT结构单元的含不同侧链的共轭聚合物DFBT812和DFBT1014,并应用于聚合物太阳电池中,考察烷基侧链对分子聚集,给受体共混形貌以及光伏性能的影响。研究表明含2-辛基十二烷基的共轭聚合物DFBT812的太阳电池器件的能量转换效率(PCE)更高,达到6.25%。
2 实验部分
2.1 仪器和试剂
用于聚合反应的三(邻甲基苯基)磷(P(-tol)3),三(二亚苄基丙酮)二钯(Pd2(dba)3),无水氯苯(纯度为99.8%)从Stream公司或Sigma-Aldrich公司购买;常用溶剂无水甲醇,正己烷,二氯甲烷,三氯甲烷,氯苯购自广州化学试剂厂,如无特别说明则直接使用。
聚合物分子量采用PL-GPC220型凝胶渗透色谱仪测试,温度为150 °C,流动相为1,2,5-三氯苯,使用标准聚苯乙烯校准曲线;采用循环伏安法测定聚合物的氧化还原电位即采用CHI660E电化学工作站测定,扫描速度为100 mV∙s−1;电化学测试以铂碳电极为工作电极,铂丝电极作为对电极,饱和甘汞电极作为参比电极,电解质为四丁基六氟磷酸铵,配成乙腈为溶剂的0.1 mol∙L−1的电解质溶液,测试前用二茂铁标定;采用Shimadzu UV-3600紫外可见光仪测得聚合物的紫外-可见吸收光谱(UV-vis);采用Netzsch TG209测得聚合物的热重分析(TG),在N2气氛中测定,升温速率为10 °C∙min−1;采用Nano-scope NS3A系统测得原子力显微镜图(AFM);采用JEM-2100F仪器测得透射电镜图(TEM);采用FLuorolog-3荧光光谱仪测得共轭聚合物及共混膜的光致荧光发射光谱。
2.2 单体和共轭聚合物的合成
4,7-双[5-溴-4-(2-辛基十二烷基)噻吩-2-基]-5,6-二氟-2,1,3-苯并噻二唑M125,4,7-双[5-溴- 4-(2-癸基十四烷基)噻吩-2-基]-5,6-二氟-2,1,3-苯并噻二唑M227,()-2,3-双(5-(三甲基锡)噻吩-2-乙烯基)氰基CNTVT-Sn35的合成路线按照文献报道的方法制备。
2.2.1 共轭聚合物DFBT812的制备
将单体M1(106 mg,0.1 mmol),CNTVT-Sn (54.3 mg,0.1 mmol)加入到15 mL反应管中,然后加入P(-tol)36 mg,Pd2(dba)34 mg,在氮气保护的手套箱里面抽换气三次,加入无水氯苯1.6 mL,转移到油浴锅中。加热至160 °C,反应48 h。待温度降下来后,往反应液中加入3 mL氯苯,然后将反应液滴到甲醇中。收集固体沉淀,依次用甲醇、正己烷、二氯甲烷、氯仿抽提除去齐聚物。然后用氯苯抽提,将抽提液体浓缩并在甲醇中重沉淀,收集固体并真空干燥,得到紫黑色固体99.5 mg。产率87.3%。
M= 51.8 kg∙mol−1,M= 81.9 kg∙mol−1,PDI = 1.58
2.2.2 共轭聚合物DFBT1014的制备
将单体M2(117 mg,0.1 mmol),CNTVT-Sn (54.3 mg,0.1 mmol)加入到15 mL反应管中,然后加入P(-tol)36 mg,Pd2(dba)34 mg,在氮气保护的手套箱里面抽换气三次,加入无水氯苯1.6 mL,转移到油浴锅中,加热至160 °C,反应48 h。待反应液降到室温后,将其滴到甲醇中。收集固体并依次用甲醇,正己烷,二氯甲烷抽提除去齐聚物,然后用氯仿抽提,将抽提液体浓缩并滴掉甲醇中,收集固体并真空干燥,得到紫黑色固体109 mg。产率87.2%。
M= 24.5 kg∙mol−1,M= 44.1 kg∙mol−1,PDI = 1.80
2.3 太阳电池器件的制备
聚合物太阳电池器件采用正装结构,以氧化铟锡(ITO)玻璃衬底作为空穴收集电极,ITO玻璃依次用丙酮、洗涤剂、去离子水和异丙醇超声洗涤,然后放入烘箱80 °C过夜烘干。空穴传输层PEDOT:PSS(聚(3,4-乙烯基二氧噻吩)与聚磺酸基苯乙烯的混合物)在氮气保护的手套箱里通过匀胶机以5000 r∙min−1的转速旋涂在干燥冷却后的ITO衬底上,紧接着在150 °C下烘15 min,最后得到40 nm左右的PEDOT:PSS膜。聚合物与富勒烯衍生物[6,6]-苯基-C61-丁酸甲酯(PC61BM)的质量比为1 : 1.5的混合溶液(溶剂为氯苯)旋涂在PEDOT:PSS膜上面作为活性层。随后在活性层上旋涂5 nm左右的聚[(9,9-二辛基-2,7-芴)-交替-(9,9-双(,-二甲基胺丙基)二溴芴)](PFN-Br39,40)作为阴极界面层。紧接着在3 × 10−4Pa的真空度下蒸镀80 nm左右的Ag作为阴极,器件的有效面积为0.04 cm2。最后器件在通过环氧树脂覆盖有效器件面积,在紫外固化炉固化5 min来包封器件以隔绝水氧对器件的影响。器件测试,功率转换效率(PCE)是在 AM1.5G,Japan,SAN-EI,XES-40S1 Class Solar Simulator(太阳模拟灯型号)下测得的。太阳模拟灯的光强通过标准硅太阳电池标定为100 mW∙cm−2。电池器件的电流密度−电压(−)曲线是通过 Keithley 2400 Source Measure Unit记录测得的。
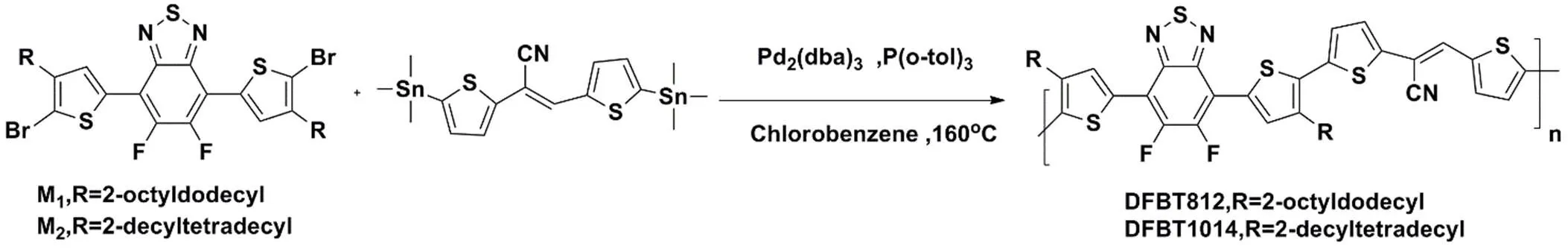
意图1 共轭聚合物DFBT812和DFBT1014的合成路线
Scheme 1 Synthetic routes of DFBT812 and DFBT1014.
3 结果与讨论
3.1 二氟苯并噻二唑聚合物给体的合成
基于二氟苯并噻二唑和双噻吩丙烯腈的共轭聚合物的合成路线如示意图1所示。首先根据文献合成分别带有2-辛基十二烷基和2-癸基十四烷基链的二氟苯并噻二唑的单体M1和M2,然后分别与单体CNTVT-Sn采用Stille偶联在无水无氧的氯苯溶剂下反应48 h。用索氏抽提除去齐聚物和催化剂后,真空干燥即得共轭聚合物DFBT812和DFBT1014,产率均超过85%。含烷基链相对比较短的共轭聚合物DFBT812只能溶于氯苯、邻二氯苯等高沸点溶剂,但共轭聚合物DFBT1014能溶于四氢呋喃、氯仿、氯苯等有机溶剂。
通过热失重分析法分析了共轭聚合物DFBT812和DFBT1014的热稳定性,相应的热失重曲线如图1所示。共轭聚合物DFBT812和DFBT1014质量损失5%的温度(d)分别为414 °C和410 °C,两者相差很小,这主要是因为这两个共轭聚合物的主链结构一样。共轭聚合物DFBT812与DFBT1014的d都比较高,这表明共轭聚合物具有良好的热稳定性能,有利于获得更好的器件效果及器件寿命。
3.2 共轭聚合物的光学性质
共轭聚合物DFBT812和DFBT1014在氯苯溶液和薄膜状态下的紫外−可见吸收光谱如图2(a, b)所示。由于共轭聚合物的主链结构一样,DFBT812和DFBT1014展现出相似的光学特征。在溶液和薄膜的吸收光谱中,共轭聚合物在400 nm到800 nm,左右都有两个主要吸收峰,在650 nm附近出现的吸收峰是给电子单元与吸电子单元间的分子内电荷转移吸收峰;而在690 nm附近出现的吸收峰归因于共轭聚合物的堆积产生的聚集峰。相比共轭聚合物DFBT1014的吸收光谱,含烷基链较短的共轭聚合物DFBT812展现更强的聚集效应,这是因为共轭聚合物的烷基链变短后,有利于主链更加紧密堆积。相比于共轭聚合物DFBT1014的最大薄膜吸光系数为3.0 × 104cm−1,DFBT812的最大薄膜吸收系数达到1.0 × 105cm−1,这表明共轭聚合物DFBT812的吸光能力更强,能够吸收更多的光子,有利于获得更高的短路电流。为了更好地了解共轭聚合物分子间的聚集随温度的变化,我们对共轭聚合物的氯苯溶液进行了变温吸收光谱的表征,如图2(c, d)所示。当温度从20 °C升高到90 °C,两个共轭聚合物的聚集峰逐渐减弱,这主要是归因于共轭聚合物随着温度的升高后分子间的−堆积减弱。当温度达到90 °C时,共轭聚合物DFBT1014的聚集已基本消失,并在572 nm出现了一个吸收峰,但共轭聚合物DFBT812仍然呈现出一定程度的分子间的聚集,这同样表明含烷基链更短的共轭聚合物DFBT812的聚集作用更强,更有利于载流子的传输。共轭聚合物的光学带隙根据其薄膜吸收边计算得到。共轭聚合物DFBT812和DFBT1014的光学带隙分别为1.61 eV和1.58 eV,见表1。

图1 共轭聚合物的热失重曲线,升温速率为10 °C∙min−1
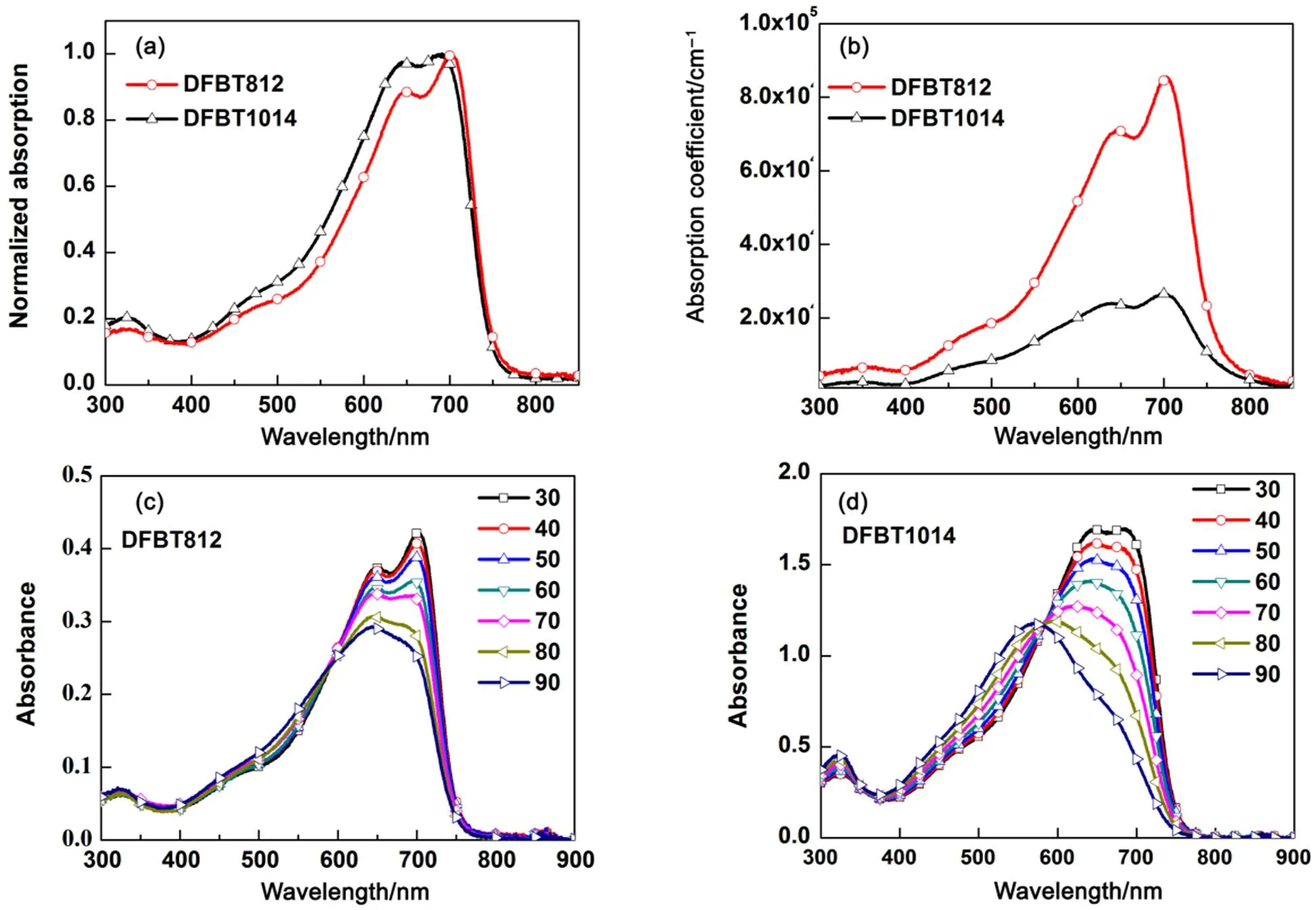
图2 共轭聚合物DFBT812和DFBT1014在溶液(a)和在薄膜(b)中的紫外-可见吸收光谱;(c)和(d)分别是DFBT812和DFBT1014在氯苯溶液中的紫外-可见变温吸收光谱

表1 共轭聚合物的光学和电学性能
3.3 共轭聚合物的电化学性质
利用循环伏安法测得的共轭聚合物DFBT812和DFBT1014相对于二茂铁的氧化电位分别为0.72 V和0.73 V,还原电位分别−1.8和−1.78 V,如图3所示。相应的HOMO能级和最低未占有分子轨道能级(LUMO能级)通过以下的公式计算得到:
HOMO= −(4.8 +ox) eV
LUMO= −(4.8 +red) eV
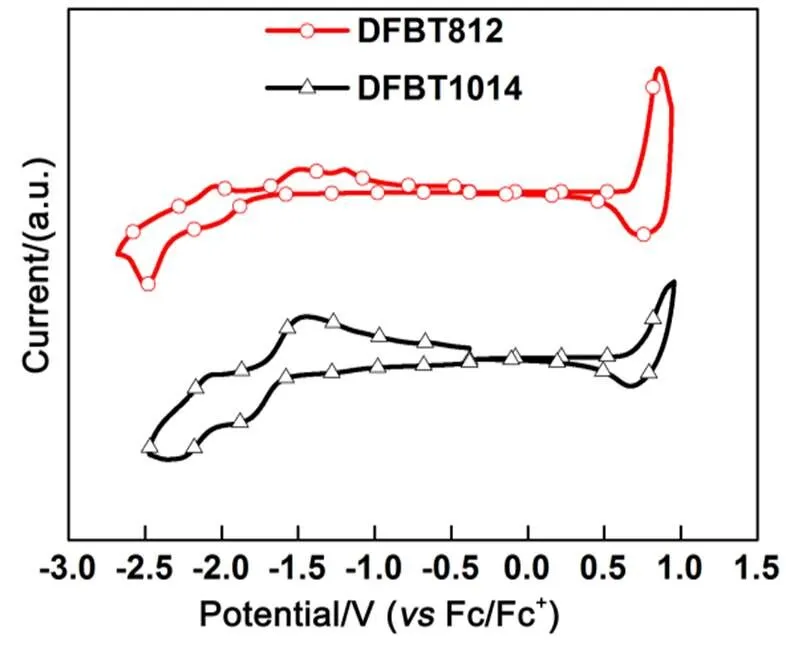
图3 DFBT812和DFBT1014的循环伏安特性曲线
通过计算可以得到共轭聚合物DFBT812和DFBT1014的HOMO能级分别为−5.52和−5.53 eV,LUMO能级分别为−3.00和−3.02 eV,对应的电化学带隙分别为2.52和2.51 eV。电化学测试结果表明烷基链并未显著影响这类共轭聚合物的前线分子轨道能级。相比于Lee等34报道的未引入氰基的共轭聚合物PV4T2FBT的HOMO能级为−5.27 eV,我们报道的共轭聚合物DFBT812和DFBT1014的HOMO能级降低了约0.25 eV,这表明通过引入吸电子基团氰基可以有效降低聚合物的HOMO能级,进一步提高器件的开路电压。
3.4 聚合物的光伏器件特性
为了研究共轭聚合物DFBT812和DFBT1014的的光伏器件性能,我们制备器件结构为ITO/PEDOT:PSS/共轭聚合物:PC61BM/PFN-Br/Ag的聚合物太阳电池器件。经过给体与受体比例优化,我们得到最优的共轭聚合物和PC61BM的质量比为1:1.5。光活性层均采用氯苯作为旋涂溶剂,其厚度约为200 nm。所有的器件测试条件均为AM 1.5G模拟太阳灯,光强为100 mW∙cm−2。器件的曲线和EQE曲线如图4(a, b)所示,相应的光伏性能参数见表2。
基于共轭聚合物与PC61BM的光伏器件的oc都在0.9 V左右,这说明共轭聚合物中引入氰基吸电子基团降低HOMO能级来提高光伏器件的oc的方法是有效的。基于共轭聚合物DFBT1014和PC61BM共混时制备正装光伏器件的光电转换效率为1.73%,其中oc为0.91 V,短路电流(sc)为3.04 mA∙cm−2,填充因子FF为65.60%。采用相同条件制备基于共轭聚合物DFBT812与PC61BM的光伏器件,器件的光电转换效率明显提升,达到6.25%。这主要归因于器件的短路电流明显提升,从3.04 mA∙cm−2提高到11.13 mA∙cm−2。为了验证基于电流()−电压()特性曲线得到的器件短路电流值,对器件的外量子效率曲线(EQE)进行了表征,如图4(b)所示。共轭聚合物在300−800 nm波长范围内均有光电流产生,但是基于共轭聚合物DFBT812的EQE响应值高达40%,远远超过同样条件下DFBT1014的EQE响应值。基于EQE曲线计算的短路电流和采用−曲线测试的短路电流值在误差范围内,证实了器件测试结果的可靠性。
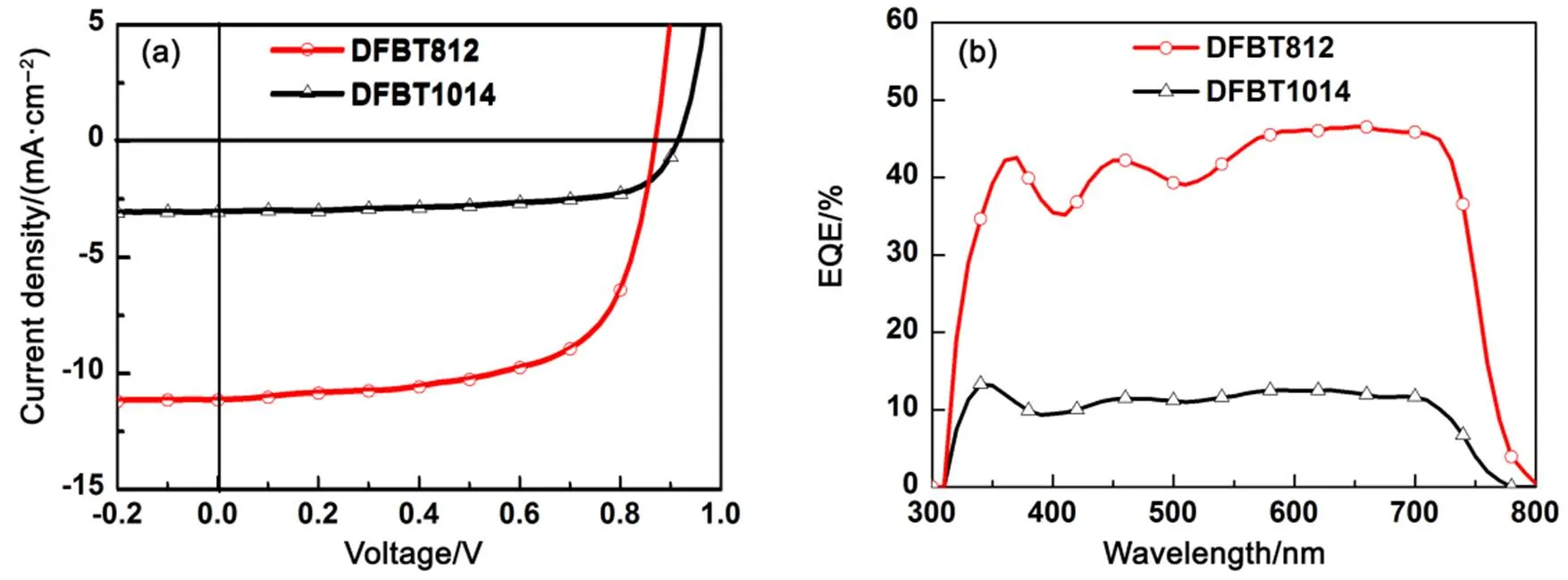
图4 聚合物太阳电池器件的电流−电压(J−V)特性曲线(a)和外量子效率(EQE)曲线(b);器件结构:ITO/PEDOT:PSS/共轭聚合物:PC61BM/PFN-Br/Ag

表2 基于共轭聚合物与PC61BM太阳电池器件的性能参数
器件的短路电流与活性层的吸光特性、迁移率以及活性层形貌有关。为了进一步研究这两个聚合物巨大的光伏性能差异,我们采用空间电荷限制电流(SCLC)方法对活性层的载流子迁移率进行了表征,相应的1/2−特性曲线如图5所示。器件结构为ITO/PEDOT:PSS/共轭聚合物:PC61BM/PFN-Br/Ag。通过公式可以算出基于共轭聚合物DFBT812和DFBT1014的活性层的载流子迁移率分别是8.56 × 10−3cm2∙V−1∙s−1和4.03 × 10−3cm2∙V−1∙s−1,载流子迁移率属于同一个数量级,因此,载流子迁移率变化对器件短路电流的差别没有显著影响。
通过光致荧光发射光谱对纯聚合物薄膜以及聚合物和PC61BM共混膜的光致发光情况进行研究,如图6(a, b)。相比于共轭聚合物DFBT1014,聚合物DFBT812与PC61BM的共混薄膜的发光淬灭程度更高,这表明DFBT812和PC61BM共混膜的激子的解离更有效。这与DFBT812器件获得更高的短路电流的结果是一致的。
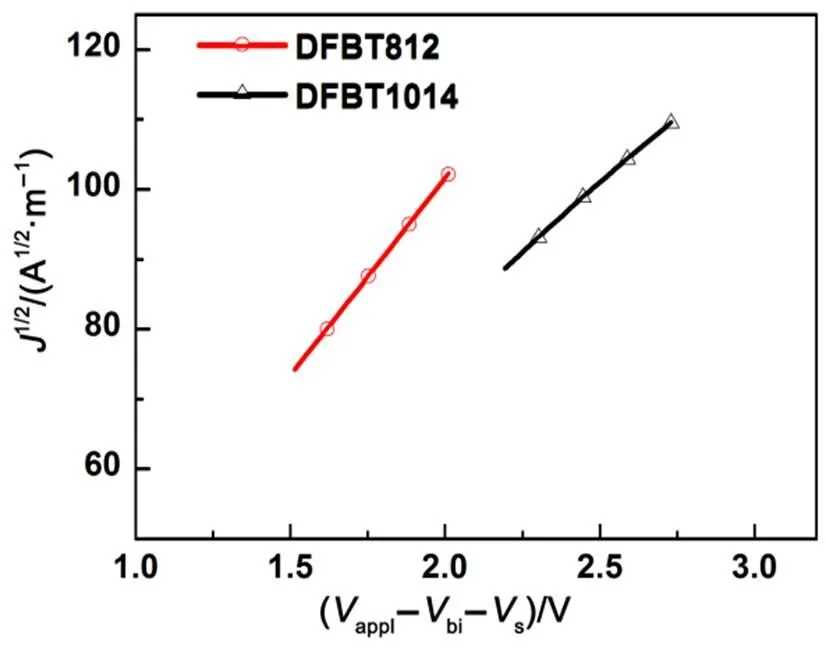
图5 聚合物的单空穴电流(J1/2)对电压(V)特性曲线
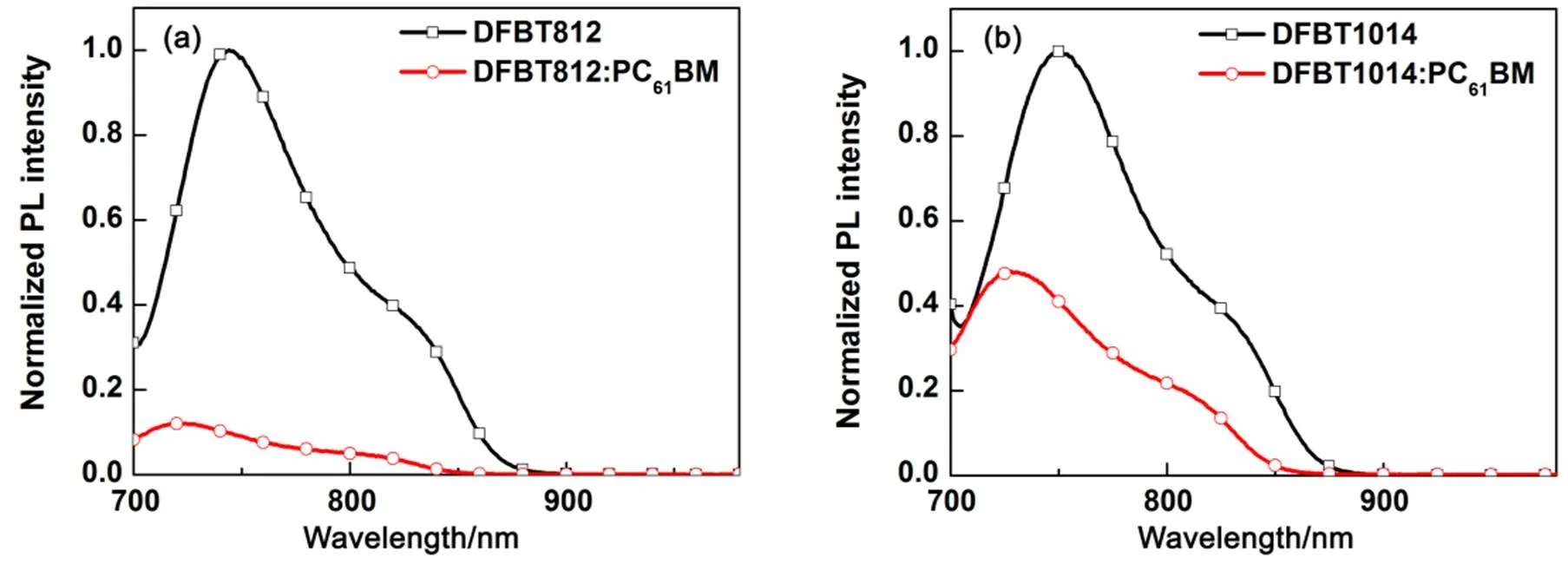
图6 纯聚合物薄膜和共混膜的光致荧光发射光谱(在700 nm处激发)
(a) DFBT812 and (b) DFBT1014

图7 共混膜的AFM图像:(a) DFBT812:PC61BM和(b) DFBT1014: PC61BM;共混膜的TEM图像:(c) DFBT812: PC61BM和(d) DFBT1014: PC61BM
进一步采用原子力显微镜(AFM)和透射电镜(TEM)对共混膜的形貌进行研究,以揭示器件短路电流差异的原因。在图7(a, b)和(c, d)中,可以发现基于DFBT812器件的薄膜形貌均匀(RMS = 2.77 nm),形成了比较良好的互穿网络结构;相反,基于DFBT1014器件的膜的粗糙度比较大(RMS = 10.9 nm),共混膜的相分离尺寸比较大。大的相分离尺寸会导致电荷载流子的聚集和更多非孪生电荷发生复合,从而使得器件的电流降低,电池能量转化效率降低。我们组研究发现,含侧链2-辛基十二烷基的共轭聚合物与富勒烯衍生物的共混膜更倾向“面对面”堆积方式排列,从而器件性能远远高于含侧链2-癸基十四烷基的共轭聚合物的器件性能21。由此推测,共轭聚合物DFBT812在共混膜中可能采取的也是“面对面”结晶取向,能够减小链与链之间−堆积间距,从而表现出更高的光电转换效率。
进一步研究了基于共轭聚合物DFBT812活性层厚度在80−280 nm的器件性能,如表3所示。活性层的膜厚膜厚从80 nm增加到280 nm时,光伏器件的oc基本上保持着不变;电流先随着膜厚从80 nm增加到280 nm时,光伏器件的oc基本上保持着不变;电流先随着膜厚增加而增加,随后再缓慢下降;填充因子在200 nm前对厚度并不敏感,一直维持着在70%左右,在厚度逐渐从200 nm增加后才开始逐渐下降。未来聚合物太阳电池卷对卷大面积印刷的加工方式也需要活性层材料在厚膜的条件下仍能保持良好的性能41,42。由此可见共轭聚合物DFBT812可以作为一种有潜力的大面积加工的聚合物太阳电池的给体材料。
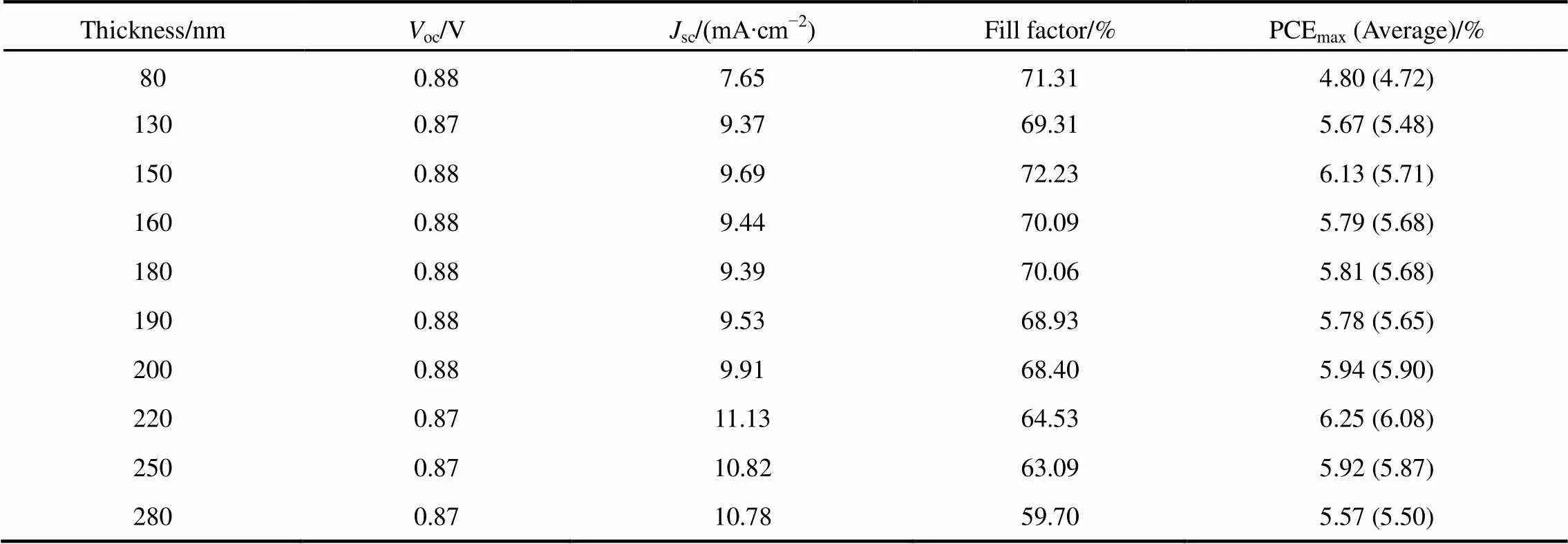
表3 不同厚度条件下DFBT812:PC61BM(质量比例为1 : 1.5)共混膜的光电器件性能
4 结论
我们发展了两种新型基于二氟苯并噻二唑和双噻吩丙烯腈的共轭聚合物给体材料,其中氰基基团的引入成功地降低了共轭聚合物的HOMO能级,提高了电池器件的开路电压。并且基于2-辛基十二烷基链的共轭聚合物DFBT812的电池器件性能表现远高于烷基链较长的DFBT1014的电池器件性能。这主要是由于前者对光子有更好的吸收,以及和PC61BM共混形成的更理想的相分离形貌。除此之外,共轭聚合物DFBT812在厚膜器件的光电性能表现也比较好,在活性层厚度为220 nm时仍具有6%的能量转换效率,在未来卷对卷加工的聚合物太阳电池器件中具有一定潜力。
(1) Yu,G.; Gao,J.; Hummelen, J. C.; Wudl, F.; Heeger, A. J.1995,, 1789. doi:10.1126/science.270.5243.1789
(2) Cheng, Y. J.; Yang, S. H.; Hsu, C. S.2009,, 5868.doi:10.1021/cr900182s
(3) Li, W. N.; Yao, H. F.; Hou, J. H.. 2016,,71. [李婉宁, 姚惠峰, 侯建辉, 高分子通报, 2016,, 71.] doi:10.14028/j.cnki.1003-3726.2016.09.007
(4) Hu, Z. C.; Ying, L.; Huang, F.; Cao, Y.. 2017,. doi:10.1007/s11426-016-0424-9
(5) Zhang, Z. G.; Li, Y. F.. 2014,, 192. doi:10.1007/s11426-014-5260-2
(6) Lin, Y. F.; Zhan, X. W.. 2016,, 175. doi:10.1021/acs.accounts.5b00363
(7) Duan, C. H.; Zhang, K.; Zhong, C. M.; Huang, F.; Cao, Y.. 2013,, 9071. doi: 10.1039/c3cs60200a
(8) Zhang, K.; Liu, X. Y.; Xu, B. W.; Cui, Y.; Sun, M. L.; Hou, J. H.. 2017,, 219. doi:10.1007/s10118-017-1888-7
(9) Wu, Z. H.; Sun, C.; Dong, S.; Jiang, X. F.; Wu, S.; Wu, H. B.; Yip, H.-L.; Huang, F.; Cao, Y.. 2016,, 2004. doi:10.1021/jacs.5b12664
(10) Jia, T.; Zheng, N. N.; Cai, W. Q.; Zhang, J.; Ying, L.; Huang, F.; Cao, Y.. 2016,, 269. doi: 10.1007/s10118-017-1890-0
(11) Li,M. M.; Gao, K.; Wan,X. J.; Zhang, Q.; Kan,B.; Xia, R. X.; Liu, F.; Yang, X.; Feng,H. R.; Ni,W.; Wang,Y. C.; Peng, J. B.; Zhang,H. T.; Liang,Z. Q.;Yip, H.-L.; Peng,X. B.; Cao,Y.; Chen,Y. S.. 2017,, 85. doi:10.1038/nphoton.2016.240
(12) Zhang, K.; Gao, K.; Xia, R. X.; Wu, Z. H.; Sun, C.; Cao, J. M.; Qian, L.; Li, W. Q.; Liu, S. Y.; Huang, F.; Peng, X. B.; Ding, L. M.; Yip, H. L.; Cao, Y.. 2016,, 4817. doi:10.1002/adma.201506270
(13) He, Z. C.; Zhong, C. M.; Su, S. J.; Xu, M.; Wu, H. B.; Cao, Y.2012,, 593. doi:10.1038/nphoton.2012.190
(14) Cabanetos,C.; Labban,A. El; Bartelt,J. A.; Douglas, J. D.; Mateker,W. R.; Fréchet, J. M.J.; McGehee, M. D.; Beaujuge, P. M.2013,, 4656.doi:10.1021/ja400365b
(15) Liu, P.; Dong, S.; Liu, F.; Hu, X. W.; Liu, L. Q.; Jin, Y. C.; Liu, S. J.; Gong, X.; Russell, T. P.; Huang, F.; Cao, Y.. 2015,, 6458. doi:10.1002/adfm.201501878
(16) Zhang, G. C.; Zhang, K.; Yin, Q. W.; Jiang, X. F.; Wang, Z. Y.; Xin, J. M.; Ma, W.; Yan, H.; Huang, F.; Cao, Y.2017,, 2387. doi:10.1021/jacs.6b11991
(17) Li, S. S.; Ye, L.; Zhao, W. C.; Zhang, S. Q.; Mukherjee, S.; Ade, H.; Hou, J. H.. 2016,, 9423. doi:10.1002/adma.201602776
(18) Huang, F.; Cao, Y.2016,, 399. [黄 飞, 曹 镛, 高分子学报, 2016,, 399.] doi:10.11777/j.issn1000-3304.2016.16111
(19) Duan, C. H.; Huang, F.; Cao, Y.. 2012,, 10416. doi:10.1039/c2jm30470h
(20) Price, S. C.; Stuart, A. C.; Yang, L. Q.; Zhou, H. X.; You, W.. 2011,, 4625. doi:10.1021/ja1112595
(21) Jin, Y. C.; Chen, Z. M.; Dong, S.; Zheng, N. N.; Ying, L.; Jiang, X. F.; Liu, F.; Huang, F.; Cao, Y.. 2016,, 9811. doi:10.1002/adma.201603178
(22) Liu, T.; Pan, X. X.; Meng, X. Y.; Liu, Y.; Wei, D. H.; Ma, W.; Huo, L. J.; Sun, X. B.; Lee, T. H.; Huang, M. J.; Choi, H.; Kim, J. Y.; Choy, W. C. H.; Sun, Y. M.. 2017,, doi:10.1002/adma.201604251
(23) Hu, H. W.; Jiang, K.; Yang, G. F.; Liu, J.; Li, Z. K.; Lin, H. R.; Liu, Y. H.; Zhao, J. B.; Zhang, J.; Huang, F.; Qu, Y. Q.; Ma, W.; Yan, H.2015,, 14149. doi:10.1021/jacs.5b08556
(24) Kawashima, K.; Fukuhara, T.; Suda, Y.; Suzuki, Y.; Koganezawa, T.; Yoshida, H.; Ohkita, H.; Osaka, I.; Takimiya, K.. 2016,, 10265. doi: 10.1021/jacs.6b05418
(25) Liu, Y. H.; Zhao, J. B.; Li, Z. K.; Mu, C.; Ma, W.; Hu, H. W.; Jiang, K.; Lin, H. R.; Ade, H.; Yan, H.2014,, 5293. doi:10.1038/ncomms6293
(26) Jheng, J. F.; Lai, Y. Y.; Wu, J. S.; Chao, Y. H.; Wang, C. L.; Hsu, C. S.. 2013,, 2445. doi:10.1002/adma.201300098
(27) Chen, Z. H.; Cai, P.; Chen, J. W.; Liu, X. C.; Zhang, L. J.; Lan, L. F.; Peng, J. B.; Ma, Y. G.; Cao, Y.2014,, 2586. doi:10.1002/adma.201305092
(28) Jung, J. W.; Russell, T. P.; Jo, W. H.. 2015,, 13666. doi:10.1021/acsami.5b03446
(29) Chen, H. J.; Guo, Y. L.; Yu, G.; Zhao, Y.; Zhang, J.; Gao, D.; Liu, H. T.; Liu, Y. Q.. 2012,, 4618. doi:10.1002/adma.201201318
(30) Lim, B. B.; Baeg, K.-J.; Jeong, H. G.; Jo, J.; Kim, H.; Park, J.-W.; Noh, Y.-Y.; Vak, D.; Park, J.-H.; Park, J.-W.; Kim, D.-Y.. 2009,, 2808. doi:10.1002/adma.200803700
(31) Chen, H. J.; Guo, Y. L.; Mao, Z. P.; Yu, G.; Huang, J. Y.; Zhao, Y.; Liu, Y. Q.2013,, 3589. doi:10.1021/cm401130n
(32) Jung, E. H.; Jo, W. H.. 2014,, 650. doi:10.1039/c3ee42297f
(33) Wu, K. Y.; Chiu, C. C.; Chuang, W. T.; Wang, C. L.; Hsu, C. S.. 2015,, 1309. doi:10.1039/c4py01361a
(34) Lee, J.; Singh, R.; Sin, D. H.; Kim, H. G.; Song, K. C.; Cho, K.2016,, 69. doi:10.1002/adma.201504010
(35) Yun, H.-J.; Kang, S.-J.; Xu, Y.; Kim, S. O.; Kim, Y.-H.; Noh, Y.-Y.; Kwon, S.-K.. 2014,, 7300. doi:10.1002/adma.201403262
(36) Yun, H.-J.; Choi, H. H.; Kwon, S.-K.; Kim, Y.-H.; Cho, K.. 2015,, 5898. doi:10.1021/acsami.5b00073
(37) Park, J. M.; Park, S. K.; Yoon, W. S.; Kim, J. H.; Kim, D. W.; Choi, T. L.; Park, S. Y.. 2016,, 2985. doi:10.1021/acs.macromol.5b02761
(38) Kim, H. G.; Kim, M.; Clement, J. A.; Lee, J.; Shin, J.; Hwang, H.; Sin, D. H.; Cho, K.2015,, 6858. doi:10.1021/acs.chemmater.5b03256
(39) Huang, F.; Wu, H. B.; Wang, D. L.; Yang, W.; Cao, Y.. 2004,, 708.doi:10.1021/cm034650o
(40) Lu, J. M.; Cai, W. Q.; Zhang, G. C.; Liu, S. J.; Ying, L.; Huang, F.. 2015,, 1153. [卢俊明, 蔡万清, 张桂传, 刘升建, 应 磊, 黄 飞. 化学学报, 2015,, 1153.] doi:10.6023/A15080546
(41) Duan, C. H.; Huang, F.; Cao, Y.. 2015,, 8081. doi:10.1039/c5py01340b
(42) Li, Y. F.2017,, 447. [李永舫. 物理化学学报, 2017,, 447.] doi: 10.3866/PKU.WHXB201702132
Design, Synthesis and Photovoltaic Performance of Novel Conjugated Polymers Based on Difluorobenzothiadiazole and 2,3-Bis[thiophen-2-yl]acrylonitrile
ZHENG Jiang-Bo CHEN Zhi-Ming HU Zhi-Cheng ZHANG Jie*HUANG Fei*
()
In this study, two novel difluorobenzothiadiazole (DFBT)-based polymeric donors, poly[(5,6-difluoro-benzo[c][1,2,5]thiadiazol-4,7-yl)--(()-2,3-bis(3'-(2-octyldodecyl)-(2,2'-bithiophen)-5,5'-yl) acrylonitrile)] (DFBT812) and poly[(5,6-difluoro-benzo[c][1,2,5]thiadiazol-4,7-yl)--(()-2,3-bis(3'-(2- decyltetradecyl)-(2,2'-bithiophen)-5,5'-yl) acrylonitrile)] (DFBT1014), possessing 2-octyldodecyl and 2-decyltetradecyl side chains, respectively, were designed, synthesized, and applied for polymer solar cells. Alkyl chains of 2-octyldodecyl and 2-decyltetradecyl were incorporated into the polymer to tune the solubility and crystallization of the polymers and morphology of the blend films. Morphological study showed that the blend film of DFBT812 with PC61BM presented much better phase separation domain, which is beneficial for charge transport and collection of charge carriers in the blend film. Photovoltaic devices based on DFBT812 exhibited a power conversion efficiency (PCE) of 6.25%, outperforming those based on DFBT1014. Moreover, DFBT812-based photovoltaic devices exhibited a PCE over 6% even when the thickness of the active layer was 220 nm.
Difluorobenzothiadiazole; 2,3-Bis[thiophen-2-yl]acrylonitrile; Side chain engineering;Polymer donor; Polymer solar cells
March 15, 2017;
April 13, 2017;
April 24, 2017.
Corresponding authors.HUANG Fei,Email: msfhuang@scut.edu.cn. ZHANG Jie, Email: msjzhang@scut.edu.cn.
10.3866/PKU.WHXB201704244
O646
The project was supported by the National Natural Science Foundation of China (51403070, 21520102006).
国家自然科学基金(51403070, 21520102006)资助项目
