溶剂交换法制备淀粉纳米颗粒及表征
2017-12-13吴修利姜雪段蕾郭春香
吴修利,姜雪,段蕾,郭春香
(长春大学食品科学与工程学院,吉林长春130012)
溶剂交换法制备淀粉纳米颗粒及表征
吴修利,姜雪,段蕾,郭春香
(长春大学食品科学与工程学院,吉林长春130012)
采用沉淀技术以二甲基亚砜为溶剂,短链醇为不良溶剂利用溶剂交换法制备淀粉纳米颗粒。实验考察了不良溶剂种类,乙醇体积浓度和溶剂/不良溶剂体积比对颗粒尺寸的影响,并对获得的淀粉纳米颗粒结构与形态进行了红外光谱、扫描电镜以及X-射线衍射分析。结果表明:采用无水乙醇为不良溶剂,当溶剂与不良溶剂体积比1∶20情况下,制备的淀粉纳米颗粒尺寸(218.8±4.66)nm,粒子尺寸分布较均匀,化学结构未发生改变,晶体结构被破坏,衍射峰消失。
淀粉纳米颗粒;溶剂交换法;结构;研究
纳米颗粒通常定义为尺寸直径为10 nm~1 000 nm的固体或胶体微粒。由于纳米颗粒具有小尺寸效应、表面效应等特殊的物理和化学性质而备受关注[1-2]。到目前为止,有机高分子材料制备的纳米颗粒已经广泛应用于医药、化工、生物和食品等诸多领域[3-5]。
与其它人工高分子材料相比,淀粉为原料制备的纳米材料具有一系列的优点,尤其在安全性和降解性要求较高的领域方面更表现出较强的优异性能。纳米粒子的特性与制备工艺具有一定关联性,目前国内外制备纳米颗粒方法有很多[6-8]。
本实验采用溶剂交换法是制备淀粉纳米颗粒,首先将淀粉溶于溶剂相二甲基亚砜中,然后滴加到另一种不良溶剂短链醇分散相中,由于淀粉在该分散相中不溶解,当两相接触淀粉悬浮液便发生聚集迅速形成淀粉纳米粒子。溶剂交换法具有操作简单,快速易完成,纳米粒子分布峰较窄,重现性好,所需有机溶剂较少等优点。
1 材料与方法
1.1 材料与仪器
玉米淀粉:长春大成玉米淀粉有限公司;乙醇(分析纯)和二甲基亚砜(分析纯):北京化工厂。
高速离心机(LG10-2.4 A):北京雷勃尔离心机有限公司;高功率数控超声波清洗器(KQ-600KDE):昆山市超声仪器有限公司;电子天平(AL104):梅特勒-托利多仪器有限公司;磁力搅拌器(JB-3):上海雷磁新泾仪器有限公司;纳米粒径电位分析仪(Nano-ZS90):马尔文公司(英国);场发射扫描电镜(JSM-670 0F):日本 JEOL 公司;红外分析仪(Spectrum One):美国PE仪器公司;电热恒温鼓风干燥箱(101A-3):上海博迅实业有限公司医疗设备厂。
1.2 方法
1.2.1 淀粉纳米颗粒的制备
90℃条件下,将质量浓度10 g/L淀粉二甲基亚砜溶液保温0.5 h,磁力搅拌下,滴加到乙醇中,分散后离心,舍去上清液,再用醇洗3次,备用。
1.2.2 粒径动态光散射
配制浓度为10 mg/mL的淀粉纳米颗粒水溶液,通过激光粒度仪进行颗粒尺寸检测。25℃条件下,每个样品测试3次取平均值。
1.2.3 傅里叶变换红外光谱
采用溴化钾(KBr)压片法进行红外光谱分析。测试条件:光谱分辨率为4 cm-1,扫描范围为4 000 cm-1~400 cm-1,扫描次数32次。
1.2.4 扫描电镜分析
用导电胶把样品固定在样品台上,经真空镀金膜后进行观察和拍摄。
1.2.5 X-射线衍射分析
采用 Cu 靶特征射线 Kα(λ =1.542 Å),石墨单色器,电流30 mA,工作电压40 kV,扫描速度8.000°/min,步长0.02°,扫描范围5.00°~40.00°。测试前,样品50℃烘至恒重。
2 结果与讨论
溶剂交换法制备淀粉纳米颗粒,淀粉应能够很好地溶解于溶剂,而在不良溶剂中则需要完全不溶,溶剂与不良溶剂二者之间应具有良好的混溶性,基于此条件,实验对不良溶剂的类型、乙醇浓度以及良溶剂/不良溶剂体积比进行了考察。
2.1 不良溶剂种类对淀粉纳米粒径的影响
以脂肪醇尤其是短链醇为不良溶剂,更有利于得到稳定的纳米粒子悬浮液。当淀粉-二甲基亚砜溶液与短链醇接触时,体系介电常数(ε)发生改变,二甲基亚砜与短链醇互相扩散,短链醇分子会占据先前二甲基亚砜分子的空间位置而使混合液极性降低,淀粉溶解度下降。图1表明淀粉纳米粒径尺寸随不良溶剂变化情况。
随短链醇碳原子数增多,介电常数逐渐下降,粒径尺寸略有增加,但增幅较小,只有戊醇为不良溶剂时制备的粒子尺寸较大,这可能与其具有较低的介电常数(ε=13.9),呈现出非极性溶剂性质有关[9]。考虑成本及毒性问题,实验采用乙醇作为不良溶剂。
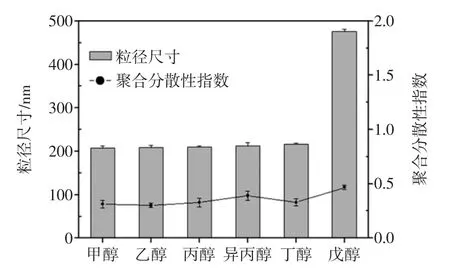
图1 不良溶剂种类对淀粉纳米粒子尺寸的影响Fig.1 Effect of non-solvent type on the size of starch nanoparticles
2.2 乙醇浓度对淀粉纳米粒径尺寸的影响
以乙醇为不良溶剂,考察乙醇体积浓度对淀粉纳米粒径尺寸的影响,结果见图2。
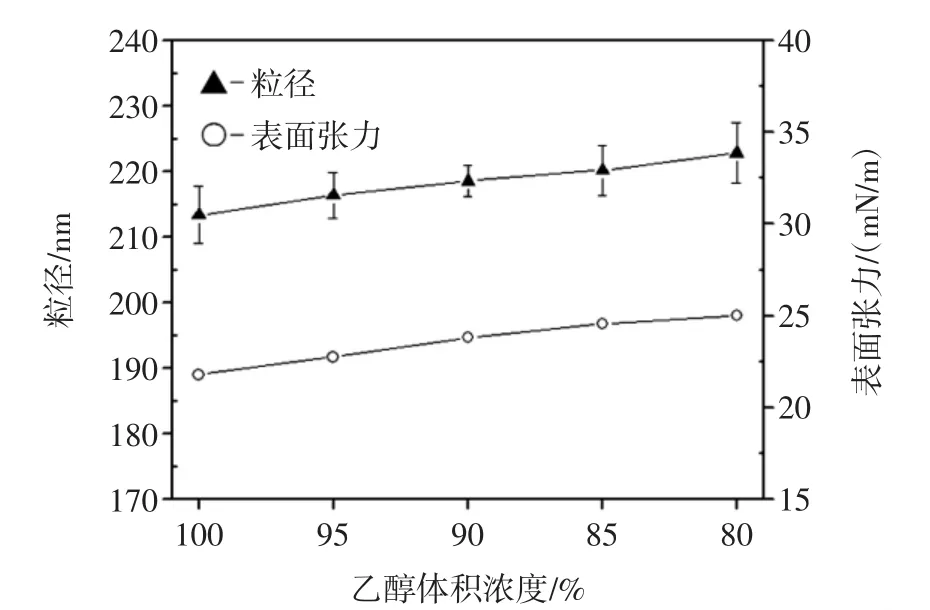
图2 不良溶剂乙醇体积浓度与表面张力及粒径尺寸之间的相关性Fig.2 Correlation between the alcohol volume concentration and the surface tension and particle size
由如图2可知,当乙醇中水分逐渐增加时,表面张力也会逐渐增大,制备的纳米粒子尺寸也呈现逐渐增大的趋势,当以无水乙醇为不良溶剂时获得的粒子尺寸最小。可能的原因是,乙醇中水分的增加导致溶剂能力提升,加快了Ostwald熟化[10],因而粒子尺寸增大。当乙醇体积浓度低于80%时,在沉淀过程中粒子会发生团聚粘附至杯内壁,而粒子在重新溶解过程甚至出现聚集,部分沉淀难以分散溶解。因而实验选择无水乙醇作为不良溶剂。
2.3 溶剂/不良溶剂体积比
溶剂/不良溶剂体积比对于纳米粒子的形成也非常重要。溶剂与不良溶剂不同体积比制备淀粉纳米颗粒扫描电镜图如图3所示。
由图3可知,当两者体积比1∶5时,动态光散射检测粒子的等效粒径尺寸为(219.9±0.81)nm,而当体积比增加到1∶20时,此时测得的粒径为(209.2±4.31)nm,通过观测颗粒形态,图3显示粒子外貌差别较明显,溶剂/不良溶剂体积比越大,球形粒子边缘越清晰,粒子越小越均匀。

图3 溶剂与不良溶剂不同体积比制备淀粉纳米颗粒扫描电镜图Fig.3 Scanning electron microscope of starch nanoparticles prepared by different volume ratio of solvent and non-solvent
3 淀粉与淀粉纳米颗粒的结构表征
3.1 淀粉及纳米淀粉的颗粒粒径分布与扫描电镜图
玉米淀粉和淀粉纳米颗粒的扫描电镜及动态光散射图如图4所示。
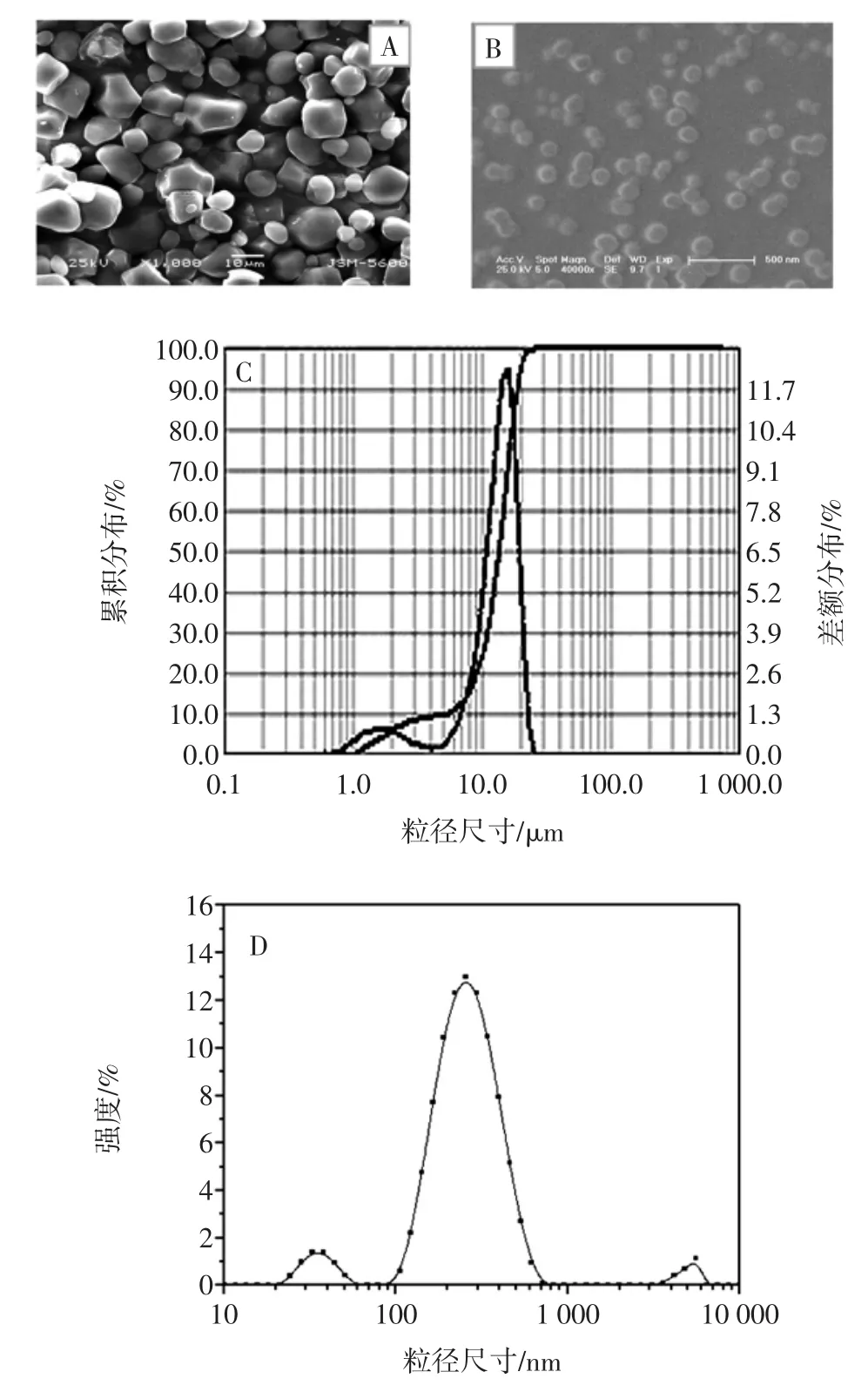
图4 玉米淀粉和淀粉纳米粒径分布及电镜图Fig.4 Particle size distribution and scanning electron microscope of corn starch and starch nanoparticles
从图4A玉米淀粉扫描电镜照片可清晰的看到,原淀粉颗粒的尺寸在5 μm~20 μm之间,形貌不规则大小不均一。动态光散射检测(图C)平均粒径14.4 μm。而制备的纳米淀粉颗粒(图B)形貌规整,直径在150 nm~250 nm之间,动态光散射(图D)检测平均粒径尺寸为(218.8±4.66)nm,这与扫描电镜所观测的数据基本一致,说明动态光散射可作为淀粉纳米颗粒分散液尺寸分布的检测工具。图D还显示,在水溶液中淀粉纳米粒子尺寸分布主要集中在3个区域,大尺寸的颗粒主要来自在水溶液中纳米粒子聚集,而孤立淀粉纳米颗粒尺寸约30 nm~40 nm,扫描电镜图上也证实了粒子存在的不同状态。
3.2 淀粉与淀粉纳米颗粒的晶体结构
玉米淀粉和淀粉纳米颗粒X-射线衍射图如图5所示。
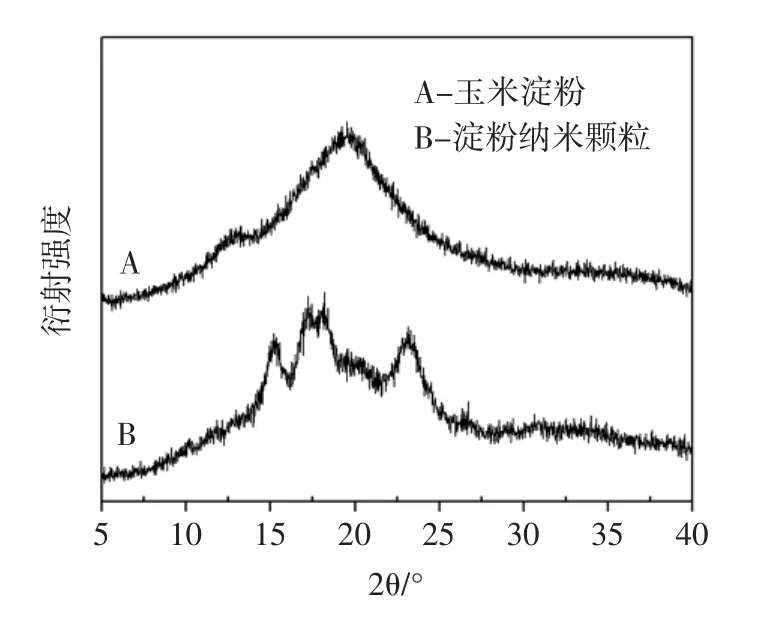
图5 玉米淀粉和淀粉纳米颗粒X-射线衍射图Fig.5 X-ray diffraction pattern of corn starch and starch nanoparticles
天然淀粉结晶类型可分为V型、A型、B型和C型[11]。玉米淀粉为典型的A型结晶图谱,从图5A可以看出曲线由尖峰衍射特征和弥散衍射特征两部分组成,在衍射角 15 °,17 °,18 °,23 °处有尖锐的衍射峰[12]。而淀粉纳米颗粒(B)谱图明显不同于原淀粉,结晶峰消失,这表明随着淀粉颗粒在二甲基亚砜中溶胀,二甲基亚砜分子减弱或者破坏淀粉原有的分子内和分子间氢键,致使淀粉螺旋结构区域伸展,淀粉的晶体结构也随之被破坏,导致衍射峰消失。
3.3 淀粉与淀粉纳米颗粒的红外光谱表征
玉米淀粉(A)和淀粉纳米颗粒(B)的红外光谱图如图6所示。
对比二者红外光谱图可以看出在峰形峰位方面没有明显的差别。在淀粉纳米颗粒谱图上也未发现二甲基亚砜分子中-CH3基团和-S=O基团的特征吸收峰,说明二甲基亚砜在体系中仅作为溶剂,并没有与淀粉基团发生作用。
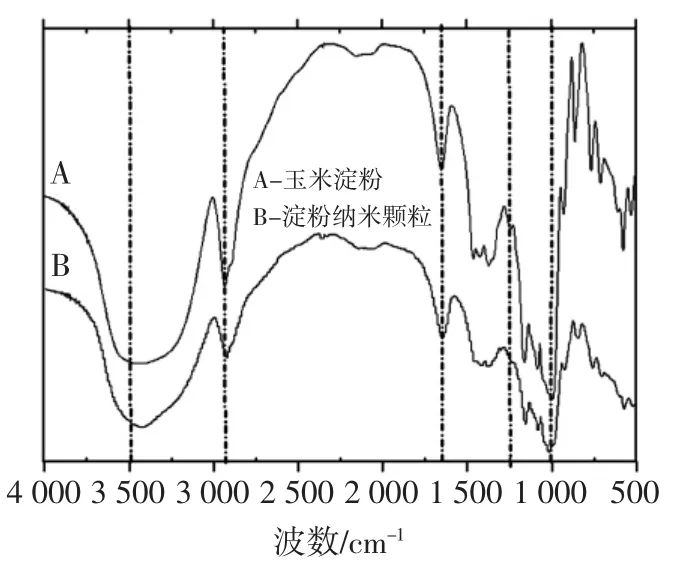
图6 玉米淀粉和淀粉纳米颗粒的红外光谱图Fig.6 Infrared spectra of corn starch and starch nanoparticles
4 结论
以二甲基亚砜作为溶剂,采用溶剂交换法制备淀粉纳米颗粒过程,不良溶剂的选取,其体积浓度以及溶剂与不良溶剂体积比都对制备的淀粉纳米颗粒尺寸和形态产生较大影响。采用无水乙醇为不良溶剂,当溶剂与不良溶剂体积比1∶20,制备的淀粉纳米颗粒尺寸(218.8±4.66)nm,粒子尺寸分布较均匀。结构表征表明,制备的淀粉纳米化学结构未发生改变,晶体结构被破坏,衍射峰消失,颗粒形态为球形均一粒子,改变制备条件调整相应参数可对粒径尺寸进行调控。
[1]Verma A,Ratnawat S,Gua A K,et al.PLGA nanoparticles for delivery of Losartan Potassium through intranasal route:Development and Characterization[J].International Journal of Drug Development&Research,2013,5(1):185-196
[2]Vauthier C,Bouchemal K.Methods for the Preparation and Manufacture of Polymeric Nanoparticles[J].Pharmaceutical Research,2009,26(5):1025-1058
[3]Ju-Nam Y,Lead J R.Manufactured nanoparticles:An overview of their chemistry,interactions and potential environmental implications[J].Science of the Total Environment,2008,400(1/3):396-414
[4]周雨佳,肖茜,邓放明.纳米淀粉的制备及其在可食性薄膜中的应用研究进展[J].食品与机械,2016,32(9):229-232
[5]Sekhon B S.Food nanotechnology-an overview.[J].Nanotechnol Science&Applications,2010,3(10):1-15
[6]刘葆媛,陶希三,荣会,等.玉米淀粉纳米颗粒的制备研究[J].辽宁师范大学学报(自然科学版),2015(3):370-374
[7]涂宗财,任维,刘成梅,等.纳米级大米淀粉的制备及性质[J].农业工程学报,2008,24(1):250-253
[8]徐晖,姬雅菊,王绍宁,等.聚合物纳米颗粒的制备及其应用(Ⅱ)利用合成聚合物或天然大分子制备纳米颗粒[J].中国药剂学杂志:网络版,2004(4):93-102
[9]王寿甫.物质的溶解度与溶剂性质的关系[J].张家口师专学报:自然科学版,1993(1):12-17
[10]吴志方,刘超.二元互不溶体系中第二相颗粒的Ostwald熟化[J].材料导报,2016,30(5):23-26
[11]王梦嘉,叶晓汀,吴金鸿,等.淀粉冻融稳定性的研究进展[J].粮油食品科技,2016,24(5):19-23
[12]杨景峰,罗志刚,罗发兴.淀粉晶体结构研究进展[J].食品工业科技,2007(7):240-243
Preparation and Characterization of Starch Nanoparticles by Solvent Exchange Method
WU Xiu-li,JIANG Xue,DUAN Lei,GUO Chun-xiang
(College of Food Science and Engineering,Changchun University,Changchun 130012,Jilin,China)
The starch nanoparticles were prepared by solvent exchange method using two dimethyl sulfoxide as solvent and short chain alcohol as non-solvent.The influence of non-solvent type,concentration and solvent/non-solvent volume ratio on particle size was investigated,and the particle structure and morphology was also characterized by FT-IR spectrascopy,scanning electron microscope and X-ray diffraction.The results showed that the size of starch nanoparticles was (218.8±4.66)nm when absolute ethanol as solvent,solvent/non-solvent volume ratio 1∶20.The particle size was uniform,the chemical structure was unchanged,the crystal structure was destroyed,and the diffraction peak disappeared.
starch nanoparticles;solvent exchange method;structure;investigation
10.3969/j.issn.1005-6521.2017.24.002
吉林省教育厅“十三五”科学技术研究项目(吉教科合字[2016]第301号);长春大学国家级科研项目培育项目(2016JBC26L26)作者简介:吴修利(1974—),男(汉),副教授,博士,主要从事淀粉及淀粉衍生物方向的研究。
2017-09-28
