HPLC双波长切换同时测定玄参药材中哈巴苷和哈巴俄苷的含量
2017-12-07向采芹李希冯建安黄嫣
向采芹,李希,,冯建安,黄嫣
·品种品质·
HPLC双波长切换同时测定玄参药材中哈巴苷和哈巴俄苷的含量
向采芹1,李希1,2,冯建安2,黄嫣2
目的:建立以双波长切换方式同时测定玄参药材中哈巴苷和哈巴俄苷的含量的方法。方法:采用ShimpackVP-ODS C18柱(250 mm×4.6,5 μm)色谱柱,以乙腈(A)-磷酸(0.03%)(B)为流动相进行梯度洗脱:0-10 min,3%-10%(A);10-20 min,10%-33%(A);20-25 min,33%-50%(A);25-30 min,50%-80%(A);30-35 min,80%(A);35-37 min,80%-3%(A);检测波长:前10 min为278 nm,10-15 min为210 nm,15 min后为278 nm,柱温为30 ℃,进样量为10 μL,流速为1 mL⋅min-1。结果:哈巴苷在0.011824-0.11824 mg⋅mL-1范围内与哈巴俄苷在0.00416-0.0416 mg⋅mL-1范围内线性关系良好。结论:该检测方法稳定可行 ,可用于同时测定玄参药材中哈巴苷和哈巴俄苷的含量。
HPLC双波长切换;玄参药材;哈巴苷;哈巴俄苷;含量测定
玄参是玄参科(Scrophulariace)玄参属(Scrophularia)玄参(Scrophularia,ningpoensisHemsl)的干燥根。主要功效是清热凉血,滋阴降火,补肾益气[1]。《本草纲目》中提到“肾水受伤,真阴失守,孤阳无根,发为火病,法宜壮水以制火,故玄参与地黄同功。其消瘰疬亦是散火,刘守真言结核是火病”[2]。玄参含环烯醚萜、苯丙素、微量挥发油、植物甾醇、油酸、亚麻酸、糖类、左旋天冬酰胺及生物碱等多种化学成分。具有保护心血管系统,增强免疫力等药理活性[3]。同时还具有解热,镇痛,抗炎,抗肿瘤的药理作用[4]。本文对玄参的主要成分哈巴苷和哈巴俄苷进行波长转换法同时测定,对15版药典将两个成分分开测定进行改进,使得测定方法更加高效简便。
1 仪器与试药
1.1 仪器
Agilent-1260 高效液相色谱仪 ( 美国安捷伦科技有限公司);KQ-300DE 型数控超声波清洗器 ( 昆山市超声仪器有限公司);BT-125D 型电子天平 ( 赛多利斯科学仪器北京有限公司);LK-1000A500摇摆式高速中药粉碎机 ( 浙江温岭市创力药材器械厂制造)。
1.2 药品
玄参药材(四川省中药饮片有限责任公司),哈巴苷对照品(成都瑞芬思生物科技有限公司,批号H-021-150729),哈巴俄苷对照品(中国食品药品检定研究院,批号111730-201508)。
1.3 试剂
乙腈、磷酸为色谱纯(美国 Fisher 公司);甲醇为分析纯,水为超纯水 ( 实验室自制) 。
2 试验方法与结果
2.1 对照品的制备
取哈巴苷对照品,哈巴俄苷对照品适量,精密称定,加入30%的甲醇制成每1 mL含哈巴苷60 μg,哈巴俄苷20 μg的混合对照品溶液。
2.2 玄参药材溶液的制备
取玄参药材粉末0.5 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇溶液50 mL,密塞,称定重量,浸泡一小时,超声处理(功率500 w,频率40 KHZ)45 min,放冷,再称定重量,用50%甲醇补足失重,摇匀,0.45 μm微孔滤膜过滤,取续滤液,即得。
2.3 色谱条件的确定
本文经过文献查阅[5-7],经过实验对比,最终确定的色谱条件为:AgiLent 1260型高效液相色谱仪,DAD二极管阵列检测器,采用Shim-packVP-ODS C18柱(250 mm×4.6,5 μm)色谱柱,以乙腈(A)-磷酸(0.03%)(B)为流动相进行梯度洗脱:0-10 min,3%-10%(A);10-20 min,10%-33%(A);20-25 min,33%-50%(A);25-30 min,50%-80%(A);30-35min,80%(A);35-37 min,80%-3%(A)[1];检测波长:前10 min为278 nm,10-15 min为210 nm,15 min后为278 nm,柱温为30 ℃,进样量为10 μL,流速为1 mL⋅min-1。
2.4 系统适应性试验
在上述色谱条件下,按药典规定,理论塔板数按哈巴苷与哈巴俄苷峰计算不低于5 000,分离度均大于1.5,对称因子分别为0.9和0.7,其对照品及供试品色谱图见图1。
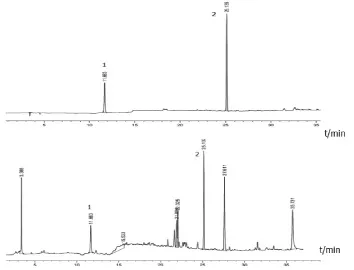
图1 哈巴苷和哈巴俄苷混合对照(A)和玄参对照药材(B)HPLC图
2.5 线性关系的考察
分别精密吸取哈巴苷(0.05912 mg⋅mL-1)对照品溶液2、4、6、8、10、20 μL及哈巴俄苷(0.0208 mg⋅mL-1)2、4、6、8、10、20 μL注入高效液相色谱仪,记录两个对照品的含量与峰面积,以哈巴苷和哈巴俄苷的含量为横坐标(X)(μg),以相应的峰面积为纵坐标(Y),得回归方程:哈巴苷:Y = 7002.1X + 1.0837,R2= 0.9999,哈巴俄苷Y = 19827X + 0.9007,R2= 0.9999,表明哈巴苷在0.011824-0.11824 mg⋅mL-1范围内与哈巴俄苷在0.00416-0.0416 mg⋅mL-1范围内线性关系良好。
2.6 精密度实验
精密量取所配制的哈巴苷与哈巴俄苷混合对照品,按照“2.3”项下的色谱条件进行连续进样6次,记录峰面积,结果显示哈巴苷和哈巴俄苷峰面积的RSD值分别为0.85%、1.01%,结果表明仪器精密度良好。
2.7 重复性实验
取同一批玄参药材,按照“2.2”项下的玄参药材供试品溶液制备方法制得6份供试品溶液,按照“2.3”项下的色谱条件进行6次实验,记录峰面积,结果显示哈巴苷和哈巴俄苷峰面积的RSD值分别为1.23%、1.58%,结果表明该方法重复性良好。
2.8 稳定性试验
取同一批玄参药材,按照“2.2”项下的玄参药材供试品溶液制备方法制得1份供试品溶液,分别在2、4、8、10、12、24 h按照“2.3”项下的色谱条件进行实验,记录峰面积,结果显示哈巴苷和哈巴俄苷峰面积的RSD值分别为0.96%、1.23%,结果表明供试品在24h内稳定。
2.9 样品测定
取同一批玄参药材,按照“2.2”项下的玄参药材供试品溶液制备方法制得玄参药材供试品溶液,按照“2.3”项下的色谱条件进行实验,测得的玄参药材中哈巴苷和哈巴俄苷的含量分别为0.1888 μg、0.5046 μg,哈巴苷与哈巴俄苷的总量经计算为0.68%>0.45%,符合药典规定。
2.10 耐用性实验
取同一批样品,按药材供试品溶液的制备方法制成供试品溶液,使用不同品牌色谱柱(分别为Shim-pack VP-ODS柱(250×4.6 mm,5 μm);AgiLent ZORBAX SB C18(4.6×150 mm,5 μm),进行耐用性试验,结果哈巴苷的含量分别为0.1865、0.1874 μg,哈巴俄苷的含量分别为0.4899、0.5012 μg。结果表明此方法可行。
3 讨论
在制备玄参药材供试品溶液之前考察玄参药材粉末的粒度,最终确定药材粉末能通过2号筛的进行试验。在玄参药材供试品溶液制备过程中考察药材的浸泡时间、超声提取时间以及提取方式,最终确定的为浸泡1 h,超声45 min。选择色谱条件时,考察前15 min均以210 nm的波长进行测定,结果发现,在药材高效液相色谱图中出现较多杂峰,分离度不够,因此在前10min选择278 nm以排除较多的杂峰,在10-15 min内采用210 nm较好的分离出目标峰,同时选用不同的分离柱考察此方法的耐用性,结果表明此方法稳定可行。本文主要通过HPLC波长切换的方法更加快速简便高效的同时测定玄参药材中哈巴苷和哈巴俄苷的含量,解决药典中两种成分需进行两次试验的繁琐,同时采用波长切换的方法除去供试样品中目标峰前后不必要的杂峰,使目标峰达到很好的分离效果,且保持峰面积稳定。可以用于玄参药材的含量测定方法,对其含玄参的复方制剂提供了更加稳定可行且简便的方法,因此,在实际操作中具有重大意义。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].北京∶ 中国医药科技出版社,2015.
[2] 李时珍.《本草纲目》∶中国言实出版社,2012年版.
[3] 许福泉,许旭东,陈士林. 玄参化学成分及药理活性研究进展[J].中国现代中药,2013,(09)∶752-759.
[4] 白宇.玄参的药味药理学初步研究[D].黑龙江中医药大学,2014.
[5] 梁晨,徐思思,聂诗明. HPLC法测定不同产地微波真空干燥玄参中哈巴苷和哈巴俄苷的含量[J]. 数理医药学杂志,2012,(06)∶688-690.
[6] 曹岗,丛晓东,蔡皓,等. HPLC-DAD法同时测定玄参炮制前后8个有效成分的含量[J]. 中国天然药物,2012,(03)∶213-217.
[7] 张雪梅,王瑞,安睿,等. HPLC同时测定玄参中5种成分的含量[J]. 中国中药杂志,2011,(06)∶709-711.
Simultaneous detection of the contents of harpagide and harpagoside in Xuanshen by Dual-wave switching HPLC
/XIANG Cai-qin1, LI Xi1,2, FENG Jian-an2, HUANG Yan2//(1.School of Pharmacy, Chengdu University of Traditional Chinese Medicine; Key Laboratory of Standardization for Chinese Herbal Medicine, Ministry of Education; National Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan;2.Sichuan Academy of Traditional Chinese Medicine sciences, Institute of TCM, Chengdu 610031, Sichuan)
Objective:To establish Dual-wave switching HPLC method to detect the contents of harpagide and harpagoside in Xuanshen.Method:The analysis was carried on a Shim-packVP-ODS C18(250×4.6 mm,5μm) column. The mobile was acetonitrile(A) and 0.3% Phosphoric Acid (B) which was in gradient elution at fl ow rate of 1mL⋅min-1as following∶ 0~10min, 3%~10% (A);10~20 min, 10%~33% (A); 20~25 min, 33%~50% (A); 25~30 min, 50%~80% (A); 30~35 min, 80% (A); 35~37min, 80%~83% (A).The wave length was set at 278 nm during 0~10 min;210 nm during 10 ~15 min;278 nm after 15 min. Column temperature was 30℃, and sample volume was 10 μL.Result:The response of harpagide in the range of 0.011824-0.11824 mg⋅mL-1and the response of harpagoside in the range of 0.00416-0.0416 mg⋅mL-1had a good linear relationship with concentration.Conclusion:The detection method is stable and feasible, which can be used for simultaneous determination the contents of harpagide and harpagoside in Xuanshen.
Dual-wave switching HPLC; Xuanshen; harpagide; harpagoside; content determination
R 282.6
A
1674-926X(2017)06-003-03
1. 成都中医药大学药学院 中药材标准化教育部重点实验室 四川省中药资源系统研究与开发利用重点实验室省部共建国家重点实验室培育基地,四川 成都 6111372;2. 四川省中医药科学院中医研究所,四川 成都 610031
向采芹(1992-),女,硕士研究生,研究方向:中药新剂型,新技术,新工艺的研究Email∶742426178@qq.com
李希(1969-),女,硕士,教授,研究方向:中药新剂型,新技术,新工艺的研究Email∶1836820767@qq.com
2017-07-21
(责任编辑:胡慧玲)
