大黄药材贮藏期间质量及药理作用变化研究
2017-12-07李倩艾青青兰志琼郑立王亚云孙雪梅卢先明
李倩,艾青青,兰志琼,郑立, 王亚云,孙雪梅,卢先明
·品种品质·
大黄药材贮藏期间质量及药理作用变化研究
李倩,艾青青,兰志琼,郑立, 王亚云,孙雪梅,卢先明
目的:研究贮藏期间大黄药材的质量以及药理作用变化情况,为临床药用提供一定的参考。方法:对贮藏两年内大黄药材的外观质量、干燥失重、浸出物含量进行动态观测,并采用炭末法、毛细玻管法及断尾法对贮藏一年后的两组大黄药材泻下、凝血、止血作用变化研究。结果:随着贮藏时间的延长,大黄药材发生变质现象、干燥失重降低、浸出物含量不符合标准;贮藏一年后的两组大黄药材仍有明显泻下作用,但止血和凝血作用不明显。结论:大黄药材在贮藏过程中,质量会不断变化;一年贮藏时间虽对大黄药材的泻下作用无明显影响,但对其止血和凝血作用影响较大。
大黄;贮藏养护;药效
大黄为蓼科植物掌叶大黄Rheum palmatumL.唐古特大黄Rheum tanguticum Maxim.ex Balf.或药用大黄Rheum officinaleBaill.的干燥根及根茎[1]。是一味常用大宗药材,味苦,性寒。具有泻热通肠,凉血解毒,逐瘀通经之功效。多用于实热便秘,血热吐衄,肠痈腹痛等证。由于大黄所含化学成分不稳定,在贮藏过程中极易受到环境影响而产生虫蛀、发霉、变色等变质现象,严重影响此类药材品质和临床疗效。本文依据课题组前期研究,对低温贮藏养护组和常温条件贮藏组大黄药材进行外观性状、干燥失重、浸出物含量等动态观测,并对贮藏一年前后两组大黄药材的泻下、止血和凝血作用作对比研究,探究贮藏前后大黄药材的质量变化规律,初步探讨贮藏时间对其相关药理作用的影响,以期为临床用药提供一定参考。
1 材料
1.1 实验药材
大黄药材:采集于四川省绵阳市平武县平通镇新远村麻子岭,经成都中医药大学卢先明教授鉴定为蓼科植物药用大黄Rheum officinaleBaill的干燥根及根茎。
1.2 实验动物
①贮藏前:昆明种小鼠(一级),雌雄各半,体重18~22g,由成都中医药大学医学动物实验中心提供,动物合格证号∶ SCXK(川)2008-11。②贮藏一年后:昆明种小鼠(一级),雌雄各半,体重18~22g,由四川省医学科学院实验动物研究所提供,动物合格证号:SCXK(川)2004-15。
1.3 受试药物
①贮藏前:大黄药材。②贮藏一年后:与贮藏前为同批药材。
2 仪器与试剂
2.1 仪器
真空干燥箱(上海森信实验仪器有限公司,DZG-6090型);电热鼓风干燥箱(上海实验仪器厂有限公司,202-2型);水浴恒温振荡器(金坛市医疗仪器厂,SHZ-88);微型植物试样粉碎机(北京中兴伟业仪器有限公司,FZ102);电子恒温水浴锅(北京中兴伟业仪器有限公司,DZKW-4型);电子天平(YP601N型,上海精密科学仪器有限公司);灌胃针;秒表;玻璃毛细管(内径0.9mm,长100mm)等。
2.2 试剂与试药
白酒(60°高粱酒重庆江津酒厂有限公司);乙醇(分析纯 成都科龙化工试剂厂,批号:20060201);活性炭末(分析纯 重庆北碚精细化工厂,批号:20040912);生理盐水(0.9%,四川科伦药业股份有限公司,批号:20071208);云南白药粉(云南白药集团股份有限公司,批号:Z53020798)。
3 实验分组
根据课题组前期研究,将大黄药材分成两组进行贮藏,一组为贮藏养护组,即低温组;另一组为大黄药材仓储常用方法,即常温组。两组具体贮藏条件见表1。

表1 大黄贮藏养护方法设计试验分组表
4 质量观测
4.1 外观质量
观察大黄药材的色泽、气味、虫蛀、吸潮、霉变五项外观质量指标的变化程度,以分数评定,每项满分2分。贮藏前均为满分10分。色泽使用RALK7色标卡进行评分,色泽浅黄色系(色标卡编号:1003~1037)和深黄色系(色标卡编号:2000~2011)不扣分,棕黄色系(色标卡编号:3000~3016)扣0.5分,黄褐色系(色标卡编号:8001~8025)扣1分;气味变淡或有异味者,扣1分;吸潮程度根据水分含量测定评分,超过2015版《中国药典》相关项下规定者,扣2分;虫蛀程度:少见虫眼(虫蛀药材百分比:0~10%)扣0.5分,多见虫眼(10%~20%)扣1分,多虫眼和蛀粉(20%~30%)扣1.5分,多蛀空成粉(30%以上)扣2分;霉变药材百分比为0~10%扣0.5分,10%~20%扣1分,20%~30%扣1.5分,30%以上扣2分。观测结果具体见表2。

表2 大黄外观质量观测结果
结果显示:大黄贮藏后外观质量会变差。常温组存放两年后外观性状差异与贮藏前相比较大,提示大黄需要科学合理的养护方法来贮藏方能确保其外观质量;因低温组与白酒同贮则有吸潮、色泽变深、白酒气味重的现象,提示白酒不宜作为大黄贮藏的对抗剂。
4.2 干燥失重
照2015版《中国药典》四部通则限量检查法项下0831干燥失重测定法[2]。由减失的重量和取样量计算大黄的干燥失重。结果见表3。

表3 大黄贮藏期间干燥失重含量
由表3可知:低温组大黄贮藏期间干燥失重明显增加,且超过了2015版《中国药典》所规定的不得过15.0%[2];常温组贮藏8个月内有吸潮现象,且干燥失重量超过了规定值,而贮藏12~24个月期间,其干燥失重量逐渐减少到规定范围内并保持一定水平,提示大黄药材在贮藏期间有吸潮现象。
4.3 浸出物含量
照2015版《中国药典》四部通则2201水溶性浸出物测定法项下的热浸法[2]。测定结果见表4。

表4 大黄贮藏期间浸出物含量
数据显示:在大黄的两年贮藏期内,两组大黄浸出物含量均低于贮藏前,但均在2015版《中国药典》规定值(不得少于25%)范围内,且常温组低于低温组,提示大黄在贮藏期间浸出物有逐渐减少的趋势。
5 大黄贮藏期间药理作用变化研究
根据大黄的功效,对贮藏前及贮藏一年后大黄药材的泻下、凝血、止血作用进行对比研究。
5.1 泻下作用(炭末法[3])
5.1.1 受试药物的制备 称取大黄粗粉100g,加8倍量水(800mL)浸泡30min[4],煮沸15min后,过滤。于40~50℃浓缩至0.5g生药/mL(200mL)。
5.1.2 实验分组贮藏前 取健康小鼠20只,雌雄各半,随机分为2组,每组10只,分别为(1)空白组(给予0.9%生理盐水0.2mL/10g体重灌胃)(2)大黄水煎液组(简称大黄组)具体分组见表5。
贮藏一年后 取健康小鼠30只,雌雄各半,随机分为3组,每组10只,分别为(1)空白组(同上)(2)常温组(3)低温组。具体分组见表6。
5.1.3 实验方法与结果 分组后连续给相应药物2d[4],日灌胃量按表5、表6。然后禁食不禁水20~24h后,给以相应炭末混悬药液,含炭末0.1g⋅mL-1。此时开始计时,将小鼠分置于铺有滤纸的笼内进行观察。记录其出现黑便的时间,排黑便的数量、性状以及稀粪沾染肛门的情况,连续观察6h。用SPSS13.0版统计软件对各组实验数据进行统计分析[5]。结果见表5、6。

表5 贮藏前大黄对正常小鼠排便时间和数量的影响

表6 贮藏一年后大黄对正常小鼠排便时间和数量的影响

注:与空白对照组相比较,***P<0.001。
结果显示:与空白组相比,贮藏前大黄泻下作用较强。贮藏一年后两组大黄药液均具有致泻作用。且大黄常温、低温组的泻下作用均较强,能明显缩短排便时间(P<0.001),增加排便数量(P<0.001)。
5.2 止血作用
5.2.1 毛细玻管法[6]受试药物制备
阳性对照组 取云南白药粉2.5g,加蒸馏水50mL,使其浓度为0.05 g⋅mL-1。
大黄组:称取大黄粗粉150g,加8倍量95%乙醇浸泡2h,过滤。减压回收乙醇,使成浸膏。浸膏用60mL的蒸馏水溶解,微加热,趁热过滤,然后再定容为120mL。使其浓度为1.25g生药/mL。
常温、低温组制法均同大黄组。
实验分组
贮藏前 取健康小鼠30只,雌雄各半,随机分为3组,每组10只,分别为(1)空白组(给予0.9%生理盐水0.2mL/10g体重灌胃)(2)阳性组(云南白药液)(3)大黄组。具体分组见表7。
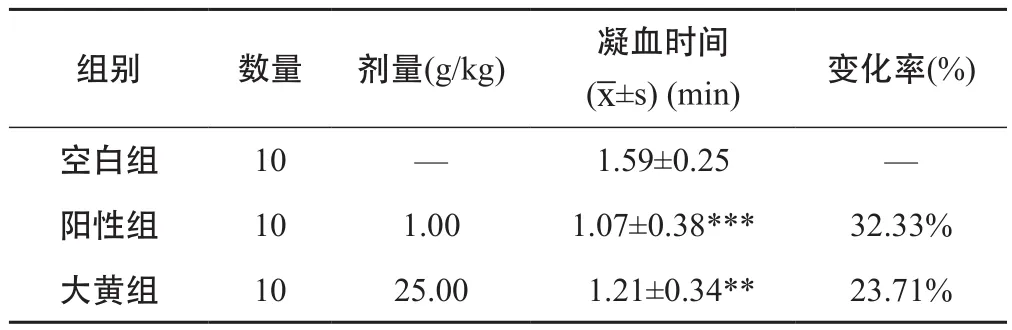
表7 贮藏前大黄对小鼠凝血时间的影响
贮藏一年后 取健康小鼠40只,雌雄各半,随机分为4组,每组10只,分别为(1)空白组(同上)(2)阳性组(同上)(3)常温组(4)低温组。具体分组见表8。
实验方法与结果
分组后连续给相应药物5d,每日一次。最后一次灌胃2h后,用毛细玻管插入小鼠眼内眦后静脉丛,深5mm,自血液流进玻管开始记时,待血液注满玻管后,取出平放于桌面上。每隔15s,折断玻管约5mm,并缓慢向左右拉开观察折断处是否有血凝丝出现,直至有血凝丝出现,所需时间即为凝血时间。计算出药物对凝血时间的缩短百分率(变化率)。结果见表7、8。
凝血时间缩短百分率= ×100%

表8 贮藏一年后大黄对小鼠凝血时间的影响
结果显示:云南白药组与空白、贮藏前大黄、贮藏后常温、低温组大黄相比较,有明显缩短凝血时间的作用,具有显著意义。且云南白药组(P<0.001)的凝血作用较强,能明显缩短凝血时间,凝血作用优于贮藏前大黄组(P<0.01);贮藏一年后大黄常温、低温组与空白组比较无明显缩短凝血时间的作用,而与云南白药组比较,常温组(P<0.01 )与低温组(P<0.001)凝血作用明显不如云南白药组。
5.2.2 小鼠断尾法止血实验[6]受试药物的制备及阳性对照药物 同毛细玻管法5.2.1.1。
实验分组
贮藏前 取健康小鼠30只,雌雄各半,随机分为3组,每组10只,分别为(1)空白组(给予0.9%生理盐水0.2mL/10g体重灌胃)(2)阳性组(云南白药液)(3)大黄组。具体分组见表9。
贮藏一年后 取健康小鼠40只,雌雄各半,随机分为4组,每组10只,分别为(1)空白组(同上)(2)阳性组(同上)(3)常温组(4)低温组。具体分组见表10。
实验方法与结果
连续给相应药物3d,每日一次。最后一次灌胃2h后,将小鼠置于固定器内,暴露其尾部,剪去尾巴尖部(约在距甩尖4mm处),此时启动秒表,这时有血液自尾巴末端流出,每隔15s左右用滤纸轻沾出血处,直至血管断端处无血液被滤纸沾取,此时所用时间为出血时间。计算出药物对出血时间的缩短百分率(变化率)。结果见表9、10。
出血时间缩短百分率= ×100%

表9 贮藏前大黄对小鼠出血时间的影响

表10 贮藏一年后大黄对小鼠出血时间的影响

注:与空白对照组相比较,**P<0.01。
结果显示:与空白组相比较,云南白药、贮藏前大黄组均有缩短出血时间的作用,均具有显著意义。云南白药组(P<0.05)和贮藏前大黄组(P<0.05 )的止血作用均强,能明显缩短凝血时间;贮藏一年后大黄常温、低温组与空白组相比对剪尾后的小鼠出血时间影响均无明显差异,不具有明显止血作用。
6 结果与讨论
6.1 本实验对大黄药材在两年贮藏期间的外观性状、干燥失重、浸出物含量进行了动态观测,发现在贮藏期间外观性状会发生变化且有吸潮现象发生,明确了大黄在存放期间浸出物有逐渐减少的趋势,综合分析观测结果,发现低温比常温条件更适宜大黄贮藏。
6.2 实验结果表明:贮藏一年后的两组大黄仍具有明显泻下作用。而贮藏前大黄具有明显的止血凝血作用,贮藏后两组实验药材均没有明显的止血和凝血作用。说明一年贮藏时间对大黄的泻下作用无明显影响,而对止血和凝血作用影响较大。宋文惠等[7]研究发现大黄在贮藏1~2年内使用最佳,此时有效成分大黄素含量高。大黄素和大黄素甲醚可明显促进血液凝固,大黄饮片在贮藏过程中随着贮藏时间的增加,其蒽醌类成分含量会下降[8-9],由此可见,大黄药材贮藏时间不宜过长。提醒临床药用应注意此问题,同时也说明了中药材及饮片有效期研究的必要性和紧迫性,以及建立中药溯源系统的实际意义。
6.3 大黄的主要有效成分为蒽醌衍生物,结合蒽醌是大黄的主要泻下成分[10]。蒽酚、蒽酮常与蒽醌同时存在,可相互转换逐渐氧化成蒽醌。所以含有蒽醌的药材采集后需储藏一定时间后才可药用,目的是使其成分氧化完全,蒽醌含量增加。大黄在一年的贮藏期内蒽醌含量会有所增加,部分药效成分并未减少,以致贮藏一年后泻下作用无明显减弱[7]。
6.4 现代研究表明:大黄的有效成分主要为蒽醌类、蒽酮类、二苯乙烯类、多糖类及鞣质类等,其药理作用为泻下、抗菌、止血、利胆、抗肿瘤等[11]。下一步应延长贮藏时间,结合化学成分来研究大黄药材药理作用变化,如大黄的蒽醌类、没食子酸和d-儿茶素等有效成分在贮藏期间的变化,以深入探讨大黄在贮藏期间的药效变化以及机制。
[1] 中华人民共和国卫生部药典委员会.中华人民共和国药典2015版一部[S].北京∶中国医药科技出版社,2015∶23.
[2] 中华人民共和国卫生部药典委员会.中华人民共和国药典2015版四部[S].北京∶中国医药科技出版社,2015∶103,202.
[3] 张大方.药理与中药药理实验[M].上海∶上海科学技术出版社,2002,52-53.
[4] 熊辉岩,张晓峰,潭大风,等.大黄属三种植物不同部分提取物清除轻基自由基的体外实验研究[J].食品科学,2003,24(1)∶128-129.
[5] 刘明芝,周仁郁.中医药统计学与软件应用[M].北京∶中国中医药出版社,2006.
[6] 陈奇.中药药理研究方法学,北京∶人民卫生出版社,1993.
[7] 宋文惠,边军昌,刘勤社.中药大黄不同储存时期内的有效成分含量研究[J].陕西中医,2014,35(7)∶913-914.
[8] 李佳,李红磊,许珊.3种大黄饮片在贮存过程中5种蒽醌成分的含量变化[J].中国实验方剂学杂志,2011,17(10)∶94-97.
[9] 邬红兵.不同炮制方法大黄饮片在贮存过程中蒽醌成分的含量变化分析[J].海峡药学,2012,24(04)∶36-37.
[10] 王阳,林鹏程,明升平,等. 四种大黄属高山药用植物蒽醌类成分含量的测定[J]. 湖北农业科学,2017,(10)∶1945-1946+1952.
[11] 曾芳,李媛.大黄有效化学成分及其药理作用[J].当代医学,2013,19(12)∶149-150.
Research on the quality and pharmacological changes of Dahuang during storage
/LI Qian,AI Qing-qing, LAN Zhiqiong ,ZHENG Li,WANG Ya-yun, SUN Xue-mei, LU Xian-ming//(School of Pharmacy, Chengdu University of Traditional Chinese Medicine; Key Laboratory of Standardization for Chinese Herbal Medicine, Ministry of Education; National Key Laboratory Breeding Base of Systematic Research, Development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan)
Objective:To investigate the quality and pharmacological changes of Dahuang during storage, and provide some reference for clinical use.Method:The exterior quality, weight loss on drying and extractum content of Dahuang were dynamically observed and measured during two years of storage. The changes of diarrhea,coagulation and hemostasis effect of two Dahuang groups that was stored for one year was investigated by charcoal method, capillary tube method and cutting tail procedure.Result:As the storage time prolonged, metamorphic Dahuang was found. Weight loss on drying decreased and the extract umcontent didn’t meet with the standard. After one year of storage, the two groups still had significant diarrhea effect, but the effects of hemostas is and coagulation was unobvious.Conclusion:The quality of Dahuang is changing during the process of storage. The storage of one year has no significant effect on the diarrhea effect of Dahuang, but greatly in fluencehemostas is and coagulation effect.
Rhubarb; storage conservation; efficacy
R 282
A
1674-926X(2017)06-001-04
国家自然科学基金基础科学人才培养基金-成都中医药大学 中药基础基地科研训练及科研能力提高项目子课题(No.J1310034-07)
成都中医药大学药学院中药材标准化教育部重点实验室四川省中药资源系统研究与开发利用重点实验室省部共建国家重点实验室培育基地,四川成都 611137
李倩(1993-),女,硕士研究生,研究方向为中药品种质量与资源开发Tel∶15680803931 Email∶1270025149@qq.com
兰志琼(1979-),女,博士,副教授,硕士生导师,第四批四川省中医药管理局学术带头后备人选,主要从事中药品种质量与资源开发的教学、科研工作Tel∶028-61800231 Email∶lanlan1979512@126.com
2017-08-25
(责任编辑:胡慧玲)
