硝基苯席夫碱衍生物的合成、结构表征及其抗肿瘤活性研究
2017-11-28易岑兰谢旭芹刘贤智袁泽利
易岑兰,谢旭芹,刘贤智, 王 玉,袁泽利
(遵义医学院 药学院,贵州 遵义 563099)
硝基苯席夫碱衍生物的合成、结构表征及其抗肿瘤活性研究
易岑兰,谢旭芹,刘贤智, 王 玉,袁泽利
(遵义医学院 药学院,贵州 遵义 563099)
目的寻找新结构的抗肿瘤先导化合物。方法将芳香醛与2,4-二硝基苯肼缩合制备得到4个新的硝基苯席夫碱衍生物(1-4)。并利用1H NMR、13C NMR、HR-MS、FT-IR等对其进行结构表征,化合物1经单晶XRD测试。采用MTT法对A549(人肺腺癌细胞)和 HepG2(人源肝癌细胞)耐药细胞株进行体外抗肿瘤活性初步筛选。结果化合物4对A549(人肺腺癌细胞)和 HepG2(人源肝癌细胞)具有中等活性。结论得到的系列硝基苯席夫碱化合物为今后的深入抗肿瘤活性研究与实践奠定了实验基础。
硝基苯;席夫碱; 合成; 表征;抗肿瘤活性
化学治疗在癌症临床治疗中具有十分重要的地位[1-2]。然而,由于动物和人实体瘤中普遍存在着乏氧细胞,这些乏氧细胞由于对化疗、放疗以及光动力治疗都不敏感,且对多种抗癌治疗(如化疗、放疗等)抗拒,从而导致肿瘤治疗失败[3-4]。已有研究证实:肿瘤乏氧细胞会为适应乏氧而发生一系列生物学改变,从而促进肿瘤的恶性表现行为[4-6]。因此,将肿瘤乏氧作为一个重要的靶点进行化学治疗药物开发成为热门研究方向之一[6-7]。已有研究表明[8-9]:具有生物还原性化疗药物能有选择性地杀死肿瘤组织中对射线有对抗性的乏氧细胞,与放疗治疗方案联用可提高肿瘤疗效。因而,生物还原性药物作为一种新型抗肿瘤药物得到了快速发展[9]。硝基芳环或者硝基芳香杂环类化合物可在乏氧条件下被硝基还原酶(Nitroreductases,NTRs)还原为亚硝基、羟胺和胺类化合物,这些还原物质可与DNA作用杀死肿瘤细胞[10]。如Chester Beatty等[11]合成的CB1954和RSU1059已证明在乏氧条件下被DT-心肌黄酶还原为羟胺后与DNA偶联,抑制癌细胞的增殖。
当前应用于临床的抗肿瘤抗生素药物中,多数均是直接作用于DNA或插入DNA的双螺旋结构,抑制以DNA为模板的RNA多聚酶而抑制RNA的合成。稠环芳烃的共平面分子结构特性,使其具有插入DNA作用而干扰模板功能[12]。一些含蒽结构的稠环芳烃化合物如多柔比星(阿霉素)、米托蒽醌、比生群等均已成功应用于临床[13]。在项目组和其他课题组的研究中均证实具有CH=N结构的席夫碱结构具有抗菌、抗肿瘤等多种生物活性[14-18]。为发展芳环硝基苯类席夫碱结构的新化合物并筛选其抗肿瘤活,本文设计合成了四个芳烃的硝基苯类席夫碱结构的化合物,并初步对其进行抗肿瘤活性筛选,以期为新的乏氧选择性化疗药物研究提供新的研究对象和实验基础。
1 实验方法
1.1 仪器与试剂 Varian 1000 FT-IR红外光谱仪(美国瓦里安公司),安捷伦400 MHz-DD2磁共振仪(美国安捷伦公司),Micromass LCT PremierXE高分辨质谱仪(德国布鲁克公司), BRUKER SMART APEX II型单晶X射线衍射仪(德国布鲁克公司),Carry-1000型红外光谱仪(美国安捷伦公司),CO2细胞培养箱(美国Thermo公司),CKX41倒置显微镜(日本Olympus公司),Varioskan Flash全波长扫描式多功能读数仪(美国Thermo 公司)。所有试剂均为分析纯,所用溶剂未经纯化直接使用。
1.2 目标化合物1-4的合成 化合物1-4的合成见图1。
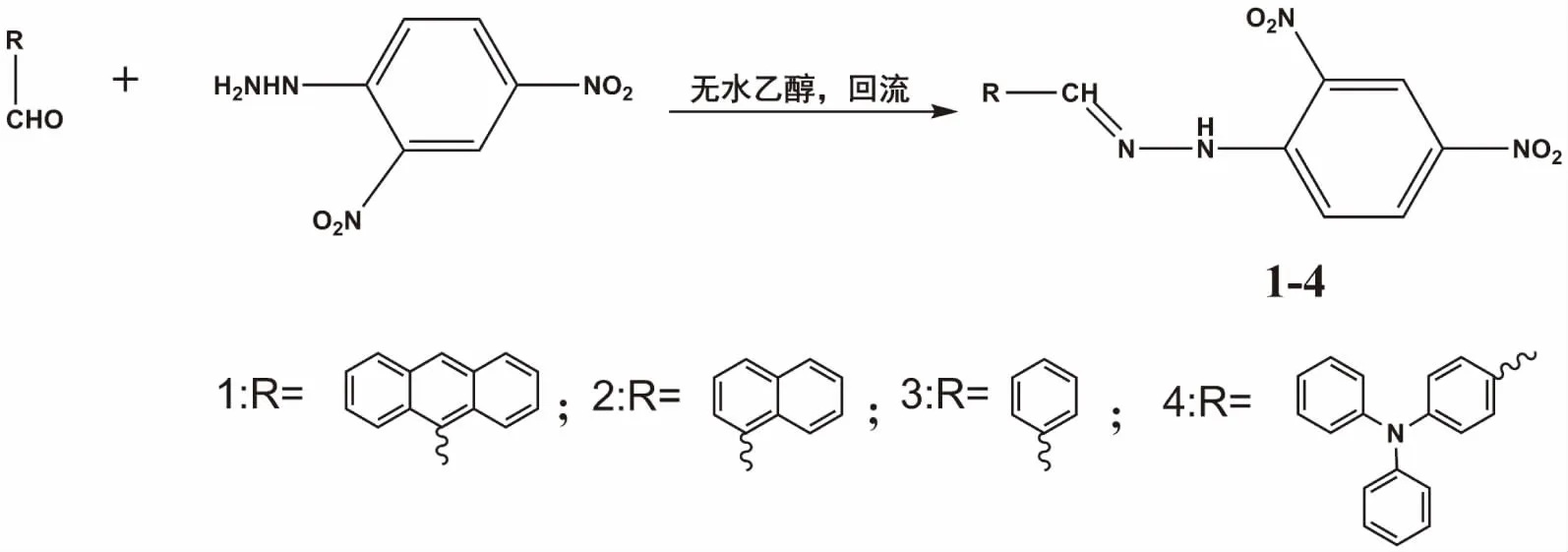
图1 目标化合物1-4的合成
以化合物1的合成为例:称取1.98 g(1 mmol)2,4-二硝基苯肼和2.06 g(1mmol)9-蒽甲醛于100 mL圆底烧瓶中,加入30 mL无水乙醇使其溶解,缓慢滴加10滴冰醋酸(作催化剂)回流12 h后,冷却,抽滤得褐色固体,将固体用DMF(N,N-二甲基甲酰胺)重结晶,即得化合物1。产率:81.8%。1H NMR(DMSO-d6,400 MHz):8.91~8.93(d,J= 8.5 Hz,1H,NH),7.91~7.93 (d,J= 8.4 Hz,1H,CH=N),7.88~7.90(m,3H,Ar-H),7.53~7.55(m,5H,Ar-H),6.95(s,2H,,Ar-H),6.78~6.80(d,J= 8.6 Hz,1H,Ar-H);13C NMR(DMSO-d6,100 MHz):153.15,150.37,136.76,133.30,129.25,129.16,127.46,124.31,122.65,121.92,121.17,115.04,107.35; HR-MS (ESI-MS) calculated for C28H30N4O4(M)+:386.1015,foundm/z:386.0977.FT-IR(4 000~400 cm-1,KBr):3459,3446,3285,3120,1617,1593,1574,1512,1401,1334,1055,827,738。
化合物2,黄色粉末固体。产率:78.6%。1H NMR(DMSO-d6,400 MHz):11.86 (s,1H,NH),9.55(s,1H,CH=N),8.88~8.89(d,J= 2.6 Hz,1H,Ar-H),8.65-8.67(d,J= 8.5 Hz,1H,Ar-H),8.40-8.43(m,1H,Ar-H),8.14~8.16 (d,J= 9.2 Hz,2H,Ar-H),8.03~8.09 (m,2H,,Ar-H),7.61~7.73(m,3H,Ar-H);13C NMR (DMSO-d6,100 MHz) :148.63,128.92,127.44,126.48,125.71,123.52,116.74; HRMS (ESI-MS) calculated for C28H30N4O4(M)+:336.0859,foundm/z:336.0816.FT-IR(4 000~400 cm-1,KBr):3546,3474,3416,3294,1617,1590,1519,1502,1398,1326,1304,1175,839,741。
化合物3,褐色晶状固体。产率:69.3%。1H NMR(DMSO-d6,400 MHz):11.76(s,1H,NH),8.85~8.86(d,J= 2.5 Hz,1H,Ar-H),8.69(s,1H,CH=N),8.36~8.39(m,1H,Ar-H),8.09~8.11(d,J= 9.6 Hz,1H,Ar-H),7.78~7.80(m,2H,Ar-H),7.48-7.49(m,3H,Ar-H);13C NMR(DMSO-d6):149.48,144.61,137.08,133.87,130.65,129.85,129.06,127.45,123.08,116.86; HRMS (ESI-MS) calculated for C13H10N4O4(M)+:286.00702,foundm/z:286.0658.FT-IR(4 000~400 cm-1,KBr):3454,3289,1620,1512,1400,1328,1274,1086,716,685。
化合物4,黄色粉末固体。产率:82.6%。1H NMR(DMSO-d6,400 MHz):11.61 (s,1H,NH) ,8.85~8.86 (d,J= 2.5 Hz,1H,Ar-H),8.61(s,1H,CH=N),8.33~8.35(d,J= 9.6 Hz,1H,Ar-H),8.02~8.04(d,J= 9.6 Hz,1H,Ar-H),7.64~7.36(d,J= 8.6 Hz,2H,Ar-H),7.35~7.39(t,J= 7.8 Hz,4H,Ar-H),7.09~7.16(m,6H,Ar-H),6.95~9.97(d,J= 8.6 Hz,2H,Ar-H);13C NMR(DMSO-d6,100 MHz):149.47,146.36,144.36,136.67,129.80,128.76,126.67,125.16,124.27,121.09; HRMS (ESI-MS) calculated for C25H19N5O4(M)+:476.1334,foundm/z:476.1319.FT-IR(4 000~400 cm-1,KBr):3546,3474,3416,3294,1617,1590,1519,1502,1398,1326,1304,1175,839,741。
1.3 晶体结构测定及解析 将化合物1溶于N,N-二甲基甲酰胺(DMF)放置于室温下缓慢挥发15d后可得粒状晶体。挑选适宜尺寸的颗粒在Bruker APEX2 Smart CCD单晶衍射仪上进行数据收集(石墨单色器单色化的Mo Kα射线(λ=0.071073 nm),φ-ω扫描方式进行单晶衍射数据收集。对强度数据经验吸收校正、LP 校正。晶体结构通过直接法解出。对全部非氢原子坐标以及它的各向异性热参数均进行全矩阵最小二乘法加以修正。计算采用SHELX-97程序得以完成。
1.4 体外抗肿瘤活性初步测试 对合成得到的新化合物1-4用MTT法分别对 A549(人肺腺癌细胞)和 HepG2(人源肝癌细胞)(细胞均来自于遵义医学院医学生物研究中心)进行体外抗肿瘤活性的初步筛选。
具体操作(化合物1为例):取对数生长期的A549或HepG2细胞 ,用0.25%的胰酶消化细胞,离心,去上清,用完全培养基(89%基础培养基,10%胎牛血清,1%双抗;其中A549用DMEM作为基础培养基,HepG2用RPMI 1640作为基础培养基)重悬细胞,使细胞悬液浓度为5×104个/mL,接种于96 孔板中(100 μL/孔),于37 ℃,5% CO2条件下培养 24 h。将新化合物1用DMSO溶解并用培养基稀释至终体积为100 μL,分别加入96 孔板中,使其最终浓度分别为5、10、20、40、60、80、100、120 μg/L,继续孵育24 h后,去培养基,每孔再加入90 μL的 培养基和10 μL (5 mg/mL) MTT 溶液,于37 ℃条件下继续孵育 4 h,小心吸去孔内液体, 加DMSO 100 μL/孔, 室温振摇5 min,并用酶联免疫检测仪测定490 nm 处的OD值。根据细胞增殖抑制率公式(1)进行计算:抑制率=1-[OD(样品)-OD(空白)]/[(OD细胞对照-OD空白)]×100% (1); IC50值用统计软件 SPSS 17.0 进行计算。同样操作测试新化合物2,3和4的体外抗肿瘤活性。
2 结果
2.1 目标化合物1-4的结构表征 在目标化合物1-4的1H NMR谱中,席夫碱结构中的CH=N质子化学位移在8.9 ppm附近出现,而在化合物2和3中,该质子化学位移出现在7.61~9.55 ppm附近。这一特征质子化学位移均符合文献报道的化学位移范围[20-21]。同时,也由于蒽环和三苯基胺结构中大的刚性π电子体系存在的影响,芳环质子化学位移也分别向高场发生移动。其积分均与预期结构吻合,这说明得到的分子为预期结构。而在目标化合物1-4的13C NMR谱中,在107~153 ppm均出现了相应芳环碳信号的出现。化合物1-4的高分辨质谱测试值与计算值吻合较好,表明它们为预期的分子组成。在化合物1-4的红外光谱中,均在1617 cm-1附近观察到了席夫碱(C=N)的特征振动吸收峰[20-21],这说明了目标化合物中均有C=N官能团的存在。因而可以确定所合成得到的化合物为预期目标化合物。
2.2 化合物1的晶体结构 化合物1的单晶X射线衍射测试结果表明:其晶体结构属于斜方晶系,P21 空间群,其分子式为C21H14N4O4(Mr=386.36),晶胞参数为a=5.6509(11) Å,b=8.1598(15) Å,c=36.879(7) Å,α=β=γ=90.00°,V= 1700.5(6) Å3,Dc= 1.509 mg/m3,μ= 0.108 mm-1,Z= 4,F(000)=800.0,光源:Mo Kα 射线(λ=0.071073 nm),R1=1.05 ,wR2=0.1065[Igt;2σ(I)]。晶体结构数据存于英国剑桥数据中心,CCDC 为 1577767 (选择性键长、键角见表1)。其晶体结构见图2。

图2 目标化合物1的分子结构 (椭球几率为30%)
表1目标化合物1的选择性键长(Å)
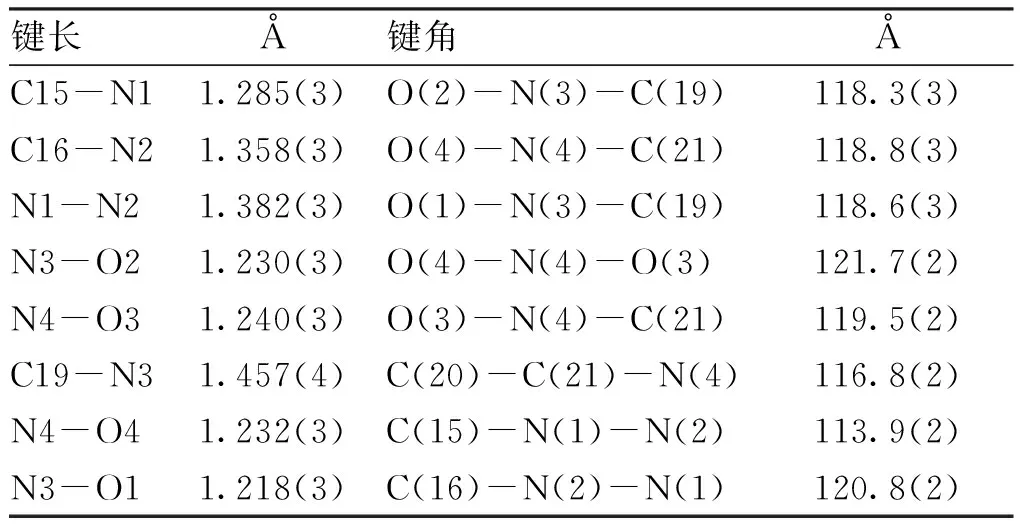
键长Å键角ÅC15-N11.285(3)O(2)-N(3)-C(19)118.3(3)C16-N21.358(3)O(4)-N(4)-C(21)118.8(3)N1-N21.382(3)O(1)-N(3)-C(19)118.6(3)N3-O21.230(3)O(4)-N(4)-O(3)121.7(2)N4-O31.240(3)O(3)-N(4)-C(21)119.5(2)C19-N31.457(4)C(20)-C(21)-N(4)116.8(2)N4-O41.232(3)C(15)-N(1)-N(2)113.9(2)N3-O11.218(3)C(16)-N(2)-N(1)120.8(2)
2.3 目标化合物1-4的初步抗肿瘤活性 采用MTT法初步考察了目标化合物1-4对 A549(人肺腺癌细胞)和 HepG2(人源肝癌细胞)的体外初步抗肿瘤活性,结果(见表2)。
表2化合物1-4的体外抗肿瘤活性

化合物IC50μmol/LA549HeGP2169.097.22gt;100gt;100381.981.8440.230.2
3 讨论
3.1 目标化合物1-4的合成及性质 目标化合物的合成用2,4-二硝基苯肼与芳香醛在冰醋酸作为催化剂的情况下,一步直接缩合即可得到,再以DMF重结晶即以较高产率获得目标化合物。目标化合物具有制备简便、产率高等优点。目标化合物微溶于甲醇、乙醇,而易溶于DMF和DMSO等有机溶剂中。
3.2 目标化合物1的晶体结构 由表1可见,化合物1的C15=N1的键长为1.285(3) Å,与文献报道的席夫碱结构的C=N键长能较好吻合[20-21]。其结构中的硝基N3-O1、N3-O2、N4-O3及N4-O4的键长分别为:1.218(3)、1.230(3)、1.240(3)和1.232(3) Å也与文献报道的硝基N-O键长相差不大[19],其余键长均在合理范围内。这进一步证实了合成得到的目标化合物为预期结构和组成。
3.3 目标化合物1-4的初步抗肿瘤活性 由表2中数据可看出,目标化合物1-3对所HeGP2细胞株均无显著性抗肿瘤活性,而化合物1和3对A549表现出一定抗肿瘤活性。值得注意的是,目标化合物4对受试的两株细胞均表现出中等抗肿瘤活性。由表2中数据还能得出总的活性顺序为4gt;1gt;3gt;2,这说明增加芳环的刚性有助于提高抗肿瘤活性,这为后续研究稠环芳烃为母核结构的先导化合物作为抗肿瘤药物筛选提供了实验基础和数据。
本文以冰醋酸作为催化剂,用2,4-二硝基苯肼与芳香醛一步成功合成得到了4个新的硝基苯类席夫碱衍生物,通过1H NMR、13C NMR、HRMS(ESI-MS)、FT-IR以及单晶X射线等方法表征结果表明获得了预期目标分子。体外抗肿瘤活性初步筛选表明增加芳环的刚性有助于提高抗肿瘤活性,为以稠环芳烃为母核结构的先导化合物的合成提供了一定的实验基础和数据。
[1] 杨大俊.聚焦抗肿瘤药物研究进展[J].药学进展,2016,40(1):1-2.
[2] Kaur R,Chaudhary S,Kumar K,et al.Recent synthetic and medicinal perspectives of dihydropyrimidinones:A review[J].Euro J Med Chem ,2017,132(26):108-134.
[3] Jeong K,Kang C S,Kim Y,et al.Development of highly efficient nanocarrier-mediated delivery approaches for cancer therapy[J].Cancer Letters ,2016,374(1):31-43.
[4] Hndskog M,Koguer P,Ponthan F,et al.Noninvasive estimation of tumor vialfility in a xenograft model of human neuroblastoma with proton magnetic resonance spectroscopy(1H MRs)[J].Br J Cancer,2003,88(3):478-485.
[5] 郭敏,刘宏,曹金发.肿瘤乏氧放射增敏剂的研究进展[J].中国药师,2015,18(5):856-858.
[6] Pellei M,Papini G,Trasatti A,et al.Nitroimidazole and glucosamine conjugated hetero- scorpionate ligands and related copper(II) complexes.Syntheses,biological activity and XAS studies[J].Dalton Trans,2011,40(38):9877-9888.
[7] Heffern M C,Yamamoto N,Holbrook R J,et al.Cobalt derivatives as promising therapeutic agents[J].Curr Opin Chem Biol,2013,17(2):189-196.
[8] Guo T,Cui L,Shen J,et al.A highly sensitive long-wavelength fluorescence probe for nitroreductase and hypoxia:selective detection and quantification[J].Chem Commun,2013,49(92):10820-10822.
[9] Williams E M,Little R F,Mowday A M,et al.Nitroreductase gene-directed enzyme prodrug therapy:insights and advances toward clinical utility[J].Biochem J,2015,471(2):131-153.
[10]Naylor M A,Jaffar M,Noian J,et al.2-cyclopropylindoloquinones and their analogues as bioreductively activated antitumor agents:Structure-activity in vitro and efficacy in vivo[J].J Med Chem,1997,40(15):2335-2346.
[11]Adams G E,Stratford I J.Hyproxia-mediated nitro-heterocyclic drugs of cancer an overview [J].Biochem Pharmacology,1986,35(1):71-76.
[12]Frederick F B,Bimal K B.Polycyclic aromatic compounds as anticancer agents:synthesis and biological evaluation of some chrysene derivatives [J].Bioorg Med Chem Let t,1998,8(20):2877-2880.
[13]郑虎.药物化学[M].第5版.北京:人民卫生出版社,2003.
[14]郑微,宋文婷,曹亚萍,等.新型含氮芥席夫碱化合物的合成及其抗肿瘤活性研究[J].遵义医学院学报,2016,39(6):547-551.
[15]曹亚萍,易芩兰,刘洪梅,等.氨基酸席夫碱氧钒(IV)配合物的合成、晶体结构及其抗肿瘤活性[J].遵义医学院学报,2016,39(2):122-128.
[16]Cao Y P,Yi C L,Liu H M,et al.Syntheses,Crystal Structures and in vitro anticancer activities of oxovanadium(IV) complexes of amino acid schiff base and 1,10-phenanthroline ligands [J].Trans Met Chem,2016,41(5):531-538.
[17]王辉,郑伟华,谢凤妮,等.香豆素席夫碱衍生物的合成及抗肿瘤活性研究[J].有机化学,2011,35(5):708-714.
[18]史真,王陆瑶.二茂铁磺酰基苯并咪唑衍生物的合成、表征及晶体结构[J].化学通报,2005,3:193-197.
[20]宋文婷,袁泽利,余光勤,等.三唑席夫碱钛(IV)配合物的合成及其与DNA相互作用[J].分子科学学报,2015,31(5):415-421.
[21]帅光平,袁泽利.新型磺胺化合物的合成、晶体结构及抗菌活性[J].遵义医学院学报,2017,40(4):389-393.
[收稿2017-07-14;修回2017-08-10]
(编辑:谭秀荣)
Synthesis,characterizationandinvitroanticanceractivitiesofnitrobenzeneSchiffbasederivatives
YiCenglan,XieXuqin,LiuXianzhi,WangYu,YuanZeli
(School of Pharmacy,Zunyi Medical University,Zunyi Guizhou 563099,China)
ObjectiveTo discover novel lead compounds for antitumor researches.MethodsFour Schiff base derivatives (1-4) were obtained by conventional synthesis of aromatic aldehyde and 2,4-Dinitrophenylhydrazine,and their structures were characterized by1H NMR,13C NMR,HR-MS and FT-IR spectrum.Compound1was further tested by single-crystal XRD techniques.Their anticancer activities were investigated against A-549 and HeGp2 cell lines by MTT assay.ResultsCompound4exhibited middle anticancer activities on the two human cancer cells.ConclusionFour Schiff base derivatives are synthesized,which serves as a good basis for further research of anticancer activities and practice.
Nitrobenzene; schiff base; synthesis; characterization; anticancer activity
国家自然科学基金资助项目(NO:81360471;NO:81660575);贵州省国际合作项目(NO:[2012]7036);贵州省大学生创新项目 (NO:201513653011);遵义医学院大学生创新项目 (NO:[2014]2906)。
袁泽利,男,博士,教授,硕士生导师,研究方向:药物设计合成及性能,E-mail:zlyuan2002@126.com。
O625.4
A
1000-2715(2017)05-0486-05
