刺五加膏遗传毒性和致畸作用实验研究
2017-11-16肖佳音王春雨李庆忠
肖佳音,王春雨,李庆忠
(黑龙江省食品药品检验检测所,黑龙江 哈尔滨 150088)
刺五加膏遗传毒性和致畸作用实验研究
肖佳音,王春雨,李庆忠*
(黑龙江省食品药品检验检测所,黑龙江 哈尔滨 150088)
目的:对刺五加膏进行遗传毒性及致畸作用评价,为其临床应用开发提供安全性试验依据。方法:采用小鼠睾丸染色体畸变试验、哺乳动物骨髓细胞染色体畸变试验、致畸试验来对刺五加膏进行评价。结果:当剂量为10.0、5.0、2.5 g/kg时,在小鼠睾丸染色体畸变试验中染色体结构畸变率分别为0.2%、0.4%、0%,早熟分离率分别为0%、0%、0.2%,互相异位率均为0%;哺乳动物骨髓细胞染色体畸变试验中染色体数目变化畸形率分别为0.3%、0.1%、0%,结构变化畸变率分别为0.8%、0.7%、0.7%。当剂量为7.5、3.75、1.875 g/kg时,致畸试验对孕鼠的体质量增长、孕鼠的胚胎毒性及对胎鼠生长发育、胎仔的内脏及骨骼均无明显异变。三项试验结果均与溶媒对照组接近,结果显示阴性。结论:在本实验条件和剂量下,刺五加膏未见遗传毒性作用及致畸作用。
刺五加膏;遗传毒性;致畸作用
刺五加[Acanthopanaxsenticosus(Rupr.et Maxin.)Hams]为多年生硬质灌木。具有补益肝肾,添精补髓,强壮筋骨之功效,用于缓解肝肾亏虚所致的暂时性脑缺血发作、脑动脉硬化及脑血栓形成,还可用于治疗冠心病、心绞痛兼有神经官能症及更年期综合征,对于应激导致的病理生理变化及炎症均有较好的疗效[1]。刺五加膏为刺五加经加工制成的浸膏,益气健脾,补肾安神,用于脾肾阳虚,体虚乏力,食欲不振,腰膝酸痛,失眠多梦。本实验通过对刺五加膏进行遗传毒性及致畸作用的研究,评价其遗传毒性,为其临床应用开发提供安全性试验依据。
1 材料和方法
1.1 样品
刺五加膏由黑龙江省食品药品检验检测所提供,为红褐色浸膏,规格为120 g/支,每次1.5 g,每日3次,阴凉干燥处保存。其人体推荐服用剂量为4.5 g/(60 kg·d)。本品为红褐色浸膏状物质,试验时以蒸馏水作为溶媒稀释后使用。
1.2 实验动物
清洁级KM种小鼠及Wistar大鼠由长春市亿斯实验动物技术有限责任公司提供,许可证号:SCXK(吉)2011-0004。饲料由长春市亿斯实验动物技术有限责任公司提供,许可证号:SCXK(吉)2010-0001。饲养环境为清洁级实验室,许可证号:SYXK(黑)2014004,温度(23±2)℃,湿度(55±10)%。
1.3 剂量选择与受试物给予方式
1.3.1 小鼠睾丸染色体畸变试验
采用经口灌胃方式给予受试物,设10.0、5.0、2.5 g/kg三个剂量组,另设溶媒对照组和环磷酰胺(40 mg/kg)阳性对照组,各组给药体积均为均为20 mL/kg。
1.3.2 哺乳动物骨髓细胞染色体畸变试验
采用经口灌胃方式给予受试物,设10.0、5.0、2.5 g/kg三个剂量组,另设溶媒对照组和环磷酰胺(40 mg/kg)阳性对照组,各组灌胃量均为20 mL/kg。
1.3.3 致畸试验
灌胃给予受试物,分别设7.5 g/(kg·d) (高剂量组,相当于人体推荐量100倍)、3.75 g/(kg·d)(中剂量组,相当于人体推荐量的50倍)、1.875 g/(kg·d)(低剂量组,相当于人体推荐量的25倍)剂量组,另设溶媒对照组和环磷酰胺20 mg/(kg·d)阳性对照组,各组给药体积均为10 mL/kg。
1.4 主要仪器与试剂
1.4.1 仪器
生物显微镜(Olympus公司,BX53);变焦体视显微镜(Olympus公司,SZX7);离心机(Sigma公司,2-6);电子天平(METTLER公司,AL204);电子天平(德国sartorius公司,BSA2201)。
1.4.2 试剂
环磷酰胺(Sigma公司,批号120M1253V);秋水仙素(aladdin Chemistry Co.Ltd,批号34723);Giemsa染液(Sigma公司,批号BCBF9150);氯化钠注射液(哈尔滨三联药业股份有限公司,批号110723A9)。
1.5 试验方法
1.5.1 小鼠睾丸染色体畸变试验[2]
取上述小鼠25只,按体质量随机分成5组,每组5只,分为受试样品高、中、低剂量组、溶媒对照组及阳性对照组。受试样品高、中、低剂量组分别灌胃给予刺五加膏10、5、2.5 g/kg,溶媒对照组灌胃给予等体积蒸馏水,灌胃体积20 mL/kg。阳性对照组腹腔注射环磷酰胺40 mg/kg,注射体积20 mL/kg。各组均每天给药1次,连续5天。第一次给药后14天腹腔注射秋水仙素6 mg/kg,注射体积10 mL/kg,注射后6 h每组取5只存活小鼠颈椎脱臼处死,取双侧睾丸分离曲细精管,低渗、固定、制片、Giemsa 染色。每只动物分析100个中期分裂相的初级精母细胞,观察项目包括染色体结构改变(断裂、裂隙、微小体)、相互易位、X-Y和常染色体的单价体(早熟分离)。
1.5.2 哺乳动物骨髓细胞染色体畸变试验[2-3]
取上述小鼠50只,雌雄各半,按性别、体质量随机分成5组,每组10只,分为受试样品高、中、低剂量组、溶媒对照组及阳性对照组。受试样品高、中、低剂量组分别灌胃给予刺五加膏10、5、2.5 g/kg,阳性对照组灌胃给予环磷酰胺40 mg/kg,溶媒对照组灌胃给予等体积蒸馏水,灌胃体积20 mL/kg。各组每天给药1次(间隔24 h),连续给药4次,末次给药后24 h小鼠颈椎脱臼处死。处死前4 h腹腔注射秋水仙素4 mg/kg。处死小鼠后取股骨以2.2%柠檬酸钠溶液反复冲洗骨髓,离心、制片、Giemsa 染色,每只动物分析100个中期相细胞。观察项目包括染色体数目改变、染色体结构改变。
1.5.3 致畸试验[4]
将性成熟雌、雄大鼠按2∶1同笼过夜,每日早晨观察阴栓,查出阴栓认为该鼠已交配,当日作为“受孕”0天。如果5天内未交配,应更换雄鼠。检出的“孕鼠”分为5组,每组12只,分别为溶媒对照组给予等体积蒸馏水,低剂量组1.875 g/kg,中剂量组3.75 g/kg,高剂量组7.5 g/kg和阳性对照组环磷酰胺20 mg/kg。阳性对照组于孕期第11天一次性腹腔注射环磷酰胺10 mL/kg,其余各组于受孕的第7~16天,灌胃给药,给药体积10 mL/kg,溶媒对照组给予同体积的蒸馏水,受孕的0、7、12、16、20天称体质量。于大鼠受孕第20天直接断头处死。剖腹取出子宫称重,记录并检查吸收胎、死胎及活胎数。记录胎仔的性别、体质量、身长、检查胎鼠外观有无异常。每窝取一半胎仔用Bouin液固定,徒手切片法检查内脏,另一半胎仔用茜素红染色,检查骨骼。
1.6 数据统计及结果判定
按卫生部《保健食品检验与评价技术规范》(2003年版)规定,计量资料采用t检验,计数资料采用χ2检验,对各试验数据结果进行统计分析并判定试验结果。
2 结果
2.1 刺五加膏小鼠睾丸染色体畸变试验
表1可见,与溶媒对照组比较,刺五加膏高、中、低剂量组小鼠睾丸染色体畸变率差别均无统计学意义;阳性对照组小鼠睾丸染色体畸变率差别有统计学意义。
2.2 哺乳动物骨髓细胞染色体畸变试验
表2可见,与溶媒对照组比较,刺五加膏高、中、低剂量组骨髓细胞染色体畸变率差别均无统计学意义;阳性对照组骨髓细胞染色体畸变率差别有统计学意义。

表1 小鼠睾丸染色体畸变试验结果

表2 最后一次给药后24 h小鼠骨髓细胞染色体畸变试验结果
2.3 致畸试验
由表3~6可知,刺五加膏各剂量组对孕鼠的体质量增长与溶媒对照组相比,差别无统计学意义(P>0.05)。对孕鼠的胚胎毒性及对胎鼠生长发育的影响,与溶媒对照组相比,差别亦无统计学意义(P>0.05)。胎仔的内脏及骨骼的检查结果表明,刺五加膏各剂量组对胎仔的内脏及骨骼均无明显异变,与溶媒对照组相比,差别无统计学意义。

表3 刺五加膏对孕鼠不同天数体质量增长的影响
注:与溶媒对照组比较,*P>0.05。

表4 刺五加膏对孕鼠体质量增重的影响
注:与溶媒对照组比较,*P>0.05。

表5 刺五加膏对孕鼠胚胎毒性的影响
注:与溶媒对照组比较,*P>0.05。
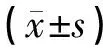
表6 刺五加膏对胎鼠生长发育的影响
注:与溶媒对照组比较,*P>0.05。
3 讨论
刺五加作为中药历史悠久,应用广泛,在历代本草均有记载,具有益气健脾、补益安神、益精壮骨之功效。《本草纲目》称刺五加为“本经上品”,能“补中益气,坚筋骨强意志,久服轻身耐老”。近年来研究表明,刺五加具有抗焦虑症的药理作用。刺五加膏以中医理论为指导,中药刺五加为原料,采用现代工艺加工而成,具有益气健脾,补肾安神之功,用于脾肾阳虚,体虚乏力,食欲不振,腰膝酸痛,失眠多梦。
本实验从小鼠睾丸染色体畸变试验、哺乳动物骨髓细胞染色体畸变试验、 致畸试验三项试验作为切入点,其目的是为安全性评价提供资料、降低使用风险。在三项试验中,刺五加膏高、中、低剂量组与溶媒对照组无差别,按照卫生部《保健食品检验与评价技术规范》(2003年版)进行评价,证实在本实验条件和剂量下,刺五加膏未见遗传毒性及致畸作用。
[1] 赵丹江.刺五加的药用价值[J].中医药信息,2011,28(5):115-117.
[2] 梁婕,张颖,俞萍,等.杨梅花青素的安全性评价研究[J].环境与健康杂志,2016,33(9):820-823.
[3] 齐彦,王瑶,郭丽新,等.桦菌芝多糖的抗突变作用研究[J].中医药信息,2011,28(1):21-23.
[4] 郭艳,兰真,曾凡骏,等.赶黄草的安全性毒理学评价研究[J].预防医学情报杂志,2016,32(5):476-481.
StudyonGeneticToxicityandTeratogenicityofAcanthopanaxSenticosus
XIAO Jia-yin, WANG Chun-yu, LI Qing-zhong*
(HeilongjiangInstituteforFoodandDrugControl,Harbin150088,China)
Objective:To study genetic toxicity and teratogenicity ofAcanthopanaxsenticosusand to provide safety testing basis for clinical application. Methods: This research adopted the mice testicle chromosome aberration test, bone marrow cell chromosome aberration test, and teratogenic test to evaluate genetic toxicity and teratogenicity of Acanthopanax senticosus ointment. Results: When the dose was 10.0, 5.0, 2.5 g/kg, the chromosome structure distortion rates were 0.2%, 0.4% and 0% respectively, premature separation rates were 0%, 0% and 0.2% respectively, ectopic rates were all 0%; Chromosome deformity were 0.3%, 0.1% and 0% respectively, in bone marrow cell chromosome aberration test, structural change aberration rates were 0.8%, 0.7% and 0.7% respectively. When the dose was 7.5, 3.75, 1.875 g/kg, teratogenic test showed that weight gain of pregnant rats, pregnant rat embryo toxicity, was the growth and development of fetal rats,and embryo of internal organs and bone were not aberrant.Conclusion: Under this experimental condition,Acanthopanaxsenticosusointment does not show genetic toxicity and teratogenicity.
Acanthopanaxsenticosusointment;Genetic toxicity;Teratogenication
R28
A
1002-2406(2017)06-0035-03
黑龙江省教育厅科学技术研究项目(No. 12541259)
肖佳音(1978-),女,博士,副主任药师,主要研究方向:药检药理,药品、保健食品及化妆品安全性评价。
李庆忠*(1962-),男,主任药师,主要研究方向:药品、食品,医疗器械、药包材安全性评价。
2017-03-21
修回日期:2017-04-10
