N′-(1, 3-二甲基亚丁基)-3-羟基-2-萘酰腙的合成与表征
2017-11-10徐启杰王康康刘景民
徐启杰,王康康,柳 准,喻 淼,张 宁,李 伟,刘景民
(1.黄淮学院 化学化工系,河南 驻马店 463000; 2.河南省华鼎高分子合成树脂有限公司,河南 驻马店 463000)
N′-(1,3-二甲基亚丁基)-3-羟基-2-萘酰腙的合成与表征
徐启杰1*,王康康1,柳 准1,喻 淼1,张 宁1,李 伟1,刘景民2
(1.黄淮学院 化学化工系,河南 驻马店 463000; 2.河南省华鼎高分子合成树脂有限公司,河南 驻马店 463000)
酰腙类化合物是一类新型的功能橡胶改性剂,具有非常大的应用潜力. 以3-羟基-2-萘甲酰肼与4-甲基-2-戊酮为原料,在酸性条件下,通过失水缩合反应合成N′-(1,3-二甲基亚丁基)-3-羟基-2-萘酰肼酰腙类化合物(简称BMH). 并通过红外光谱(FTIR)、紫外-可见吸收光谱(UV-vis)、高效液相色谱(HPLC)、核磁共振波谱仪(NMR)和质谱分析仪(MSA)等设备对所得产物的结构进行了表征,确定了该化合物的结构.
BMH;酰腙;合成;表征
酰腙类化合物由于含有O、N等多个配位原子,因此具有非常强的配位能力. 将酰腙类化合物引入聚合体系,作为一种橡胶合成添加剂,可有效地提高乳液、橡胶的抗氧化、抗老化能力以及机械性能等,进而提高乳液、橡胶的热稳定性、力学性能和使用寿命. 通过在日本专利局、欧洲专利局、美国专利局、中国专利局的查询,BMH合成专利共查到1篇(特开平11-292834),专利权人为大塚化学珠式会社,合成方法是利用萘甲酰肼衍生物[1]和酮类化合物为原料,用甲醇、甲苯、乙酸乙脂等为溶剂,对甲苯磺酸或乙酸为催化剂,利用油水分离装置分离出反应中生成的水,经过0.5~24 h的反应得到生成产物.
目前被报道的对苯二胺类和喹啉类[2]防老剂是重要的橡胶添加剂,而有关3-羟基-2-萘甲酰肼[3]的酰腙类化合物的合成方法尚未见报道. 基于此,本文作者拟在酸性条件下,通过3-羟基-2-萘甲酰肼[4]与4-甲基-2-戊酮的失水缩合反应合成N′-(1, 3-二甲基亚丁基)-3-羟基-2-萘酰腙[5]化合物. 并通过红外光谱、紫外-可见吸收光谱、高效液相色谱、核磁共振波谱仪和质谱分析仪等设备对产物的光谱学性能和结构进行表征.
1 实验部分
1.1 试剂及仪器
3-羟基-2-萘甲酸(AR,杭州鼎燕化工有限公司),4-甲基-2-戊酮(AR,梯希爱上海化成工业发展有限公司), 水合肼(AR,济南天将化工有限公司),乙醇(AR,山东青州鑫海科技开发有限公司),其他试剂均为市售分析纯. 实验用蒸馏水为自制.
Cary100 型紫外分光光度计(Cary 100型,澳大利亚),高效液相色谱仪(LC-100双泵型,济南赛畅科学仪器有限公司),质谱分析仪(HPA 220型,上海伯东企业有限公司),核磁共振波谱仪(AV400D型,瑞士布鲁克公司),傅立叶红外光谱仪(TENSOR27型,安合盟天津科技发展有限公司).
1.2 目标产物的合成
1.2.1 3-羟基-2萘甲酸甲酯的合成
将3-羟基-2萘甲酸与甲醇反应,以硫酸作为催化剂,在70 ℃的反应温度下,反应24 h后,得到黄色粉末状产物,即3-羟基-2萘甲酸甲酯[4],其合成方程式如图1所示.

图1 3-羟基-2-萘甲酸甲酯的合成Fig.1 Synthesis of 3-hydroxy-2 naphthyl methyl formate
1.2.2 3-羟基-2-萘甲酰肼的合成
将上述制备的3-羟基-2萘甲酸甲酯与水合肼以1∶1.2的比例加入三口烧瓶中,在70 ℃的反应条件下,反应3 h,得到3-羟基-2-萘甲酰肼[5],其合成方程式如图2所示.

图2 3-羟基-2-萘甲酰肼的合成Fig.2 Synthesis of 3-hydroxy-2-naphthalene formyl hydrazine
1.2.3 BMH的合成
将3-羟基-2-萘甲酰肼与4-甲基-2-戊酮以1∶1.2的比例加入三口烧瓶中,以醋酸作为催化剂,在85 ℃的条件下合成目标产物3-羟基-2-萘甲酰腙(BMH)[6],BMH的合成方程式如图3所示. 将所得产品经过无水乙醇重结晶后,颜色接近于白色,纯度达到了99.4%以上.
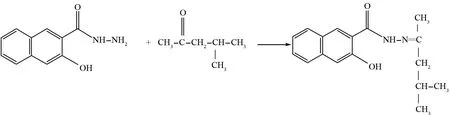
图3 BMH的合成Fig.3 Synthesis of BMH
2 结果与讨论
2.1 产品技术指标
将所得产品进行初步测试,达到了相关橡胶添加剂的基本要求,纯度超过98%,达到99.4%;熔点与其接近,为145 ℃,所得相关数据如表1所示.

表1 BMH的相关技术指标Table 1 Technical parameters of BMH
2.2 BMH检测报告
表2为所得产品BMH的详细测试报告,通过对所得产品的技术指标和相应的物理、化学性能测试,并结合相应的谱图分析,证实成功合成了目标产品BMH,其纯度达到99%以上.

表2 BMH的测试报告Table 2 Testing report of BMH
2.3 高效液相检测图谱分析
将所得产品BMH在乙醇中多次结晶纯化后,以甲醇和水为流动相,测得产品BMH的高效液相色谱图如图4所示.
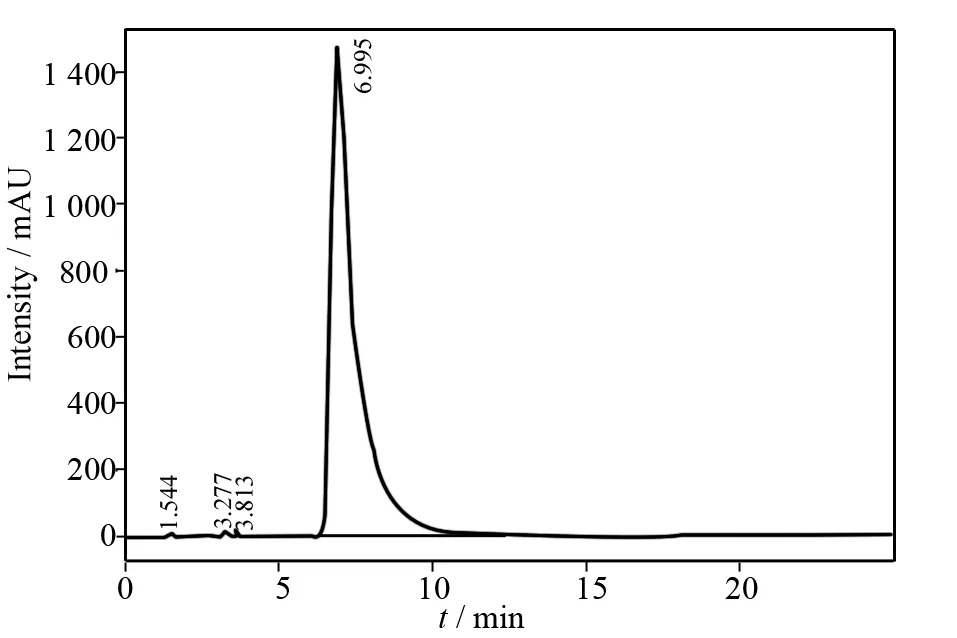
图4 BMH的高效液相色谱图Fig.4 High performance liquid chromatogram of BMH
由图4可知,在保留时间为1.544至3.813 min的范围内出现少许杂峰,且峰面积、峰宽、峰高较小,几乎可以忽略,分析其产生原因可能是仪器测定前淋洗不充分;在保留时间为6.995 min附近出现主峰,且峰面积较大,约为99.433 9%,干扰因素存在较少,这说明实验得到的目标产物BMH的纯度较高,杂质较少.
2.4 MSA检测谱图分析
图5为纯化后的产品BMH的质谱图. 由图可知,在质核比为170.9处裂分的碎片为3-羟基-2萘甲酮正离子;质核比为143.0处裂分的碎片为3-羟基萘正离子;质核比为187.0处裂分的碎片为3-羟基-2萘甲酰胺;质核比为113.7处裂分的碎片为N′-(1,3-二甲基亚丁基);质核比为141.9处裂分的碎片为上述碎片(即核质比113.7处)端位氮原子上多一个羰基基团;质核比为98.0处裂分的碎片为1,3-二甲基丁胺;质核比为242.1处裂分的碎片为N′-异丙基-3-羟基-2-萘酰肼;质核比为227.1处裂分的碎片为 N′-乙基-3-羟基-2-萘酰肼. 综合以上信息,分析该质谱图所显示的化合物可能为目标产物BMH的结构.

图5 BMH的质谱图Fig.5 MS detection spectrum of BMH
2.5 H-NMR检测谱图分析
由H-NMR(DMSO)谱图显示可知(官能团以萘环上碳原子编号来说明):0.90(m,6H)即为取代基1,3-二甲基亚丁基上三位碳原子上的两个甲基、1.93(s,3H)为取代基1,3-二甲基亚丁基上一位碳原子上的甲基、2.00(m,1H)为取代基1,3-二甲基亚丁基上三位碳原子上的单独氢原子、2.17(m,2H)为取代基1,3-二甲基亚丁基上的-CH2-基团、7.38(m,2H)为萘环上6位和7位碳原子上的氢、7.46(m,1H)为萘环上5位碳原子上的氢、7.75(m,1H)为萘环上8位碳原子上的氢、7.95(m,1H)为萘环上4位碳原子上的氢、8.58(m,1H)为萘环上1位碳原子上的氢、11.15(b,1H)为-OH、11.65(b,1H)为-NH-. 综合以上分析,该H-NMR谱图所显示的化合物为目标产物BMH的结构[7].
3 结论
综合高效液相色谱分析、MS检测图谱分析、H-NMR检测谱图分析等,对合成的目标产物BMH进行了光谱结构和相关性能的表征. 利用3-羟基-2-萘甲酰肼与4-甲基-2-戊酮为原料通过失水缩合过程合成的N′-(1,3-二甲基亚丁基)-3-羟基-2-萘酰肼化合物在外观形态上呈现出浅黄色,技术指标符合要求,且纯度高达99.4%以上,有望用做橡胶助剂.
[1] 麻宝成, 马兴铭, 闫兰, 等. 2-羧甲氧基苯甲醛苯甲酰腙及其稀土配合物的合成、表征和抑菌活性[J]. 应用化学, 2004, 21(8): 841-842.
MA B C, MA X M, YAN L, et al. Synthesis, and bacteriostatic activity of 2-(carboxymethoxyl) benzaldehyde benzoyl hydrazone and its rare earth complexes [J]. Chinese Journal of Applied Chemistry, 2004, 21(8): 841-842.
[2] DAIMAY L V, NORMAN C, WILLIAN F, et al. The handbook of infrared and Raman characteristic frequtencies of organic molecules [M]. New York: Academic Press, 1991: 199-239.
[3] 杨正银, 杨汝栋. 邻羧基苯甲醛苯甲酰腙稀土配合物的合成和抗氧化活性[J]. 中国稀土学报, 2002, 20(4): 366-369.
YANG Z Y, YANG R D. Synthesis of 2-carboxybenzaldehyde benzoyl hydrazone rare earth complexes and their antioxidative activity [J]. Journal of the Chinese Rare Eearth Society, 2002, 20(4): 366-369.
[4] ALEXIOU M, TSIVIKAS I, DENDRINOU-SAMARA C, et al. High nuclearity nickel compounds with three, four or five metal atoms showing antibacterial activity [J]. Journal of Inorganic Biochemistry, 2003, 93(4): 256-264.
[5] BOVIO B, BONATI F, BANDITELLI G. X-ray crystal structure of tris [mu]-3, 5-bis (trifluoromethyl) pyrazolato-N, N′] trigold (I), a compound containing an inorganic nine membered ring [J]. Inorganica Chimica Acta, 1984, 87(1): 25-33.
[6] DENDRINOU-SAMARA C, PAPADOPOULOS A N, MALAMATARI D A, et al, Inter conversion of 15-MC-5 to 12-MC-4 manganese metallacrowns: structure and bioactivity of metallacrowns hosting carboxylato complexes [J]. Journal of Inorganic Biochemistry, 2005, 99(3): 864-875.
[7] FAN N T. Dictionary of organic synthesis [M]. Beijing: Beijing Institute of Technology Press, 1988: 614.
SynthesisandcharacterizationofN′-(1,3-dimethylbutylidene)-3-hydroxy-2-naphthylacylhydrazone
XU Qijie, WANG Kangkang1, LIU Zhun1, YU Miao1, ZHANG Ning1, LI Wei1, LIU Jingmin2
(1.DepartmentofChemistryandChemicalEngineering,HuanghuaiUniversity,Zhumadian463000,Henan,China; 2.HuaDinglimitedCompanyforPolymerSyntheticResinofHenanProvince,Zhumadian463000,Henan,China)
Acylhydrazone compounds as novel rubber additive have great potential application. A compound N′-(1,3-dimethylbutylidene)-3-hydroxy-2-naphthly acylhydrazone (noted as BMH) was synthesized via condensation reaction between 3-hydroxy-2-naphthoic hydrazide and 4-methyl-2-pentanone. The obtained BMH was characterized by infrared spectrometer (FTIR), UV-vis spectrometer (UV-vis), high performance liquid chromatography (HPLC), nuclear magnetic resonance spectrometer (NMR), and mass spectrum analyzer (MSA), to confirm its structure.
BMH; acyl hydrazone; synthesis; characterization
O622.4
A
1008-1011(2017)05-0580-04
2016-06-12.
2016年度河南省高等学校重点科研项目资助计划(16A150054), 驻马店市科技攻关项目(15025), 黄淮学院校级科研项目(201512713, 201512701).
徐启杰(1981-),男,副教授,主要研究方向为聚合物基复合材料的制备及性能.*
,E-mail:qijie001@163.com.
[责任编辑:刘红玲]
