L-赖氨酸-D-阿拉伯糖美拉德反应产物抗氧化活性研究
2017-11-10章银良蔡亚玲
章银良 ,蔡亚玲 ,李 鑫
(1.郑州轻工业学院 食品与生物工程学院,河南 郑州 450002;
2.食品生产与安全河南省协同创新中心,河南 郑州 450001)
L-赖氨酸-D-阿拉伯糖美拉德反应产物抗氧化活性研究
章银良1,2,蔡亚玲1,2,李 鑫1
(1.郑州轻工业学院 食品与生物工程学院,河南 郑州 450002;
2.食品生产与安全河南省协同创新中心,河南 郑州 450001)
以DPPH自由基清除率和还原力作为美拉德反应产物(MRPs)抗氧化活性指标分析模拟体系L-赖氨酸-D-阿拉伯糖MRPs的抗氧化活性。考察了不同影响因素(反应温度、反应时间、反应初始pH和反应底物物质的量之比)对MRPs抗氧化活性的影响,再通过均匀试验得到最佳工艺条件。通过单因素和均匀试验分析,确定了该模拟体系在温度110℃、反应时间68 min、反应初始pH为8、反应底物物质的量之比为1∶2的条件下,MRPs对DPPH自由基的清除率由原来的80.69%提高到89.81%,其抗氧化活性增强。
L-赖氨酸;D-阿拉伯糖;MRPs;抗氧化活性
0 引言
随着健康饮食观念的不断普及,人们对食品的质量与安全问题也越发重视。而食品在加工和贮藏过程中,会不断地和空气中的氧气发生氧化反应,从而导致食品中的油脂酸败、褐变及营养物质损失,甚至会产生影响人体健康的物质,食品的营养价值不仅会因此降低,而且其安全性也会受到影响。为了防止食品在加工过程中的氧化腐败,延长食品的贮藏期,在食品中添加具有抗氧化活性的天然物质已成为科研工作者的主要研究方向。
美拉德反应(Maillard reaction,MR)是一种非常普遍的非酶褐变反应,游离的氨基和羰基是MR过程的主要参与者。MR会产生大量的紫外吸收中间体、具有特殊风味的物质和高分子褐变聚合物类黑精[1-4]等,把这些物质归类为美拉德反应产物(Maillard reaction products,MRPs)。 无论是在食品的颜色和风味,还是在食品在贮藏过程中的稳定性和货架期等方面[5],这些产物均发挥着重要的作用。大量研究表明,MR的程度和温度、时间、系统中的组分、水分活度以及pH有关[6]。由此可见,MRPs不仅对食品的颜色、风味、货架期和稳定性等发挥着非常关键的作用,而且具有多种多样的生物活性,如抗氧化、抗增殖、抗病毒、抗诱变和降血压等。目前对MRPs抗氧化活性的研究已经成为热点,其常用于食品加工、生产与储藏过程当中。
还原糖是MR的主要底物之一,五碳糖褐变速度是六碳糖的10倍[7]。刘海燕等[8]以阿拉伯糖与赖氨酸或甘氨酸为原料,制备了一系列不同反应条件下的MRPs,以硫氰酸铁法为抗氧化测定指标和合成抗氧化剂TBHQ相对比。结果发现,阿拉伯糖-赖氨酸体系MRPs的抗氧化活性高于阿拉伯糖-甘氨酸体系,且在一定的浓度条件下,模拟体系所制备出的MRPs的抗氧化能力比TBHQ好。而在羰基化合物中,碱性的氨基酸要比中性和酸性的氨基酸和蛋白质反应要快。Jayathilakan K等[9]研究了葡萄糖与5种不同的氨基酸(甘氨酸、蛋氨酸、色氨酸、天冬氨酸和赖氨酸)的模拟体系,在5种组合中发现葡萄糖和赖氨酸或甘氨酸的组合具有良好的抗氧化活性。而在目前的研究中,对赖氨酸和阿拉伯糖模拟体系的研究相对较少。由此,本研究通过L-赖氨酸-D-阿拉伯糖在恒温油浴槽内进行MR,以DPPH自由基清除率和还原力作为测定指标考察其抗氧化活性,后采用均匀试验进行优化试验,从而得到最佳的L-赖氨酸和D-阿拉伯糖模拟MR条件,以便为日后开发天然的抗氧化剂及更深入地研究L-赖氨酸和D-阿拉伯糖MRPs的其他功能特性提供基础研究和参考。
1 材料与方法
1.1 材料
L-赖氨酸、D-阿拉伯糖:Solarbio试剂公司;生化试剂;无水乙醇、磷酸二氢钠、磷酸氢二钠、铁氰化钾、三氯乙酸、三氯化铁和DPPH(1,1-二苯基-2-苦肼基自由基)等均为分析纯;去离子水。
1.2 主要设备
SQP电子天平:赛多利斯科学仪器(北京)有限公司;HJ-3恒温磁力加热搅拌器:常州国华电器有限公司;pH计:瑞士梅特勒-托利多公司;HH-1智能型数显恒温油浴槽:巩义市予华仪器有限责任公司;T6新世纪紫外可见分光光度计:北京普析通用仪器有限责任公司;HH-S型水浴锅:巩义市英峪予华仪器厂;TG16-WS台式高速离心机:湖南湘仪实验室仪器开发有限公司。
1.3 试验方法
1.3.1 单因素试验制备美拉德反应产物[10-11]
参考大量的研究结果,综合考虑各个因素对MR过程的影响,以温度、时间、pH和底物物质的量之比4个主要因素对L-赖氨酸和D-阿拉伯糖进行研究。制备MRPs的具体操作过程如下所示:
(1)反应温度对MRPs抗氧化活性的影响:准确称取L-赖氨酸1.480 5 g和D-阿拉伯糖1.519 5 g(物质的量之比为1∶1),溶解于90 mL去离子水中,分别用6 mol/L的NaOH溶液和4 mol/L的HCl溶液调整pH为9,并用调好的pH值为9的去离子水定容至100 mL,充分混匀后取10 mL溶液转移至25 mL具塞试管中,密封好后,分别将配制好的反应液置于 45、60、75、90、105、120、135 ℃的恒温油浴槽内反应30 min。反应结束后将制备好的样品放置在流动水中冲凉后进行相关测定,并将剩余样品冷冻在冰箱中保存备用。
(2)反应时间对MRPs抗氧化活性的影响:准确称取L-赖氨酸1.480 5 g和D-阿拉伯糖1.519 5 g(物质的量之比为1∶1),溶解于90 mL去离子水中,分别用6 mol/L的NaOH溶液和4 mol/L的HCl溶液调整反应物的pH值为9,并用调好的pH值为9的去离子水定容至100 mL,充分混匀后取10 mL溶液转移至25 mL具塞试管中,密封好后,在 105 ℃恒温油浴槽内分别反应 20、30、60、90、120、150、180、210、240、270 min。 反应结束后将制备好的样品放置在流动水中冲凉后进行相关测定,并将剩余样品冷冻在冰箱中保存备用。
(3)初始pH对MRPs抗氧化活性的影响:准确称取L-赖氨酸0.296 1 g和D-阿拉伯糖0.303 9 g(物质的量之比为 1∶1),溶解于 20 mL去离子水中,分别用6 mol/L的NaOH溶液和4 mol/L的HCl溶液调整 pH 为 4、5、6、7、8、9、10、11、12、13,并用调好相对应pH值的去离子水定容至20 mL,充分混匀。然后依次将配好后的各pH值溶液分别量取10 mL移至25 mL具塞试管中,密封好后,一起固定在105℃恒温油浴槽内反应30 min。反应结束后将制备好的样品放置在流动水中冲凉后进行相关测定,并将剩余样品冷冻在冰箱中保存备用。
(4)L-赖氨酸与D-阿拉伯糖物质的量之比对MRPs抗氧化活性的影响:准确称取一定量的L-赖氨酸和D-阿拉伯糖,使它们的物质的量之比分别为 1∶1、1.5∶1、2∶1、2.5∶1、3∶1、1∶3、1∶2.5、1∶2、1∶1.5,先溶解在15 mL的去离子水中,用6 mol/L的NaOH溶液和4 mol/L的HCl溶液调整pH为9,再用调好的pH为9的去离子水定容至20 mL,充分混匀后量取10 mL反应溶液转移至25 mL具塞试管中,密封好后,一起固定在105℃恒温油浴槽内反应30 min。反应结束后将制备好的样品放置在流动水中冲凉后进行相关测定,并将剩余样品冷冻在冰箱中保存备用。
1.3.2 DPPH自由基清除率的测定
参考Mohsen等[12]的方法,并稍作修改来研究MRPs对DPPH自由基清除率的影响。取1 mL经10倍稀释后的样品溶液和配好的2 mL DPPH无水乙醇溶液(0.1 mmol/L,每次都现用现配),充分混匀后在室温黑暗条件下反应30 min。最后在517 nm处测定该吸光度值,记为A样品。同操作、同条件下,以1 mL去离子水代替稀释后的样品溶液,作为空白组,记为A空白;以无水乙醇代替DPPH溶液作为对照组,记为A对照。MRPs对DPPH自由基清除率用下式计算:
DPPH 清除率 (%)=[1-(A样品-A对照)/A空白]×100。
1.3.3 MRPs还原能力的测定
MRPs还原力的测定采用铁氰化钾还原法进行评价,参考章银良等[13]的测定方法。首先取1 mL不同反应条件下的MRPs经10倍稀释、加入pH 6.6的磷酸盐缓冲液2.5 mL和2.5 mL 1%的铁氰化钾溶液,以上反应液在10 mL离心管中经充分混匀后放在恒温水浴锅中(50℃)反应20 min,迅速冷却后加2.5 mL的TCA溶液(10%),然后在3 000 r/min的条件下离心10 min。完成后,取上清液2.5 mL,并加2.5 mL去离子水和1 mL三氯化铁溶液(0.1%),充分混匀后在700 nm波长下测定其吸光度值。一般情况下,还原力的大小和抗氧化能力呈正相关关系。即吸光度值越大,MRPs还原能力越强,表明其抗氧化能力也越强。
2 结果与分析
2.1 单因素试验结果
2.1.1 加热温度对MRPs抗氧化活性的影响
加热温度对MRPs抗氧化活性的影响如图1所示。由图1可知,随着加热温度的升高,无论是MRPs的还原能力还是对DPPH自由基的清除率都呈现出逐渐增大的趋势。当加热温度低于90℃时,MRPs的抗氧化能力非常弱,DPPH自由基清除率低于24.91%,当加热温度为105℃时,DPPH自由基的清除率则上升至61.21%,并且随着加热温度的不断升高清除率持续增大,这说明MRPs中具有抗氧化活性的物质在高温条件下更利于生成。

图1 反应温度对MRPs抗氧化性的影响Fig.1 Changes in antioxidant activity of MRPs at different temperatures
2.1.2 反应时间对MRPs抗氧化活性的影响
不同反应时间对MRPs抗氧化活性的影响见图2。
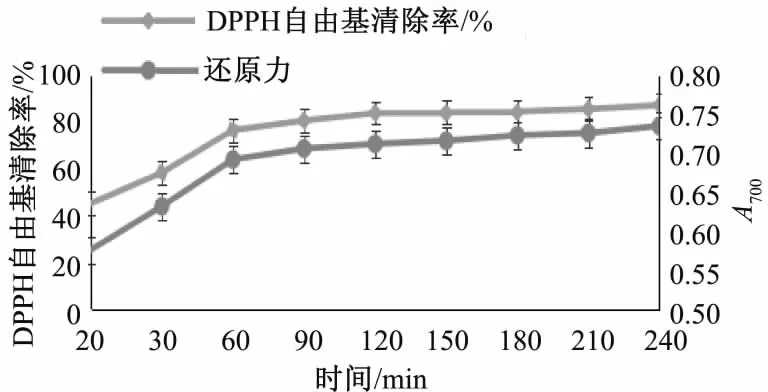
图2 反应时间对MRPs抗氧化活性的影响Fig.1 Changes in antioxidant activity of MRPs heated for different durations
由图2可知,随着时间的延长,MRPs的抗氧化活性整体呈现先增加后变缓的趋势。在反应前60 min内,无论是DPPH自由基清除率还是MRPs的还原力都与反应时间呈正比,其中DPPH自由基的清除率由45.20%增至76.51%,之后MRPs抗氧化活性增加趋势变缓。这说明MRPs中具有抗氧化活性的物质形成于反应初期,并在反应体系中保持相对稳定的状态。
2.1.3 反应初始pH对MRPs抗氧化活性的影响
反应初始pH值对MRPs抗氧化活性的影响见图3。由图3可知,一定的初始pH条件有利于L-赖氨酸和D-阿拉伯糖MR抗氧化活性物质的生成,相对于其他范围内的pH值,在8~10的范围内MRPs具有相对较强的抗氧化活性,DPPH自由基的清除率在pH=8时达到最大,为60.50%,还原力在pH=10时达到最大,其吸光度值为0.788。MRPs的DPPH自由基清除率和还原力分别在初始pH值为8和10时测定为最强,这表明了还原力的变化趋势和DPPH自由基清除率在表征抗氧化能力大小上具有一定的差异,即其在测定抗氧化性的机理上是不同的。
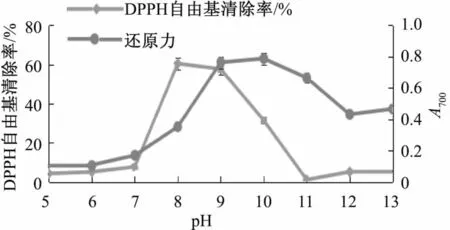
图3 不同反应初始pH对MRPs抗氧化性的影响Fig.3 Changes in antioxidant activity of MRPs wnder different reaction initial pH values
2.1.4 底物物质的量之比对MRPs抗氧化活性的影响
底物物质的量之比对MRPs抗氧化活性的影响见图4。
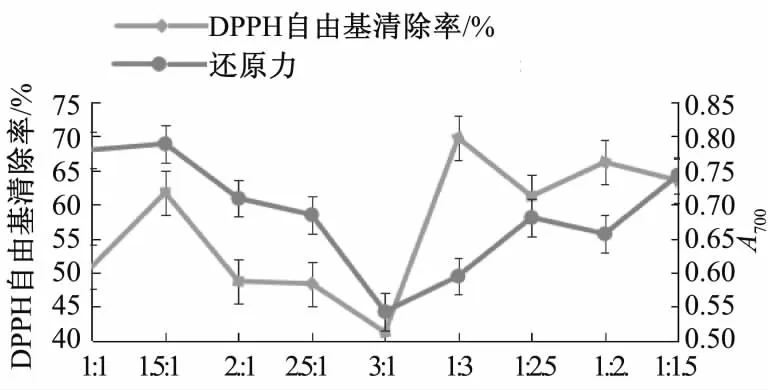
图4 反应底物物质的量之比对MRPs抗氧化性的影响Fig.4 Changes in antioxidant activity of MRPs under different molar ratio
从图4可以看出,底物的物质的量之比(L-赖氨酸∶D-阿拉伯糖)对MRPs的抗氧化活性的影响没有一定的规律可循,但总体上D-阿拉伯糖含量即羰基含量的增加,更有利于产物抗氧化能力的增强。通过对数据的分析,可以看到底物物质的量之比对试验的影响较小,DPPH自由基的清除率从3∶1时的41.28%增加到1∶3时的 69.75%,还原力的大小从3∶1时的0.543增加到1.5∶1时的 0.789。
2.2 均匀试验
2.2.1 均匀试验因素水平设计
根据单因素试验结果,选取合适的反应温度、时间、反应液初始pH值和底物物质的量之比4个因素进行均匀试验,以DPPH自由基清除率作为检测指标来优化L-赖氨酸和D-阿拉伯糖的MRPs,对均匀试验的设计表采用U7(74),对各个因素水平的设计见表1。
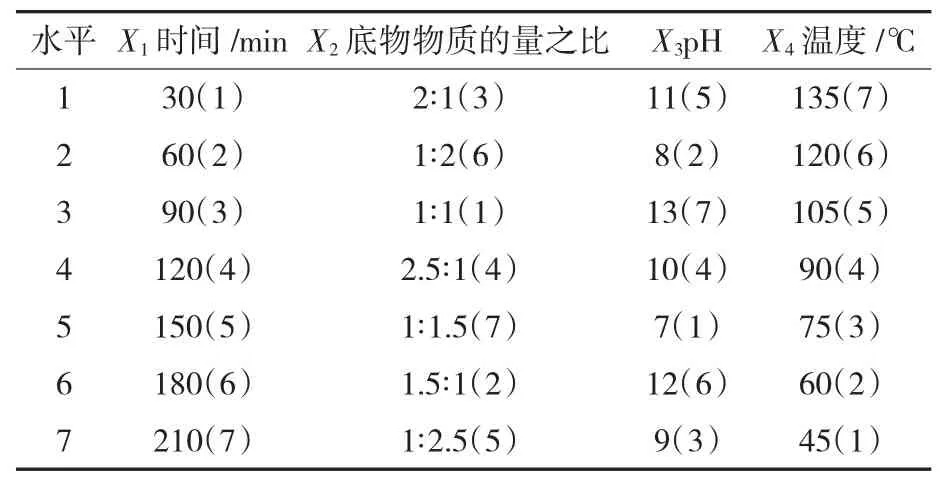
表1 U7(74)均匀试验因素与水平Table 1 Levels and factors of U7(74)uniform experiment
2.2.2 均匀试验结果
根据表1在相应的条件下分别进行反应得到相应的MRPs,并依照1.3.2的方法对每组试验所得的MRPs进行DPPH自由基清除率的测定,结果如表2所示。
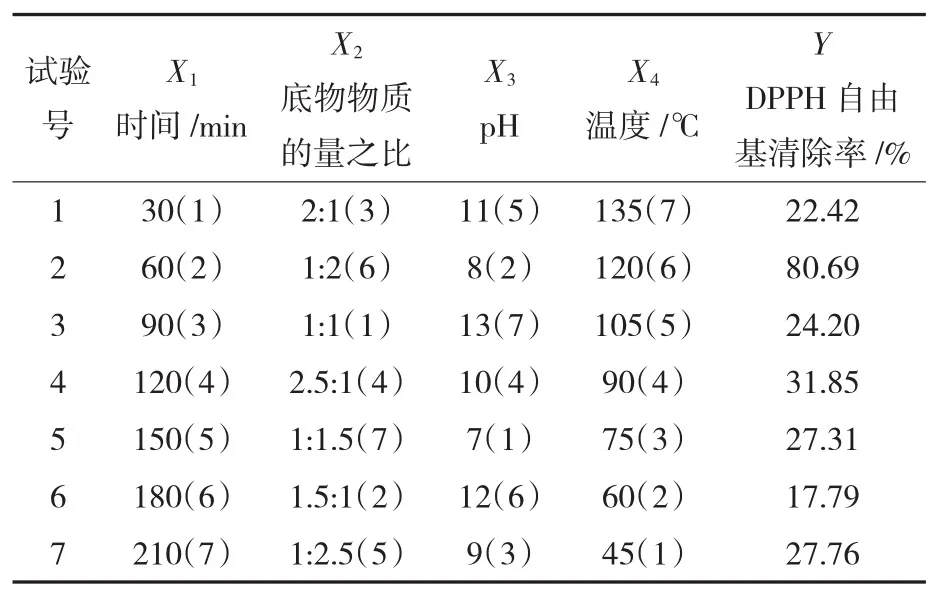
表2 均匀试验结果Table 2 Results of uniform experiment
2.2.3 软件分析
对均匀试验得出的结果采用Mathematics 4.0软件进行分析,结果如表3、表4所示。
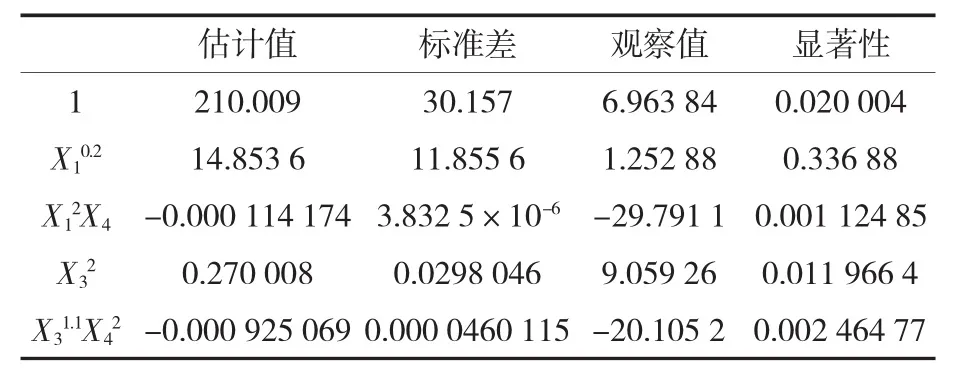
表3 回归参数Table 3 Regression parameters
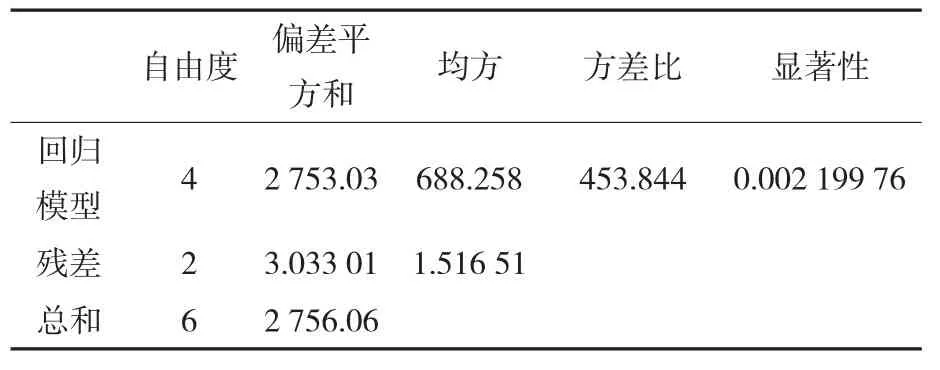
表4 回归方差分析Table 4 Regression variance analysis
由Mathematics 4.0软件分析表明,反应初始pH对MRPs抗氧化活性具有显著影响,加热时间与反应温度、初始pH与反应温度之间均具有极显著交互作用。影响MRPs抗氧化活性的主次因素顺序为:pH(X3)>温度(X4)>时间(X1)>底物物质的量之比(X2)。回归方程:Y(自由基清除率)=210.0+14.85X10.2-0.000 114 2X12X4+0.270 0X32-0.000 9251 X31.1X42。在测试条件范围内,从回归方程可得到最佳条件为:温度110℃、反应时间68 min、反应初始pH 8、L-赖氨酸与D-阿拉伯糖物质的量之比为1∶2,此时从理论上计算出MRPs对DPPH自由基的清除率为93.51%,抗氧化活性最强。经实际试验验证,在此优化条件下得到的MRPs对DPPH自由基的清除率为89.81%,与理论值的相对误差为3.70个百分点。说明均匀试验优化后的最优条件组合制备的MRPs具有强的抗氧化活性,优化结果可靠。
3 结论
本试验以L-赖氨酸与D-阿拉伯糖为底物,通过普通油浴加热制备不同反应条件的MRPs,以DPPH自由基清除率为检测指标来表征MRPs的抗氧化活性。结果表明:反应初始pH对MRPs抗氧化活性具有显著影响,加热时间与反应温度、初始pH与反应温度之间均具有极显著交互作用。优化反应条件为温度110℃、反应时间68 min、反应初始pH 8、L-赖氨酸与D-阿拉伯糖物质的量之比为1∶2,经过均匀试验优化后所制备出的MRPs其抗氧化能力得到显著提高,对DPPH自由基的清除率为89.81%,其抗氧化能力比各试验组都强。
[1]JING H,KITTS D D.Antioxidant activity of sugar-lysine Maillard reaction products in cell free and cell culture systems[J].Archives of Biochemistry&Biophysics,2004,429(2):154-163.
[2]LAROQUE D,INISAN C,BERGER C,et al.Kinetic study on the Maillard reaction.Consideration ofsugarreactivity [J].Food Chemistry,2008,111(4):1032-1042.
[3]MORALES F J,JIMÉNEZ-PÉREZ S.Free radical scavenging capacity of Maillard reaction products as related to colour and fluorescence[J].Food Chemistry,2001,72(1):119-125.
[4]WIJEWICKREME A N,KITTS D D.Influence of reaction conditions on the oxidative behavior of model Maillard reaction products[J].Journal of Agricultural and Food Chemistry,1997,45(12):4571-4576.
[5]YILMAZ Y,TOLEDO R.Antioxidant activity of water-soluble Maillard reaction products[J].Food Chemistry,2005,93(2):273-278.
[6]章银良,周文权.均匀试验优化酪蛋白-木糖美拉德反应产物的抗氧化活性[J].食品工业,2013(1):27-30.
[7]章银良,卢慢慢,张陆燕.不同条件下美拉德反应产物抗氧化活性的研究综述[J].中国调味品,2015(11):120-127.
[8]刘海燕,李卫宁,刘伟华.阿拉伯糖与赖氨酸或甘氨酸的模式Maillard反应产物抗氧化性研 究 [J]. 安 徽 农 业 科 学 ,2011,39(10):6077-6079.
[9]JAYATHILAKAN K,SHARMA G K.Role of sugar amino acid interaction products(MRPs)as antioxidants in a methyl linoleate model system[J].Food Chemistry,2006,95(4):620-626.
[10] 章银良,卢慢慢,张陆燕,等.均匀试验优化鲢鱼蛋白-D-木糖美拉德反应产物的抗氧化活性[J].河南工业大学学报(自然科学版),2015,36(2):28-31.
[11] 章银良,张陆燕.4种氨基酸与木糖美拉德反应产物的抗氧化活性研究[J]中国调味品,2014,39(10):65-69.
[12] MOHSEN S M,AMMAR A S M.Total phenolic contents and antioxidant activity of corn tassel extracts[J].Food Chemistry,2009,112(3):595-598.
[13] 章银良,周文权,左婷婷.酪蛋白-木糖体系美拉德反应产物的抗氧化活性[J].食品科技,2012(7):65-70.
STUDY ON ANTIOXIDANT ACTIVITY OF MAILLARD REACTION PRODUCTS DERIVED FROML-LYSINE ANDD-ARABINOSE
ZHANG Yinliang1,2,CAI Yalin1,2,LI Xin1
(1.School of Food and Bioengineering,Zhengzhou University of Light Industry,Zhengzhou450002,China;2.Collaborative Innovation Center for Food Production and Safety in Henan Province,Zhengzhou450001,China)
The purpose of this paper was to study the antioxidant activity of Maillard reaction products(MRPs)derived fromL-lysine andD-arabinose. In this experiment,DPPH radical scavenging rate and reducing power were used as the antioxidant activity index of MRPs. First,we studied the influences of different factors (reaction temperature,reaction time,initial pH and substrate molar ratio) on the antioxidant activity of MRPs,then detemrined the optimum conditions through uniform experiments. Results showed that the optimum conditions were as follows: temperature 110 ℃ ,reaction time 68 min,initial pH 8,substrate molar ratio (L-lysine:DArabinose) 1: 2. Under the optimum conditions,DPPH radical scavenging rate of MRPs was improved from 80.69% to 89.81%,therefore,the antioxidant activity was enhanced.
L-lysine;D-arabinose;maillard reaction products;antioxidant activity
TS 201.2 文献标志码:B
1673-2383(2017)05-0063-05
http://kns.cnki.net/kcms/detail/41.1378.N.20171030.0936.024.html
网络出版时间:2017-10-30 9:36:38
2017-02-12
食品生产与安全河南省协同创新中心研究生创新基金(FCICY201610)
章银良(1963—),男,浙江上虞人,教授,博士,主要研究方向为食品科学与质量安全。
