快速溶剂提取-高效液相色谱法测定PM2.5中16种多环芳烃
2017-11-06袁小雪杨长晓谢碧俊
袁小雪 江 阳 杨长晓 谢碧俊 雍 莉 胡 彬 刘 滔
(四川省疾病预防控制中心理化检验所, 成都 610041)
快速溶剂提取-高效液相色谱法测定PM2.5中16种多环芳烃
袁小雪 江 阳 杨长晓 谢碧俊 雍 莉 胡 彬 刘 滔*
(四川省疾病预防控制中心理化检验所, 成都 610041)
建立大气细颗粒物(PM2.5)中16种多环芳烃(PAHs)的快速溶剂提取-直接进样-高效液相色谱测定方法。PM2.5经玻璃纤维滤膜收集,采样后的滤膜直接用乙腈经快速溶剂萃取仪提取,以乙腈和水作为流动相,提取液通过ZORBAX Eclipse PAH液相色谱柱分离,紫外串联荧光检测器检测。16种PAHs分离效果良好,在0.025~5.000 μg/mL范围内线性相关系数r≥0.9998,方法加标回收率为78.3%~113.2%,相对标准偏差为0.5%~9.5%,检出限为0.007~0.062 ng/m3。本方法操作简便、快速、准确、灵敏,适于PM2.5中16种PAHs的同时测定。
快速溶剂提取; PM2.5; 多环芳烃; 高效液相色谱法
2017-04-26收稿; 2017-09-04接受
* E-mail: liutaoschx@126.com
1 引 言
近年来,雾霾污染天气在我国频繁出现,尤其在一些大中城市,雾霾天气在冬季几乎成为常态。雾霾主要由可吸入颗粒物、硫化物及氮氧化物组成,而在可吸入颗粒物中,PM2.5占有相当大的比重[1]。多环芳烃(PAHs)作为PM2.5吸附的一类持久性有机污染物,指分子中含有两个及两个以上苯环的碳氢化合物,因长久存在于环境中,可通过呼吸进入人体上呼吸道、支气管及肺泡,在人体内很难代谢,并具有强的致毒性、致癌性而引起广泛关注[2]。2012年环保部发布空气质量新标准,新增了PM2.5成分的检测项[3]。2013年起,国家卫计委在全国多个城市同时开展空气污染(雾霾)人群健康影响监测工作。因而,准确测定PM2.5中PAHs浓度,对于评价大气污染程度及维护公众健康具有重要的意义。
目前,已报道的PM2.5中PAHs的预处理方法有索氏萃取法[4,5]、超声辅助萃取法[6,7]、微波辅助萃取法[8,9]、固相(微)萃取法[10~12]、二级热脱附法[13]和超临界流体萃取法[14]等。快速溶剂萃取法作为一种较新的PAHs提取方法应用则相对较少[15~17]。该方法主要通过高温、高压原理来加速固体或半固体样品中待测物在萃取剂中的溶解,具有操作简便、有机试剂用量少、萃取速度快、效率高和重现性好等优点。文献报道的测定PM2.5中PAHs的方法有荧光法(FL)[18]、室温燐光光谱法(RTPS)[19]、气相色谱法(GC)[20]、高效液相色谱法(HPLC)[21,22]、气相色谱-质谱联用法[6,12,23]和气相色谱-串联质谱法(GC-MS/MS)[24,25]等。其中,FL法灵敏度高,但需预分离, 且该方法对基体复杂样品分离效果差; RTPS法简便、快速、干扰小,但其灵敏度较低; GC法分析高沸点PAHs及对其同分异构体的分离存在一定的困难; GC-MS法具有高灵敏、高定性能力,但与GC法存在同样问题; GC-MS/MS法灵敏度高,但仪器昂贵。 HPLC法不受PAHs挥发性和热稳定性限制,具有操作简便、快速、灵敏度高、成本低等优势。
本研究以美国环境保护署提出的16种优控PAHs作为目标化合物,直接用乙腈作为萃取剂,提取液不经浓缩、氮吹、过滤等复杂后续操作过程,直接进样分析,有效控制了PAHs的损失,建立了快速溶剂提取-直接进样-高效液相色谱测定PM2.5中16种PAHs的新方法,并将其用于成都市大气采样样品中PAHs的测定。
2 实验部分
2.1仪器与试剂
1260高效液相色谱仪(配紫外和荧光检测器,美国安捷伦公司); ZORBAX Eclipse PAH液相色谱柱(150 mm × 4.6 mm × 5 μm,美国安捷伦公司); Milli-Q超纯水仪(美国Millipore公司); N-EVAP-112型氮吹仪(美国Organomation公司); ASE350快速溶剂提取仪(美国戴安公司); TH-150C型PM2.5采样器(武汉市天虹仪表有限责任公司),玻纤滤膜(直径90 mm,美国Pall公司)。
16种PAHs(萘、苊烯、苊、芴、菲、蒽、荧蒽、芘、苯并[a]蒽、屈、苯并[b]荧蒽、苯并[k]荧蒽、苯并[a]芘、二苯并[a,h]蒽、苯并[g,h,i]芘、茚并[1,2,3-cd]芘的英文简写分别为:Nap、AcPy、Acp、Flu、PA、Ant、FL、Pyr、BaA、CHR、BbF、BkF、BaP、DBA、BghiP、IND,其编号分别为1~16)混合标准溶液500 μg/mL(美国Accstandard试剂公司),乙腈、二氯甲烷、正己烷、丙酮(色谱纯,美国Scientific试剂公司),超纯水。
2.2样品采集
参照HJ 646、647-2013采样方法,在成都市设置3个采样点,于2016年1~3月每月连续采样7天(其中3月为雾霾天气,连续采样12天),采样流量100 L/min,采样时间24 h,采样点均避开污染源及障碍物。
2.3样品前处理
采用快速溶剂提取仪,在一定静态萃取时间内,施以高温、高压, 加速待测物在萃取剂中的溶解。具体操作步骤:将玻纤滤膜样品切为4等份,取1/4剪碎,与硅藻土混匀后放入ASE 350快速溶剂提取仪的5 mL萃取池内,再加入2 mL乙腈萃取,萃取温度100℃,压力1500 psi,静态萃取时间5 min,循环1次,N2吹扫30 s,提取液直接进样分析。
2.4仪器分析条件
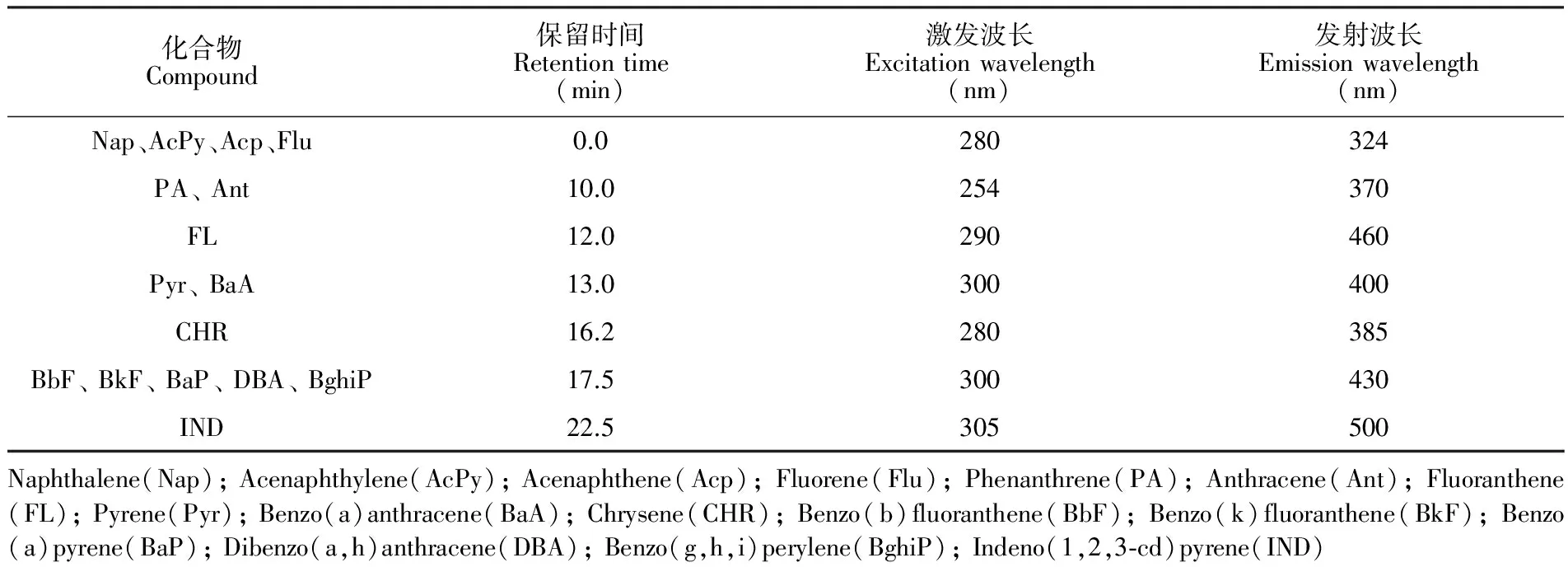
参考HJ 647-2013标准方法并进行改进。具体分析条件如下:乙腈和超纯水分别为流动相A和B相,流速2.0 mL/min。梯度洗脱程序为:0~20 min,40% A; 20~25 min,40%~100% A; 25~30 min,40% A。柱温25℃,进样量10 μL。如表1,设定荧光检测器波长切换程序。因苊烯无荧光,故采用紫外定量,波长为220 nm。
表1 荧光检测器波长切换程序
Table 1 Wavelength switching program for fluorescence detector
化合物Compound保留时间Retentiontime(min)激发波长Excitationwavelength(nm)发射波长Emissionwavelength(nm)Nap、AcPy、Acp、Flu0.0280324PA、Ant10.0254370FL12.0290460Pyr、BaA13.0300400CHR16.2280385BbF、BkF、BaP、DBA、BghiP17.5300430IND22.5305500Naphthalene(Nap);Acenaphthylene(AcPy);Acenaphthene(Acp);Fluorene(Flu);Phenanthrene(PA);Anthracene(Ant);Fluoranthene(FL);Pyrene(Pyr);Benzo(a)anthracene(BaA);Chrysene(CHR);Benzo(b)fluoranthene(BbF);Benzo(k)fluoranthene(BkF);Benzo(a)pyrene(BaP);Dibenzo(a,h)anthracene(DBA);Benzo(g,h,i)perylene(BghiP);Indeno(1,2,3⁃cd)pyrene(IND)
2.5质量控制
每批次玻纤滤膜均进行滤膜空白实验,确保滤膜中的萘与菲的含量低于50 ng,其它PAHs含量均低于10 ng[27]。每个采样点每天均采集空白样品。样品应密闭、低温、避光保存,在效期内完成提取和测定。每次实验先进行试剂空白和实验室空白实验,每测定10个样品,进一针标准溶液,测定值应在10%标准值内。
3 结果与讨论
3.1萃取条件优化
3.1.1萃取溶剂选择考虑到溶剂的膨胀系数和极性因素,分别选取正己烷-丙酮、二氯甲烷-丙酮、正己烷-二氯甲烷(3对溶剂体积比均选择1∶1和2∶1两组)和单独乙腈作为萃取剂,固定萃取温度为120℃、压力为1500 psi、静态萃取时间为7 min进行实验。结果表明,采用乙腈提取时,平均加标回收率最高,故选择乙腈作为萃取剂。选择2、3、4和5 mL乙腈分别实验,所得平均回收率均在85%以上,且无明显差异,综合考虑方法灵敏度和溶剂用量问题,乙腈用量最终选择2 mL。
3.1.2萃取温度选择分别设定萃取温度为80、90、100、110 和 120℃进行实验。当萃取温度为100℃时,平均加标回收率最高,故最佳萃取温度为100℃。
3.1.3萃取压力选择分别设定萃取压力250、500、1000、1500和2000 psi进行实验,平均加标回收率随着萃取压力的升高而提高,当达到1500 psi后,不再发生明显变化,因此,确定最佳萃取压力为1500 psi。
3.1.4静态萃取时间选择静态萃取时间分别设为3、5、7、9 和 11 min进行实验,当萃取5 min时,平均加标回收率已达到90%,继续延长萃取时间,回收率不再发生显著变化,故最佳静态萃取时间为5 min。

图1 不同前处理方法对16种PAHs加标回收率的影响Fig.1 Effect of pretreatment methods on recoveries of 16 kinds of polycyclic aromatic hydrocarbons (PAHs)
3.2不同前处理方法萃取效果比较
本研究将快速溶剂提取法与超声和索氏提取两种常见前处理方法进行了实验比对。由图1可知,快速溶剂提取法的萃取效率明显高于超声提取法(特别是低环PAHs),甚至优于索氏提取法。因为高温、高压可增加PAHs在萃取剂中的溶解度,从而直接提高萃取效率。而且,快速溶剂提取仪密封性好,使得易挥发的低环PAHs在前处理过程中损失减少,加之提取液直接进样分析,也较大程度减少了样品中PAHs因后处理带来的损失,从而间接提高了萃取效率。
3.3方法学考察

图2 标准溶液的紫外(A)和荧光(B)检测色谱图Fig.2 Chromatograms of standard solution with ultraviolet detector (A) and fluorescence detector (B)
3.3.1方法线性、检出限及定量限采用乙腈分别配制浓度为0.025、0.05、0.1、0.5、1.0和5.0 μg/mL的混合标准系列,依次进样分析,荧光和紫外色谱如图2,由图2可知,16种PAHs分离良好。连续进样10次接近于试剂空白的混合标准溶液,以3倍标准偏差为标准溶液检出限,4倍标准溶液检出限为标准溶液定量限,然后以采样体积144 m3、采集效率90%计算方法检出限和定量限,结果见表2,16种PAHs在0.025~5.000 μg/mL范围内具有良好的线性关系,方法检出限为0.007~0.062 ng/m3,定量限为0.028~0.248 ng/m3。
表2 线性方程、线性相关系数、方法检出限及定量限
Table 2 Linear equations, linear correlation coefficients, detection limits and limits of quantitation

化合物Compound线性回归方程Linearequation相关系数Correlationcoefficient检出限Detectionlimit(ng/m3)定量限Limitofquantitation(ng/m3)Napy=7.78754x+0.09331.00000.0350.140AcPyy=49.0365x-0.40770.99990.0100.040Acpy=21.5922x+0.07451.00000.0090.036Fluy=34.3272x+0.31770.99990.0210.084PAy=30.0023x+0.38970.99990.0470.188Anty=23.8890x+0.21490.99990.0230.092FLy=8.8276x+0.01810.99990.0150.060Pyry=12.3672x-0.01390.99990.0170.068BaAy=14.4147x+0.06811.00000.0500.200CHRy=16.8610x+0.02471.00000.0310.124BbFy=18.7203x+0.05341.00000.0620.248BkFy=112.7012x+4.28370.99980.0100.040BaPy=47.3973x+0.55620.99990.0280.112DBAy=9.5437x+0.02810.99990.0070.028BghiPy=14.1368x+0.04581.00000.0090.036INDy=3.7781x-0.04250.99990.0110.044
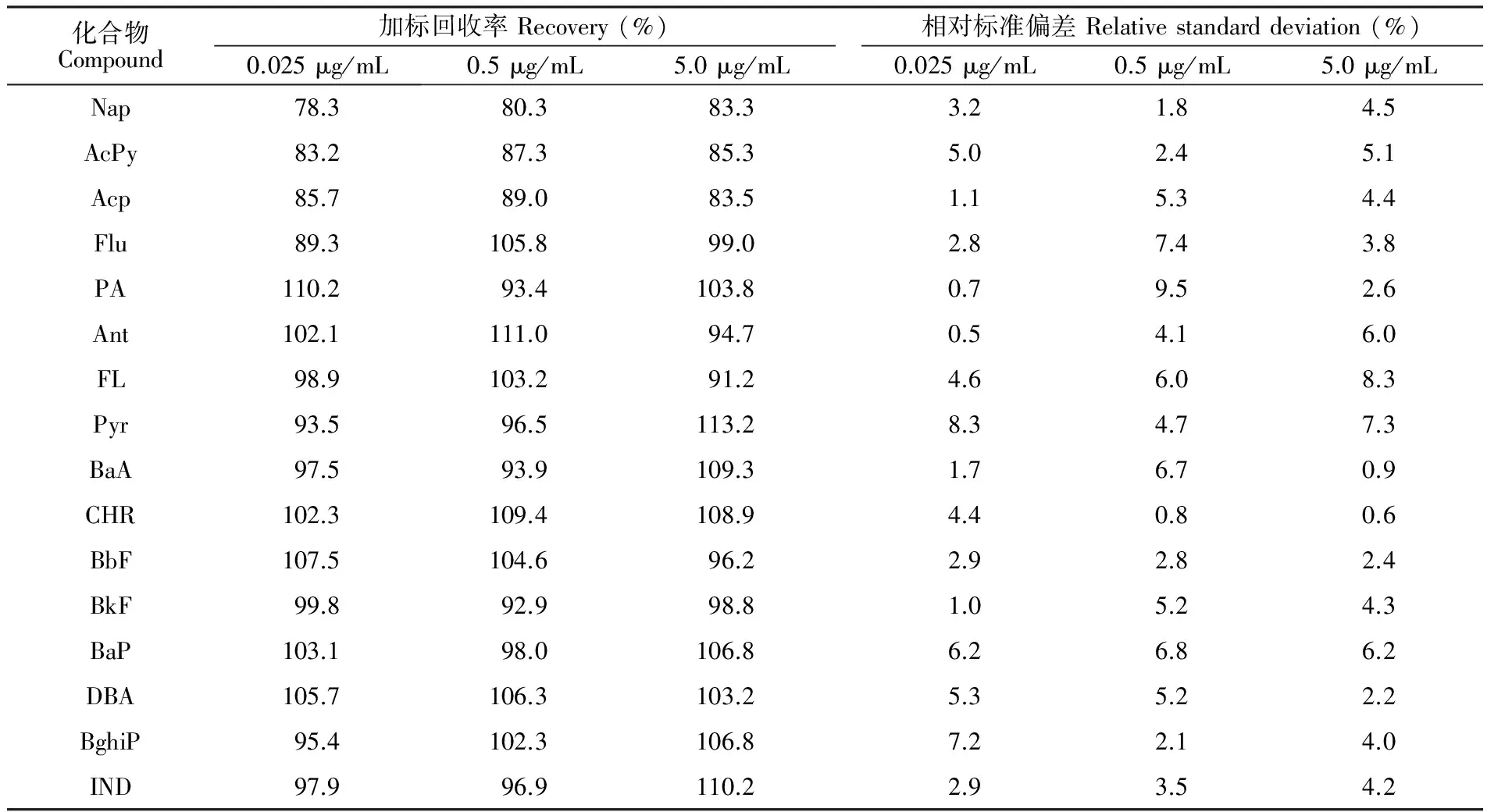
3.3.2方法精密度与准确度在标准线性范围内,取低、中、高浓度的混合标准溶液分别加到11份空白滤膜上,按照2.3和2.4节进行前处理及测定,并计算相对标准偏差; 取加入低、中、高浓度混合标准的样品加标滤膜,经相同处理后测定,并计算加标回收率,结果见表3,本方法加标回收率为78.3%~113.2%, 相对标准偏差为0.5%~9.5%。
表3 16种多环芳烃的加标回收率和相对标准偏差
Table 3 Recoveries and relative standard deviations of 16 kinds of PAHs
化合物Compound加标回收率Recovery(%)0.025μg/mL0.5μg/mL5.0μg/mL相对标准偏差Relativestandarddeviation(%)0.025μg/mL0.5μg/mL5.0μg/mLNapAcPyAcpFluPAAntFLPyrBaACHRBbFBkFBaPDBABghiPIND78.383.285.789.3110.2102.198.993.597.5102.3107.599.8103.1105.795.497.980.387.389.0105.893.4111.0103.296.593.9109.4104.692.998.0106.3102.396.983.385.383.599.0103.894.791.2113.2109.3108.996.298.8106.8103.2106.8110.23.25.01.12.80.70.54.68.31.74.42.91.06.25.37.22.91.82.45.37.49.54.16.04.76.70.82.85.26.85.22.13.54.55.14.43.82.66.08.37.30.90.62.44.36.22.24.04.2
3.4方法实际应用
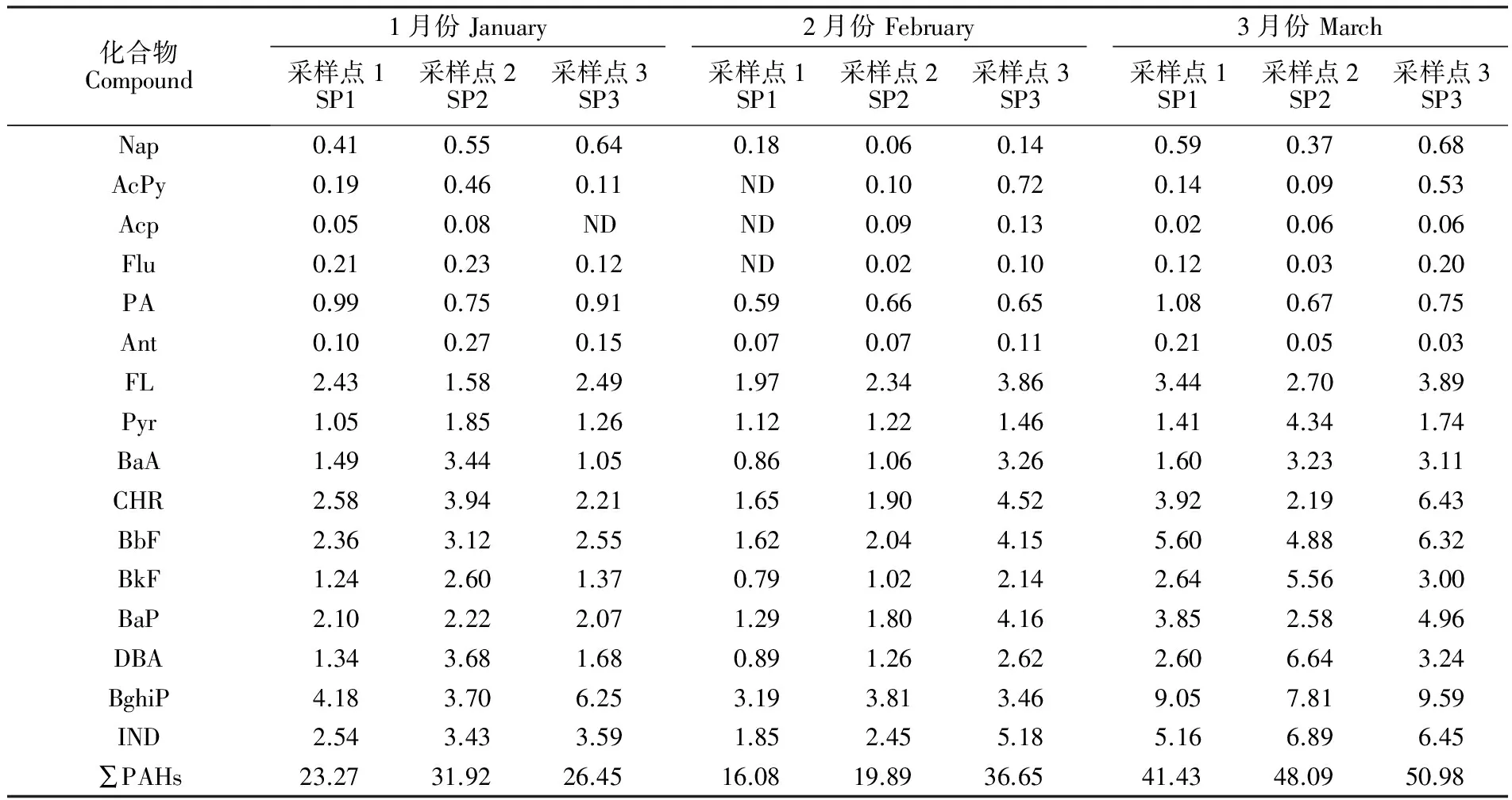
将采自于2016年1~3月的3个采样点所有滤膜样品按照本方法进行前处理及测定,并计算16种PAHs 的平均浓度及总浓度,所得结果见表4。各采样点PAHs总浓度变化范围为16.08~50.98 ng/m3。 其中,1月和2月样品浓度较低,3月样品浓度较高(特别是高环PAHs),因为3月多为雾霾天气。3个采样点中,测得的2~4环PAHs含量均较低,因为低环PAHs在大气中主要以气相形式存在。
表4 成都市3个采样点PM2.5中16种PAHs的平均浓度及总浓度(ng/m3)
Table 4 Average and total concentrations of 16 PAHs in PM2.5 at three sampling points (SP) in Chengdu (ng/m3)
化合物Compound1月份January采样点1SP1采样点2SP2采样点3SP32月份February采样点1SP1采样点2SP2采样点3SP33月份March采样点1SP1采样点2SP2采样点3SP3NapAcPyAcpFluPAAntFLPyrBaACHRBbFBkFBaPDBABghiPIND∑PAHs0.410.190.050.210.990.102.431.051.492.582.361.242.101.344.182.5423.270.550.460.080.230.750.271.581.853.443.943.122.602.223.683.703.4331.920.640.11ND0.120.910.152.491.261.052.212.551.372.071.686.253.5926.450.18NDNDND0.590.071.971.120.861.651.620.791.290.893.191.8516.080.060.100.090.020.660.072.341.221.061.902.041.021.801.263.812.4519.890.140.720.130.100.650.113.861.463.264.524.152.144.162.623.465.1836.650.590.140.020.121.080.213.441.411.603.925.602.643.852.609.055.1641.430.370.090.060.030.670.052.704.343.232.194.885.562.586.647.816.8948.090.680.530.060.200.750.033.891.743.116.436.323.004.963.249.596.4550.98
4 结 论
本研究建立了PM2.5中16种PAHs的快速溶剂提取-直接进样-高效液相色谱测定方法。快速溶剂提取法较索氏提取、超声提取等前处理方法的萃取效率更高; 操作更智能、快速; 萃取剂使用量少,对环境更友好; 提取液直接进样分析,基体无干扰,且避免了后续处理过程中待测物的损失及产生的相应误差,使分析结果更加准确、可靠。本方法操作简便、快速、准确、灵敏,适于PM2.5中16种PAHs的同时检测,可为PM2.5中PAHs的污染分布特征及源解析提供有力的数据支持。
1 Ma Q X, Wu Y F, Zhang D Z, Wang X J, Xia Y J, Liu X Y, Tian P, Han Z W, Xia X G, Wang Y, Zhang R J.Sci.TotalEnviron.,2017, 599(11): 246-253
2 Kim K, Jahan S A, Kabir E, Brown R J.Environ.Int.,2013, 60(5): 71-80
3 GB 3095-2012, Ambient Air Quality Standard. National Standards of the People's Republic of China
环境空气质量标准. 中华人民共和国国家标准. GB 3095-2012
4 ZHAO Bo, LI Yu-Qing, ZHANG Su-Kun, HAN Jing-Lei, XU Zhen-Cheng, FANG Jian-De.ChineseJournalofChromatography,2014, 32(9): 960-966
赵 波, 黎玉清, 张素坤, 韩静磊, 许振成, 方建德. 色谱,2014, 32(9): 960-966
5 Dallarosa J B, Mnego J G, Teixeira E C, Stefens J L, Wiegand F.Atmos.Environ.,2005, 39(9): 1609-1625
6 ZHAO Hong-Shuai, LIU Bao-Xian, CHANG Miao, SHEN Xiu-E, WANG Xiao-Ju, XU Su-Shi, ZHAO Qi-Yue.ChineseJ.Anal.Chem.,2014, 42(5): 729-734
赵红帅, 刘保献, 常 淼, 沈秀娥, 王小菊, 徐稣士, 赵起越. 分析化学,2014, 42(5): 729-734
7 Ma N X, Ban W, Li R J, Geng H, Zhang J G, Dong C, Shuang S M, Cai Z W.Anal.Methods,2015, 7(9): 3967-3971
8 Purcaro G, Moret S, Conte L S.MeatSci.,2009, 81(1): 275-280
9 WANG Mei-Fei, YANG Li-Li, HU En-Yu.ChineseJournalofChromatography,2017, 35(6): 669-673
王美飞, 杨丽莉, 胡恩宇. 色谱,2017, 35(6): 669-673
10 Zhang M, Xie J F, Wang Z T, Zhao L J, Zhang H, Li M.Atmos.Res.,2016, 178(10):401-414
11 Koziel J A, Odziemkowski M,Pawliszyn J.Anal.Chem.,2001, 73(1): 47-54
12 LIU Fei, DUAN Feng-Kui, LI Hai-Rong, MA Hai-Liang, HE Ke-Bin, ZHANG Qian.ChineseJ.Anal.Chem.,2015, 43(4): 540-546
刘 斐, 段凤魁, 李海蓉, 马永亮, 贺克斌, 张 倩. 分析化学,2015, 43(4): 540-546
13 Yamasaki D, Kajiwara H, Kirii M, Ohira S, Todai K.BunsekiKagaku,2015, 64(8): 571-579
14 Han Y H, Ren Y M, Xu K, Yang F, Li Y F, Cheng T T, Kang X M, Xu C M, Shi Q.J.Chromatogr.A,2015, 1395(21): 1-6
15 Xu T C.J.Sep.Sci.,2016, 39(10): 1892-1899
16 ZHANG Ya-Nan, YANG Xing-Lun, BIAN Yong-Rong, GU Cheng-Gang, WANG Dai-Zhang, JIANG Xin.ChineseJ.Anal.Chem.,2016, 44(10): 1514-1520
张亚楠, 杨兴伦, 卞永荣, 谷成刚, 王代长, 蒋 新. 分析化学,2016, 44(10): 1514-1520
17 Belo R F C, Figueiredo J P, Nunes C M, Pissinatti R, Souza S V C, Junqueira R G.J.Chromatogr.B,2017, 1053(14): 87-100
18 Pena E A, Ridley L M, Murphy W R, Sowa J R, Bentivegna C S.Environ.Toxicol.Chem.,2015, 34(9): 1946-1958
19 CUI Wen-Tan, YAO Wei-Xi, XU Xiao-Bai.ChineseJ.Anal.Chem.,1992, 20(11): 1247-1251
崔文坦, 姚渭溪, 徐晓白. 分析化学,1992, 20(11): 1247-1251
20 CHEN Yue-Meng, ZHAO Min, WANG Qian, TONG Yue-Chan, WANG Jin-Feng.PhysicalTestingandChemicalAnalysisPartB:ChemicalAnalysis,2014, 50(11): 1409-1411
陈月萌, 赵 敏, 王 千, 童月婵, 王金凤. 理化检验:化学分册,2014, 50(11): 1409-1411
21 Rocío-Bautista P, Pino V, Ayala J H, Pasan J, Ruiz-Perez C, Afonso A M.J.Chromatogr.A,2016, 1436(10): 42-50
22 Wang H, Zhao X L, Meng W, Wang P F, Wu F Cg, Tang Z, Han X J, Giesy J P.Anal.Chem.,2015, 87(15): 7667-7675
23 Li Y J, Zhu J P.Anal.Chim.Acta,2017, 961(13): 67-73
24 WANG Dao-Wei, ZHAO Shi-Min, JIN Wei, SHEN Qiu-Ying, HU Ping, HUANG Bin, PAN Xue-Jun.ChineseJ.Anal.Chem.,2013, 41(6): 861-868
王道玮, 赵世民, 金 伟, 沈秋莹, 胡 平, 黄 斌, 潘学军. 分析化学,2013, 41(6): 861-868
25 LIU Bao-Xian, ZHAO Hong-Shuai, WANG Xiao-Ju, SHEN Xiu-E, ZHANG Da-Wei, SHI Ai-Jun.JournalofChineseMassSpectrometrySociety,2015, 36(4): 372-379
刘保献, 赵红帅, 王小菊, 沈秀娥, 张大伟, 石爱军. 质谱学报,2015, 36(4): 372-379
26 NIU Xiao-Mei, CHEN Su-Jun.JournalofEnvironmentalHygiene,2015, 5(1): 65-70
牛晓梅, 陈素军. 环境卫生学杂志,2015, 5(1): 65-70
Determinationof16KindsofPolycyclicAromaticHydrocarbonsinAtmosphericFineParticlesbyAcceleratedSolventExtractionCoupledwithHighPerformanceLiquidChromatography
YUAN Xiao-Xue, JIANG Yang, YANG Chang-Xiao, XIE Bi-Jun, YONG Li, HU Bin, LIU Tao*
(SichuanCenterforDiseaseControlandPrevention,InstituteofPhysicochemicalDetection,Chengdu610041,China)
A method for determination of 16 kinds of polycyclic aromatic hydrocarbons (PAHs) in atmospheric fine particles (PM2.5) was developed based on accelerated solvent extraction-direct injection coupled with high performance liquid chromatography (HPLC). PM2.5 was collected by glass fiber membrane filter and pretreated with acetonitrile by accelerated solvent extraction. The extract was separated by ZORBAX Eclipse PAH column with acetonitrile and water as mobile phase, and detected by ultraviolet and fluorescence detectors. The result showed that the 16 kinds of PAHs were well separated and there were good linear relationships (r≥0.9998) in the concentration range of 0.025-5.00 μg/mL. The recoveries were from 78.3% to 113.2%. The relative standard deviations ranged from 0.5% to 9.5%. The detection limits were 0.007-0.062 ng/m3. The method was simple, rapid, accurate and sensitive, and suitable for the simultaneous determination of 16 kinds of PAHS in PM2.5.
Accelerated solvent extraction; Atmospheric fine particles; Polycyclic aromatic hydrocarbons; High performance liquid chromatography
26 April 2017; accepted 4 September 2017)
10.11895/j.issn.0253-3820.170262
