用化学沉淀法去除黑臭水体中氨氮工艺研究
2017-11-03罗翊文殷海江夏邵峰
楚 广,童 应,罗翊文,殷海江,夏邵峰,苏 莎
(1.中南大学冶金与环境学院,湖南 长沙410083;2.湖南中湘春天环保科技有限公司,湖南长沙410045;3.湖南有色金属研究院,湖南长沙410100)
·环 保·
用化学沉淀法去除黑臭水体中氨氮工艺研究
楚 广1,童 应1,罗翊文1,殷海江2,夏邵峰2,苏 莎3
(1.中南大学冶金与环境学院,湖南 长沙410083;2.湖南中湘春天环保科技有限公司,湖南长沙410045;3.湖南有色金属研究院,湖南长沙410100)
用化学沉淀法对含氨氮300~1 000 mg/L的高浓度氨氮废水进行了去除氨氮的试验。试验结果表明:化学沉淀法可用于处理各种不同浓度的氨氮废水,而且在处理高浓度的氨氮废水时效果更好。最佳工艺条件为:pH值在9.0~10.5之间,反应时间为20 min左右,在常温(25~35℃)下进行反应,试剂添加比例为 n(P)∶n(Mg)∶n(N)=1.2∶1.2∶1或 1.2∶1.1∶1。
氨氮废水;沉淀;磷酸铵镁
氨氮是指溶于水的氨气或者铵根离子中的氮原子。水中N的存在形式主要有氨氮、有机氮、硝酸盐和亚硝酸盐中的氮。含氮物质可以通过一定的降水降尘和生物固氮等自然过程进入水体,也可以通过人类活动进入水体。氨氮废水的主要来源有工业废水、生活污水、农业废水。氨氮废水的存在会危害水生植物,造成水体富营养化,饮用水中含NO3-N可引发高铁血红蛋白症,严重时引起窒息,而当NO2-N和胺作用时会生成亚硝胺,会引起致癌、致畸和致突变等。
不同种类的氨氮废水氨氮浓度差异很大,除氨氮浓度外,废水中含有的杂质种类和性质也是千差万别,所以选择氨氮废水的处理方法时要根据实际情况而定,在考虑去除效果的同时还要考虑经济性等。目前,生物法、化学沉淀法、化学氧化法、膜分离法、吹脱法和离子交换法等[1~13]是氨氮废水的处理技术中研究得比较深入的。赵宗升等人[14]对垃圾填埋场渗滤液进行了传统硝化反硝化处理,把氨氮含量1 300 mg/L的废水降到了含氨氮10 mg/L以下,但对总氮作用不明显,去除率才有20%~30%。朱晓君等人[15]采用同步硝化反硝化技术对上海市松江污水厂的污水进行了处理,结果表明:若曝气池中的溶解氧浓度在0.5~1.0 mg/L,总氮去除率可达80%。朱明石等人[16]也对氨氮废水进行了厌氧氧化处理,他们采用了一个生物膜反应器,对于氨氮初始浓度340 mg/L的废水,其去除率达到了84%。胡亮等用次氯酸钠对去除重金属后的铅锌冶炼废水(简称二次水)进行氨氮去除试验研究,结果表明,次氯酸钠去除氨氮最适合工艺条件是:pH=7~8、次氯酸钠溶液(含有效氯10%)投加量为0.2%(体积比)、反应时间30 min。经处理后氨氮含量低于8 mg/L,达到《铅、锌工业污染物排放标准》(GB 25466-2010)。德国的Inlenberg厂利用反渗透的方法来处理沉积污水效果良好,处理的含氨氮577 mg/L的废水达到了 98.54%以上的去除率[17]。黄军等[18]对某化工企业废水采用吹脱法进行预处理,将氨氮含量1 200 mg/L的废水降低至60 mg/L,再经过深度处理后,最终氨氮浓度降低至5 mg/L。
化学沉淀法工艺简单、处理对象广泛,而且沉淀物还可作为肥料,这种方法已得到国内外学者的广泛研究[19~35]。本文考察了化学沉淀法去除氨氮的最佳试验条件。
1 化学沉淀法去除氨氮的研究过程
1.1 试验原理
化学沉淀法去除水中的氨氮的原理为将Na3PO4作为PO3-4源,将MgSO4作为Mg2+源加入到含有氨氮的黑臭水体中,使其与水中的铵根离子发生下列反应:
Mg2++NH+4+PO3-4+6H2O=MgNH4PO4·6H2O在反应过程中生成的MgNH4PO4·6H2O俗称鸟粪石,可以作缓释肥(SRFS),因此化学沉淀法在脱除氨氮的同时还能将废物进行利用。
1.2 试验过程
取氨氮废水100 mL,加入一定量的磷酸钠和硫酸镁(经计算),搅拌均匀;再用1 mol/L浓盐酸调节溶液pH至预定值,调节过程要快,将烧杯置于恒温加热水浴磁力搅拌器中在预定条件下搅拌反应;反应结束后过滤,用纳氏试剂分光光度法分析滤液的氨氮含量。
1.3 水中氨氮浓度的分析方法
水中氨氮浓度的分析方法采用纳氏试剂分光光度法。首先取8个200 mL烧杯洗净烘干,分别准确移取0.00 mL、0.50 mL、1.00 mL、2.00 mL、4.00 mL、6.00 mL、8.00 mL和10.00 mL氨氮标准工作溶液稀释至50 mL后倒入烧杯内,分别加入酒石酸钾钠溶液1 mL并摇匀,随后分别加入纳氏试剂1.5 mL,摇匀后静置10 min,以水作参比在420 mm处测量吸光度。把矫正后的吸光度作为纵坐标,氨氮含量(单位为μg)作为横坐标,绘制一条标准曲线如图1所示。

图1 纳氏试剂标准曲线
水中氨氮浓度计算公式如式(1)所示:

式中:ρ(N)为氨氮浓度/mg·L-1;As为水样的吸光度;Ab为空白试样的吸光度;α为校准曲线的截距;b为校准曲线的斜率;V为试料体积/mL。因此,按图1所示的标准曲线得到氨氮浓度的计算如式(2)所示:

2 结果与分析
2.1 原液中氨氮初始浓度对氨氮去除率的影响
将配制的混合原液加热至 20℃,按 n(P)∶n(Mg)∶n(N)=1∶1∶1的比例加入一定量的 Na3PO4、MgSO4作为沉淀剂,控制pH值为10,反应20 min后过滤。探究原液中氨氮浓度分别为300 mg/L、400 mg/L、500 mg/L、600 mg/L、700 mg/L、800 mg/L、900 mg/L、1 000 mg/L时氨氮的去除率。加入试剂后轻微搅拌溶液即变成白色乳浊液,氨氮浓度越高,其浑浊程度越大,过滤后得到白色沉淀物质。
氨氮初始浓度不同时的试验结果如图2所示。从图中可以明显看出,对于氨氮初始浓度为300 mg/L的废水,氨氮去除率为87.14%,氨氮去除率随着氨氮初始浓度的升高而逐渐升高。此外,从图中还可以看出,虽然氨氮去除率随氨氮初始浓度的升高,但是变化非常缓慢,由此可见,化学沉淀法对各种浓度的氨氮废水具有很强的适应性,而且越是浓度高的氨氮废水,其处理效果越好。

图2 氨氮初始浓度对氨氮去除率的影响
同时,虽然氨氮去除率接近90%,但纵使是初始浓度最低的300 mg/L的废水,其剩余氨氮浓度依然达到了38.58 mg/L,还未达到直接排放的要求,所以可用化学沉淀法预处理高浓度氨氮废水,再用其它方法,如用离子交换法进行后续处理即可使氨氮浓度达到较低水平。
2.2 pH值对氨氮去除率的影响
将氨氮浓度为 1 000 mg/L的原液,加热至20℃,按 n(P)∶n(Mg)∶n(N)=1∶1∶1的比例加入一定量的Na3PO4、MgSO4作为沉淀剂,控制反应时间为 20 min,探究其 pH分别为 8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5时氨氮的去除率。
pH值不同时的试验结果如图3所示。从图中可以看出pH=9.5时的氨氮去除率最高,达到了92.85%,同时,pH在9.0~10.5时都有较好的氨氮去除效果,氨氮去除率超过了90%。当pH<8时,发生强烈水解(),4大量转变为了,所以不利于MgNH4PO4的形成。当 pH>11时,有利于 Mg(OH)2的形成(Mg2++2OH-=Mg(OH)2,=1.8×10-11),从而也会影响MgNH4PO4沉淀的生成,降低氨氮的去除率。从试验的结果来看,保持pH在9.5左右可以得到最佳的除氨氮效果。

图3 pH值对氨氮去除率的影响
2.3 反应时间对氨氮去除率的影响
将氨氮浓度为1 000 mg/L的原液,加热至 20℃,按 n(P)∶n(Mg)∶n(N)=1∶1∶1的比例加入一定量的Na3PO4、MgSO4作为沉淀剂,控制pH为10,探究其反应时间分别为10 min、20 min、30 min、40 min、50 min、60 min时氨氮的去除率。
反应时间不同时的试验结果如图4所示。从图中可以看出,反应在10 min时已基本完成,氨氮去除率超过了90%,延长反应时间并不能明显提高氨氮去除率,特别在30 min后,氨氮去除率已不再增加。所以反应时间控制在20 min为宜,既可以保证良好的氨氮去除效果,又可以节省时间,增大生产效益。
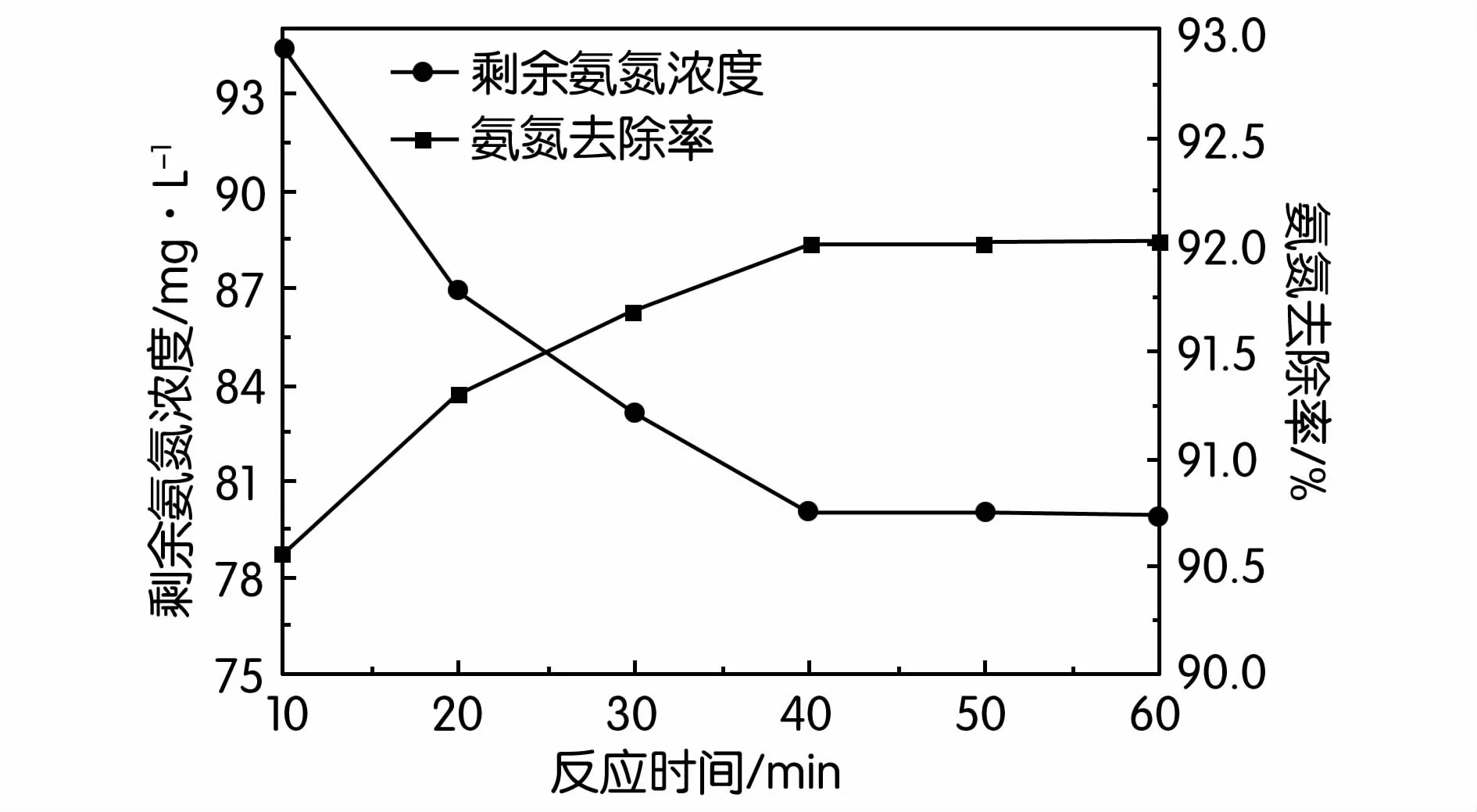
图4 反应时间对氨氮去除率的影响
2.4 反应温度对氨氮去除率的影响
对于氨氮浓度为1 000 mg/L的原液,按n(P)∶n(Mg)∶n(N)=1∶1∶1的比例加入一定量的 Na3PO4、MgSO4作为沉淀剂,控制pH为10,反应时间为20 min,探究其反应温度分别为20℃、30℃、40℃、50℃、60℃时氨氮的去除率。
温度不同时的试验结果如图5所示。从图中可以看出,随温度升高,氨氮去除效果反而下降,且降低幅度略大,当温度为60℃时,氨氮去除率已经降到了80.18%。因此,化学沉淀法不适合于高温条件。温度可以影响MgNH4PO4的溶解度和晶体形态。温度升高,MgNH4PO4的溶解度会有所增大,溶液的过饱和度降低,生成沉淀的推动力减弱,所以温度升高不利于MgNH4PO4沉淀的生成,温度也可以影响溶质的相对扩散速率,故反应在常温(25~35℃)下为宜。

图5 温度对氨氮去除率的影响
2.5 沉淀剂比例对氨氮去除率的影响
氨氮浓度为1 000 mg/L的原液,加热至20℃,控制反应时间为20 min,pH值为10,探究按n(P)∶n(Mg)∶n(N)=(1.2∶1.2∶1)、(1.1∶1.2∶1)、(1∶1.2∶1)、(1.2∶1.1∶1)、(1.1∶1.1∶1)、(1∶1.1∶1)、(1.2∶1∶1)、(1.1∶1∶1)、(1∶1∶1)的比例加入一定量的Na3PO4、MgSO4作为沉淀剂时氨氮的去除率。
加入试剂后轻微搅拌溶液即变成白色乳浊液,其中Na3PO4和MgSO4较多的溶液浑浊程度更大,反应过程中溶液一直维持乳浊状态,过滤后得到白色沉淀物质。沉淀剂添加比例不同时的氨氮去除效果如图6所示。

图6 沉淀剂添加比例不同对氨氮去除率的影响
从图中可以看出,当沉淀剂添加比例增加,也即是Na3PO4和MgSO4同时增加时有利于MgNH4PO4沉淀的生成,氨氮去除率有一定的提高,例如当n(P)∶n(Mg)∶n(N)=1.2∶1.2∶1和1.2∶1.1∶1时,氨氮去除率分别达到了95.34%和94.23%。同时注意到,当控制Na3PO4添加量不变而增加MgSO4时,氨氮去除率呈现逐渐降低的趋势,这是因为过量的Mg2+与NH+4抢夺PO3-4所致。控制MgSO4添加量不变而增加Na3PO4时,能提高氨氮去除率。从以上分析可以得出结论,当沉淀剂添加比例为 n(P)∶n(Mg)∶n(N)=1.2∶1.2∶1和 1.2∶1.1∶1时可取得最佳氨氮去除效果。
3 结 论
本文通过探索了化学沉淀法除氨氮在不同条件下的试验效果,分析了影响化学沉淀法去除氨氮工艺的影响因素,得出以下结论:
1.化学沉淀法对不同浓度的氨氮废水具有良好的适应性,尤其处理高浓度氨氮废水时具有较高的氨氮去除率。
2.化学沉淀法处理氨氮废水尤其是高浓度的氨氮废水时的最佳反应条件为:pH在9.0~10.5之间,反应时间为20 min,反应温度为常温,沉淀剂添加比例 n(P)∶n(Mg)∶n(N)=1.2∶1.2∶1或 1.2∶1.1∶1。
[1] 叶铁林.化学元素百宝箱[M].北京:化学工业出版社,2011.
[2] 项斯芬,严宣申,曹庭礼,等.无机化学丛书(第四卷)[M].北京:科学出版社.2011.3-4.
[3] 司学芝,刘捷.无机化学[M].北京:化学工业出版社,2009.
[4] 侯燕卿.反渗透在氨氮废水处理中的应用研究[D].西安:长安大学,2010.
[5] 王莉萍,曹国平,周小虹.氨氮废水处理技术研究进展[J].化学推进剂与高分子材料,2009,(3):26-32.
[6] 杨志水,姜斌.城镇生活污水中氨氮的去除研究[J].环境工程,2010,(S1):147-149.
[7] 刘伟才,丁锋.我国农业污水处理技术的现状与处理方式[J].湖南生态科学学报,2015,(4):40-45.
[8] 罗智文,耿安锋.富营养化与氨氮废水的处理现状研究[J].内江科技,2009,(6):27.
[9] 黄骏,陈建中.氨氮废水处理技术研究进展[J].环境污染治理技术与设备,2002,(1):65-68.
[10]鲁秀国,罗军,赖祖明.氨氮废水处理技术发展现状[J].华东交通大学学报,2015,(2):129-135.
[11]姜瑞,曾红云,王强.氨氮废水处理技术研究进展[J].环境科学与管理,2013,(6):131-134.
[12]钟理,谭春伟,胡孙林,等.氨氮废水降解技术进展[J].化工科技,2002,(2):59-62.
[13]沈连峰,申艳萍,刘文霞,等.物化-水解酸化-A/O组合法处理焦化废水[J].水处理技术,2007,(9):90-93.
[14]赵宗升,刘鸿亮,袁光钰,等.A2/O与混凝沉淀法处理垃圾渗滤液研究[J].中国给水排水,2001,(11):13-16.
[15]朱晓君,周增炎,高廷耀.低氧活性污泥法脱氮除磷工艺生产性研究[J].中国给水排水,1997,(S1):12-16+2-3.
[16]朱明石,周少奇.厌氧氨氧化-反硝化协同脱氮研究[J].化工环保,2008,(3):214-217.
[17]黄军,邵永康.高效吹脱法+折点氯化法处理高氨氮废水[J].水处理技术,2013,(8):131-133.
[18]蒙爱红,左剑恶,杨洋.高浓度氨氮废水的短程硝化研究[J].中国给水排水,2002,(11):43-45.
[19]林建清,方宏达,杨春霖,等.厌氧氨氧化去除垃圾渗滤液中氨氮的实验[J].华侨大学学报(自然科学版),2008,(1):61-63.
[20]孙体昌,崔志广,寇珏,等.废水中氨氮沉淀物的结晶状态及其与捕收剂的作用机理[J].北京科技大学学报,2006,(3):231-236.
[21]马倩玲,林星杰,肖沃辉.化学沉淀法处理含氨氮废水的研究[J].矿冶,2008,(4):71-74.
[22]徐志高,黄倩,张建东,等.化学沉淀法处理高浓度氨氮废水的工艺研究[J].工业水处理,2010,(6):31-34.
[23]文艳芬,唐建军,周康根.MAP化学沉淀法处理氨氮废水的工艺研究[J].工业用水与废水,2008,(6):33-36.
[24]刘恒嵩,彭玉玲,丁伟.折点氯化法处理废水中氨氮工艺研究[J].农村经济与科技,2016,(2):145-146.
[25]钟理.臭氧湿式氧化氨氮的降解过程研究[J].中国给水排水,2000,(1):14-17.
[26]付迎春.催化湿式氧化法处理氨氮废水的研究[D].南京:南京工业大学,2004.
[27]邵刚.液膜法处理含锌废水[J].工业水处理,1985,(2):21-24.
[28]刘华,李静,孙丽娜,等.蒸氨/氨吹脱两级工艺处理高浓度氨氮废水[J].中国给水排水,2013,(20):96-99.
[29]张希衡.水污染控制工程(第2版)[M].北京:冶金工业出版社,1993.
[30]刘玉亮,罗固源,阙添进,等.斜发沸石对氨氮吸附性能的试验分析[J].重庆大学学报(自然科学版),2004,(1):62-65.
[31]李晔,王建兵,肖文浚,等.沸石去除水源中低浓度氨氮的实验研究[J].武汉理工大学学报,2003,(2):4-6.
[32]王利平,冯俊生,陈莉荣,等.用沸石吸附稀土冶炼氯铵废水中的氨氮[J].化工环保,2005,(3):214-216.
[33]李忠,符瞰,夏启斌.改性天然沸石的制备及对氨氮的吸附[J].华南理工大学学报(自然科学版),2007,(4):6-10.
[34]缪应祺.水污染控制工程[M].南京:东南大学出版社,2002.
[35]王燕飞.水污染控制技术[M].北京:化学工业出版社,2001.175-185.
Ammonia-Nitrogen Removal from Black and Odorous Water by Chemical Precipitation
CHU Guang1,TONG Ying1,LUO Yi-wen1,YIN Hai-jiang2,XIA Shao-feng2,SU Sha3
(1.School of Metallurgical and Environment,Central South University,Changsha 410083,China;2.Hunan Spring Environmental Protection Technology Co.,Ltd.,Changsha 410045,China;3.Hunan Research Institute of Nonferrous Metals,Changsha 410100,China)
Treatment of high concentration ammonia nitrogen wastewater with nitrogen concentration of 300~1 000 mg/L was carried out by chemical precipitation method.The experimental results show that the chemical precipitation method can adapt well to ammonia nitrogen wastewater with different concentration,and it is more effective in treating high concentration of ammonia nitrogen wastewater.The optimum conditions were as follows:the pH value was between 9.0~10.5 and the reaction time was about 20 min.The reaction was carried out at room temperature(25~35℃).The ratio of reagent addition was n(P)∶n(Mg)∶n(N)=1.2∶1.2∶1 or 1.2∶1.1∶1.
ammonia-nitrogen containing wastewater;precipitation;magnesium ammonium phosphatte
X703.5
A
1003-5540(2017)05-0054-04
楚 广(1958-),男,教授,主要从事有色金属资源循环利用及环境保护研究工作。
2017-08-26
