Meta分析:洗必泰预防化疗诱导致口腔黏膜炎的作用
2017-11-01路燕燕姜元喜
路燕燕,姜元喜
(同济大学附属同济医院,上海 200065)
Meta分析:洗必泰预防化疗诱导致口腔黏膜炎的作用
路燕燕,姜元喜
(同济大学附属同济医院,上海 200065)
口腔黏膜炎;化学疗法;洗必泰;口腔护理;Meta分析
有40%的恶性肿瘤患者在化疗后会发生口腔黏膜炎,严重的口腔黏膜炎会导致生活质量的显著下降、营养摄入不足甚至需要延期化疗[1]。因此,预防化疗患者口腔黏膜炎的发生对于改善患者的生活质量及预后有重要作用[2]。漱口液漱口是有效预防口腔黏膜炎的重要手段之一。目前,临床应用的漱口液多种多样,洗必泰是最常应用的漱口液之一[3]。此外,还有小苏打溶液、生理盐水溶液等。然而,尽管洗必泰漱口在临床上广为应用,但其确切的作用尚未得到研究证实。一些小样本研究认为洗必泰预防化疗患者口腔黏膜炎优于其他漱口液,但由于样本量较小,其可信度受到质疑。本研究通过Meta分析的方法,对既往的多项研究进行整合分析,探讨洗必泰在预防化疗患者口腔黏膜炎中的作用。
1 资料与方法
1.1 纳入和排除标准 纳入标准:按照PICOD原则,研究对象为因恶性肿瘤需要化疗的患者,干预措施为洗必泰漱口液,对照措施为安慰剂或其他漱口液,结局评估为口腔黏膜炎的程度。研究设计类型为随机对照试验。排除标准:①非随机对照试验;②资料不全或无法获取完整资料的研究;③病例报道;④动物实验或临床前研究。口腔黏膜炎的程度通过口腔评估指南(oral assessment guide,OAG)[4]或 WHO分级标准[5]进行评估。OAG共有“声音”、“吞咽”、“口唇”、“唾液”、“口腔黏膜”、“齿龈”、“牙齿”、“舌头”8个评估项目,每项分为3级,每级1分,总分24分,其评分越高,说明口腔黏膜炎越重。WHO口腔黏膜炎分级标准按照黏膜炎的程度分为5级,0级为正常,1级为口腔黏膜局限性充血,2级为弥漫性充血、点状溃疡,可以进食固体食物,3级为弥漫性充血、片状溃疡,仅能进食流质,4级为口腔大面积溃疡、剧痛,无法进食。一般认为0~1级为轻度黏膜炎,2~4级为严重黏膜炎。
1.2 检索策略 联机检索Cochrane图书馆临床对照试验库、Pubmed数据库、EMBase数据库和中国期刊全文数据库(CNKI)、中国生物医学文献数据库(CBM)、万方数据库,英文检索词包括“mucositis”,“oral mucositis/stomatitis”,“chemotherapy”,“prevention”,“mouthwashes”和“chlorhexidine/CHG”。中文检索词包括“洗必泰/口泰”、“化疗”、“口腔黏膜炎/口腔溃疡”。发表时间无限制。语言限制为中英文。
1.3 文献质量评价 纳入的随机对照研究采用Cochrane偏倚风险评估工具进行质量评价,包括6个方面:①随机分配方法;②分配隐藏方案;③盲法;④结果数据的完整性;⑤无选择性报告研究结果;⑥无其他偏倚来源[6]。针对每1项研究结果,对上述6条分别作出“是”(低度偏倚)、“否”(高度偏倚)和“不清楚”(缺乏相关信息或偏倚情况不确定)的判断[7]。
1.4 数据提取 收集纳入文献的资料来源、干预方法、样本量、OAG评分、WHO分级等信息。
1.5 资料分析统计 使用Cochrane协作网提供的RevMan 5.1软件进行合并分析。OAG评分采用权重的均数差(WMD)表示,WHO口腔黏膜炎分级标准采用OR值表示。区间估计采用95%可信区间(95%CI)。首先,对各纳入研究进行随机效应模型统计分析:若P≥0.1、I2≤50%,则说明各研究间无异质性,采用固定效应模型;若P<0.1且I2<50%,说明研究间具有异质性但在可接受的范围内,采用固定效应模型进行合并;若P<0.1、I2>50%,则说明各研究间异质性显著,采用随机效应模型。
2 结果
初检出5 135篇文献,经过阅读摘要和全文后,有10篇文献符合纳入标准[8-17],其中4篇文献采用OAG评估标准[8-10,13],4篇文献采用 WHO分级标准[14-17],另2篇文献则分别采用了不同的评估方法,无法进行合并分析,故排除[11-12]。最终纳入 8篇文献[8-10,13-17],其中7篇为英文文献,1篇为中文文献。纳入文献的质量评价,见表1。纳入研究中除1篇为洗必泰凝胶外[15],其余均为洗必泰漱口液,对照组包括对照组漱口液包括混合液、盐水、清水、制真菌素、苄达明、碳酸氢钠等。有 3篇文献[9,10,14]可同时提取出两组数据。研究对象均为患有血液肿瘤或实体肿瘤并需行化疗的患者,从化疗开始使用洗必泰或对照方法预防口腔黏膜炎。纳入研究的基本特征,见表2。
2.1 口腔黏膜炎OAG评分 共有4篇文献采用OAG评分评估口腔黏膜炎的程度[8-10,13],其中2篇文献可同时提取出两组数据。异质性检验显示各研究间无异质性存在(P=0.69,I2=0%),采用固定效应模型。洗必泰组共有283例,对照组252例。Meta分析结果显示,洗必泰组OAG评分与对照组比较,差异无统计学意义(P=0.56,WMD 0.12,95%CI:-0.28~0.51),见图1。其中1篇文献洗必泰浓度为0.2%[13],而其余文献中洗必泰浓度均为0.12%,去除该篇文献后再进行整合分析,结果无改变(P=0.29,WMD 0.09,95%CI:-0.08~0.27)。
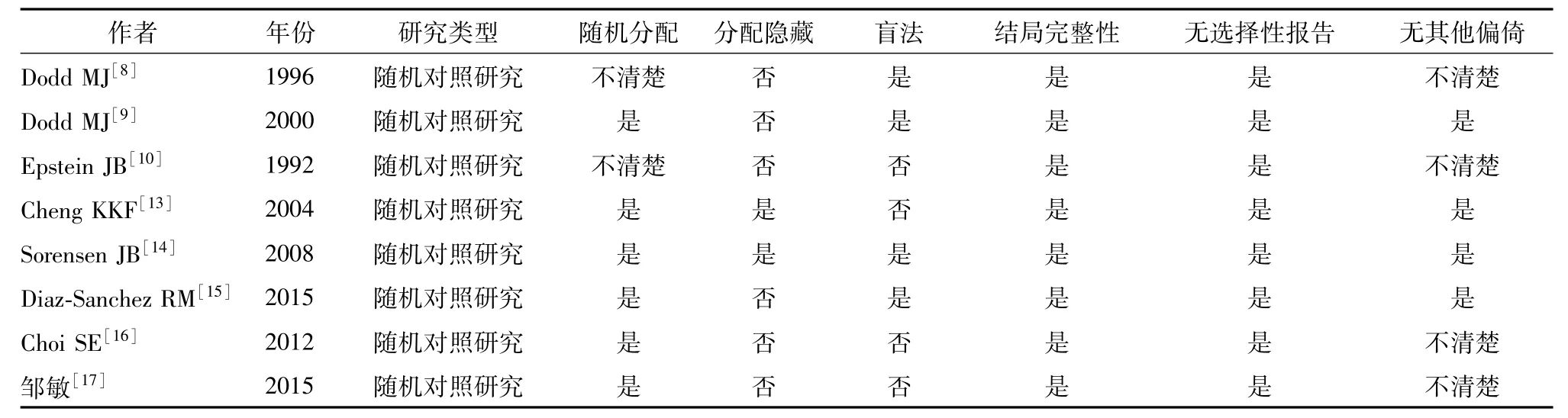
表1 纳入文献质量评价

表2 纳入研究基本特征
2.2 口腔黏膜炎WHO分级 共有4篇文献采用WHO分级评估口腔黏膜炎的程度[14-17],其中1篇文献可同时提取出两组数据。异质性检验显示各研究间存在异质性(P=0.0005,I2=80%),采用随机效应模型。洗必泰组共有199例,对照组185例。Meta分析结果显示,洗必泰组WHO分级重度口腔黏膜炎患者比例(74/199,37.2%)与对照组(62/185,33.5%)比较,差异无统计学意义(P=0.79,OR 1.57,95%CI:0.51~4.81),见图2。其中1篇文献洗必泰为0.2%凝胶[15],而其余文献中洗必泰均为0.1%漱口液,去除该篇文献后再进行整合分析,结果没有改变(P=0.34,OR 1.78,95%CI:0.54~5.89)。

图1 洗必泰与对照组对于预防化疗患者口腔黏膜炎的对比(OAG评分)
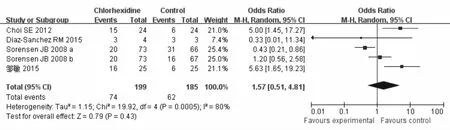
图2 洗必泰与对照组对于预防化疗患者口腔黏膜炎的对比(WHO分级)
3 讨论
化疗患者极易发生口腔黏膜的损伤而导致口腔黏膜炎。口腔黏膜的损伤主要是由于化疗药物直接作用于口腔黏膜而引起,多发生于化疗后的第4~7天。病变主要以局部发红、水肿以及溃疡形成为特点,可以产生痛感,甚至影响进食。1项多中心的调查研究显示,化疗患者口腔黏膜炎的发生与住院时间、住院费用甚至病死率均有相关性[18]。因此,有效预防化疗患者口腔黏膜炎的发生是改善化疗患者生活质量的重要措施之一。为减少化疗患者口腔黏膜炎的发生,减轻炎症程度,缓解症状,各种漱口水、凝胶等被广泛应用。洗必泰是临床常用的药物,可以有效预防牙菌斑的积聚和牙龈炎的发生[19]。并且,由于它具有较强的口腔表面结合能力及广谱抗菌活性,被广泛用于口腔黏膜炎的预防,但其确切作用仍然存在较大争议,多为经验性用药,而仅有的几项临床研究也多为小样本研究。此外,应用洗必泰漱口还存在着一些缺点,如牙齿变色、口感较苦甚至会产生不愉快的感觉,系统评价洗必泰对化疗患者口腔黏膜炎的预防作用,对更好的预防化疗患者的口腔黏膜炎,提高患者生活质量,改善预后,具有重要意义。本研究将既往多项研究进行整合分析,系统探讨洗必泰在预防化疗诱发口腔黏膜炎中的应用价值,为临床诊疗提供理论依据。除了洗必泰之外,临床常用的预防化疗患者口腔黏膜炎的药物还包括碳酸氢钠、0.9%氯化钠、苄达明、制霉菌素、洋甘菊等,但临床应用不如洗必泰广泛,并且临床疗效不确切。
本研究中口腔黏膜炎的程度采用公认的OAG评分和WHO分级进行评价。尽管两种评价系统均为公认的评级方法,但评价条目存在较大区别,无法进行整合,故各自进行。此外,应用不同的评级方法对结果进行评估,也可以避免评级方法本身的局限性,使结果更加全面、可靠。
纳入的研究中,除1篇洗必泰剂型为凝胶外[15],其余研究中洗必泰均为漱口液,这与临床应用习惯相符合。而对照组则包括混合液、碳酸氢钠溶液以及安慰剂(清水、生理盐水)等不同药物和剂型。合并分析显示,无论应用OAG评分还是应用WHO分级进行评估,洗必泰对化疗患者口腔黏膜炎的预防作用均与对照组无明显差异,并不优于对照组。纳入研究中洗必泰浓度包括0.1%、0.12%、0.2%,将相同浓度、相同剂型的研究进行整合分析,洗必泰与对照组相比仍没有差异。因此,临床上对于因各种恶性肿瘤需要行化疗的患者,洗必泰在预防口腔黏膜炎方面并不具有优势,需要积极探索其他的预防方法,以预防口腔黏膜炎的发生,减轻患者症状,提高患者生活质量,改善患者预后。
对漱口液的使用方法进行分析发现,在漱口次数相同的情况下,每次漱口60 s的OAG评分要明显低于每次漱口20 s[8-10],提示延长漱口时间或增加漱口次数有可能增加疗效,但由于缺乏对比,无法进行进一步分析,将来还需要随机对照试验进行研究。
本研究的优点在于采用了不同的评估方法,避免了单纯一种评估方法的局限性,使结果更加全面、可靠。对不同浓度、不同剂型的洗必泰进行亚组分析,更有利于临床应用。同时,纳入研究均为随机对照试验,研究质量有保障,使整合结果更加可靠。当然,我们的研究也存在一定的局限性。各研究中纳入的患者包括血液系统肿瘤及各部位的实体肿瘤,原发疾病的不同导致化疗方案各异,化疗药物、化疗时限及联合用药等差异均会对口腔黏膜炎的程度产生影响。因此,将来的研究中需要针对特定的肿瘤及化疗方案进行分析,以寻求最适合的预防方案。
本研究显示,洗必泰并不能有效预防化疗患者口腔黏膜炎的发生,临床上需要积极探索其他的预防方法,针对不同的肿瘤及化疗方案也需要进一步的大样本随机对照试验来探讨。
[1]Potting CM, Uitterhoeve R, Op Reimer WS, et al. The effectiveness of commonly used mouthwashes for the prevention of chemotherapy-induced oral mucositis:a systematic review[J].Eur JCancer Care(Engl),2006,15(5):431-439.
[2]McGuire DB,Fulton JS,Park J,et al.Systematic review of basic oral care for the management of oral mucositis in cancer patients[J].Support Care Cancer,2013,21(11):3165-3177.
[3]Soares AF,Aquino AR,Carvalho CH,et al.Frequency of oral mucositis and microbiological analysis in children with acute lymphoblastic leukemia treated with 0.12%chlorhexidine gluconate[J].Braz Dent J,2011,22(4):312-316.
[4]Eilers J,Berger AM,Petersen MC.Development,testing,and application of the oral assessment guide[J].Oncol Nurs Forum,1988,15(3):325-330.
[5]Quinn B,Potting CM,Stone R,et al.Guidelines for the assessment of oral mucositis in adult chemotherapy,radiotherapy and haematopoietic stem cell transplant patients[J].Eur J Cancer,2008,44(1):61-72.
[6]Higgins JPT,Green S.Cochrane handbook for systematic reviews of interventions[M].Hoboken,NJ:Wiley-Blackwell,2008.
[7]王家良.临床流行病学:临床科研设计、测量与评价[M].上海:上海科学技术出版社,2009:258-259.
[8]Dodd MJ,Larson PJ,Dibble SL,et al.Randomized clinical trial of chlorhexidine versus placebo for prevention of oral mucositis in patients receiving chemotherapy[J].Oncol Nurs Forum,1996,23(6):921-927.
[9]Dodd MJ,Dibble SL,Miaskowski C,et al.Randomized clinical trial of the effectiveness of 3 commonly used mouthwashes to treat chemotherapy-induced mucositis[J].Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2000,90(1):39-47.
[10]Epstein JB,Vickars L,Spinelli J,et al.Efficacy of chlorhexidine and nystatin rinses in prevention of oral complications in leukemia and bone marrow transplantation[J].Oral Surg Oral Med Oral Pathol,1992,73(6):682-689.
[11]Pitten FA,Kiefer T,Buth C,et al.Do cancer patients with chemotherapy-induced leukopenia benefit from an antiseptic chlorhexidine-based oral rinse? A double-blind, blockrandomized,controlled study[J].J Hosp Infect,2003,53(4):283-291.
[12]Rutkauskas JS, Davis JW. Effects of chlorhexidine during immunosuppressive chemotherapy.A preliminary report[J].Oral Surg Oral Med Oral Pathol,1993,76(4):441-448.
[13]Cheng KK,Chang AM,Yuen MP.Prevention of oral mucositis in paediatric patients treated with chemotherapy;a randomised crossover trial comparing two protocols of oral care[J].Eur J Cancer,2004,40(8):1208-1216.
[14]Sorensen JB,Skovsgaard T,Bork E,et al.Double-blind,placebocontrolled,randomized study of chlorhexidine prophylaxis for 5-fluorouracil-based chemotherapy-induced oral mucositis with nonblinded randomized comparison to oral cooling(cryotherapy)in gastrointestinal malignancies[J]. Cancer,2008,112(7):1600-1606.
[15]Diaz-Sanchez RM,Pachón-Ibá?ez J,Marín-Conde F,et al.Double-blind,randomized pilot study of bioadhesive chlorhexidine gel in the prevention and treatment of mucositis induced by chemoradiotherapy of head and neck cancer[J].Med Oral Patol Oral Cir Bucal,2015,20(3):e378-e385.
[16]Choi SE, Kim HS. Sodium Bicarbonate Solution versus Chlorhexidine Mouthwash in Oral Care of Acute Leukemia Patients Undergoing Induction Chemotherapy:A Randomized Controlled Trial[J].Asian Nurs Res(Korean Soc Nurs Sci),2012,6(2):60-66.
[17]邹敏.碳酸氢钠溶液与洗必泰溶液对急性白血病诱导化疗患者口腔护理对比研究[J].河北医科大学学报,2015,(4):401,423,427.
[18]Sonis ST,Oster G,Fuchs H,et al.Oral mucositis and the clinical and economic outcomes of hematopoietic stem-cell transplantation[J].JClin Oncol,2001,19(8):2201-2205.
[19]Nashwan AJ.Use of chlorhexidine mouthwash in children receiving chemotherapy:a review of literature[J].J Pediatr Oncol Nurs,2011,28(5):295-299.
R473.78
B
1009-8399(2017)05-0067-05
2015-03-18
路燕燕(1985—)女,护师,本科,主要从事临床护理。
(本文编辑:张梦佳)
