微陶材料对铀的吸附特性
2017-11-01朱锐之李力力朱留超赵立飞赵永刚
朱锐之,李力力,朱留超,赵立飞,赵永刚
中国原子能科学研究院 放射化学研究所,北京 102413
微陶材料对铀的吸附特性
朱锐之,李力力,朱留超,赵立飞,赵永刚*
中国原子能科学研究院 放射化学研究所,北京 102413
采用多种方法对微陶材料进行了表征,分别采用静态法和动态法研究了溶液pH、吸附时间、铀初始浓度、吸附剂用量、解吸流速、吸附剂粒度等因素对微陶材料吸附铀的影响;探究了微陶材料对模拟放射性废水的处理能力。实验结果表明,扫描电镜显示微陶材料底部为层状结构,能谱显示其表面主要成分为铝元素,还有少量(质量分数6.00%)的铁元素;XRD结果显示微陶材料表面无明显Fe的衍射峰;红外光谱显示微陶材料对铀进行了吸附;当pH=5、吸附时间为1 h、铀初始质量浓度为100 μg/L、微陶材料用量为50 mg时,微陶材料对铀的吸附率达到95%以上;动态法中流速和粒度对吸附影响较小;微陶材料对铀的吸附等温线符合Freundlich吸附等温模型;采用准二级反应动力学模型描述微陶材料对铀的吸附,吸附过程主要为化学吸附;微陶材料对模拟放射性废水中铀的吸附率均在90%以上,对锶、铯也有一定的吸附能力。
微陶材料;铀;吸附性能;放射性废水
随着核能工业的快速发展,经济、高效的放射性废物处理新技术越来越受到关注。自日本福岛核事故以后,核安全以及核废物处理的重要性凸显。开展放射性废物处理新技术以及相关的机理研究,对放射性废物减量化、预防放射性污染、保障社会的核生态环境安全、促进核事业的健康良性发展,具有重要的社会意义、经济意义和环境意义[1]。
吸附法[2]是常见的放射性废物处理方法,具有操作简单、铀去除率高且经济高效等优点。其中,选择合适的吸附剂是吸附法研究的关键。现有的吸附剂存在吸附量低、吸附速率慢和选择性吸附效果不强等缺点,因此寻找新型功能化吸附剂具有非常重要的现实意义[3-4]。
目前纳米技术的应用一直是研究的热点领域,但纳米铁易团聚,影响其对金属的去除效果。而以广泛存在于土壤中的粘土矿物为支撑材料合成复合材料——粘土矿物纳米零价铁,具有大比表面积、微孔量高、耐热性好、表面酸性强等特点,能改善团聚现象,增大表面积,大大提高吸附性能[5]。微陶材料就是依此合成的新型介孔复合材料,常以天然硅藻土和高岭土为主要原料、将其高温烧结并进行除硅处理后制得的陶瓷颗粒经负载纳米零价铁得到,是一种价格较低而且吸收效率较好的材料[6]。
本工作拟采用材料表征、动态法和静态法相结合等方式,探究微陶材料吸附铀的特性和机理,并通过微陶材料对模拟废水样品的吸附验证,为微陶材料应用于含铀废水吸附以及铀污染扩散应急预防等方面提供思路。
1 实验部分
1.1主要试剂与仪器
微陶材料(60目,粒径0.250 mm),苏州微陶重金属过滤科技有限公司;铀标准溶液,GBW(E)080173,核工业北京化工冶金研究院;六水氯化锶(S110516)、氯化铯(无水级),上海阿拉丁生化科技股份有限公司;硝酸(BV-Ⅲ级),北京化学试剂研究所;硝酸钠,分析纯,西陇化工股份有限公司。
JSM6360LV型扫描电镜,JEOL(日本电子)公司;Sc7620型镀金仪,英国Quorum Technologies公司;双面碳导电胶带,NISSIN EM.CO.LTD,日本Tokyo公司;D8 Advance型X射线粉末衍射仪,德国Bruker公司;Nicolet IS50型傅里叶变换红外光谱仪,美国Thermo Fisher公司;XP205型电子天平,精度0.000 1 g,美国Mettler Toledo公司;SHA-C型水浴恒温振荡器,常州市华普达教学仪器有限公司;Nexion 300Q型四级杆质谱仪,美国Perkin Elmer公司。
1.2材料表征实验
将微陶材料用导电双面胶粘在铝桩上,真空下溅射一层极薄的金膜,置入扫描电镜进行微观形貌分析。
把微陶材料颗粒均匀洒入样品架中,使颗粒在窗孔内摊匀堆好,采用压片法制作试片。X射线衍射测试条件:Cu Kα射线(波长为0.154 06 nm),扫描范围10°~90°,扫描速率0.05°/s,以连续扫描方式收集数据。
使用KBr压片法制样,将制得的压片置入红外光谱仪进行测量。
1.3静态法实验
将100 mg/L的标准铀溶液用去离子水稀释1 000倍以配制初始质量浓度为100 μg/L的铀溶液,取500 mL置于锥形瓶中,使用硝酸和氢氧化钠调节pH值,加入微陶材料,封盖后放入恒温水浴振荡器中,在常温下以200 r/min振荡。反应达到平衡后取样,用微孔滤膜对溶液进行过滤,取滤液测铀浓度。按照相同步骤,保持pH值不变,分别改变吸附时间、铀初始浓度、微陶材料用量,研究主要的影响因素。
计算得到平衡吸附量qeq、吸附率和吸附分配系数Kd。这三者可用来衡量吸附剂的吸附性能,三者的计算方法分别如式(1)、(2)、(3)所示。
qeq=(ρ0-ρeq)V/m
(1)
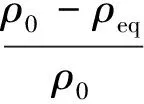
(2)
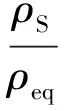
(3)
其中:ρ0为放射性核素的起始质量浓度;ρeq为实验终态放射性核素的质量浓度;V为静态吸附实验所用溶液的体积,mL;m为所用微陶材料的质量,g;ρS为单位质量微陶材料中铀的质量,mg/g。
吸附等温线实验:在一系列锥形瓶中分别加入50 mg微陶材料和500 mL pH=5的铀初始浓度不同的含铀水溶液,在恒温水浴振荡器中充分振荡6 h至达到吸附平衡时,测量铀的平衡浓度,计算出平衡吸附量,并采用Langmuir和Freundlich吸附等温线来拟合微陶材料吸附铀的等温吸附过程。
模拟放射性废水实验:根据文献[7]模拟制备压水堆乏燃料后处理过程中产生的放射性废水,分别在微陶材料适量和过量以及废水中是否含盐等多种条件下进行变量实验,得到对应条件下微陶材料对废水中核素的吸附率和吸附分配系数。
1.4动态法实验
称取5.00 g微陶材料,去离子水浸泡后湿法装柱,玻璃色层柱两端用聚四氟乙烯丝填充。在一定流速下分别用不同pH值的铀溶液淋洗,隔一定时间收集一定体积的流出液,用四级杆质谱测其中的铀浓度,将流出液和初始溶液中铀的浓度对比计算即可得到对应吸附率。同样的步骤下保持浓度不变,通过分别调节溶液流速、改变材料粒度重复上述实验过程,进行流速、pH值及材料粒度对吸附铀的影响程度研究。
2 结果与讨论
2.1材料表征

图1 微陶材料的SEM图Fig.1 SEM results of micro ceramic materials
2.1.1扫描电镜表征 电子显微镜是研究介孔材料微观结构形貌最直接最常用的手段,借助扫描电镜(SEM)可观察介孔材料的宏观形貌和规整性。通过扫描电镜表征所得结果示于图1。由图1可看出,微陶材料在底部呈层状结构,是较好的负载纳米零价铁的载体,在上部颗粒较大,比较杂乱,微观形貌没有明显的规律性。能谱结果示于图2。如图2所示,由于进行了除硅处理,在微陶材料表面没有检测到黏土矿物中常见的硅元素,主要成分是铝元素,还有少量(质量分数6.00%、原子百分数2.99%)的铁元素。
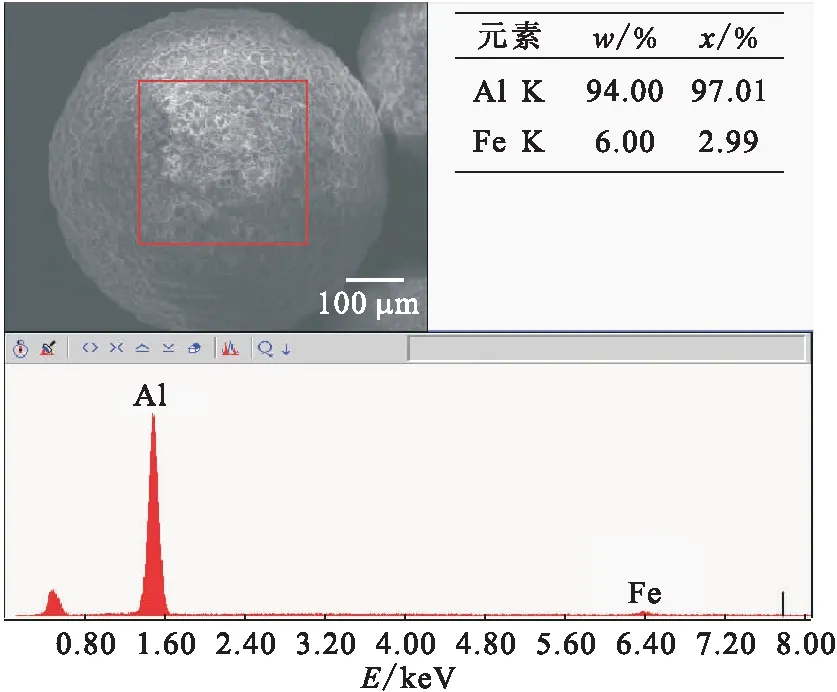
图2 微陶材料的能谱图Fig.2 Energy spectrum of micro ceramic materials
2.1.2X射线衍射分析结果 微陶材料的X射线衍射分析结果示于图3。从图3可以看出,没有明显的Fe的衍射峰,推测纳米零价铁在载体表面分散较好,没有形成达到XRD检测限的大颗粒,分散度好,有助于微陶材料对铀的吸附。
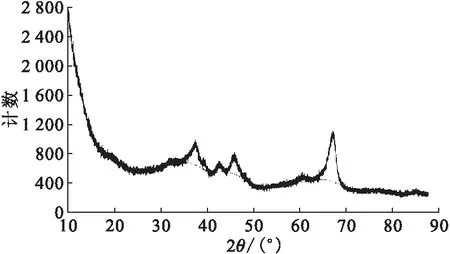
图3 微陶材料的XRD衍射图Fig.3 XRD results of micro ceramic materials
2.1.3红外光谱分析结果 微陶材料吸附铀前后的红外光谱图示于图4。其中,曲线1是吸附前的曲线,曲线2是吸附后的曲线。红外光谱区分为两个区域,波数1 300~4 000 cm-1之间为基团频率区,在该区基团与频率的对应关系比较明确;波数400~1 300 cm-1为指纹区,在该区谱带的特征归属不完全符合规律。从图4可以看出,在3 400~3 500 cm-1(吸附前为3 471 cm-1,吸附后为3 451 cm-1)处为羟基的伸缩振动峰,在1 640 cm-1处为H-O-H的弯曲振动峰[8],在1 385 cm-1处为微陶材料中Al-O-H的弯曲振动峰,吸附前曲线在559 cm-1处有Fe-O的伸缩振动峰[9],在吸附后发生了偏移,右移至525 cm-1处,峰形变尖,推测是吸附后H与O作用使Fe-O键长增加,导致伸缩振动减弱,从而引起波数减小。值得注意的是,吸附后曲线在426 cm-1处出现了新的峰,因为是在吸附铀后形成的,且400~700 cm-1之间是Fe-O、U4+-O的特征振动范围[10],推测有两种可能:一是零价铁与铀发生化学反应被氧化,形成Fe-O-H的弯曲振动峰或者U4+-O的伸缩振动峰,两者峰有重叠;二是零价铁表面的高度羟基化铁氧化膜有利于与铀形成Fe-O-U键,从而出现对应的Fe-O-U弯曲振动峰。从红外谱图上可以看出,微陶材料对铀进行了吸附,主要是由于材料表面负载的纳米铁的作用引起的。

1——吸附前,2——吸附后图4 微陶材料的红外光谱图Fig.4 FTIR results of micro ceramic materials
2.2静态法实验
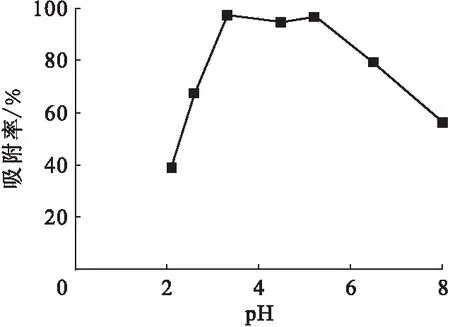
图5 溶液pH对微陶材料吸附铀效果的影响 Fig.5 Effect of pH on adsorption of micro ceramic materials

2.2.2吸附时间的影响 微陶材料用量50 mg、溶液pH=5、铀初始质量浓度为100 μg/L、溶液体积为500 mL时,吸附时间对铀吸附效果的影响示于图6。由图6可看出,微陶材料对铀的吸附率在1 h内随时间的增加而增大,在1 h时吸附率达到95%以上,吸附量达到平衡吸附量的95.2%。在1 h以后随着时间的增加吸附率缓慢增加,均稳定保持在95%以上。
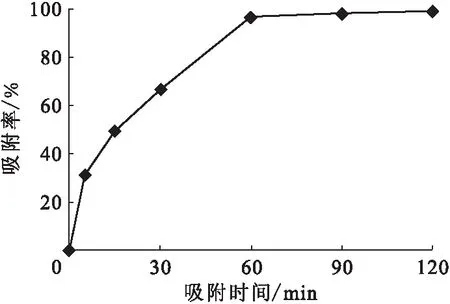
图6 吸附时间对微陶材料吸附铀效果的影响Fig.6 Effect of time on adsorption of micro ceramic materials
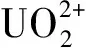
2.2.4微陶材料用量的影响 铀初始质量浓度为100 μg/L、溶液体积为500 mL、溶液pH=5、吸附时间为1 h时,微陶材料用量对铀吸附效果的影响示于图8。由图8可看出,当微陶材料用量达到50 mg时,对铀的吸附率达到95%以上,Kd>190 L/g,此时微陶材料对铀具有较好的吸附能力。随着微陶材料用量的不断增加,固相中铀的量逐渐增加,而固相和液相中铀的总量不变,因此其对铀的吸附率逐渐升高,理论推导与图8中的实验结果十分吻合。与此同时,从实验结果可以看出平衡吸附量随着微陶材料的用量增加而减少。
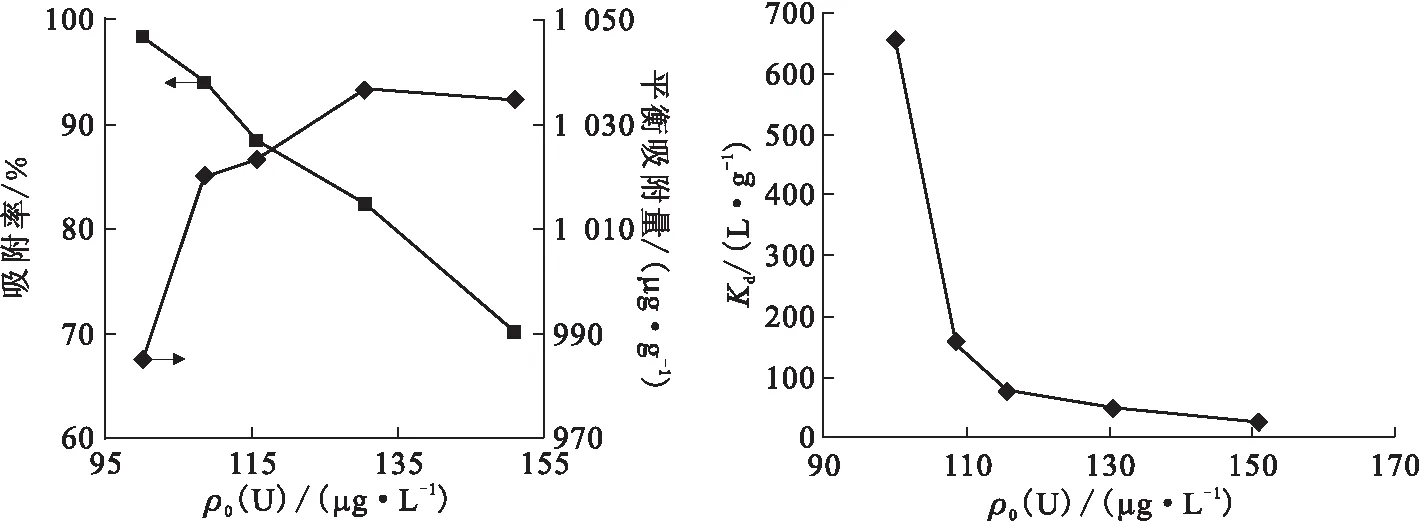
图7 铀初始质量浓度对微陶材料吸附铀效果的影响Fig.7 Effect of original concentration of uranium on adsorption of micro ceramic materials
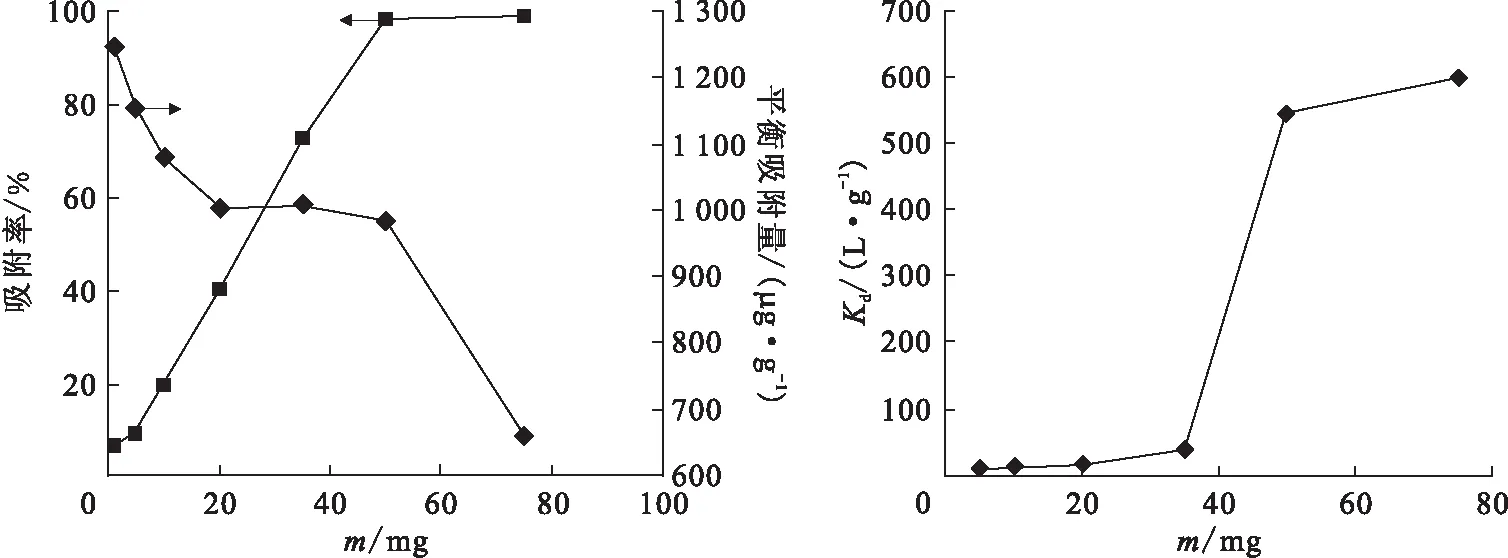
图8 微陶材料用量对其吸附铀效果的影响Fig.8 Effect of dosage of micro ceramic materials on adsorption
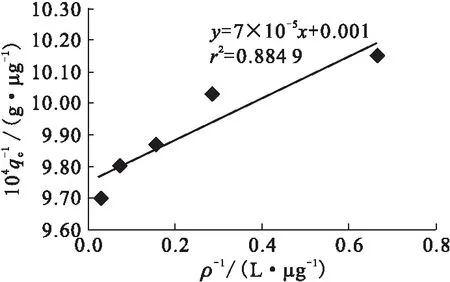
图9 微陶材料对铀的Langmuir吸附等温线Fig.9 Langmuir adsorption isotherm of micro ceramic materials on uranium
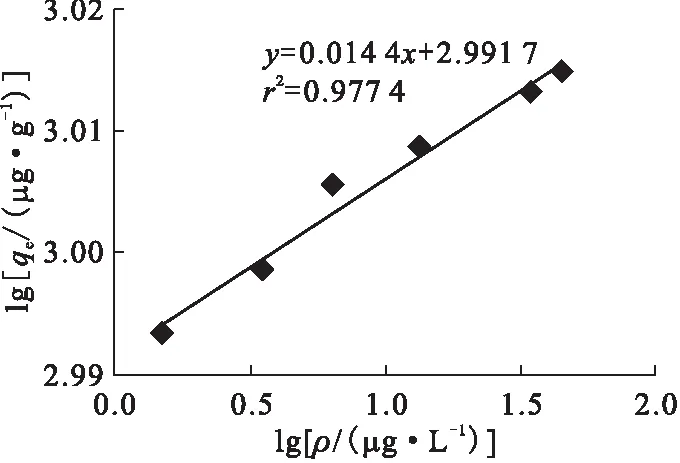
图10 微陶材料对铀的Freundlich吸附等温线Fig.10 Freundlich adsorption isotherm of micro ceramic materials of uranium
2.2.5微陶材料对铀的吸附等温线 溶液pH=5、吸附时间为6 h、溶液体积为100 mL、微陶材料用量为50 mg时,改变铀初始浓度,探究平衡吸附量与平衡浓度之间的关系。采用Langmuir和Freundlich吸附等温线来拟合微陶材料吸附铀的等温吸附过程,结果示于图9和图10。由图9、图10可知,微陶材料对铀的吸附与Lang-muir吸附等温模型拟合的相关系数为0.884 9,而与Freundlich吸附等温模型拟合的相关系数为0.977 4,因此,微陶材料对铀的吸附较好地符合Freundlich吸附等温模型。Freundlich方程是一个经验方程,没有Langmuir方程中单分子层吸附、所有吸附位点均相同、被吸附的粒子完全独立等假设条件,其方程形式线性化后如下所示:
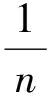

2.2.6微陶材料对铀的吸附动力学 固体吸附剂对溶液中溶质的吸附动力学过程可用准一级反应动力学模型和准二级反应动力学模型来进行描述。本研究采用准一级反应动力学模型和准二级反应动力学模型对微陶材料对铀的吸附过程进行拟合,结果示于图11和图12。由图11、12可以看出,准一级反应动力学模型对吸附过程进行拟合所得的相关系数为0.947 9,而准二级反应动力学模型对吸附过程进行拟合所得的相关系数为0.991 5,准二级反应动力学模型对微陶材料吸附铀过程的拟合结果明显好于准一级反应动力学模型,因此微陶材料吸附铀的过程可采用准二级动力学模型描述,可以推测吸附过程中,尽管外扩散和内扩散过程影响了吸附,但是化学吸附速率更慢,是整个吸附过程的决速步。

图11 吸附过程的准一级反应动力学模型Fig.11 Pseudo-first-order model of adsorption
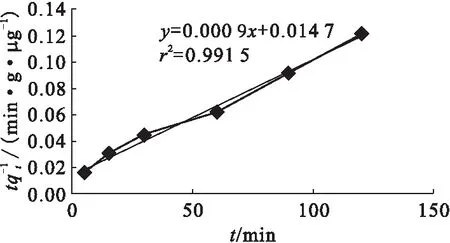
图12 吸附过程的准二级反应动力学模型Fig.12 Pseudo-second-order model of adsorption
2.3模拟放射性废水吸附实验
所配制的模拟放射性废水中铀、锶、铯的初始质量浓度分别为100、10、10 μg/L,溶液体积为100 mL,溶液pH=6.5,吸附时间为1 h,探究微陶材料对模拟废水中铀、锶、铯的吸附性能,结果列于表1。由表1看出,当微陶材料用量为静态法实验中所得出的50 mg时,用量为适量。在此条件下,微陶材料对铀的吸附率均达到90%以上,而对锶、铯的吸附率则很低,不到2%,显然微陶材料对铀的吸附性能更好。当有大量盐分存在时,吸附率与无盐分时的吸附率无明显区别,可见离子强度对微陶材料的吸附影响较小,这些金属离子也不会对吸附率造成影响。当微陶材料用量为200 mg时,用量为过量。在此条件下,微陶材料对铀、锶、铯的吸附率均在98%以上。因为在过量条件下,吸附位点充足,能充分吸附铀、锶、铯。同样,大量盐分对吸附率的影响较小。
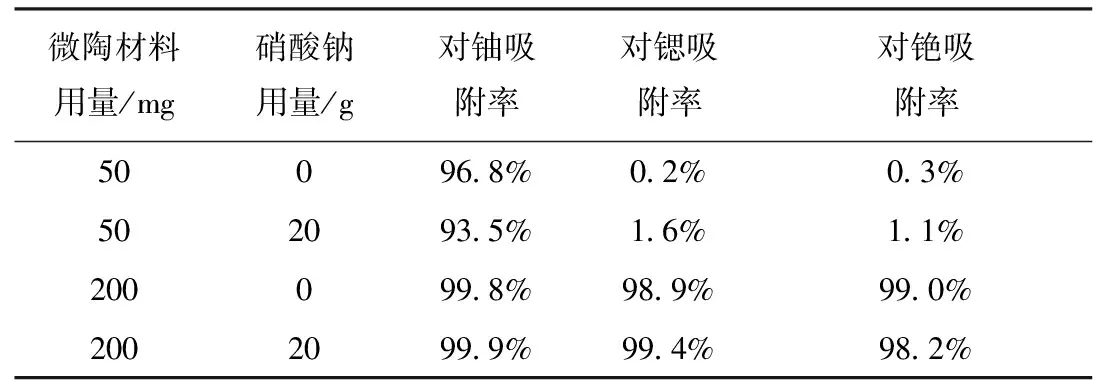
表1 微陶材料对模拟放射性废水的吸附实验结果Table 1 Experimental results of adsorption of simulated radioactive wastewater
2.4动态法实验
2.4.1pH的影响 称取5.00 g粒度为0.250 mm的微陶材料湿法装柱,在一定流速下分别用不同pH的铀溶液淋洗,隔一定时间收集一定体积的流出液,用四级杆质谱法测铀浓度,得到结果示于图13。由图13可看出,动态法的实验结果与静态法吻合较好,溶液pH对微陶材料吸附铀的效果影响也比较大。当溶液pH=2时,微陶材料对铀的吸附率较低,稳定在35%~45%之间;当溶液pH=5时,微陶材料对铀的吸附率稳定高效,吸附率接近100%,且吸附率随pH变化不大,可以认为微陶材料在此pH下吸附效果最好;当溶液pH=8时,微陶材料对铀的吸附率也比较低,在45%~55%之间。具体的原因与静态法类似。
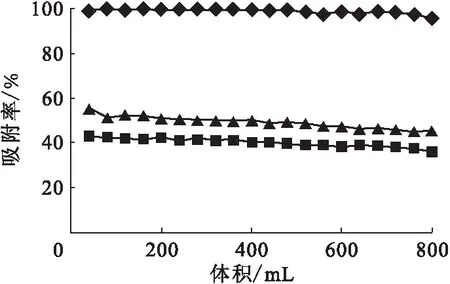
◆——pH=5,■——pH=2,▲——pH=8图13 溶液pH对微陶材料吸附铀效果的影响Fig.13 Effect of pH on adsorption of micro ceramic materials
2.4.2溶液解吸流速的影响 称取5.00 g粒度为0.250 mm的微陶材料湿法装柱,在不同解吸流速下用pH=5的铀溶液淋洗,隔一定时间收集一定体积的流出液,用四级杆质谱法测其中的浓度,得到结果示于图14。由图14可以看出,解吸流速对微陶材料吸附铀的影响比较小,在三种流速下吸附率均稳定高效,在95%以上。可见微陶材料对铀的吸附速率较快,图14中曲线互有交叉的原因可能是由于铀的量较小导致误差较大引起的。
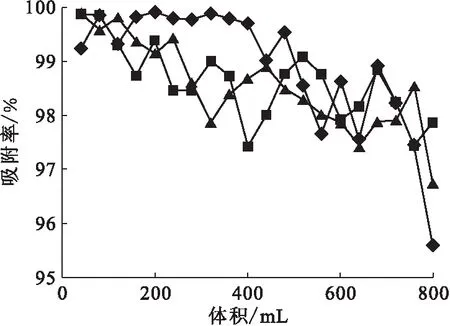
◆——5.0 mL/min,■——2.5 mL/min,▲——1.2 mL/min图14 溶液解吸流速对微陶材料吸附铀效果的影响Fig.14 Effect of flow velocity on adsorption of micro ceramic materials
2.4.3微陶材料粒度的影响 分别称取5.00 g不同粒度的微陶材料湿法装柱,在相同流速下用pH=5的铀溶液淋洗,隔一定时间收集一定体积的流出液,用四级杆质谱法测其中的浓度,得到结果示于图15。由图15可以看出,虽然粒径0.250 mm的微陶材料与溶液接触的表面积更大,但是由于微陶材料过量,因此粒径0.420 mm和0.250 mm的微陶材料的吸附率并无较大差别,均有较高的吸附率。图15中曲线互有交叉的原因可能是因为选取的材料粒径是平均值导致的误差较大。
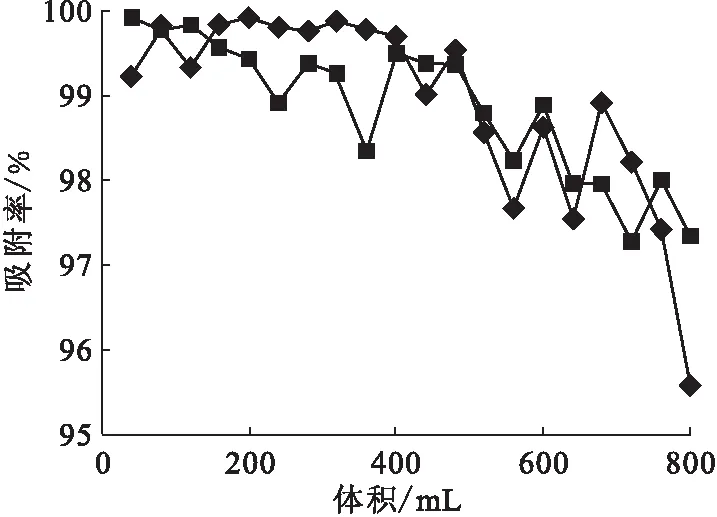
◆——粒径0.420 mm,■——粒径0.250 mm图15 吸附剂粒度对微陶材料吸附铀效果的影响Fig.15 Effect of granularity on adsorption of micro ceramic materials
3 结 论
(1) 采用了多种表征手段,其中扫描电镜结果表明微陶材料底部为层状结构,能谱显示其表面主要成分为铝元素,还有少量(质量分数6.00%)的铁元素;XRD结果显示微陶材料表面无明显Fe的衍射峰;红外光谱显示微陶材料对铀进行了吸附。
(2) 采用静态法和动态法相结合的手段研究了微陶材料对铀的吸附性能。当pH=5、吸附时间为1 h、铀初始质量浓度为100 μg/L、溶液体积为500 mL、微陶材料用量为50 mg时,微陶材料吸附铀的效率达到95%以上,解吸流速和粒度对吸附影响较小;微陶材料吸附铀的吸附等温线符合Freundlich吸附等温模型;采用准二级反应动力学模型描述微陶材料对铀的吸附,吸附过程主要为化学吸附。
(3) 微陶材料对模拟放射性废水中铀的吸附效率高达90%以上,当吸附剂过量时对废水中的锶、铯也有很好的吸附效果。
[1] 王建龙,刘海洋.放射性废水的膜处理技术研究进展[J].环境科学学报,2013,33(10):2639-2656.
[2] Valsala T P, Sonavane M S, Kore S G. Treatment of low level radioactive liquid waste containing appreciable concentration of TBP degraded products[J]. J Hazard Mater, 2011, 196: 22-28.
[3] 李宏宇,申利红,张乐,等.咪唑型功能离子液体合成及其对铀(Ⅳ)的萃取[J].原子能科学技术,2014,48(3):390-394.
[4] 刘淑娟,李金英,罗明标,等.甲醛改性多壁碳纳米管吸附铀的性能研究[J].原子能科学技术,2013,47(1):7-13.
[5] 徐佳丽.蒙脱石负载纳米零价铁对水溶液中铀的去除研究[D].武汉:中国地质大学,2014.
[6] Dong Liangjie. Iron coated pottery granules for arsenic removal from drinking water[J]. J Hazard Mater, 2009(168): 626-632.
[7] 郑宇.回收铀过程废水中放射性锶的去除研究[D].北京:中国原子能科学研究院,2015.
[8] 卢涌泉,邓振华.实用红外光谱解析[M].北京:电子工业出版社,1989.
[9] 闻辂,梁婉雪,章正刚,等.矿物红外光谱学[M].重庆:重庆大学出版社,1988.
[10] 张淑苓.利用红外光谱法研究铀和含铀矿物[J].世界核地质科学,1986(3):25-28.
[11] 李坤全,郑正,蒋剑春,等.铅在棉秆基活性炭上的吸附动力学与热力学[J].环境科学,2010,31(5):1402-1408.
[12] Bachmaf S, Merkel B. Sorption of uranium(Ⅵ) at the clay mineral-water interface[J]. Envir Earth Sci, 2011, 63(5): 925-934.
[13] 刘娟,陈迪云,张静,等.铀在凹凸棒石上的吸附特性与机制研究[J].环境科学,2012,33(8):2889-2894.
[14] 彭国文,肖方竹,孙世雄,等.功能化碳基磁性介孔材料的制备及其对铀的吸附性能[J].原子能科学技术,2015,49(12):2138-2144.
[15] 王洁,黄晓乃,刘迎九,等.壳聚糖吸附铀的机理探讨[J].金属矿山,2009(5):149-151.
AdsorptionofUranium(Ⅵ)onMicroCeramicMaterials
ZHU Rui-zhi, LI Li-li, ZHU Liu-chao, ZHAO Li-fei, ZHAO Yong-gang*
China Institute of Atomic Energy, P. O. Box 275(8), Beijing 102413, China
Multiple material symbolization methods were used to symbolize micro ceramic materials. Static and dynamic methods were used to study how different factors such as pH value, adsorption time, original uranyl concentration, dosage of adsorbent, flow velocity and particle size of adsorbent affect the adsorbability of micro ceramic materials. The processing capacity for simulative radioactive wastewater was also explored. Experimental results show that bottom of micro ceramic materials is stratified under SEM; micro-energy spectrum reveals that main components of the surface are Al and a small amount of Fe (percentage of quality is 6.00%); XRD result shows there is no detectable diffraction peak of Fe on the surface; FTIR shows ceramic materials does adsorb uranium. When pH is 5, adsorption time is 1 h, original mass concentration of uranium is 100 μg/L, and dosage of micro ceramic materials is 50 mg, the adsorption efficiency for uranium can reach 95% or even higher. In dynamic methods, flow velocity and particle size are proved to be less influential. The adsorption isotherm keeps good agreement with Freundlich isothermal adsorption model. Pseudo-second-order model was used to describe the process of adsorption, which is mainly chemical adsorption. Micro ceramic materials has an adsorption rate of more than 90% on uranium in simulated radioactive wastewater, it also adsorbs strontium and cesium.
micro ceramic materials; uranium; adsorbability; radioactive wastewater
TL941.1
A
0253-9950(2017)05-0377-08
2016-05-10;
2016-06-01
朱锐之(1990—),男,江苏扬州人,硕士研究生,分析化学专业,E-mail: 646487996@qq.com
*通信联系人:赵永刚(1966—),男,河南开封人,博士,研究员,核燃料循环与材料专业,E-mail: zhaoyg@ciae.ac.cn
10.7538/hhx.2017.YX.2016051
