HPLC法同时测定康复新液中两种成分的含量
2017-10-19石金凤张臻宋芹章津铭傅超美何瑶刘彬
石金凤,张臻*,宋芹,章津铭*,傅超美,何瑶,刘彬
·炮制制剂·
HPLC法同时测定康复新液中两种成分的含量
石金凤1,张臻1*,宋芹2,章津铭1*,傅超美1,何瑶1,刘彬3
目的:建立同时测定康复新液中尿苷和黄嘌呤含量的方法。方法:采用HPLC法,Diamonsil C18(250 mm×4.6 mm,5 μm)色谱柱,甲醇-水(5:95) 作为流动相,于254 nm波长下检测,流速1.0 mL.min-1,柱温30 ℃。结果:尿苷、黄嘌呤分别在0.10~3.96 μg.mL-1(r2=0.9998)、0.52~20.80 μg.mL-1(r2=0.9992)浓度范围内线性关系良好,平均加样回收率分别为97.86%(RSD=1.25%)、97.39%(RSD= 0.68%)。测定5批次康复新液中尿苷和黄嘌呤的含量范围分别为1.69~1.76 μg.mL-1、12.76~13.06 μg.mL-1,说明各批样品质量较均一。结论:本文建立的方法精密度高、重复性好,操作简便快速,可用于康复新液的质量控制。
HPLC;尿苷;黄嘌呤;康复新液
康复新液是昆虫美洲大蠊(Periplaneta americanaL.)干燥虫体的乙醇提取物制成的口服和外用制剂。该药临床应用广泛,效果良好,副作用小,具有通利血脉、养阴生肌等作用。内服可用于瘀血阻滞,胃痛出血,胃,十二指肠溃疡;以及阴虚肺痨,肺结核的辅助治疗。外用可用于金疮,外伤,溃疡,瘘管,烧伤,烫伤,褥疮之创面[1]。同时它对化疗性疾病、妇科疾病,小儿手足口等病也具有较好疗效[2~4]。康复新液中化学成分较复杂,主要为多元醇类、核苷类、肽类、粘糖氨酸、多种氨基酸等小分子类成分[5],这对康复新液的质控带来困难,其现有质量标准[6]仅以测定总氨基酸含量来评价制剂品质的高低,难以达到全面质量控制的目的。
核苷类成分为美洲大蠊的抗炎成分之一[7],同时核苷类物质不仅是构成核酸 RNA、DNA单体的前体,也是生物氧化、能量代谢中的能源物质和抗病毒、抗肿瘤药物的中间体,具有重要的生物活性[8]。其中,尿苷和黄嘌呤是主要的核苷成分,常被用于作为动物药的质控指标,如地龙[9]、海马[10]、冬虫夏草[11]等。目前尚未见有将尿苷、黄嘌呤两种成分作为康复新液质量控制方式的报道,因此本文旨在采用高效液相色谱仪(HPLC)建立一种同时测定康复新液尿苷和黄嘌呤的分析方法,用以更好地控制和完善康复新液的质量标准。
1 仪器与试药
1.1 仪器
DL-720D数控超声波清洗器(上海之信仪器有限公司);UPH-I-10T优普超纯水器(成都超纯科技有限公司);BS200S电子天平(北京赛多利斯天平有限公司);DZKW-4电子恒温水浴锅(北京中兴伟业仪器有限公司);SHZ-D(III)循环水式真空泵(巩义市予华仪器有限责任公司);SSI series 1500高效液相色谱仪(美国SSI公司);Diamonsil C18(250×4.6mm,5μm)色谱柱。
1.2 试药
康复新液(规格:100mL/瓶 四川好医生攀西药业有限责任公司 批号分别为:140230、140905、150353、150723、151001);尿苷对照品(成都瑞芬思生物科技有限公司,批号:N-025-150730);黄嘌呤对照品(成都瑞芬思生物科技有限公司,批号:H-069-150729);甲醇(色谱纯,美国Fisher公司);超纯水(成都超纯科技有限公司);三氯甲烷、盐酸等其他试剂均为分析纯(成都科龙化学试剂厂)。
2 方法与结果
2.1 色谱条件
Diamonsil C18色谱柱(250 mm×4.6mm,5μm);流动相为甲醇-水(5∶95);体积流量1.0 mL.min-1;检测波长254 nm;柱温30 ℃;进样量10 μL。
2.2 混合对照品溶液的制备
取尿苷和黄嘌呤对照品,精密称定,置50 mL容量瓶中,加水溶解并稀释至刻度,制成浓度分别为尿苷19.80 μg.mL-1、黄嘌呤104.00 μg.mL-1的混合对照品贮备液。
2.3 供试品溶液的制备
精密量取康复新液20 mL,加三氯甲烷12 mL、1 mol.L-1盐酸3.4 mL,搅拌至析出的晶体完全溶解,置分液漏斗中,弃去三氯甲烷,再用三氯甲烷8 mL,洗涤,弃去三氯甲烷,重复两次。精密量取6 mL,置10 mL容量瓶中,加水稀释至刻度,摇匀,用0.22 μm微孔滤膜滤过,取续滤液,即得。
2.4 阴性样品溶液的制备
按处方比例制成不含康复新的阴性样品,并按”2.3”供试品溶液的制备项下方法制得阴性样品溶液。
2.5 线性关系的考察
精密吸取上述对照品贮备液0.05,0.1,0.25,0.5,1,2 mL,分别至10 mL容量瓶中,加水稀释至刻度,摇匀,制得不同浓度梯度标准溶液。分别吸取10 μL进样,以对照品浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,计算回归方程。见表1。
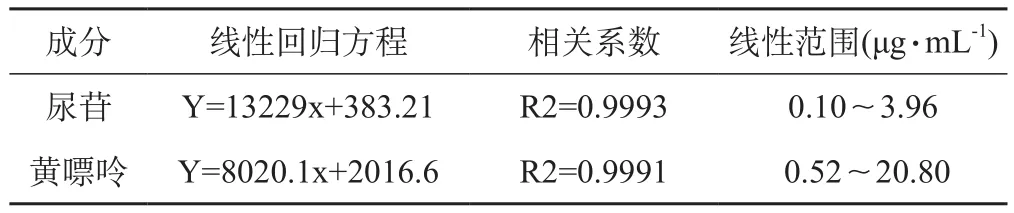
表1 线性范围考察结果
2.6 专属性试验
取阴性样品溶液、混合对照品溶液、供试品溶液各10 μL,分别注入液相色谱仪,记录色谱图,按“2.1”项下色谱条件测定,见图1。
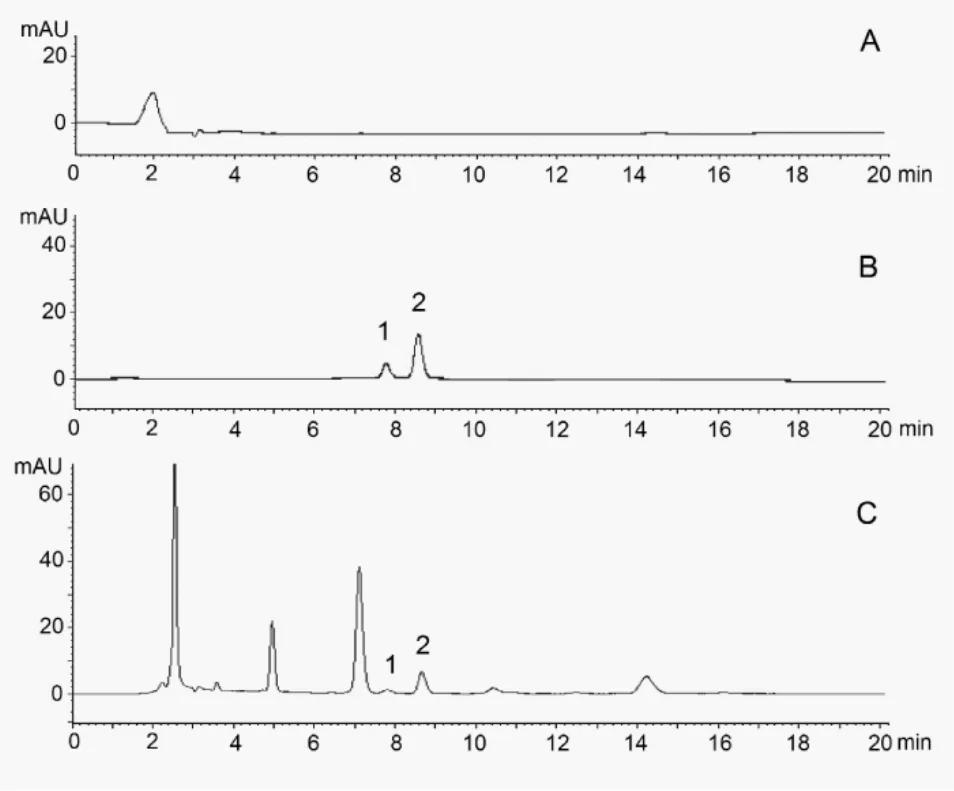
图1 阴性样品(A)、混合对照品(B)和康复新液样品(C)的HPLC色谱图
可见阴性样品溶液在此条件下在与尿苷、黄嘌呤对照品相同的保留时间处未见干扰峰出现,表明其专属性良好。
2.7 精密度试验
取对照品溶液,连续进样6次,每次10 μL,以峰面积计算,见表2。尿苷、黄嘌呤的RSD分别为:1.64%、1.81%,实验结果表明仪器精密度良好。
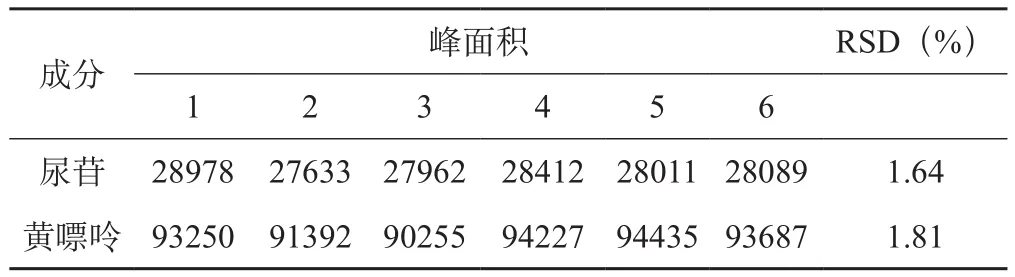
表2 精密度试验数据表
2.8 重复性试验
取同一批号的供试品溶液20 mL,共6份,按照供试品溶液的制备和检测方法制备样品溶液并进行检测,结果见表3。尿苷、黄嘌呤的平均含量分别为1.72 μg.mL-1、13.06 μg.mL-1,RSD分别为1.32%、1.92%,表明本方法重复性良好。
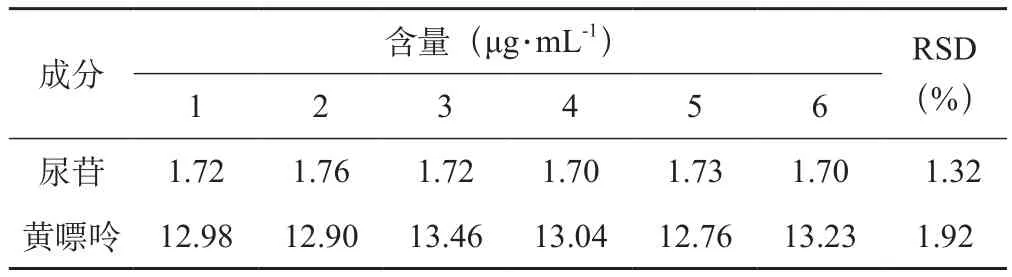
表3 重复性试验数据表
2.9 稳定性试验
取同一份康复新液供试品溶液,按试验所得方法,分别于0,2,4,6,8,10,12 h取10 μL进样,结果见表4。供试品溶液中尿苷、黄嘌呤的峰面积RSD 分别为1.69%、1.90%,表明供试品溶液在12 h内稳定性良好。

表4 供试品稳定性试验数据表
2.10 加样回收率试验
精密称取尿苷对照品1.0 mg加入10 mL容量瓶中,加水定容至刻度,作为尿苷对照品储备液;精密称取黄嘌呤对照品5.5 mg加入50 mL容量瓶中,加水定容至刻度,再吸取上述溶液4 mL至10 mL容量瓶中,加水定容至刻度,作为黄嘌呤对照品储备液。精密量取康复新液样品10 mL共9份,每组分别加入一定量的尿苷对照品储备液和黄嘌呤对照品储备液,使其含量分别达到样品中尿苷和黄嘌呤含量的80%、100%、120%,每个浓度做3份,均照样品含量测定项下制备供试液,再按“2.1”项下色谱条件测定,计算加样回收率,结果见表5。
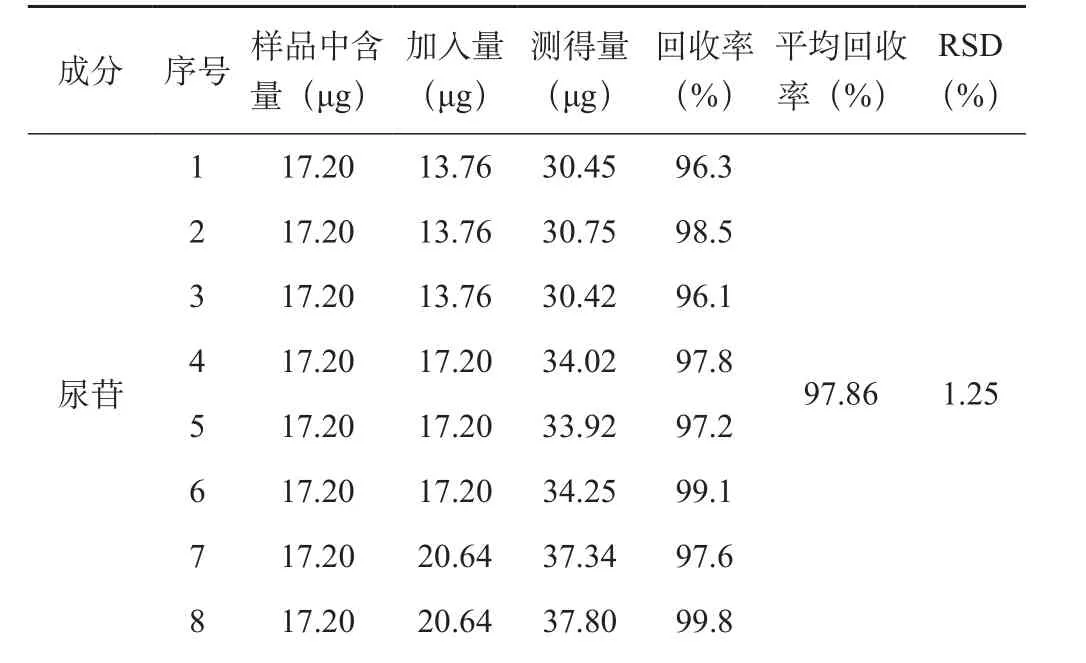
表5 加样回收率试验结果 (n=6)
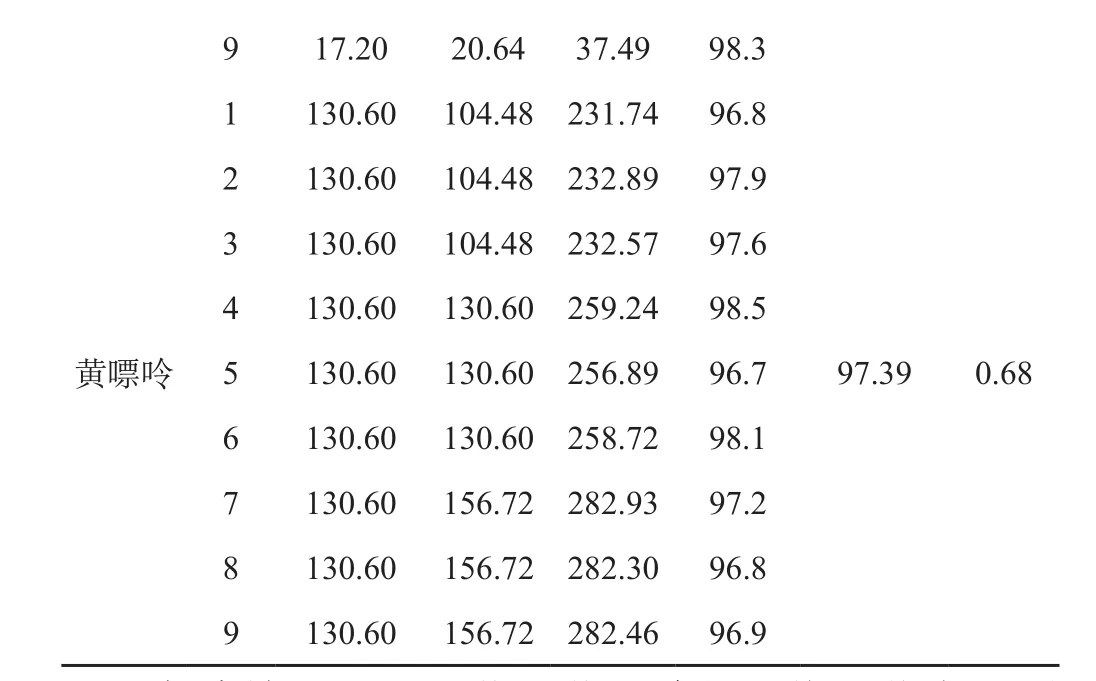
9 17.20 20.64 37.49 98.3 1 130.60 104.48 231.74 96.8黄嘌呤2 130.60 104.48 232.89 97.9 3 130.60 104.48 232.57 97.6 4 130.60 130.60 259.24 98.5 5 130.60 130.60 256.89 96.7 6 130.60 130.60 258.72 98.1 7 130.60 156.72 282.93 97.2 8 130.60 156.72 282.30 96.8 9 130.60 156.72 282.46 96.9 97.39 0.68
实验结果显示尿苷和黄嘌呤的平均回收率分别为97.86%、97.39%,RSD分别为1.25%、0.68%,表明所建立方法可满足实验要求。
2.11 样品含量测定
取5个批次的样品,按“2.3”项下方法制备溶液,按“2.1”项下色谱条件及方法测定样品中的尿苷和黄嘌呤的含量,结果见表6。

表6 5批康复新液样品含量测定结果(n=3)
实验结果表明,5批康复新液中尿苷的含量范围为1.69~1.76 μg.mL-1,黄嘌呤的含量范围为12.76~13.06 μg.mL-1,各批次中尿苷和黄嘌呤含量较均一、稳定。
3 讨论
康复新液中含一定的附加剂,如果样品不经处理,对尿苷和黄嘌呤含量测定会带来很大干扰,因此要除去溶液中的附加剂。通过多次考察试验,康复新液20 mL,加1 mol.L-1的盐酸3.4 mL,分别用三氯甲烷12 mL,8 mL,8 mL萃取洗涤三次即可。
在研究中,筛选了甲醇-水、甲醇-0.1%冰醋酸、含0.07%冰醋酸的3%甲醇溶液三个流动相系统;考察了甲醇-水(2:98)、甲醇-水(5:95)、甲醇-水(10:90)三个流动相比例;考察了0.6mL.min-1、0.8mL.min-1、1.0mL.min-1三个流速。结果表明:除了甲醇-水系统能实现将两种成分分离,其余流动相系统均不能实现对两种成分的分离。甲醇-水系统能够得到基线平稳、稳定性好、分离度好、色谱峰峰形较好的HPLC图谱。在流速小于1.0mL.min-1时,尿苷和黄嘌呤2种核苷类成分出峰时间稍长,峰宽较宽;而选择1.0mL.min-1的流速时,两种成分能够在10 min内快速同时分离。
本品为动物类中成药,其质量标准难以控制产品质量,目前康复新液质量标准[6]采用单一成分丙氨酸为对照品,对总氨基酸进行测定,利用茚三酮比色法,由于不同氨基酸所显颜色不尽相同,导致该法专属性不强,也不够准确;另一方面茚三酮显色不稳定,受外界及试剂因素的影响较大,且对环肽和内酰胺类化合物需特殊处理,操作较为复杂。采用 HPLC 法测定康复新液中尿苷和黄嘌呤的含量,具有精密度高,回收率和专属性好的优点,符合《中国药典》2015年版四部通则高效液相色谱法的各项要求,可作为提高康复新液质量标准的检测指标。
[1] 国家药品监督管理局国家药品标准[S]. WS3-B-3674-2000.
[2] 舒崇湘, 冉新泽, 程天民, 等. 全身放射损伤对皮肤伤口组织细胞的影响及康复新的促愈作用[J]. 中国临床康复, 2003,7(11): 1644.
[3] 王静. 康复新液治疗慢性宫颈炎的临床观察[J]. 中外健康文摘, 2007, 4(1): 29.
[4] 谢杨学, 何淑君. 康复新液治疗小儿手足口病疗效分析[J].现代预防医学, 2012, 39(1): 52.
[5] 焦春香, 刘光明, 周萍. 天然药物康复新的研究进展[J]. 时珍国医国药, 2008, 19(11): 2623.
[6] 中国人民共和国卫生部. 中华人民共和国卫生部药品标准中药成方制剂. 第19册[S]. 北京:人民卫生出版社,1998:176.
[7] 肖小琴, 汪世平, 徐绍锐, 等. 美洲大蠊提取物抗炎、镇痛作用的实验研究[J].中国病原生物学杂志, 2007, 2(2): 140.
[8] 冷玲颖, 蔡志强, 孙铁民. 核苷类抗病毒前药的研究进展[J].中国药物化学杂志, 2008, 18(4): 310.
[9] 李伟, 文红梅, 钟进, 等. HPLC测定地龙中次黄嘌呤、黄嘌呤、尿嘧啶、尿苷的含量[J]. 中药材, 1996, 19(12): 625.
[10] 赵晓莉, 崔小兵, 狄留庆, 等. HPLC法测定海马中次黄嘌呤、黄嘌呤的含量[J]. 中药材, 2002, 25(10): 716.
[11] 靳丹虹, 梁芳慧, 董丽丹, 等. RP-HPLC 测定冻干鹿茸中的尿嘧啶和尿苷[J]. 现代科学仪器, 2013, (2): 141.
( 责任编辑:何瑶)
Simultaneous determination of two components in Kangfuxin Ye by HPLC/
SHI Jin-feng1, ZHANG Zhen1, SONG Qin2,ZHANG Jin-ming1, FU Chao-mei1, HE Yao1, LIU Bin3//(1. College of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, Sichuan;2.College of bioengineering, Chengdu University, Chengdu 610106, Sichuan;3. Sichuan good doctor Pharmaceutical Group Co., Ltd, chengdu 610075, Sichuan).
Objective:To establish a method to detect xanthine and uridine content in Kangfuxin Ye at the same time.Method:HPLC method was established. The separation was carried out on a Diamonsil C18column (250 mm×4.6 mm, 5 μm)at 254 nm. The mobile phase was consist of MeOH and H2O (5:95) at the fl ow rate of 1 mL.min-1, and the column temperature was set at 30℃.Result:The linear ranges of uridine and xanthine were 0.10~3.96 μg.mL-1(r2=0.9993) and 0.52~20.80 μg.mL-1(r2=0.9991), respectively. The average recoveries of uridine and xanthine were 97.86% (RSD=1.25%) and 97.39% (RSD=0.68%),respectively. The method was applied in the determination of 5 batches of Kangfuxin Ye. The content ranges of uridine and xanthine were1.69~1.76 μg.mL-1and 12.76~13.06 μg.mL-1, respectively, which suggested that the quality of each batch was uniform.Conclusion:The method has high precision, good repeatability, simple and rapid operation. It can be used to control the standard of Kangfuxin Ye.
HPLC; uridine; xanthine; Kangfuxin Ye
R 283.6
A
1674-926X(2017)02-010-04
成都中医药大学科技发展基金(030018052)
1.成都中医药大学药学院,四川 成都 611137;2. 成都大学生物工程学院,四川 成都 610106;3.四川好医生药业集团有限公司,四川 成都 610075
石金凤(1993-),女,汉,重庆垫江人,中药药剂学专业在读硕士研究生,研究方向为中药新制剂, Email:191006842@qq.com
1.张臻(1987-),女,汉,四川乐山人,讲师,中药药剂学, Email:zhangzhendr@126.com 2.章津铭(1987-),男,汉,四川内江人,讲师,中药药剂学, Email:zhangjinming1987@126.com
2016-11-24
