腹腔镜胰腺中段切除术技巧与体会
2017-09-21徐晓武郭卫东牟一平张炳远
周 斌,徐晓武,郭卫东,牟一平,张炳远
(1.青岛大学附属医院,山东 青岛,266003;2.浙江省人民医院)
·专家论坛·
腹腔镜胰腺中段切除术技巧与体会
周 斌1,徐晓武2,郭卫东1,牟一平2,张炳远1
(1.青岛大学附属医院,山东 青岛,266003;2.浙江省人民医院)
胰腺中段切除术(central pancreatectomy,CP)又称为节段性胰腺切除术(segmental pancreatectomy)、中间段胰腺切除术(median pancreatectomy,middle segment pancreatectomy)等。优点是保留了更多的正常胰腺组织、胃肠道、胆道结构及脾脏,降低了术后患者胰腺内外分泌不足、感染、免疫、凝血功能等异常的风险。但由于同时存在胰头、胰体尾两个切端,加之胰中段肿瘤右侧切缘大于胰体尾部肿瘤,使得CP胰瘘发生率高于胰十二指肠切除术及远端胰腺切除术[1]。因此,如何最大化发挥器官保留的优点,降低胰瘘、出血等并发症发生率是讨论的热点,目前随着微创外科、术后加速康复理念的发展,腹腔镜胰腺中段切除术(laparoscopic central pancreatectomy,LCP)越来越多的应用于临床,由于LCP术后胰肠吻合技术、胰腺残端关闭技术与胰瘘发生密切相关,本文现就这些方面作一讨论。
1 LCP的指征范围
LCP主要适于胃十二指肠动脉左侧、近脾静脉与肠系膜下静脉汇合处之间,即胰颈部与胰颈体交界部的良性病变或低度恶性肿瘤。对于恶性肿瘤尤其导管腺癌,节段切除往往达不到根治性要求,不宜行CP。其次,肿瘤较大,残留的远端胰腺<5 cm或萎缩(可术中测量剩余远端胰腺长度,如果太少保留意义不大,可直接行胰体尾切除术);胰体尾血供单独来自胰横动脉(胰背动脉左支),切除中段胰腺,胰体尾有缺血可能者均为手术禁忌。
2 LCP与开腹胰腺中段切除术(open central pancreatectomy,OCP)的比较
关于LCP与OCP的临床研究较少,这与CP本身较其他术式开展少、而LCP开展更少有关,最近有研究回顾性分析了LCP与OCP,认为LCP是安全、可行的,在术后胰瘘率、并发症发生率及死亡率方面两种术式差异无统计学意义,但在术中出血量、术后康复、生活质量方面LCP更具优势[2-3]。笔者认为,LCP同其他腹腔镜胰腺术式一样,在大规模的胰腺腹腔镜中心LCP的效果不次于OCP,未来期望有大样本量的前瞻性研究进一步证明LCP的优势。
3 LCP手术切除要点
我们通常采用五孔法,V字形分布,也有学者采用四孔法,主刀立于患者右侧。分离大网膜至小网膜囊腔,可将胃后壁用2-0 VICRYL悬吊暴露胰颈,术中超声探头可通过12 mm主操作孔定位肿瘤。胰腺下缘解剖显露肠系膜上静脉,一般在此处左侧有一支小静脉进入胰腺,分离胰腺背侧门静脉,建立胰后隧道,丝带悬吊胰腺,将胰腺向头侧牵拉,向胰腺远近端游离约2 cm,再用切割闭合器切断封闭近端胰腺。继续向胰腺远端分离脾动、静脉,一般会有1支胰背动脉从脾动脉发出、1~2支胰腺静脉汇入脾静脉,需要仔细处理。远端胰腺可先用超声刀缓慢仔细切开,发现管道结构后换用剪刀切断,以方便寻找胰管,胰管周围胰腺断面出血可用电钩、双极电凝或4-0 Prolene线缝扎止血。标本可经脐下切口或绕脐稍延长切口取出。术中冰冻病理检测胰腺远、近端切缘。如果胰颈部肿瘤较大压迫门静脉难以显露,我们通常采用easy first原则,先切断肿瘤远端胰腺,显露脾静脉,自左至右沿脾静脉分离至门静脉,减少盲目分离胰腺下缘时造成的出血等并发症。
4 LCP消化道重建方式
常见的LCP消化道重建方式有两种:胰胃吻合与胰肠吻合,以胰肠吻合为主。胰胃吻合相对便捷,不破坏消化道结构,且胃壁血供丰富,利于吻合口愈合,胃酸降低胰酶活性,减少了胰瘘的风险[4]。但也有研究表明[5],胰胃吻合患者进食时间、住院时间延长,胃排空障碍发生率高于胰肠吻合。尽管目前临床主流仍是胰肠吻合,而且胰肠吻合术后患者在内外分泌功能方面的长期预后结果更佳,但目前两者在胰瘘[6]、出血[7]方面差异并无统计学意义,随着胰胃吻合技术的推广与熟练相信其应用也会逐渐增多。
胰肠吻合在各种消化道重建中最具挑战性,文献报道的吻合方式很多,胰瘘的发生率相差并不大,胰腺质地、胰管直径是胰瘘发生的两个关键因素。目前胰肠吻合方式多采取结肠后行远端胰腺-空肠Roux-en-Y吻合,根据术者习惯可采用4-0 Prolene或VICRYL缝线行单层或双层、间断或连续缝合胰腺断端与空肠前后壁,或胰腺断端与空肠贯穿间断缝合,胰管对黏膜或套入式等方法,由于Prolene缝线针眼小并带有一定的弹性、张力好,有的术者更喜欢用其进行胰肠吻合。多数临床医生认可,最熟悉、最熟练的吻合方式即是适合自己的,有经验的术者可能在具体情况下稍稍改变自己的吻合方式,但总体吻合习惯基本不变。
目前多数学者认为,胰管对空肠黏膜优于胰腺空肠套入吻合,可根据胰管直径用5-0 PDS缝线缝合胰管4~6针,但前者的操作较后者复杂很多,尤其在腹腔镜下学习推广的难度要大于后者,由于多数LCP患者胰管扩张不明显,这更增加了胰管吻合的难度,需要在精准缝合尤其各种运针方式上多加练习。其中胰管支撑管的置入对胰瘘发生也至关重要,临床多采用硅胶脑室引流管作为支撑管,可将支撑管缝合或捆绑固定在胰管上,目前还可借助术前薄层CT扫描判断胰管直径,结合日趋成熟的3D打印技术,利用生物材料术前制作合适管径的支撑管。
5 LCP胰腺近端残端处理方式
关于胰腺残端闭合方式也有不少争论,有学者认为闭合器不优于手工缝合[8-9],也有研究认为闭合器并不次于手工缝合[10],并能降低胰瘘发生率[11]。切割闭合器封闭在LCP、腹腔镜胰体尾切除术中应用广泛,笔者认为术中应根据胰腺实质的厚度选用合适钉仓,通常多选用白色或蓝色钉仓,闭合压榨胰腺过程缓慢,针对压榨时间,不同术者经验多为90~120 s。切除完毕可沿钉线施加数枚钛夹或用4-0 Prolene连续缝合,以防止胰瘘或出血。采取何种手术方式应视胰头残端情况决定,有时胰头残端过于宽大不能使用闭合器,就需要手工缝合[12]。手工缝合技术在开腹CP、胰体尾切除术中还有不少单位采用,对于胰管,可单独结扎或“8”字缝扎,近端胰腺一般先切成鱼嘴状然后间断缝合关闭[13],以利宽大胰腺进行缝合。一些学者认为,间断缝合胰腺残端优于交锁缝合,后者可减少缝合侧血供,从而导致胰瘘发生率升高。此外,还有学者采用“nonclosure”技术[14]、LigaSure[15]关闭残端,虽然效果良好,但未在临床广泛应用,尚待进一步研究。封闭的残端可喷涂纤维蛋白胶水,以进一步减少胰瘘与出血。
有学者提出难以直接缝合时需要行空肠胰腺“Ω”形吻合[8],即不关闭胰腺近切端,而分别行胰腺近、远端-空肠Roux-en-Y所谓的“双吻合”。由于Oddi括约肌的存在,近端胰腺残端胰管压力较远端残留胰腺高,胰瘘也常发生于非吻合的近端残端[16],因此双吻合在引流胰液、减轻胰管压力方面具有优势[17],但增加了一个吻合口尤其对于LCP而言,增加了手术复杂性及吻合口瘘的发生率[12]。这种双吻合目前在国际报道较少,在LCP中报道更为罕见,尚不能做出合理评判。
我们通常在胰肠吻合结束后于胰肠吻合口远端采用类似“Ω”形吻合的方法,将空肠浆膜面与封闭的近端胰腺残端用4-0 Prolene间断缝合3~4针(图1),这样可减轻空肠与远端胰腺吻合口张力[2],这种方式与Buchler教授关于远端胰腺切除术后胰腺残端的处理方式类似(用游离带蒂的肝圆韧带或胃肠浆膜面与胰腺残端缝合)[13],既可以覆盖胰腺残端预防分支小胰管渗漏,减少术后胰瘘的发生,又可通过浆膜层加固缝合胰腺残端,并将残端与后方血管隔离,减少术后出血的可能,但具体效果尚待进一步随机对照研究结果。
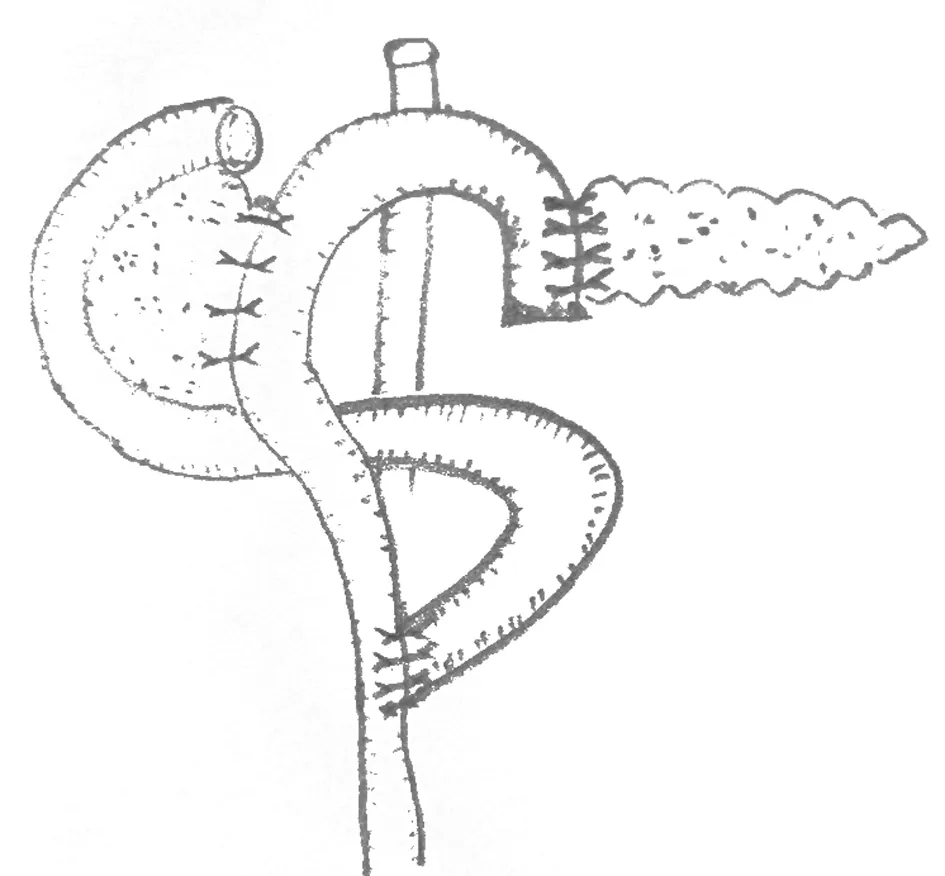
图1 LCP胰肠吻合、空肠浆膜面与封闭的近端胰腺残端缝合示意图
6 结 语
LCP手术本身在技术上要求较高,兼具腹腔镜胰头十二指肠切除术与保留脾脏远端胰腺切除术的技术要点,施行LCP的确增加了外科医生的操作难度,但随着腹腔镜技术水平的提高及胰腺周围解剖的熟练掌握,相信可跨越LCP高峰。此外,多观摩高水平腹腔镜操作,不仅可快速通过学习曲线,还可增强自己完成腹腔镜胰腺手术的信心。最重要的是适合LCP的患者预后好,具有合理的长期预期寿命,因此,制定、推广标准的LCP手术程序可使这些患者受益更大,进一步改善其生活质量与治疗效果。
[1] Beger HG,Siech M,Poch B,et al.Limited surgery for benign tumours of the pancreas:a systematic review[J].World J Surg,2015,39(6):1557-1566.
[2] Zhang RC,Zhang B,Mou YP,et al.Comparison of clinical outcomes and quality of life between laparoscopic and open central pancreatectomy with pancreaticojejunostomy[J].Surg Endosc,2017 Apr 19.[Epub ahead of print]
[3] Song KB,Kim SC,Park KM,et al.Laparoscopic central pancreatectomy for benign or low-grade malignant lesions in the pancreatic neck and proximal body[J].Surg Endosc,2015,29(4):937-946.
[4] 苗毅,蒋奎荣,徐泽宽.中段胰腺切除治疗胰腺良性或低度恶性肿瘤[J].中国实用外科杂志,2008,28(5):346-349.
[5] Ferrone CR,Warshaw AL,Rattner DW,et al.Pancreatic fistula rates after 462 distal pancreatectomies:staplers do not decrease fistula rates[J].J Gastrointest Surg,2008,12(10):1691-1697.
[6] 陈金水,胡先贵,金钢,等.切割闭合器在胰体尾切除术中的应用[J].肝胆胰外科杂志,2013,25(1):13-15.
[7] Okano K,Kakinoki K,Yachida S,et al.A simple and safe pancreas transection using a stapling device for a distal pancreatectomy[J].J Hepatobiliary Pancreat Surg,2008,15(4):353-358.
[8] 陈实,沈柏用,邓侠兴,等.胰腺中段切除术后胰瘘分析[J].中华外科杂志,2010,48(16):1201-1205.
[9] Hassenpflug M,Hinz U,Strobel O,et al.Teres Ligament Patch Reduces Relevant Morbidity After Distal Pancreatectomy (the DISCOVER Randomized Controlled Trial)[J].Ann Surg,2016,264(5):723-730.
[10] Kitagawa H,Ohta T,Tani T,et al.Nonclosure technique with saline-coupled bipolar electrocautery in management of the cut surface after distal pancreatectomy[J].J Hepatobiliary Pancreat Surg,2008,15(4):377-383.
[11] Hartwig W,Duckheim M,Strobel O,et al.LigaSure for pancreatic sealing during distal pancreatectomy[J].World J Surg,2010,34(5):1066-1070.
[12] Boggi U,Amorese G,De Lio N,et al.Central pancreatectomy with inframesocolic pancreatojejunostomy[J].Langenbecks Arch Surg,2012,397(6):1013-1021.
[13] Francone E,Berti S,Celoria GM,et al.Double pancreaticojejunostomy in pure laparoscopic central pancreatectomy:an uncommon reconstructive strategy[J].Minerva Chir,2016,71(2):156-158.
[14] Abood GJ,Can MF,Daouadi M,et al.Robotic-assisted minimally invasive central pancreatectomy:technique and outcomes[J].J Gastrointest Surg,2013,17(5):1002-1008.
[15] Venara A,de Franco V,Mucci S,et al.Central pancreatectomy:comparison of results according to the type of anastomosis[J].J Visc Surg,2012,149(2):e153-158.
[16] Clerveus M,Morandeira-Rivas A,Picazo-Yeste J,et al.Pancreaticogastrostomy versus pancreaticojejunostomy after pancreaticoduodenectomy:a systematic review and meta-analysis of randomized controlled trials[J].J Gastrointest Surg,2014,18(9):1693-1704.
[17] Watanabe M,Usui S,Kajiwara H,et al.Current pancreatogastrointestinal anastomotic methods:results of a Japanese survey of 3109 patients[J].J Hepatobiliary Pancreat Surg,2004,11(1):25-33.
1009-6612(2017)08-0574-03
10.13499/j.cnki.fqjwkzz.2017.08.574
2017-07-02)
