基于甘油二酯塑性脂肪的结晶特性和相容性研究
2017-09-16王晓晨徐怀义
杨 雪,刘 尊,宋 佳,王晓晨,张 宁,徐怀义,汪 勇
(1.暨南大学食品科学与工程系,暨南大学-萨斯喀切温大学“油料生物炼制与营养”联合实验室,广州 510632;2.广州市微生物研究所 广州工业微生物检测中心,广州 510663; 3.广州嘉德乐生化科技有限公司,广州 510630)
油脂化学
基于甘油二酯塑性脂肪的结晶特性和相容性研究
杨 雪1,2,刘 尊1,宋 佳1,王晓晨1,张 宁1,徐怀义3,汪 勇1
(1.暨南大学食品科学与工程系,暨南大学-萨斯喀切温大学“油料生物炼制与营养”联合实验室,广州 510632;2.广州市微生物研究所 广州工业微生物检测中心,广州 510663; 3.广州嘉德乐生化科技有限公司,广州 510630)
在鼓泡式反应器中,利用Lipozyme 435催化棕榈液油甘油解合成棕榈液油甘油二酯(POL-DAG),并通过分子蒸馏获得DAG含量达82.6%的POL-DAG。利用差示扫描量热仪及脉冲核磁共振仪分析由山茶油(CO)、棕榈油硬脂(PS)和POL-DAG组成的塑性脂肪的结晶特性和相容性。结果表明:混合物的熔点、结晶起始点和结晶焓随CO含量的增加而降低,随PS和POL-DAG含量的增加而升高;当CO、PS与POL-DAG以1∶1∶1混合时相容性最差,而以4∶1∶1混合时相容性最好,其次是1∶4∶1和1∶1∶4。
甘油二酯;脂肪酶;塑性脂肪;结晶特性;相容性
甘油二酯(DAG)是由两分子脂肪酸和一分子甘油形成的结构脂质,具有1, 3-DAG和1, 2(2, 3)-DAG两种异构体,二者比例约为7∶3[1]。DAG作为天然存在于油脂中的微量成分,含量通常不足10%,是一类广泛应用于食品、化工、医药、化妆品等行业的多功能添加剂[2-3]。富含DAG(含量高于80%)的功能性烹调油可防止肥胖症的发生[4-5]。2000年,DAG通过美国食品药品管理局(FDA)的食品安全审查,被批准为公认安全食品[6]。除了用作烹调油,DAG也作为食品成分用于一些油脂产品中,如蛋黄酱、沙拉酱、人造黄油、起酥油、巧克力和冰淇淋等[7]。2016年8月,DAG被国家卫计委批准为新食品原料。
一般而言,塑性脂肪[8]的塑性取决于固体脂肪含量(SFC)、脂肪的晶型及熔化温度范围。市场上商业化的塑性脂肪产品主要有黄油、人造奶油、起酥油、巧克力和冰激凌等。固体脂肪中的饱和脂肪酸和反式脂肪酸与肥胖及心血管疾病密切相关,因此如何减少固体脂肪的使用,同时不降低食品专用油脂的品质成为油脂工业的重大挑战。
将棕榈油硬脂作为基料油制备的人造奶油、起酥油等具有较宽的塑性范围,是我国塑性脂肪制品中的主要成分[9]。山茶油由于具有90%以上的不饱和脂肪酸可降低塑性脂肪的饱和度并增强产品的塑性[10]。棕榈液油甘油二酯(POL-DAG)的功能特性赋予塑性脂肪抑制脂肪积累、降低餐后血糖等功能,且有研究表明1, 3-DAG的熔点比含有相同脂肪酸组成的TAG高10℃左右,在TAG产品中添加DAG可在保持SFC的前提下减少产品中含饱和脂肪酸的TAG,故可用DAG替代或者部分替代固体脂肪应用于食品专用油脂中[7,11-13]。
油脂的相容性会影响油脂产品的品质及货架期,相容性差的油脂混合后得到的食品专用油脂会出现起砂、析油及酪化性下降等问题[14]。油脂加工产品的物理性质在很大程度上依赖于油脂的结晶特性,因此了解并改善油脂的结晶行为在油脂加工产品中具有重要的意义。本研究以一定比例将POL-DAG与山茶油和棕榈油硬脂混合并对其结晶特性和相容性进行研究,为DAG作为功能性食品专用油脂基料的应用开发提供理论基础。
1 材料与方法
1.1 试验材料
1.1.1 原料与试剂
棕榈油硬脂(熔点约为45℃)、棕榈液油:广州美晨集团股份有限公司;山茶油:市售金龙鱼油茶籽油;Lipozyme 435:固定化脂肪酶,酶活力为10 U/mg,诺维信中国生物技术有限公司;甘油、正己烷:分析纯,天津市富宇精细化工有限公司。
1.1.2 仪器与设备
鼓泡式反应器、MD-80型分子蒸馏设备:广州汉维机电有限公司;Agilent 7820A气相色谱仪:美国安捷伦科技有限公司;DSC1型差示扫描量热仪,梅特勒-托利多公司;NM-2型核磁共振分析仪:上海纽迈电子科技有限公司。
1.2 试验方法
1.2.1 POL-DAG的酶法制备
采用鼓泡式反应器制备粗POL-DAG。在500 mL烧杯中加入棕榈液油及甘油(摩尔比为1∶20),并加入4% Lipozyme 435(以底物质量计)。搅匀后倒入鼓泡式反应器的进样高位槽预热,待反应器的恒温水浴装置达到80℃时,将物料放入反应器中反应2.5 h。反应结束后,收集反应液,静置30 min后,得到上层油层和下层甘油层。收集上层油层为粗POL-DAG。
1.2.2 POL-DAG的纯化
采用两步分子蒸馏分离纯化甘油解产物中的POL-DAG。第一步,在蒸馏压力0.5~1 Pa、蒸发面温度200℃、冷却水温度60℃、进料温度80℃、刮膜电机转速300 r/min条件下,除去游离脂肪酸和单甘酯(MAG)。第二步,将第一步所得重相在蒸馏压力0.1~0.5 Pa、蒸发面温度250℃,其他条件不变时所得轻相即为较纯的POL-DAG。
1.2.3 甘油酯组成分析
采用高温气相色谱测定原料油及POL-DAG的甘油酯组成。取样品50.0 mg,用正己烷定容至5.0 mL后用0.45 μm过滤膜过滤。参照Wang等[15]所用气相色谱条件:DB-1ht型毛细管柱(15 m × 0. 25 mm × 0.1 μm);氢火焰离子化检测器;进样量0.5 μL,分流比40∶1;进样口压力108.3 kPa,载气为氮气,分析采用恒流模式;程序升温为50℃保持1 min,以50℃/min的速率升温至100℃,以80℃/min升至220℃,以30℃/min升至290℃,再以50℃/min升至330℃保持2 min,最后以50℃/min的速率升至380℃保持3 min。
1.2.4 甘油酯脂肪酸组成分析
利用气相色谱测定原料油及POL-DAG的脂肪酸组成。样品经甲酯化(方法参照GB / T 17376—2008)后,进行气相色谱分析。采用DB-wax型毛细管柱(10 m×0.1 mm×0.1 μm);进样量0.5 μL,分流比为40∶1;载气为氮气;进样口、检测器温度均为240℃;升温程序为初始温度100℃,以10℃/min的速率升温至220℃保持2 min,再以40℃/min的速率升温至240℃保持4 min。
1.2.5 塑性脂肪的制备
将山茶油、棕榈油硬脂、POL-DAG以一定的比例混合,制成塑性脂肪样品。
1.2.6 塑性脂肪结晶熔化性质分析
利用差示扫描量热仪分析塑性脂肪样品的结晶熔化性质。精确称取样品8.0~12.0 mg,氮气流量50 mL/min。设定程序控温如下:在密封的铝盒中加热样品至80℃并保持10 min,消除结晶记忆后,以5℃/min的速率降温至-50℃,得到结晶过程中的DSC结晶曲线;在-50℃保持10 min后,以5℃/min的速率升温至80℃,得到熔化过程中的熔化曲线。所得数据采用随机所带软件进行处理。
1.2.7 塑性脂肪SFC的测定
采用脉冲核磁共振仪测定塑性脂肪样品的SFC。称取1.5 g左右的样品于专用玻璃样品管中,在80℃水浴中加热30 min消除结晶记忆后,转移至低温恒温器中,在0℃下保留90 min后测其SFC。然后将样品依次在5~45℃温度范围内,每隔5℃恒温保留30 min后,测定其SFC。利用Design-expert 8.0软件绘制等固图(平面图及3-D图)。
1.2.8 塑性脂肪相容性分析
油脂间的相容性除了用等固图分析,还可以用ΔSFC来评价[16]。ΔSFC指实测混合体系的SFC与其理论的SFC间的差值,即ΔSFC=SFC实测-SFC理论,其中理论SFC可按下式计算:
SFC理论=XASFCA+XBSFCB+XCSFCC
式中:XA、XB、XC分别表示混合体系中A、B、C组分的质量分数,SFCA、SFCB、SFCC分别表示在所测温度下A、B、C组分的SFC。以温度为横坐标、ΔSFC为纵坐标绘制曲线,若实测SFC比理论SFC高,即ΔSFC为正值则认为出现偏晶现象,反之则为共晶现象,一般认为ΔSFC在±1.5%以内为完全相容。
1.2.9 数据统计分析
采用Microsoft Excel 2013软件对数据进行分析,结果为“平均值±标准偏差”(n=2)。
2 结果与讨论
2.1 原料油及POL-DAG的甘油酯组成分析
对原料油山茶油、棕榈油硬脂及POL-DAG的甘油酯组成进行分析,结果如表1所示。

表1 原料油及POL-DAG的甘油酯组成及含量%
由表1可知,经过两次分子蒸馏,POL-DAG中DAG含量达到82.6%。山茶油与棕榈油硬脂中均含有极少量的DAG,含量分别为3.4%、4.2%。
2.2 原料油及POL-DAG的脂肪酸组成分析
对原料油山茶油、棕榈油硬脂及POL-DAG的脂肪酸组成进行分析,结果如表2所示。
由表2可知,山茶油中不饱和脂肪酸的含量高达91.1%,以油酸为主,含量为81.9%,饱和脂肪酸为棕榈酸,含量为8.9%;而棕榈油硬脂中饱和脂肪酸的含量最高,达到67.6%,棕榈酸含量高达61.6%,不饱和脂肪酸中油酸含量为28.0%;POL-DAG中不饱和脂肪酸的含量为59.0%,饱和脂肪酸含量为41.0%,分别以油酸(41.2%)和棕榈酸(36.5%)为主。
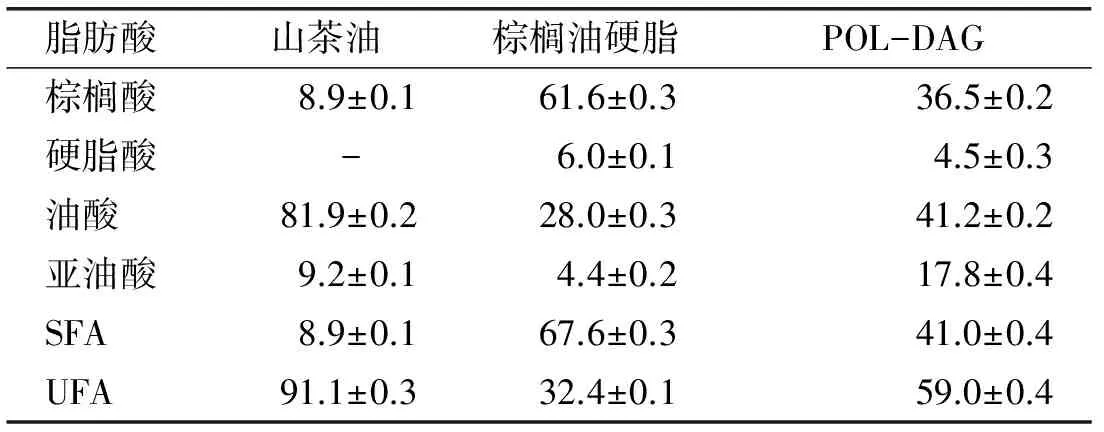
表2 原料油及POL-DAG的脂肪酸组成及含量%
注:SFA,饱和脂肪酸;UFA,不饱和脂肪酸。
2.3 结晶熔化特性
对两种原料油(山茶油CO、棕榈油硬脂PS)、POL-DAG及其混合物进行差示扫描量热分析,结果见图1和图2,其熔点、结晶起始点及结晶焓结果见表3。
由图1、图2可知,CO(A)有2个结晶峰,1个熔化峰;而PS(B)含2个结晶峰,4个熔化峰;POL-DAG(C)有4个结晶峰,3个熔化峰。CO由于不饱和脂肪酸含量为91.1%,故其结晶起始点和熔点都很低;POL-DAG中的饱和脂肪酸(41.0%)少于PS(67.6%),但其结晶起始点及熔点与PS相比差别不大,这是因为在相同脂肪酸组成下DAG的熔点高于TAG[7]。与两种原料油和POL-DAG相比,二元及三元混合物的结晶及熔化曲线都更加复杂,这是因为原料之间复杂的相互作用[17]。
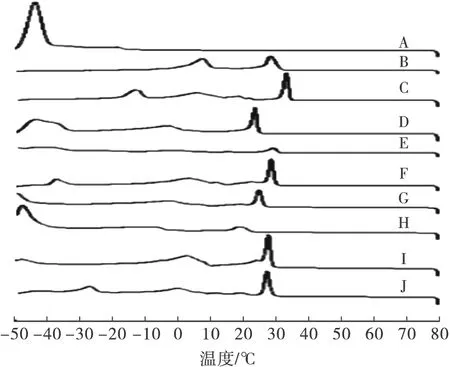
注:A,CO;B,PS;C,POL-DAG;D,CO、PS为1∶1;E,CO、POL-DAG为1∶1;F,PS、POL-DAG为1∶1;G,CO、PS、POL-DAG 为1∶1∶1;H,CO、PS、POL-DAG为4∶1∶1;I,CO、PS、POL-DAG为1∶4∶1;J,CO、PS、POL-DAG为1∶1∶4。下同。
图1原料油、POL-DAG及其混合物的结晶曲线
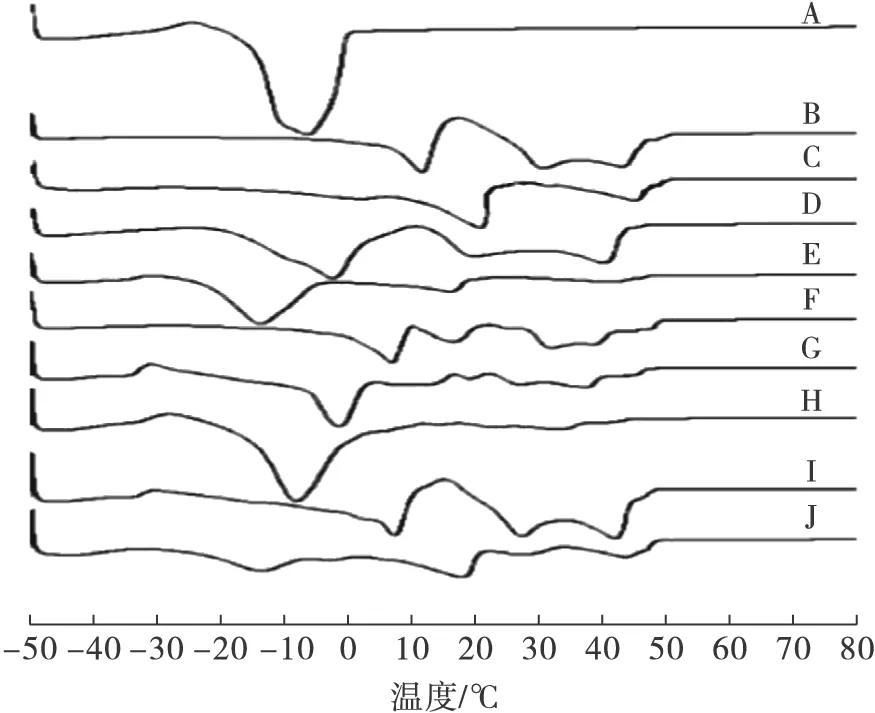
图2 原料油、POL-DAG及其混合物的熔化曲线
由表3可知,当向PS加入相同比例的CO时(D),混合物的熔点、结晶起始点和结晶焓都比PS低,同样当向POL-DAG加入相同比例的CO时(E),混合物的熔点、结晶起始点和结晶焓都低于POL-DAG,这是由于CO的稀释效应[3]。而PS、POL-DAG为1∶1(F)的熔点、结晶起始点和结晶焓都比PS和POL-DAG略低。这可能是由于PS和POL-DAG发生了轻微的共晶作用。有研究表明当将棕榈仁油加入到等量的葵花籽油与POL-DAG混合物中时亦出现同样的情况[3]。
当混合物中CO的含量由0%增加到33.33%、66.66%及100%(F,G,H,A)时,其熔点和结晶起始点及结晶焓逐渐降低;而当混合物中PS的含量由33.33%增加到100%(G,I,B)时,其熔点和结晶起始点、结晶焓逐渐升高;当混合物中POL-DAG的含量由0%增加到100%(D,G,J,C)时,其熔点和结晶起始点及结晶焓逐渐升高。
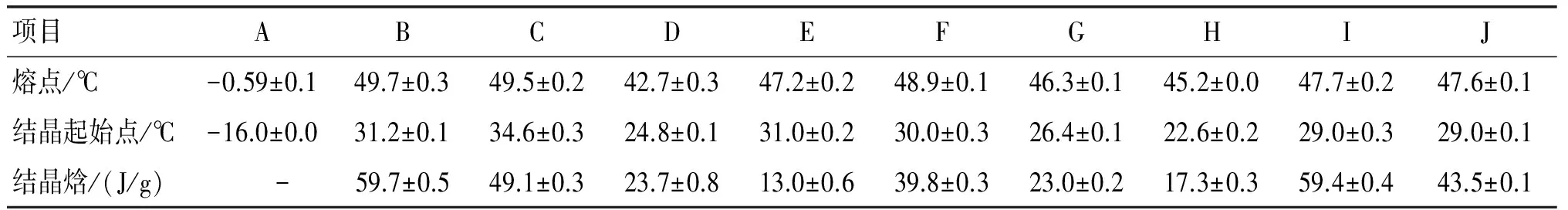
表3 原料油、POL-DAG及其混合物的熔点、结晶起始点及结晶焓
2.4SFC及三相性质
两种原料油、POL-DAG及其混合物在不同温度下的SFC如表4所示。
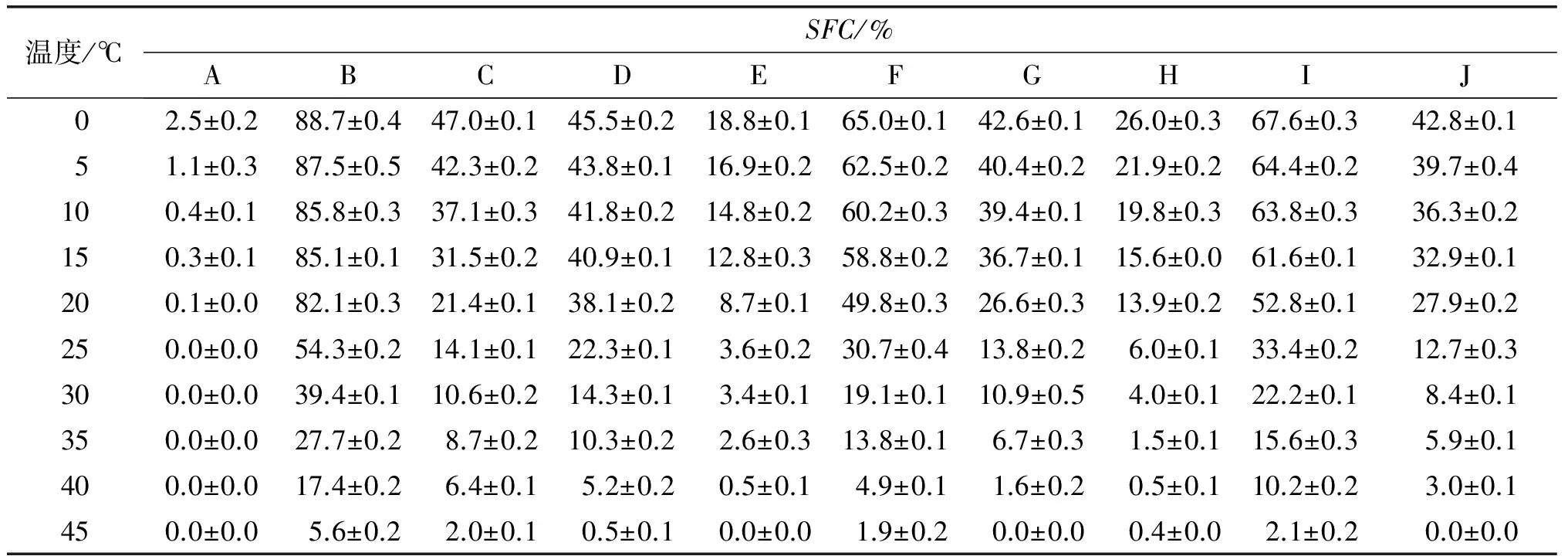
表4 原料油、POL-DAG及其混合物的在不同温度下的SFC
由表4可以看出,随着温度的升高,原料油及混合物的SFC都呈下降的趋势。就单一原料油而言,CO的SFC最小,PS的SFC最大,而POL-DAG的SFC居中,这是由于物质中的脂肪酸组成不同,CO中含有91.1%的不饱和脂肪酸,而PS中饱和脂肪酸达到67.6%(见表2)。二元体系CO与PS比1∶1(D)、CO与POL-DAG比1∶1(E)及PS与POL-DAG 比1∶1(F)的SFC大多在两种原料油的SFC之间。在40~45℃时,PS与POL-DAG比1∶1(F)的SFC低于二者的单体,这意味着二者发生了共晶作用,差示扫描量热分析也得到类似结果。
当CO含量由0%增加到33.33%、66.66%及100%(F,G,H,A)时,其SFC在所有温度下呈下降趋势;随着PS含量的增加(E,G,I,B),其SFC在所有温度下呈现升高趋势。当POL-DAG含量由33.33%增加到100%(G,J,C)时,其SFC在各个温度下都相差不大,但其在高温下呈升高趋势。这与差示扫描量热分析结果基本一致。
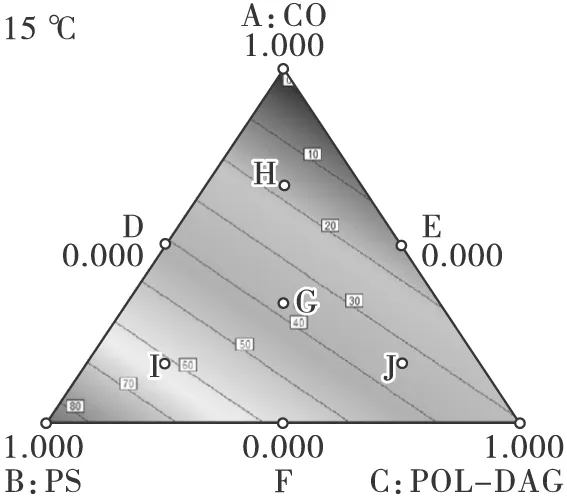
原料油及混合物在不同温度下的三元等固图如图3所示。图中每条线表示相同的SFC(即等固线)。由图3可知,随着温度由15℃升高到40℃,等固线呈现减小的趋势。在15~20℃时,等固线完全为直线,说明该三元体系处于完全相容状态[18]。当温度超过25℃时,添加POL-DAG到等量的CO和PS混合物中有共晶作用,因为在25~40℃时三者等量混合物(G)的SFC低于POL-DAG和混合物D。共晶作用是评价油脂相容性程度的指标之一[3]。也就是说,POL-DAG与CO和PS的等量混合物在25~40℃相容性较差。这是由于POL-DAG中含有82.6%的DAG,而CO和PS中以TAG为主。除了甘油酯组成的不同导致较差的相容性外,热力学性质及脂肪酸组成与含量的差异也是重要因素[19]。

2.5 相容性分析
以不同配比混合的CO、PS及POL-DAG混合物的ΔSFC-T曲线如图4所示。
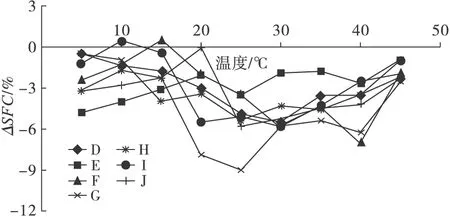
图4 混合物的ΔSFC-T曲线
一般而言,几种油脂成分的相容程度有4种情况:完全相容;部分相容,混合物体系呈共晶状态;部分相容,混合物体系呈偏晶状态;互不相容[20]。
Jin等[18]认为ΔSFC负值越大,共晶作用越明显。由图4可知,ΔSFC在20~25℃及40℃时的负值最大,说明混合物体系在此区间发生了共晶现象。在二元体系中,PS/POL-DAG的ΔSFC负值最大,其次是CO/POL-DAG和CO/PS。前者是由于PS与POL-DAG发生了共晶作用,虽然二者具有相似的脂肪酸组成和熔点,但其甘油酯组成不同,且有研究发现,显著的空间效应导致油酸很难直接与三棕榈酰甘油酯(PPP)堆积,从而限制其晶体的混合[21]。PS中含有部分PPP[22],POL-DAG的脂肪酸组成以油酸为主(41.2%)。而对于CO/POL-DAG和CO/PS,由于CO有稀释效应,D和E并不会出现共晶现象。
在三元体系中,CO、PS与POL-DAG以1∶1∶1混合(G)时,其ΔSFC负值最大,即其产生了共晶作用。这是由于3种物质的脂肪酸组成及热力学性质的差异造成的,PS是以棕榈酸为主,CO及POL-DAG是以油酸为主,而DAG和TAG的甘油酯结构的差异也是导致共晶现象的一个原因。由于三元混合物H、I和J中的主要组分即CO、PS和POL-DAG占66.66%,另外两种组分含量较低,其对主要组分的影响较小,故而其ΔSFC负值较小,即具有较好的相容性,其中以H最好,I和J其次。
3 结 论
在鼓泡式反应器中,利用Lipozyme 435催化棕榈液油甘油解合成POL-DAG,并通过分子蒸馏获得DAG含量达82.6%的POL-DAG。利用差示扫描量热仪及脉冲核磁共振仪分析由山茶油(CO)、棕榈油硬脂(PS)和POL-DAG组成的塑性脂肪的结晶特性和相容性。结果显示,混合物的熔点、结晶起始点和结晶焓随CO含量的增加而降低,而其随PS和POL-DAG含量的增加而升高。测定样品的SFC得到类似的结果。相容性分析结果显示,二元体系中,当PS与POL-DAG以1∶1混合时在30~40℃区间内出现共晶现象,相容性较差,而CO/PS与CO/POL-DAG没有发生共晶作用;三元体系中,当CO、PS与POL-DAG以1∶1∶1混合时相容性最差,而以4∶1∶1混合时相容性最好,其次是1∶4∶1及1∶1∶4。
[1] NG S P, LAI O M, ABAS F, et al. Compositional and thermal characteristics of palm olein-based diacylglycerol in blends with palm super olein[J]. Food Res Int, 2014, 55: 62-69.
[2] VU P L, PARK R K, LEE Y J, et al. Two-step production of oil enriched in conjugated linoleic acids and diacylglycerol[J]. J Am Oil Chem Soc, 2007, 84(2): 123-128.
[3] SABERI A H, LAI O M, MISKANDAR M S. Melting andsolidification properties of palm-based diacylglycerol, palm kernel olein, and sunflower oil in the preparation of palm-based diacylglycerol-enriched soft tub margarine [J]. Food Bioprocess Technol, 2012, 5(5): 1674-1685.
[4] NAGAO T, WATANABE H, GOTO N, et al. Dietary diacylglycerol suppresses accumulation of body fat compared to triacylglycerol in men in a double-blind controlled trial[J]. J Nutr, 2000, 130: 792-797.
[5] KAMPHUIS M M J W, MELA D J, WESTERTERP-PLANTENGA M S. Diacylglycerols affect substrate oxidation and appetite in humans[J]. Am J Clin Nutr, 2003, 77: 1133-1139.
[6] SONI M, KIMURA H, BURDOCK G. Chronic study of diacylglycerol oil in rats[J]. Food Chem Toxicol, 2001, 39(4): 317-329.
[7] LO S K, TAN C P, LONG K, et al. Diacylglycerol oil—properties, processes and products: a review[J]. Food Bioprocess Technol, 2008, 1(3): 223-233.
[8] 毕艳兰. 油脂化学[M]. 北京: 化学工业出版社, 2005.
[9] 姚伯龙, 蒋敏海. 棕榈油和棕榈仁油的地位和现状[J]. 食品与机械, 2001, 6(4):4-5.
[10] PANDE G, AKOH C C. Enzymatic modification of lipids fortrans-free margarine[J]. Lipid Tech, 2013, 25(2): 31-33.
[11] SAITO S, YAMAGUCHI T, SHOJI K, et al. Effect of low concentration of diacylglycerol on mildly postprandial hypertriglyceridemia[J]. Atherosclerosis, 2010, 213: 539-544.
[12] MITSUHASHI Y, NAGAOKA D, ISHIOKA K, et al. Postprandial lipid-related metabolites are altered in dogs fed dietary diacylglycerol and low glycemic index starch during weight loss[J]. J Nutr, 2010, 140:1815-1823.
[13] HIBI M, SUGIURA Y, YOKOYAMA R, et al. The short-term effect of diacylglycerol oil consumption on total and dietary fat utilization in overweight women[J]. Obesity, 2011, 19: 536-540.
[14] LIDA H, ALI A. Physicochemical characteristics of palm based oil blends for production of reduced fat spreads[J]. J Am Oil Chem Soc, 1998, 75: 1625-1631.
[15] WANG L, WANG Y, HU C, et al. Preparation of diacylglycerol-enriched oil from free fatty acids using lecitase ultra-catalyzed esterification[J]. J Am Oil Chem Soc, 2011, 88: 1557-1565.
[16] 张阜青, 王兴国, 胡鹏, 等. 棕榈油与棕榈油中熔点分提产物相容性及结晶形态研究[J]. 中国油脂, 2009, 34(3): 24-28.
[17] SABERI A H, LAI O M, MISKANDAR M S. Physical properties of palm-based diacylglycerol and palm-based oils in the preparation of shelf-stable margarine[J]. Eur J Lipid Sci Technol, 2011, 113: 627-636.
[18] JIN Q, ZHANG T, SHAN L, et al. Melting and solidification properties of palm kernel oil, tallow, and palm olein blends in the preparation of shortening[J]. J Am Oil Chem Soc, 2008, 85(1): 23-28.
[19] TIMMS R E. Phase behaviour of fats and their mixtures[J]. Prog Lipid Res, 1984, 23(1): 1-38.
[20] 张婷, 金青哲, 王兴国. 棕榈仁油与五种油脂相容性的研究[J]. 中国油脂, 2006, 31(11): 26-29.
[21] HAMILTON R J, BHATI A. Recent advances in chemistry and technology of fats and oils[M]. Champaign: AOCS Press, 2000: 1-11.
[22] 池娟娟. 乳化剂对棕榈油基人造奶油结晶行为的影响[D]. 江苏 无锡: 江南大学, 2012.
Crystallizationbehaviorandcompatibilityofdiacylglycerol-basedplasticfat
YANG Xue1,2, LIU Zun1, SONG Jia1, WANG Xiaochen1, ZHANG Ning1, XU Huaiyi3, WANG Yong1
(1.Guangdong Saskatchewan Oilseed Joint Laboratory, Department of Food Science and Engineering, Jinan University, Guangzhou 510632, China; 2.Guangzhou Testing Center of Industrial Microbiology, Guangzhou Institute of Microbiology, Guangzhou 510663, China; 3.Cardlo Biochemical Technology Co., Ltd., Guangzhou 510630, China)
Palm olein-based diacylglycerol (POL-DAG) was synthesized through Lipozyme 435-catalyzed glycerolysis of palm olein in a bubble column reactor, and POL-DAG with DAG content of 82.6% was obtained after being purified by molecular distillation. The crystallization behavior and compatibility of the plastic fat composed of oil-tea camellia seed oil (CO), palm stearin (PS) and POL-DAG were analyzed by differential scanning calorimeter and pulsed nuclear magnetic resonance. The results showed that the melting point, crystallization onset and crystallization enthalpy decreased when the CO content increased, while PS and POL-DAG showed opposite results. Compatibility was the worst when CO, PS and POL-DAG were mixed in a ratio of 1∶1∶1, while it was the best when in a ratio of 4∶1∶1, followed by 1∶4∶1 and 1∶1∶4.
diacylglycerol; lipase; plastic fat; crystallization behavior; compatibility
2016-09-09;
:2017-01-26
国家自然科学基金项目(31371785);广东省科技计划项目(2013B090800009);教育部“新世纪优秀人才”支持计划(NCET-12-0675);广州市科技计划项目(2014Y2-00192)
杨 雪(1991),女,硕士,研究方向为功能性油脂(E-mail)yangx0613@163.com。
张 宁,副教授,博士(E-mail)tzhning@jnu.edu.cn;汪 勇,研究员,博士(E-mail)twyong@jnu.edu.cn。
TS225.6;TQ641
:A
:1003-7969(2017)07-0024-06
