注射用血塞通与滤芯相容性研究
2017-09-16陈晨
陈晨
哈尔滨珍宝制药有限公司
注射用血塞通与滤芯相容性研究
陈晨
哈尔滨珍宝制药有限公司
目的评估注射用血塞通与密理博公司的聚偏二氟乙烯滤芯相容性。方法测定在进行除菌过滤前后滤芯的泡点差异、流速差异及聚集性差异,以此评察血塞通药液与滤芯的相容性;对可获得的提取物进行紫外、红外及生物分析,对可提取物进行毒理学评估;通过微生物挑战试验,验证滤芯对细菌截留能力;对生产过程中溶液相关指标进行测定,评价滤芯对药液的影响。结果:泡点、流速及聚集性差异测定结果符合要求,毒理学评估结果符合要求,药液与滤芯之间无相互作用。结论:血塞通溶液与滤芯相容性良好,聚偏二氟乙烯滤芯可用于注射用血塞通样品生产时除菌过滤。
过滤系统;相容性;验证
药品在生产过程中的除菌过滤是在不影响产品质量的前提下,通过过滤系统(滤芯)去除药液微生物及不溶性微粒的工艺过程,该过程是注射剂产品生产过程中主要生产工序。注射剂在除菌过滤时选择合适的滤芯尤为关键,所用的滤芯与药液不应发生相互作用,即药液与滤芯之间的相容性要符合要求,如相容性不好,患者用药时会存在极大安全隐患,为保证患者用药安全,我们对注射用血塞通与滤芯相容性进行验证[1-3],评价相容性是否符合要求。
1.实验材料及设备
密理博聚偏二氟乙烯(孔径0.22微米,10英寸);注射用水、纯化水、药液;挑战微生物为B.diminuta美国标准菌库19146;密理博Integritest 4完整性测试仪,蠕动泵。
2.验证过程
2.1.泡点、流速及聚集性差异测定。
上述考察指标是药液与滤芯相容性是否符合指标的关键考察项,试验药液使用血塞通溶液作为浸泡液,注射用水作为后冲洗溶液,在22±4℃条件下用药液将滤芯浸泡16小时,测定泡点差异、流速差异及聚集性差异(测定结果均应小于5.0%),结果表明滤芯与药液相容性良好,详细测定结果见表1。
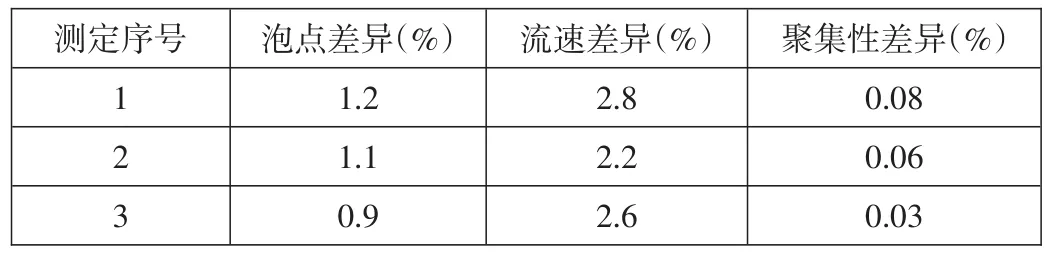
表1 差异测定
2.2 毒理学评估
实验开始前,将滤芯在121℃的条件下湿热灭菌30min,重复灭菌五次。然后在35℃的条件下置于无水乙醇中浸泡24小时。经离心后分析检测,确定聚偏二氟乙烯滤芯的最大析出物量为56.8mg,因此,处理一批注射用血塞通后,过滤最大析出物量约为56.8mg。采用相同处理方法,对所得浸提液进行紫外分析,在230nm至350nm进行紫外扫描,结果所有样品的紫外吸收均小于0.002,可见溶出物量极小,并且在无紫外吸收。采用溴化钾压片法对所得物进行红外光谱测定分析,结果红外吸收峰与聚乙二醇及聚乙烯比咯烷酮吸收峰一致,测定结果与滤芯成分相符。除进行上述试验研究外,我们委托默克密理博生物中心对浸出物[4]进行生物安全性试验,结果显示聚偏二氟乙烯滤芯部件是没有毒性的,不存在安全隐患。
2.3 微生物挑战试验
注射用血塞通为非终端灭菌制剂,按照无菌操作法相关要求及本品剂型特点,无菌过滤验证为关键步骤。验证滤芯对药液中浸入B.diminuta菌的截留能力。试验溶液中每cm2含细胞(B. diminuta)数量应大于等于107个。实验用滤芯预先经过泡点试验,预先灭菌,完整性符合要求。先将试验用挑战物加入血塞通溶液中进行培养,结果表明药液对挑战菌无影响,因此,不需要替代方法进行试验,可将挑战菌加入药液中进行测试。在实验过程中采用药液在最差条件(产品工艺规程中规定的上限或者下线条件组合)下进行微生物挑战试验。挑战时温度在22±4℃的温度条件下,压力大于等于58psi,需要总时间为12小时。取末端溶液进行培养,挑战物质B.diminuta在SLB培养基上进行培养,通过TSA涂布技术测定,在实验前后需要将涂布板在30±2℃条件下培养48到72小时,接种后,检验每块板并记录菌落数,实验过程中同时进行阴性对照试验,结果表明滤芯可对验证菌进行有效截留。
2.4 生产过程中验证
对三批大生产样品进行验证,结合产品特点,进行相应工艺验证,滤芯过滤时的取样点为精滤前药液及终端过滤后药液,对各取样点的性状、pH值、可见异物、溶液澄清度与颜色、不溶性微粒、有关物质及含量进行测定,结果三批样品在各个取样点的各项考察指标无明显差异,表明滤芯对药液的各项指标无影响。对生产过程中过滤前后滤芯的泡点进行测试,结果均符合规定,过滤前后药液的测定结果见表2。
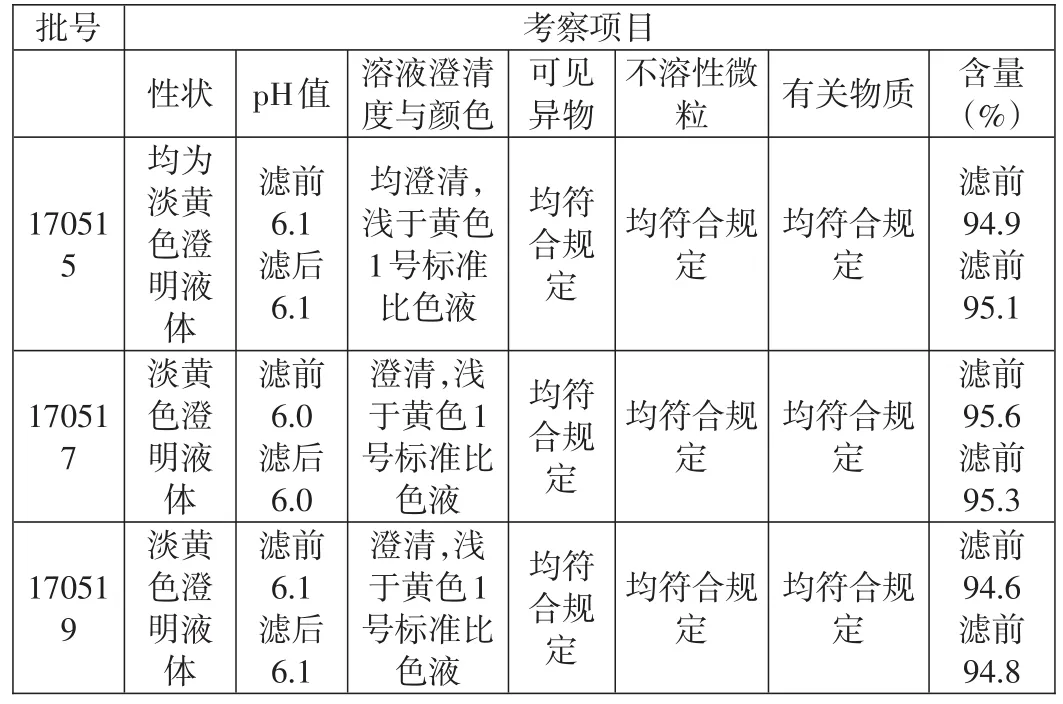
表2 理化测定结果
3.讨论
无菌检查符合要求是注射剂产品的关键指标之一,在使用滤芯对药液进行除菌过滤时,除关注药液的无菌指标外,越来越关注药液与滤芯的相互影响,在使用滤芯进行除菌过滤时,药液及滤芯之间应无相互影响。为提高产品质量,保证患者用药安全,我们对血塞通药液与密理博10inch聚偏二氟乙烯滤芯的相容性进行研究,泡点、流速及聚集性差异的测定结果表明药液对滤芯无影响,细菌截留试验表明该滤芯可保证生产过程中有效除菌,生产过程中药液各项指标考察结果表明滤芯对药液无影响,上述研究结果表明血塞通与密理博的聚偏二氟乙烯相容性良好。
[1]黄晓龙,董巍,唐燕.除菌过滤器验证(一):法规要求概述.中国新药杂志,2011,20(10):861-865.
[2]李芳,范运,张俊伟.注射液生产过程中过滤系统的验证.中国医药工业杂志,2012,43(7):628-631.
[3]叶璇,罗娇,胡明.液体除菌过滤器和除菌过滤工艺的验证.医药工程设计,2012,33(4):19-22.
[4]洪海燕,唐燕,董巍,谢婷.除菌过滤器验证(三):溶出物/析出物验证.中国新药杂志,2011,20(14):1266-1269.
