基于聚丙烯酸交联组装单层SiO2纳米粒粗糙表面及其细胞捕获
2017-08-31魏同洪丁海洋陈小波何欢欢游思佳谢洪平
魏同洪,刘 玲,丁海洋,陈小波,何欢欢,游思佳,谢洪平
(苏州大学 药学院,江苏 苏州 215123)
基于聚丙烯酸交联组装单层SiO2纳米粒粗糙表面及其细胞捕获
魏同洪,刘 玲,丁海洋,陈小波,何欢欢,游思佳,谢洪平*
(苏州大学 药学院,江苏 苏州 215123)
以玻片为载体(Subs),聚丙烯酸(PAA)为交联剂和柔性体,SiO2纳米粒为刚性体,人B淋巴细胞瘤Ramos细胞为目标细胞,TD05适体为细胞捕获配体(Apt),在载体上交联组装了结构为Subs-PAA1-SiO2-PAA2-Apt的细胞捕获支架。该支架既有小尺度的刚性结构,即SiO2纳米粒,又有柔性结构,即聚丙烯酸PAA1和PAA2。前者增加了载体的粗糙度,而后者不仅能够固载多重捕获配体,也能够有效降低宏观载体对细胞捕获的空间位阻。结果表明,支架具有良好的纳米粒结构,未发现纳米粒的融合甚至消失;支架的特异性捕获是非特异性吸附的16倍,被捕获细胞表现出较高的纯度;同时,支架具有较高的捕获效率,捕获细胞数是通常的单层刚性纳米粒支架的8.3倍。由此表明,该文构建的结构新颖的纳米粒柔性支架实现了目标细胞的高效率、高纯度捕获,将为肿瘤细胞的分析检测提供可靠的样本。
支架;细胞;捕获;纳米粒;聚电解质
由于循环肿瘤细胞(CTC)可以作为实体瘤早期检测和诊断的可靠标记物,因此,稀有细胞CTC的捕获成为分析检测的关键问题[1-4]。阳性富集和阴性分选均是将待测样本与固载了特异性捕获配体的载体(如磁珠)经混合、振荡和分离,从而获得干扰细胞明显减少的、富集的CTC检测样本。由于CTC的含量极低,而干扰细胞的含量极高,捕获常出现假阴性。其原因关键在于CTC捕获效率低。当前主要采用微流控芯片、提高载体基质粗糙度和CTC多价键合3类技术以提高捕获效率[1-3,5-14]。其中,提高载体基质粗糙度是主要手段,即在宏观载体上构建一个小尺度的支架,以减小宏观载体对被固定于支架上的捕获配体捕获CTC时的空间位阻。主要技术手段包括化学腐蚀、光刻蚀、纳米粒的化学沉积和电沉积[2,5,7-8,13-14]。事实上,在提高粗糙度的同时,空间位阻并未明显减小,通常提高特异性捕获效率的同时,支架的非特异性吸附也明显增强。主要原因在于,构建的支架为大尺度的微米级支架或者纳米粒结构消失的纳米粒沉积支架[6,13-14]。本文以玻片为载体,以极大分子量的聚丙烯酸(PAA)为交联剂组装SiO2纳米粒,并在纳米粒上进一步修饰PAA,以此固定多重配体,构建了结构新颖的纳米粒支架,实现了对人B淋巴细胞瘤Ramos细胞的特异、高效捕获。
1 实验部分
1.1 试剂与仪器
聚丙烯酸(PAA,25%,Mw=240 000)购于阿拉丁试剂(上海)有限公司。TD05适配体(序列为5′-CAC CGG GAG GAT AGT TCG GTG GCT GTT CAG GGT CTC CTC CCG GTG TTT TT AAG GAG CAG CGT GGA GGA TA-NH2-3′)[15]购于生物工程(上海)股份有限公司。Ramos细胞购于中美合资博慧斯生物医药科技有限公司。其它试剂均为分析纯,实验用水为自制三蒸去离子水。NICOMPTM380ZLS Zeta电位及粒度分析仪(美国PSS公司)、S-4700冷场发射扫描电镜(SEM,日本日立公司)、Dimension Icon原子力显微镜(AFM,美国Bruker公司)、LS 55荧光显微镜(美国PerkinElmer公司)。
1.2 纳米粒支架制备
由于SiO2纳米粒具有良好的生物相容性和亲水性,本文以其为固载于载体上的纳米粒。按文献[16]制备并将该纳米粒表面氨基硅烷化(其中氨基硅烷化纳米粒的浓度为2.2 mg/mL)。
硅烷化载体基片的制备:将30%双氧水与98%硫酸按体积比3∶7混合制成洗液。将载玻片裁成25.4×19 mm2大小的玻片作为载体基质。用水和无水乙醇分别洗涤,吹干,放入洗液,80~100 ℃下加热1 h,取出并自然冷却。用水冲洗,冷风吹干。置于2% 3-氨丙基三乙氧基硅烷的无水乙醇溶液中反应18 h,取出,用水冲洗,120 ℃烘6 h,即得氨基硅烷化的载体基片(Subs-NH2)。
PAA羧基的活化:取100 μL 25%的PAA于10 mL单颈瓶中,加入5 mL水,摇匀,加入2 mL 0.8 mg/mL 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC·HCl)和2 mL 2.2 mg/mL N-羟基硫代琥珀酰亚胺(sulfo-NHS),摇匀,37 ℃水浴活化60 min,用水稀释至50 mL,PAA羧基被部分活化,即得PAA-NHS溶液(0.5 mg/mL)。
载体上纳米粒支架的制备:将氨基硅烷化的载体基片置于5 mL PAA-NHS溶液,37 ℃下反应1 h,取出基片,收集反应液。用水洗涤基片2次,N2吹干,置于5 mL表面硅烷化的SiO2纳米粒溶液中37 ℃反应3 h,取出基片,收集反应液。用水洗涤基片2次,N2吹干,置于5 mL PAA-NHS溶液中37 ℃反应1 h,取出基片,收集反应液。用水洗涤基片2次,N2吹干,即得Subs-PAA1-SiO2-PAA2结构的基片。
1.3 捕获适体的连接与细胞捕获
在纳米粒支架上层(PAA2)的PAA众多活化羧基中,部分与已固载纳米粒的表面氨基反应,以实现PAA2的固载,而剩余的活化羧基将用于固载氨基化的细胞捕获适体TD05。将基片Subs-PAA1-SiO2-PAA2置于13 mL TD05适配体溶液(5.0×104μmol/L,用PBS缓冲液配制),37 ℃振荡反应1 h。取出基片,用水冲洗2次,置于3 mL 0.1 mol/mL甘氨酸的PBS溶液中,以封闭PAA2上剩余的活化羧基,防止活化羧基对细胞膜蛋白的非特异性反应。基片用N2吹干,即得固载适体的纳米粒捕获支架。该支架具有Subs-PAA1-SiO2-PAA2-Apt结构,作为实验组备用。除了TD05适配体未被使用以外,其它所有过程均平行实验,即得未连接适体的纳米粒捕获支架,作为对照组备用。
TD05适配体的靶细胞为Ramos,细胞用橙红色的DiI染料染色,并将细胞重悬于6 mL PBS配制的结合缓冲液中,细胞密度为1.0×106个/mL。将六孔板置于固载纳米粒支架的基片上,每个孔加1 mL细胞悬液,放置培养箱中37 ℃孵育1.5~2 h,每30 min轻轻振摇1次,结束后用37 ℃的洗涤缓冲液(PBS配制)洗涤2次,干燥后置于荧光显微镜下成像,并计数,整个过程避光操作。
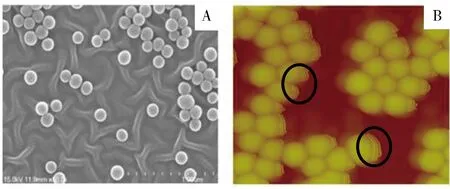
图1 捕获支架的SEM(A)和AFM(B)表征Fig.1 SEM(A) and AFM(B) images of capture scaffold
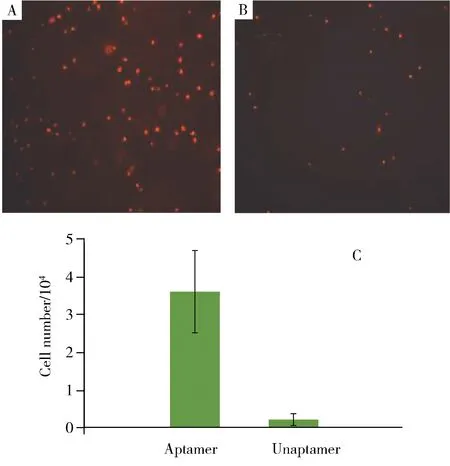
图2 构建的支架特异性捕获(A)和非特异性吸附(B)目标细胞的荧光成像及其细胞计数(C)Fig.2 Fluorescent imagings of the objective cells specially captured(A) and non-specially adsorbed(B)by the built scaffolds and their cell counts(C)
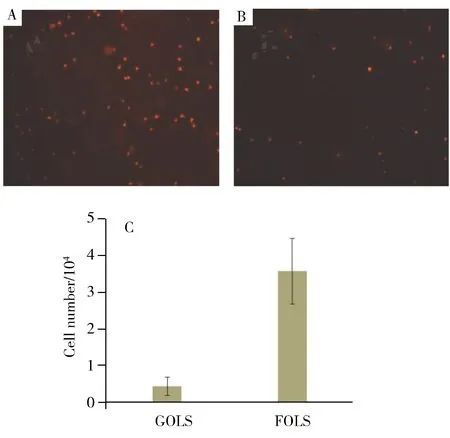
图3 柔性(FOLS,A)与刚性(GOLS,B)支架捕获细胞的荧光成像及其细胞计数(C)Fig.3 Fluorescent imagings of the objective cells captured by the flexible(A) and rigid(B) scaffolds,and their cell counts(C)
2 结果与讨论
2.1 SEM与AFM表征
本文利用扫描电镜(SEM)表征了捕获支架中纳米粒的形貌、粒径以及固载基片表面形态,同时利用原子力显微镜(AFM)表征了其纳米粒结构特征与聚积状态(图1)。由图可见,基片上SiO2纳米粒子形态均匀,粒径约为100 nm(图1A),基片表面出现了预处理所产生的纹路。被PAA交联固载的纳米粒形成了单层的纳米粒结构,并未出现无序的多层堆积(图1B)。同时,粒子表面出现了大量波纹状的包覆层(图1B黑色圈标注),可能是被固载在纳米粒上的聚电解质PAA的残余大分子链在表征时为非溶液状态,从而沉积在粒子表面,即Subs-PAA1-SiO2-PAA2结构中的PAA2。
2.2 特异性捕获与非特异性吸附
当基片的纳米粒支架上固载特异性识别适体TD05后,即可实现对靶细胞Ramos的特异性捕获(图2)。由图可见,以未固定捕获适体的支架(图2B)为对照,在支架上的TD05适体表现出高的捕获效率(图2A),且为对照的16倍(图2C);非特异性吸附捕获仅占特异性捕获的6.19%,表现出极低的非特异性吸附。同时也表明本文构建支架捕获的目标细胞具有较高的纯度。粗糙表面往往存在明显的非特异性吸附[6-7],而该捕获支架表现出的良好性能主要在于其支架的特殊结构。在支架的Subs-PAA1-SiO2-PAA2-Apt结构中,SiO2纳米粒是通过聚电解质PAA1的大量羧基而固载于基片上,捕获适体Apt是利用聚电解质PAA2上的大量羧基而固载,即PAA2上一部分羧基与SiO2纳米粒连接,一部分羧基与适体Apt连接,保证了支架结构中PAA1、PAA2和SiO2纳米粒上均存在极其丰富的负电荷,从而可阻止对表面负电荷的目标细胞的非特异性吸附。因此,即使粗糙度增加仍然表现出极低的非特异性吸附。
2.3 支架的柔性与高效细胞捕获
对于固载于基片上的支架Subs-PAA1-SiO2-PAA2-Apt,刚性的SiO2纳米粒可增加基片粗糙度,进而提高细胞捕获效率;同时支架中的聚电解质大分子PAA1和PAA2表现出一定的柔性,可能会降低支架刚性结构的空间位阻,具有增加捕获效率的潜能,因此构建了一个SiO2纳米粒的刚性支架作为对照。以环氧基硅烷化试剂KH570对SiO2纳米粒子进行处理后得到环氧化的纳米粒,无需PAA进行交联,而直接利用环氧基与氨基的反应将环氧化的纳米粒直接固载于氨基化的基片上,再利用纳米粒上剩余的环氧基直接固载氨基化的TD05适体,即得Subs-SiO2-Apt结构的支架。柔性与刚性支架对目标细胞的捕获见图3,从图3可以发现,构建的具有柔性结构的支架Subs-PAA1-SiO2-PAA2-Apt相对于刚性支架Subs-SiO2-Apt表现出更高的捕获效率,前者(图3A)捕获的细胞远多于后者(图3B),且前者的捕获细胞数为后者的8.3倍(图3C)。由此表明,在均为一层纳米粒的相同粗糙度的情况下,Subs-PAA1-SiO2-PAA2-Apt中的柔性结构PAA1和PAA2对于提高捕获效率具有较大的贡献,其原因是柔性结构能够明显降低支架刚性结构的空间位阻。
3 结 论
本文以玻片为载体、PAA为交联剂、氨基化SiO2纳米粒为刚性体,在载体上交联组装了用于细胞捕获的支架,并在支架上固定TD05适体,实现了目标细胞Ramos的捕获。该捕获支架具有Subs-PAA1-SiO2-PAA2-Apt结构:既有增加载体粗糙度的刚性结构(即SiO2纳米粒),又有柔性结构(即PAA1和PAA2),有效地降低了宏观载体对细胞捕获的空间位阻。支架表现出特异性高捕获和非特异性低吸附,前者的捕获率为后者的16倍,且非特异性吸附仅占特异性捕获的6.19%,捕获细胞表现出较高的纯度;相对于常用的刚性支架Subs-SiO2-Apt,本文的柔性支架捕获细胞数为刚性支架的8.3倍。由此表明,本文构建了一个结构新颖的纳米粒柔性支架,可实现目标细胞的高效率、高纯度捕获,从而为CTC的分析检测提供了可靠的样本。
[1] Zhang F L,Jiang Y,Liu X L,Meng J X,Zhang P C,Liu H L,Yang G,Li G N,Jiang L,Wan L J,Hu J S,Wang S T.NanoLett.,2016,16:766-772.
[2] Shi L,Wang K,Yang Y.ColloidsSurf.B,2016,147:291-299.
[3] Pua K F,Lia C L,Zhang N P,Wang H,Shen W J,Zhua Y M.Biosens.Bioelectron.,2017,89:927-931.
[4] Tan W H,Donovan M J,Jiang J H.Chem.Rev.,2013,113:2842-2862.
[5] Wang S T,Wang H,Jiao J,Chen K J,Owens G E,Kamei K I,Sun J,Sherman D J,Behrenbruch C P,Wu H,Tseng H R.Angew.Chem.Int.Ed.,2009,48:8970-8973.
[6] Zhang P M,Gao M X,Zhang X M.Talanta,2016,153:366-371.
[7] Sun N,Li X P,Wang Z L,Zhang R H,Wang J,Wang K W,Pei R J.ACSAppl.Mater.Interfaces,2016,8:12638-12643.
[8] Sheng W A,Chen T,Kamath R,Xiong X L,Tan W H,Fan Z H.Anal.Chem.,2012,84:4199-4206.
[9] Sheng W A,Chen T,Tan W H,Fan Z H.ACSNano,2013,7:7067-7076.
[10] Myung J H,Gajjar K A,Saric J,Eddington D T,Hong H.Angew.Chem.Int.Ed.,2011,50:11769-11772.
[11] Huang Y F,Chang H T,Tan W.Anal.Chem.,2008,80:567-572.
[12] Lin R Z,Hatch A,Antontsev V G,Murthy S K,Melero-Martin J M.TissueEng.C,2015,21:274-283.
[13] Wang Y Y,Zhou F,Liu X L,Yuan L,Li D,Wang Y W,Chen H.ACSAppl.Mater.Int.,2013,5:3816-3823.
[14] Zhou F,Li D,Wu Z,Song B,Yuan L,Chen H.Macromol.Biosci.,2012,12:1391-1400.
[15] Tang Z W,Shangguan D H,Wang K M,Shi H,Sefah K,Mallikratchy P,Chen H W,Li Y,Tan W H.Anal.Chem.,2007,79:4900-4907.[16] Ge Z L,Song T M,Chen Z,Guo W R,Xie H P,Xie L.Anal.Chim.Acta,2015,862:24-32.
Rough Surface of One-layer SiO2Nanoparticles Assembled by Polyacrylic Acid Cross-linking and Its Cell Capture
WEI Tong-hong,LIU Ling,DING Hai-yang,CHEN Xiao-bo,HE Huan-huan,YOU Si-jia,XIE Hong-ping*
(College of Pharmaceutical Sciences,Soochow University,Suzhou 215123,China)
A cell capture scaffold with a structure of Subs-PAA1-SiO2-PAA2-Apt was assembled by using a glass slide as substrate carrier(Subs),polyelectrolyte polyacrylic acid(PAA) as cross-linking agent and flexible body,SiO2nanoparticles as rigid body,and TD05 aptamer(Apt) as capture ligand of objective cell Ramos.Here there are a small scale and rigid structure(i.e.SiO2nanoparticle),but also a flexible structure(i.e.polyacrylic acid PAA1 and PAA2).The former increased the roughness of carrier,and the latter could not only immobilized the multi-ligand Apt,but also decreased the steric hindrance from the scaffold itself and the carrier for cell capture.The results indicated that the as-assembled scaffold had a good nanoparticle structure and fusing even disappearing of the nanoparticle structure was not found.For the scaffold,its specific capture was 16 times of the non-specific adsorption,and the captured cell showed a higher purity.Meanwhile the captured cell has also a higher captureefficiency,and the capture cell number was 8.3 times of that of the usual rigid scaffold with one-layer nanoparticle.It was shown that the nanoparticle flexible scaffold with a novel structure was fabricated,which could realize the high purity and the high efficiency for cell capture.
scaffold;cell;capture;nanoparticle;polyelectrolyte
2017-03-09;
2017-04-07
10.3969/j.issn.1004-4957.2017.08.017
O766.1;O652.6
A
1004-4957(2017)08-1043-04
*通讯作者:谢洪平,博士,教授,研究方向:药物与生物分析,Tel:0512-65883022,E-mail:hpxie@suda.edu.cn
