高效液相色谱-内标法测定碘硝酚原料及其注射液中碘硝酚的含量
2017-08-31孙婷婷王洪礼田春莲刘明春牛生吏
孙婷婷,田 凯,王洪礼,杨 杰,田春莲,刘明春,牛生吏*
(1.沈阳农业大学 畜牧兽医学院,辽宁 沈阳 110866;2.沈阳伟嘉牧业技术有限公司,辽宁 沈阳 110027)
实验技术
高效液相色谱-内标法测定碘硝酚原料及其注射液中碘硝酚的含量
孙婷婷1,田 凯2,王洪礼2,杨 杰1,田春莲1,刘明春1,牛生吏1*
(1.沈阳农业大学 畜牧兽医学院,辽宁 沈阳 110866;2.沈阳伟嘉牧业技术有限公司,辽宁 沈阳 110027)
建立了碘硝酚的高效液相色谱(HPLC)-内标法检测方法。用甲醇将样品配制成测试浓度后过滤,经依利特SinoChrom C18(4.6 mm×200 mm,5 μm )色谱分析柱进行色谱分离,流动相为0.02 mol/L磷酸二氢钾溶液(pH 2.6)-甲醇(30∶70),流速为1 mL/min,紫外检测波长为235 nm,柱温为30 ℃,内标物为硝氯酚,进样量为20 μL。结果表明,碘硝酚的质量浓度在20~120 mg/L范围内呈线性关系,相关系数(r)为0.999 6;在3个不同浓度(64、80、96 mg/L)加标水平下,平均回收率为90.4%~98.2%,相对标准偏差(RSD)为0.18%~0.72%;检出限(LOD,S/N=3)为0.15 mg/L,定量下限(LOQ,S/N=10)为1.5 mg/L。该方法的精密度、稳定性以及重复性良好,且操作简便,结果准确,可用于碘硝酚原料药及注射液的含量测定。
碘硝酚;硝氯酚;含量测定;高效液相色谱法;内标法
碘硝酚(Disophenol)又名双碘硝酚,化学名为2,6-二碘-4-硝基苯酚,为淡黄色粉末或淡黄色结晶性粉末,无臭无味,其熔点为155~159 ℃。碘硝酚首次合成于20世纪初,60年代逐渐发现其可用于驱杀动物体内外的寄生虫,70年代初改进了合成工艺,并获得美国食品药品监督管理局批准可用作兽药[1-3]。我国在20世纪末开始研究此类药物[4-7],1995年由农业部批准沈阳市兽药厂生产,1996年成功仿制碘硝酚,并获国家农业部批准为二类新兽药,收载于《中华人民共和国兽药典》2015年版一部[8]。碘硝酚能驱杀肝片吸虫、动物线虫、羊鼻蝇、牛皮蝇、蜱螨等寄生虫,具有广谱、长效、高效等优点,目前在国内已被广泛用作兽用驱虫药[6,9-10]。
现在市场上碘硝酚兽药仅用于牛羊寄生虫病的治疗,其在猪等其他家畜的寄生虫病治疗上仍有着广阔应用前景,但由于对碘硝酚体内药物动力学等的相关研究较少,缺乏药动学参数等原始数据支撑,从而限制了其进一步应用。为了扩大碘硝酚的应用范围并为新型兽药研发提供新的方法,应进行碘硝酚含量的准确快速测定方法研究。目前对碘硝酚的定性定量分析方法主要有氧瓶燃烧法[11]、分光光度法[12]和高效液相色谱法[13-14]。氧瓶燃烧法操作繁琐,耗时长;分光光度法专属性不强,不够准确,两者均无法满足快速、准确测定碘硝酚体外含量以及体内药动学参数的需求;高效液相色谱法具有高效、快速、灵敏度高以及高自动化、色谱柱可反复使用、样品不被破坏且易回收等优点;此外,大多数实验室均能满足高效液相色谱法的需求,故有较好的通用性,是药物体内外分析的理想方法[15-17]。但采用文献的色谱条件进行碘硝酚检测时,存在色谱峰拖尾、分离度较差、重现性不好等问题,且多数分析方法主要集中在外标法。外标法相对简便,但在实际应用中准确性受到进样量重复性、标样准确性,以及仪器稳定性等因素的影响。而内标法结合了峰面积归一化法和外标法的优点,在加入内标物后,该方法可以消除采用外标法时由于进样量重复性、仪器稳定性等变化所导致的误差,定量方法相对准确,尤其适用于分析样品含量较少的情况。对于药物的体内分析而言,因样品含量较少且处理过程较繁琐,易引入误差,而在此过程中加入内标物则可以校正误差。因而,内标法分析的准确度和精密度相对较高,是药物体内分析较为理想的选择。本文通过优化色谱条件,建立了碘硝酚的高效液相色谱-内标法检测方法,该方法灵敏,准确度、分离度和重现性较好,为碘硝酚的体外含量测定及其体内药动学研究提供了理论基础和依据。
1 实验部分
1.1 仪器与试剂
依利特P230Ⅱ型高效液相色谱仪,UV230Ⅱ紫外-可见光检测器;Gene Company Limited DICO17型离心机(基因有限公司);XW-80A型旋涡混匀器(上海精科实业有限公司);FA224型电子天平(上海舜宇恒平科学仪器有限公司);pH计(Mettler Toledo公司);DK-8D型恒温水浴锅(金坛市医疗仪器厂);KQ2200E型超声清洗仪(昆山市超声仪器有限公司);超纯水制备仪(沈阳超纯科技有限公司)。
0.22 μm针式滤器、0.45 μm水系滤膜(上海安谱实验科技股份有限公司);甲醇(色谱纯,国药集团化学试剂有限公司,含量≥99.8%);磷酸二氢钾(天津市大茂化学试剂厂,含量≥99.5%);磷酸二氢钠(国药集团化学试剂有限公司,含量≥99.0%);冰醋酸(国药集团化学试剂有限公司,含量≥99.5%);乙酸钠(沈阳沈一精细化学品有限公司,含量≥99.0%);磷酸(沈阳化学试剂厂,含量≥85%);碘硝酚标准品(实验室自制,含量98.7%);碘硝酚原料药(沈阳伟嘉牧业技术有限公司,批号15112201、15112101、15111801、15112301);碘硝酚注射液(沈阳伟嘉牧业技术有限公司,批号16080901、16052401、16022901、15082401);硝氯酚(实验室自制,纯度99.75%)。
1.2 实验方法
供试品溶液:精密称定碘硝酚原料药(粉末)10 mg,加甲醇定容于10 mL容量瓶中,再取800 μL上述溶液加甲醇定容于10 mL容量瓶,即得80 mg/L供试品溶液;精密吸取100 μL碘硝酚注射液,加甲醇定容于10 mL容量瓶中,再取400 μL上述溶液加甲醇定容于10 mL容量瓶,即得80 mg/L供试品溶液。
内标液:精密称定硝氯酚10 mg,加甲醇定容于10 mL容量瓶中,得1 mg/mL的硝氯酚内标物储备液。
1.2.2 色谱条件 色谱柱为依利特Sino Chrom C18(5 μm,4.6 mm×200 mm);流动相为甲醇-0.02 mol/L磷酸二氢钾溶液(70∶30,磷酸二氢钾溶液pH 2.6);进样量为20 μL;流速为1 mL/min;检测波长为235 nm;柱温为30 ℃。
2 结果与讨论
2.1 检测波长的选择
根据高效液相色谱仪的DAD检测器进行全波长扫描,发现碘硝酚标液在235 nm处有最大吸收响应值,因此,本实验选择检测波长为235 nm。
2.2 流动相的选择
先后采用甲醇-水[14]、甲醇-5.4%冰醋酸水溶液(pH 2.3)[13]、甲醇-0.2 mol/L磷酸二氢钠溶液(pH 5.0)、甲醇-0.15 mol/L乙酸钠溶液(pH 4.3)、甲醇-0.02 mol/L磷酸二氢钾溶液(pH 2.6)体系进行样品分析。结果表明,采用甲醇-水为流动相时,无法使目标物获得可定量分析的色谱峰形,这是由于碘硝酚结构中含有酚羟基,在邻位两个碘原子的作用下酸性较强,并在弱碱及中性环境中较易解离。因此在该条件下,碘硝酚不成峰形。
采用甲醇-5.4%冰醋酸水溶液为流动相时,碘硝酚的色谱峰出现拖尾;碘硝酚因呈酸性而易解离,可通过降低流动相的pH值,使其更加稳定。H+的增加可以有效抑制药物的电离,减少其与色谱柱中游离硅羟基的作用,防止色谱峰拖尾,从而提高检测的准确性和精密度。但在该酸性体系中,流动相经混合后形成的有机溶液中H+浓度的波动性较大,使pH值不能稳定维持在一定范围内,从而不能有效抑制碘硝酚的电离,故峰形易出现拖尾。
企业内部控制管理是以专业管理制度为基础,以风险防范和有效监督管理为目的,通过打造完善的过程性管控体系、流畅的管控流程来为企业经营发展保驾护航的一种规范性行为。有效的内部控制管理对实现企业的统筹性经营发展意义重大,在有效的内部控制管理约束下能够引导各部门员工更好的落实自己的职责,确保企业财务管理信息的真实有效,将企业发展运营过程中可能遇到的财务风险控制在合理范围内。
采用甲醇-0.2 mol/L磷酸二氢钠溶液(pH 5.0)、甲醇-0.15 mol/L乙酸钠溶液(pH 4.3)为流动相时碘硝酚的色谱峰均出现前延现象,且后者较易出现基线漂移;主要原因是被分析物和键合相硅醇基之间的离子干扰。由于一般碘硝酚溶液的pH值为4.0左右,该缓冲盐体系pH值高于药物,因此不能保证碘硝酚在溶液中以原型形式存在。
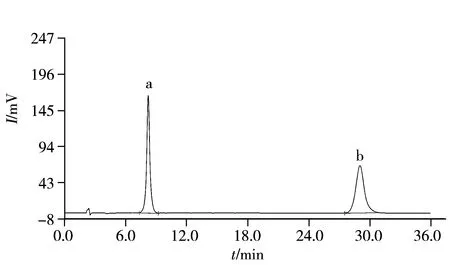
图1 甲醇-0.02mol/L磷酸二氢钾流动相条件下碘硝酚和硝氯酚的色谱图Fig.1 Chromatogram of disophenol and nitroclofene with methanol-0.02 mol/L potassium dihydrogen phosphate mobile phase a.disophenol(碘硝酚),b.nitroclofene(硝氯酚)
而采用甲醇-0.02 mol/L磷酸二氢钾溶液(pH 2.6)为流动相时碘硝酚与硝氯酚的分离度较好,峰形理想,符合试样检测要求(见图1)。在反相色谱条件下可离解的化合物可以选择合适的缓冲液离子强度以及稳定的pH值来保证可离解的官能团处于一种游离形式,从而使色谱峰形得到显著改善。经综合分析色谱条件后,最终采用甲醇-0.02 mol/L磷酸二氢钾溶液(70∶30,pH 2.6)为流动相。
2.3 色谱柱的选择
先后采用Dikma C18(5 μm,4.6 mm×250 mm)和依利特Sino Chrom C18(5 μm,4.6 mm×200 mm)色谱柱进行测试,以考察方法的适用性,结果表明两者的柱效、分离度均良好。综合考虑色谱柱的洗脱体积、保留时间等因素,最终选用依利特Sino Chrom C18(5 μm,4.6 mm×200 mm)色谱柱进行后续考察。
2.4 内标物的选择
先后采用苯甲酸和硝氯酚作为内标物,在“1.2.2”色谱条件下进样分析。结果表明,苯甲酸色谱峰出现前延现象,且色谱峰保留时间较短(为3.8 min)。使用该内标物测定碘硝酚在体内的血药浓度变化时,将不利于其与血浆中较大极性的基质进行分离,从而造成色谱峰相互干扰影响测定结果;而硝氯酚与碘硝酚的物理化学性质以及色谱行为和响应特征基本相似,色谱峰峰形较好,且硝氯酚的保留时间为29.0 min,与碘硝酚色谱峰的保留时间间隔约为20 min,当进行血药浓度测定时将有利于与血浆中极性较大的基质分离,符合作为内标物的要求。综上选用硝氯酚作为内标物。
2.5 标准曲线、检出限与定量下限
分别精密吸取适量碘硝酚标准品储备液于10 mL容量瓶并分别加入适量内标液,用甲醇定容至刻度,制得内标物浓度为60 mg/L,碘硝酚浓度分别为20、40、60、80、100、120 mg/L的系列标准液。按“1.2.2”色谱条件进行实验,以碘硝酚浓度为横坐标(x,mg/L),碘硝酚与内标物的峰面积比为纵坐标(y),绘制标准曲线。结果表明,碘硝酚质量浓度在20~120 mg/L范围内呈线性,其回归方程为:y=0.011 7x-0.015,r=0.999 6。以3倍信噪比(S/N=3)计算碘硝酚的检出限为0.15 mg/L,10倍信噪比(S/N=10)计算碘硝酚的定量下限为1.5 mg/L。
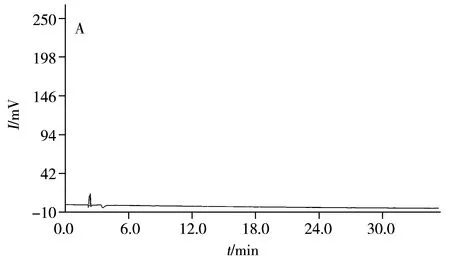

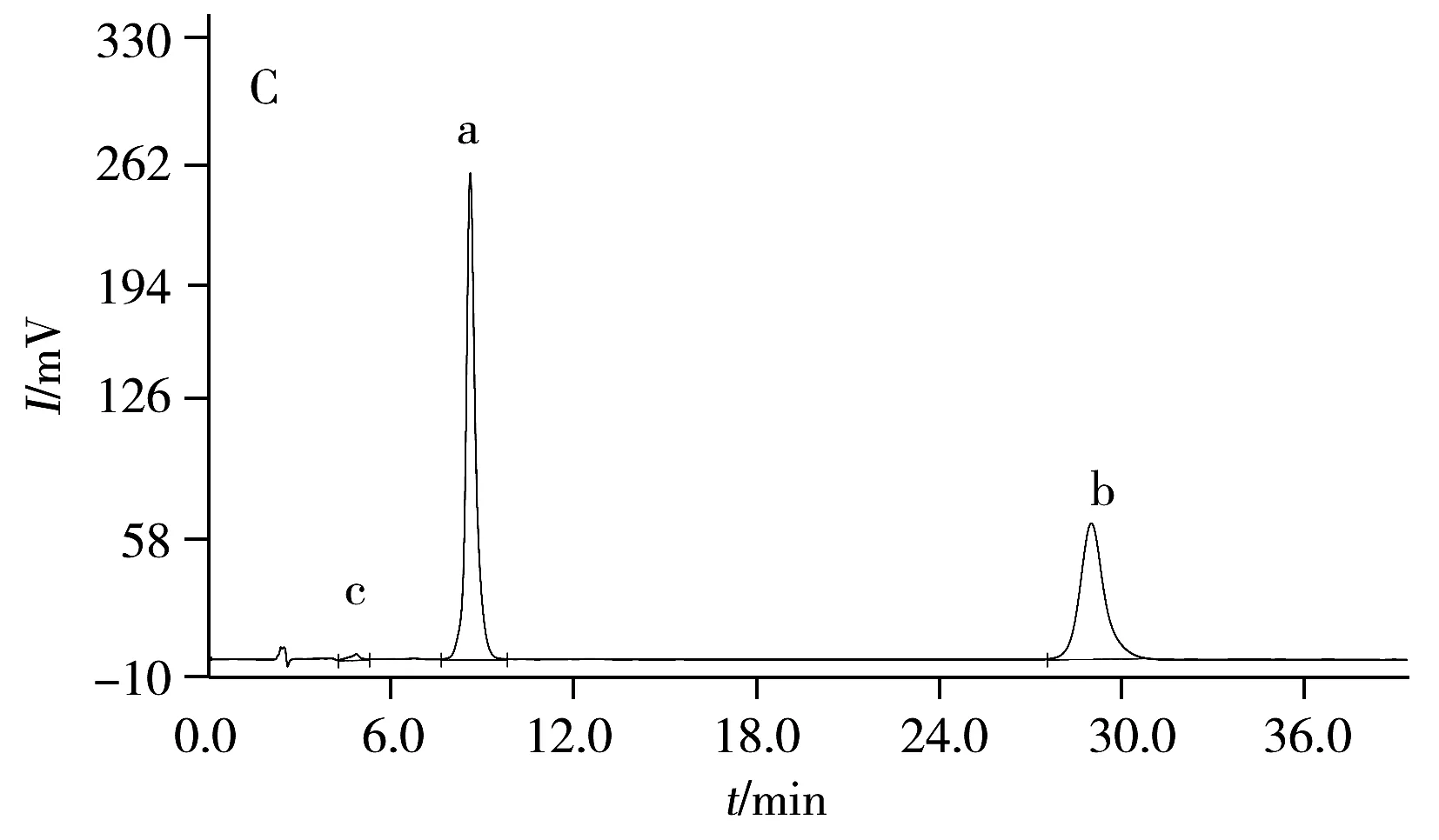
图2 溶剂、碘硝酚、硝氯酚以及实际样品的色谱图Fig.2 Chromatograms of solvent,disophenol,nitroclofene and a real sampleA.solvent,B.disophenol and nitroclofene,C.a real sample;a.disophenol,b.nitroclofene,c.impurity
2.6 专属性与系统适应性试验
分别精密吸取碘硝酚与硝氯酚的标准品溶液、供试品溶液以及溶剂各20 μL,按“1.2.2”色谱条件进行实验,测得碘硝酚的保留时间为8.3 min,硝氯酚的保留时间为29.0 min,二者分离度大于1.5,分离效果较好,色谱图见图2。
2.7 精密度与准确度
准确称取同一批号碘硝酚原料药样品3份,按“1.2.1”方法制备成80 mg/L的供试品溶液,分别加入约相当于供试品溶液中碘硝酚含量80%、100%、120%的标准品溶液,即分别加入浓度为64、80、96 mg/L的标准品溶液,并分别加入600 μL内标液,制得低、中、高3个浓度的溶液,每个浓度设6个平行,按“1.2.2”色谱条件进行实验,用内标法计算碘硝酚低、中、高3种浓度的平均回收率分别为96.0%、98.2%、90.4%,相对标准偏差(RSD)分别为0.72%、0.18%、0.18%。结果表明该方法的精密度和准确度良好。

表1 实际样品的含量测定结果
2.8 稳定性与重复性
准确称取同一批号碘硝酚原料药样品,按“1.2.1”方法制备成供试品溶液,分别在样品配制后的0、2、4、6、8、12 h按“1.2.2”色谱条件进行测定,用内标法计算得碘硝酚的平均含量为95.61%,RSD为0.34%。结果表明该方法的稳定性良好。
准确称取同一批号碘硝酚原料药样品5份,按“1.2.1”方法制备成供试品溶液,按“1.2.2”色谱条件进行测定,重复6次,用内标法计算得碘硝酚的平均含量为95.65%,RSD为0.27%。结果表明该方法的重复性良好。
2.9 实际样品的测定
分别取不同批次的待测样品按“1.2.1”方法制备成供试品溶液(其中分别加入600 μL内标溶液),按“1.2.2”色谱条件进行实验,结果见表1。结果表明,与中华人民共和国兽药典2015年版中的两种检测方法(紫外分光光度法、沉淀滴定法)相比[8],使用本方法测定的实际样品中碘硝酚含量均明显降低。原因可能为碘硝酚原料药中的有关杂质,如对硝基苯酚等与碘硝酚在紫外光谱上有着相似的最大吸收波长,传统的紫外分光光度法无法进一步区分,故含量测试结果偏高。而高效液相色谱-内标法检测碘硝酚的含量能排除有关杂质的干扰,分析精度相对较高,结果更加准确。
3 结 论
本文建立了高效液相色谱-内标法检测碘硝酚的含量,方法简便快捷,结果更加准确,可为碘硝酚质量标准的建立和优化提供参考依据,同时为碘硝酚的体内药动学研究提供理论基础,也将为改变剂型、给药途径、应用对象等方面的研究提供思路。
[1] Reinecke R K,Bruckner C,DE Villiers I L.J.SouthAfricanVeternaryAssoc.,1981,52(3):195-200.
[2] Broughton B J,Davis M,Wright D E.J.Sci.Fd.Agric.,1970,21(1):53-56.
[3] Soetedjo R,Beriajaya D,Henderson A W K,Kelly J D.Trop.Anim.HlthProd.,1980,12(4):198-202.
[4] Gao D C,Wang G M.Veter.Pharm.FeedAddit.(高德昌,王贵民.兽药与饲料添加剂),2001,3:5.
[5] Zong Z J,Wang Z M,Si Q Z R G,Da G L,Zhao R G T,Mi X G,Chen G Q,Yang Y R,Mou Y Z,Wang H T.Vet.Sci.Chin.(宗泽君,汪作民,斯钦昭日格,达古拉,昭日格图,密西格,陈国庆,杨永润,牟亚洲,王洪涛.中国兽医科技),1995,25(10):33-34.
[6] Sheng T,Chen Z,Peng F S,Wang Z Z,Zhu B F,Zhang J P,Liu H,Wang H Q,Li Y,Zhao Y G,Tao Z C,Wu C S,Zhai C Y,Wang X M.LiaoningJ.AnimalHusbandryVeter.Med.(盛涛,陈重,彭福顺,王兆智,朱宝峰,张建平,刘辉,王焕琪,李岩,赵玉贵,陶志诚,吴春生,翟成员,王晓梅.辽宁畜牧兽医),1995,25(4):32-33.
[7] Ren T W,Dong J B.GansuJ.AnimalHusbandryVeter.Med.(任天武,董建斌.甘肃畜牧兽医),2004,34(2):23.
[8] The Commission of China Veterinary Pharmacopoeia.VeterinaryPharmacopoeiaofthePeople’sRepublicofChina.Beijing:China Agriculture Publishing House(中国兽药典委员会.中华人民共和国兽药典.北京:中国农业出版社),2015:409-410.
[9] Liu H,Zhou Z F,Zou C C,Zhao J J,Sheng T,Yang J J,Liu B Q.XinjiangXuMuYe(刘辉,周自富,邹纯初,赵建杰,盛涛,杨俊杰,刘柏青.新疆畜牧业),1998,(3):35-37.
[10] Gao D H.J.Anim.HusbandryVeter.Med.(高得吼.畜牧兽医杂志),2012,31(2):13-17.
[11] Li Y Q,Pang Y H,Wang G M.Veter.Pharm.FeedAddit.(李艳芹,庞玉华,王贵民.兽药与饲料添加剂),1999,4(4):12.
[12] Li Y Q,Zhou C Y,Gao D C.Veter.Pharm.FeedAddit.(李艳芹,周成云,高德昌.兽药与饲料添加剂),2000,1:11.
[13] Chen C,Wang X L,Li Y,Xu B,Han C X.J.ShenyangPharm.Univ.(陈晨,王翔林,李阳,许彬,韩春晓.沈阳药科大学学报),2016,33(7):542-545.
[14] Liu J,Yao Y P,You M Y,Hao X,Liu Y G.Phys.Test.Chem.Anal.:Chem.Anal.(刘嘉,姚一萍,尤美云,郝星,刘迎贵.理化检验-化学分册),2016,52(2):232-234.
[15] Zhu F,Tu M Z,Wang L L,Shi D W,Wang M K.J.Instrum.Anal.(朱峰,涂貌贞,王丽莉,施点望,王明葵.分析测试学报),2013,32(3):336-339.
[16] Xu D M,Chen Y,Zhang J,Yu Y C,Feng F,Zhang F,Chu X G.J.Instrum.Anal.(徐敦明,陈燕,张缙,余宇成,冯峰,张峰,储晓刚.分析测试学报),2016,35(1):94-100.
[17] He X R,Wu Z Y,Ye Y L,Gao X D,Chen S E,Ma Z R.J.Instrum.Anal.(赫欣睿,武中庸,叶永丽,高旭东,陈士恩,马忠仁.分析测试学报),2016,35(7):922-928.
Determination of Disophenol Content in Bulk Drug and Injection by High Performance Liquid Chromatography with Internal Standard Method
SUN Ting-ting1,TIAN Kai2,WANG Hong-li2,YANG Jie1,TIAN Chun-lian1,LIU Ming-chun1,NIU Sheng-li1*
(1.Institute of Animal Husbandry and Veterinary Medicine,Shenyang Agricultural University,Shenyang 110866,China;2.Shenyang Vica Animal Husbandry Technology Limited Company,Shenyang 110027,China )
A simple and rapid method was developed for the determination of disophenol in bulk drug and injection via high performance liquid chromatography(HPLC) with the internal standard method.The sample was prepared with methanol to the test concentration,and filtrated with microfiltration membrane.Separation of analytes was achieved under isocratic elution on a C18column.The mobile phase consisted of a mixture of 0.02 mol/L potassium dihydrogen phosphate(pH 2.6) and methanol(30∶70),and was delivered at a flow rate of 1 mL/min.The UV detection was set at 235 nm,and the column temperature was maintained at 30 ℃.The internal standard was nitroclofene and the injection volume was 20 μL.Under the optimum experimental conditions,the proposed HPLC-internal standard method provided a good linearity in the range of 20-120 mg/L for disophenol with the correlation coefficients(r) of 0.999 6.The average recoveries of disophenol at three spiked concentration levels of 64,80 and 96 mg/L were in the range of 90.4%-98.2%,with relative standard deviations(RSDs) of 0.18%-0.72%.The limits of quantitation(LOQs,S/N=10) and limits of detection(LODs,S/N=3) were 1.5 mg/L and 0.15 mg/L,respectively.With good precision,stability and repeatability,the established method was simple,accurate,rapid and reliable for the determination of disophenol in bulk drug and injection.
disophenol;nitroclofene;determination;high performance liquid chromatography(HPLC);internal standard method
2017-02-24;
2017-04-23
10.3969/j.issn.1004-4957.2017.08.016
O657.72;O625.312
A
1004-4957(2017)08-1038-05
*通讯作者:牛生吏,博士,讲师,研究方向:新型兽药研发与创制,Tel:024-88487156,E-mail:niushengli1@163.com
