一种新型大环内酯类抗菌剂-泰地罗新
2017-08-30王宏磊刘义明徐飞亢继俊李秀波中国农业科学院饲料研究所国家饲料药物基准实验室
王宏磊 刘义明 徐飞 亢继俊 李秀波/中国农业科学院饲料研究所国家饲料药物基准实验室
一种新型大环内酯类抗菌剂-泰地罗新
王宏磊 刘义明 徐飞 亢继俊 李秀波/中国农业科学院饲料研究所国家饲料药物基准实验室
泰地罗新(Tildipirosin)是一种新型动物专用十六元环大环内酯类半合成抗生素,最早是由英特威国际有限公司(Intervet International BV)开发的,为泰乐菌素的衍生物。2011年3月8日,荷兰英特威公司以泰地罗新为主要成分的无菌注射液(商品名为Zuprevo)通过了欧盟兽用药品委员会(CVMP)的审批,随后在欧盟国家相继批准上市,CAS号为328898-40-4。现今,全球的猪、牛养殖业面临的主要问题是呼吸系统的高发病率和死亡率。泰地罗新是广谱抗菌药,对一些革兰氏阳性和革兰氏阴性细菌均有较强的抗菌活性,对引起猪、牛呼吸系统疾病的病原菌尤其敏感。而且具备动物专用、用量少、一次给药全程治疗、超长的消除半衰期、生物利用度高、低残留、使用安全等优点。
一、理化性质
泰地罗新是一种半合成的天然泰乐菌素的衍生物,分子式为C41H71N3O8,相对分子质量为734.02,化学名为 20,23- 二哌啶基-5-O-碳霉胺糖基-泰乐内酯,常温下为一种白色粉末,熔点为192℃,溶于极性有机溶剂(如丙酮、甲醇等),微溶于水。它是一种16个环的大环内酯类抗生素,其独特的化学结构是在C20和C23上含有两个哌啶取代基,C5上有一部分碳霉糖,其环上的三个N原子易于质子化。结构式见图1。
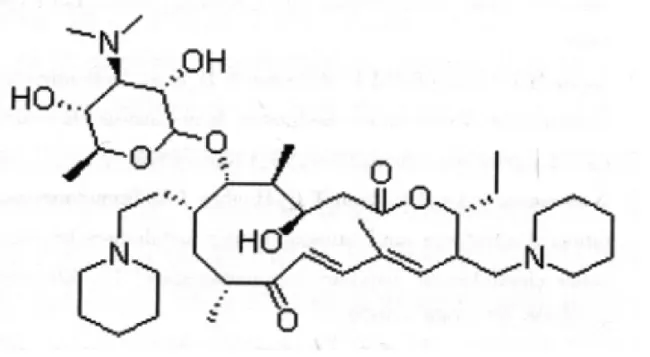
图1 泰地罗新的结构式
二、作用机制
泰地罗新与其他大环内酯类药物的作用机理相同,能不可逆地与敏感菌的核糖体50S亚基的23S rRNA结合,抑制氨酞tRNA的氨酸末端的结合,进而抑制mRNA-氨酞-tRNA-核糖的复合物的形成。但不与哺乳动物的80S核糖体结合,这可能是其毒性较小的原因之一。
三、药理学研究
1.抗菌活性。泰地罗新的体外抗菌活性受pH值的影响较大,在酸性环境时,环上的三个氨基不同程度的被质子化,使其形成不同的带电形式(0,1,2,3),导致其不溶于脂类化合物中,致使通过细菌细胞膜的能力下降,影响了抗菌效果。所以把培养基的pH控制在7.2~7.4的弱碱性环境能够获得最低抑菌浓度。泰地罗新是广谱抗菌药,对一些革兰氏阳性和革兰氏阴性细菌均具有抗菌活性,对引起猪、牛呼吸系统疾病的病原菌尤其敏感,如胸膜肺炎放线杆菌、多杀性巴氏杆菌、支气管败血波氏杆菌、副猪嗜血杆菌以及溶血性曼海姆菌、睡眠嗜组织菌等。也有研究表明泰地罗新对支原体和布氏杆菌有很好的抑菌效果,Bartram等对支原体感染的呼吸道疾病的牛研究表明,给患病牛单剂量4 mg/kg体重皮下注射后,在给药后的第14d,泰地罗新能够显著地降低肺组织的损伤、死亡率、抑郁症、不正常的呼吸。Dieste等对感染布氏杆菌的猪按单剂量或双剂量4 mg/kg体重皮下注射后,具有很好的抑菌效果。并且当和土霉素连用时,药效最佳。
European Medicines Agency(EMA)的数据资料显示,对从德国、匈牙利、西班牙、法国、荷兰、比利时、丹麦、波兰和英国在2005—2010年分离的349株猪呼吸系统病原菌和256株牛呼吸系统病原菌进行泰地罗新体外抗菌活性测定试验,结果见表1。
2.药代动力学。
Menge等按4 mg/kg体重单剂量皮下给牛注射泰地罗新后,研究了其药代动力学特征,达峰时间Tmax为 23 min,峰浓度 Cmax为 0.7 μg/ml,从给药到最后一次可测到药物浓度的平均滞留时间是6 d,半衰期T1/2为9 d。峰浓度Cmax和药时曲线下面积AUC与动物的性别无关。绝对生物利用度为78.9%,由消除相计算的分布容积(Apparent volume of distribution,Vz) 为49.4 L/kg,血浆清除率(Disposition rate constant,CL) 为 144 ml/h/kg。Rose等对猪按4 mg/kg体重单剂量肌内注射,达峰时间Tmax为 23 min,峰浓度 Cmax为 0.9 μg/ml,从给药到最后一次可测到浓度的平均滞留时间和半衰期T1/2都是4 d。药时曲线下面积不受动物的性别影响。与其他大环内酯类药物相比,如泰拉霉素Vz为11.0 L/kg、CL为180 ml/h/kg,加米霉素Vz为 24.9 L/kg、CL 为 712 ml/h/kg,替米考星 Vz为 15.3 L/kg、CL为686 ml/h/kg,泰地罗新具有分布容积大、血浆清除率低的优点。泰地罗新对支气管和肺的亲和力较高;各组织中,肺组织药物浓度最高且作用持久,支气管和肺中的药时曲线下面积远远超过血浆的。Menge等对牛皮下注射给药4 h,肺组织达峰浓度 9.2 μg/g,24 h时,峰浓度 Cmax为 14.8 μg/g,28 d 时缓慢降至2 μg/g。支气管中,泰地罗新的浓度在4 h和10 h的浓度分别为 1.5 μg/g 和 3 μg/g,在 1 d 和3 d之间保持峰浓度为3.5 μg/g,在21 d缓慢下降到1.0μg/g。泰地罗新在肺和支气管的半衰期(Elimination half-life,T1/2)接近10 d 和 11 d。随着缓慢的消除,泰地罗新迅速地、广泛地被分配到呼吸道中。Rose等对猪按4 mg/kg体重剂量皮下注射泰地罗新,于呼吸道感染部位快速聚集,2 h时肺中的浓度为3.1 μg/g,在1 d时,出现最大的浓度为4.3 μg/g,在17 d时,缓慢下降到0.8 μg/g。 在 5 d、10 d 和 14 d,支气管中的浓度分别为14.3 μg/g、7.0 μg/g 和 6.5 μg/g。 在 肺中的半衰期T1/2为7 d。给药14 d后,肺组织是血浆中药物浓度的618倍。上述试验表明,泰地罗新在胃肠消化道内吸收率很低,肌肉、皮下注射吸收迅速,达峰时间短,消除半衰期长,生物利用度高,能够很快地分布于呼吸道中,并在支气管和肺处聚集,肺处的药物浓度最高,有利于治疗猪牛的呼吸道疾病。由于其为碱性有机化合物,脂溶性较高,很容易穿过细胞膜,因此在动物体内分布广泛。
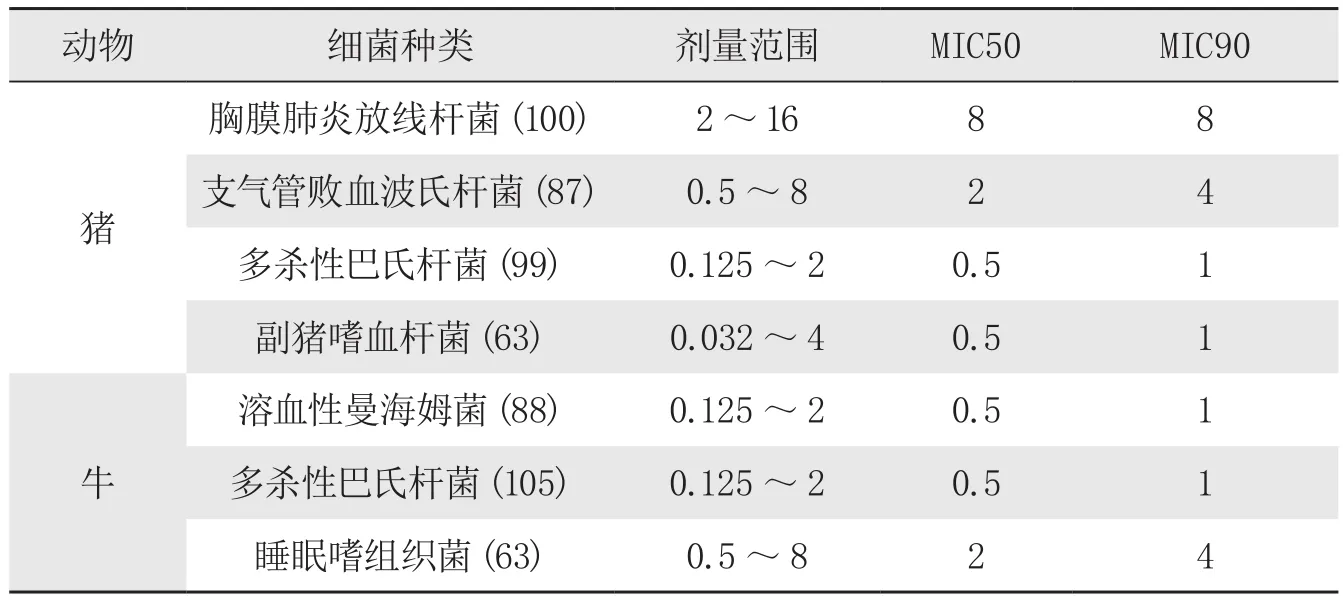
表1 泰地罗新对呼吸系统病原菌的抗菌活性。μg/ml
EMA用Wistar鼠和Beagle狗以口服给药的方式进行了泰地罗新的药动学试验。两种动物的实验都表明泰地罗新的血浆浓度没有显著地性别差异,狗的生物利用度明显高于鼠。鼠的体内试验表明,单剂量和多剂量口服给药没有明显的药物积累现象。泰地罗新主要经过粪便排泄。在25 mg/kg体重的低剂量组,雄性和雌性鼠通过粪便排泄的泰地罗新的量都是92%。在25 mg/kg体重的高剂量组,雄性和雌性鼠分别为85%和83%。雄性和雌性狗分别为65%和62%。通过尿液的排泄途径非常的少,雄性和雌性狗分别为7%和11%。排泄物中的主要代谢物是硫酸盐偶联形式,在粪便中,雄性和雌性分别占27%和34%。粪和尿液中有未降解的泰地罗新,分别占6%和16%,未降解的泰地罗新是肾脏排泄的主要形式。
EMA以放射标记的泰地罗新进行猪与牛的体内代谢试验。结果表明,泰地罗新在猪和牛体内的代谢方式大致相似,大部分通过原药形式排出体外,很少一部分通过如下方式代谢:泰地罗新水解(开环)后还原或与硫酸盐偶联、去甲基化、羟基化、与S一半胱氨酸或S一谷胱甘肽偶联,其代谢过程类似于其他大环内酯类抗生素。
四、毒理学
泰地罗新的急性毒性较小,大鼠以1 700 mg/kg体重剂量口服,未见不良反应现象;以2 000 mg/kg体重剂量口服时,轻微至中度竖起皮毛、轻度至中度镇静、驼背、协调性稍差、眼睛半闭或全闭、严重流涕。但这些不良反应都是可逆的。尸检时没有发现肉眼可见的病理变化。6.25 mg/kg体重剂量静脉给药时,大鼠出现严重的运动不协调、轻微至重度的抽搐、急促呼吸、腹侧平躺、翻滚。12.5 mg/kg体重剂量静脉给药时,大鼠有死亡的现象,高于该剂量立即死亡。尸检时没有发现肉眼可见的病理变化。大鼠在静脉给药时LD50范围为:6.25~12.5 mg/kg bw。大鼠与狗分别按每日0、40、160、640 mg/kg体重与0、20、60、180 mg/kg体重剂量,连续口服给药4个周,进行重复剂量毒性研究,结果确定大鼠NOEL(最大无作用剂量)为每日20 mg/kg体重。由于在狗的每个试验组都有副作用现象,所以没有确定狗的NOEL,狗的LOEL(最小有作用剂量)为20 mg/kg体重。EAM对大鼠和兔子进行了泰地罗新致癌、致畸、致突变的三致试验,结果表明,泰地罗新没有致癌、致畸、致突变的效应。母代和胚胎的NOEL是30 mg/kg·bw/day。猪以20 mg/kg体重单剂量肌肉注射时,未产生明显毒理变化,但注射部位出现不适及肿胀现象,白细胞、肌酸激酶、中性粒细胞和单核细胞数目增加。
五、残留
EMA对14C-泰地罗新在猪、牛的肌肉、肝、肾等可食性组织中残留研究结果表明,猪和牛的肝、肾和注射部位残留浓度最高,其次是脂肪和肌肉。由于脂肪和肌肉含有的泰地罗新最少,所以脂肪和肌肉不被认为是靶组织。且各组织的残留分布、残留标示物及总残留的比值一般是恒定的,规定猪和牛的休药期分别为9 d和47 d。泰地罗新在猪的各组织中的最大残留量分别为:肌肉 1 200 μg/kg,脂肪 800 μg/kg,肝 5000 μg/kg,肾 10 000 μg/kg,注射位点7 500 μg/kg。在牛的各组织中的最大残留量分别为:肌肉400 μg/kg,脂肪 200 μg/kg,肝2000 μg/kg,肾 3 000 μg/kg,注射位点11500 μg/kg。泰地罗新不能用于泌乳期奶牛。CVMP的研究结果表明,一般情况下,按合理的给药方案,经过休药期后,各组织的残留量均低于规定标准。
现今,检测泰地罗新残留的有效分析方法是固相萃取液一质联用(SPE—HPLC—MS/MS)技 术, 牛的肝、肾、脂肪的检测限分别为3 μg/kg、44 μg/kg、27 μg/kg,猪的肾、皮肤与脂肪的检测限分别为37 μg/kg、53 μg/kg;牛和猪各组织的定量限分别为:脂肪和脂肪与皮肤都是150 μg/kg,肝和肾都是250 μg/kg。该方法不适用于检测肌肉中的残留。
六、泰地罗新在动物生产中的应用
目前,国外已有关于泰地罗新预防、治疗猪和牛呼吸系统疾病的疗效报道。Miyake等采用肉汤微量稀释法比较泰地罗新与替米考星对巴氏杆菌的抗菌活性,。试验结果表明泰地罗新的抗菌活性明显比替米考星要好;与此同时,还比较了泰地罗新和替米考星对患有呼吸道疾病牛的治疗效果,替米考星试验组的牛每天以10 mg/kg体重皮下注射药物,泰地罗新试验组的牛以单剂量4 mg/kg体重皮下注射。5 d后,对两个试验组的牛进行死亡率和治愈率的统计,并分离鉴定细菌。结果表明,泰地罗新组的治愈率高于替米考星组。泰地罗新试验组的牛未分离到多杀性巴氏杆菌和嗜血巴氏杆菌,而替米考星试验组则能分离得到。说明泰地罗新的治疗效果要好于替米考星,并且泰地罗新对动物转运过程中的发烧症状亦有较佳的预防与治疗效果。Rose等报道了泰地罗新对牛呼吸道感染致病菌溶血性曼海姆菌的治疗效果,按4 mg/kg体重单剂量皮下注射给药,试验采集的所有样本中溶血性曼海姆菌均低于定量限 (LOQ=10 CFU/g)。英特威公司比较了泰地罗新(4 mg/kg体重单剂量肌内注射)和氟苯尼考治疗患有呼吸道系统疾病猪的治愈率,泰地罗新的治愈率要高于氟苯尼考,治愈率分别为86%和81%;还比较了泰地罗新(4 mg/kg体重单剂量肌内注射)和泰拉霉素治疗患有呼吸道系统疾病猪的治愈率,泰地罗新的治愈率和泰拉霉素的治愈率相近,治愈率分别为93%和92%,两个试验组的猪的增重没有明显的差异。Rohdich等比较了泰地罗新(4 mg/kg体重单剂量皮下注射)和泰拉霉素(2.5 mg/kg体重单剂量皮下注射)治疗患有呼吸道系统疾病牛的治愈率和死亡率,泰地罗新的治愈率明显高于泰拉霉素,治愈率分别为84.8%和79.3%,泰地罗新组没有死亡,泰拉霉素治疗组的死亡率为0.6%,说明泰地罗新在治疗牛的呼吸道系统疾病的效果明显好于泰拉霉素。Secretariat等比较了泰地罗新和泰乐菌素治疗患有呼吸道疾病牛的治愈率,结果显示,泰地罗新的治愈率为84.4%,而泰乐菌素的治愈率仅有79.3%,说明泰地罗新治疗牛的呼吸道系统疾病的治疗效果也强于泰乐菌素。
七、展望
目前,在我国兽医临床上使用较为广泛的大环内酯类抗生素是泰乐菌素、替米考星、氟苯尼考,这些药物在养殖生产中都取得了良好的效果,但随着使用时间的延长和应用范围的扩大,很多地区出现了不同程度的细菌耐药性,导致药物的预防和治疗效果在逐年下降,并且需要多次给药才能发挥药物的疗效。因此,急需要寻找一种更为有效的治疗猪牛呼吸道系统疾病的药物。泰地罗新是一种动物专用的大环内酯类半合成的新型抗生素、给药方式简单,而且一次给药全程治疗,超长的消除半衰期、生物利用度高、低残留、药效持久、使用安全等优点。泰地罗新对牛、猪的呼吸道疾病具有十分明显的治疗效果,药效强于泰乐菌素、替米考星,现今国内还没有关于该药物生产的报道,它的应用必将给动物生产带来巨大的福利,具有良好的开发前景。
(略)

