基于肾上腺血管解剖的后腹腔镜肾上腺切除技术的改进及临床应用
2017-08-22周昱霖唐朝朋徐振宇位志峰徐晓峰张征宇葛京平周文泉
周昱霖,唐朝朋,徐振宇,位志峰,徐晓峰,董 杰,张征宇,葛京平,周文泉
(1.江苏大学附属人民医院,江苏 镇江,212002;2.南京军区南京总医院)
·论 著·
基于肾上腺血管解剖的后腹腔镜肾上腺切除技术的改进及临床应用
周昱霖1,唐朝朋2,徐振宇2,位志峰2,徐晓峰2,董 杰2,张征宇2,葛京平2,周文泉2
(1.江苏大学附属人民医院,江苏 镇江,212002;2.南京军区南京总医院)
目的:基于对肾上腺血管解剖的理解,探讨后腹腔镜肾上腺切除术的新技术。方法:2013年12月至2015年5月共收治179例肾上腺肿瘤患者,其中男92例,女87例;肿瘤位于右侧88例,左侧91例;患者12~79岁,平均(47.8±9.8)岁;肿瘤直径0.8~11.5 cm,平均(2.8±1.3) cm。根据患者病情完善术前准备后均由同一术者根据以下策略行后腹腔镜肾上腺切除术:(1)腹膜后空间建立后沿腰大肌表面游离并纵行打开肾筋膜直至膈肌脚,寻及膈下动脉并结扎切断肾上腺上动脉;(2)寻及肾动脉,紧贴肾动脉及肾上极内侧缘夹角向深面游离,结扎肾上腺中、下动脉;(3)通过肾动脉及肾脏内侧缘所形成的“中央静脉三角”寻找肾上腺中央静脉并离断;(4)在肾脏、肾上腺之间游离,到达肾前融合筋膜层面,将肾上腺与肾脏重叠部分分离;(5)离断肾上腺周围相连的结缔组织,完整切除肾上腺。结果:178例手术获得成功,1例中转开放手术;手术时间12~68 min,平均(30.2±10.3) min;出血量10~110 ml,平均(20.6±12.7) ml;术后住院1.5~3.9 d,平均(2.3±0.8) d;2例术中出现腹膜损伤,术后随访期间未见肿瘤复发及转移。结论:此操作方法更加直接的处理肾上腺血供,减少了出血的几率,游离面较少,根据肾上腺解剖关系不用刻意寻找肾上腺肿瘤,操作更加省时、简单。
肾上腺肿瘤;肾上腺切除术;腹腔镜检查;腹膜后路径;解剖
自Gagner等[1]于1992年首次报道腹腔镜肾上腺切除术以来,腹腔镜肾上腺切除术已取代开放手术成为大多数肾上腺肿瘤治疗的金标准,常用手术方法包括经腹腹腔镜肾上腺切除术、腹膜后腹腔镜肾上腺切除术等,国内以经后腹腔途径为主,其中尤以张旭[2-3]的解剖性后腹腔镜肾上腺切除术应用最为广泛,经过多年的临床实践我们发现,此方法虽然实用,但存在一些需要改进之处。我们根据肾上腺的血管解剖特点总结出一种新型的后腹腔镜肾上腺切除技术与策略,应用于临床取得了很好的效果。现报道如下。
1 资料与方法
1.1 临床资料 2013年12月至2015年5月入院诊断为肾上腺肿瘤患者共179例,均为单侧病变,其中男92例,女87例;肿瘤位于右侧88例,左侧91例;患者12~79岁,平均(47.8±9.8)岁;肿瘤直径0.8~11.5 cm,平均(2.8±1.3) cm。术前诊断为醛固酮增多症27例,嗜铬细胞瘤30例,皮质醇增多症12例,髓样脂肪瘤15例,肾上腺转移癌2例,无功能腺瘤93例。
1.2 术前处理 术前诊断为醛固酮增多症的患者,予以螺内酯、补钾治疗,待患者血钾正常后再手术治疗;诊断为嗜铬细胞瘤的患者,予以酚苄明治疗至少2周,待患者血压正常后收住院,术前3 d予以扩容治疗;皮质醇增多症的患者,术前补充皮质激素,纠正水、电解质及酸碱平衡失调。
1.3 麻醉及手术方法 均气管内插管全身麻醉,术前考虑嗜铬细胞瘤的患者采用颈内静脉置管。(1)后腹腔空间的建立:患者取健侧卧位,抬高腰桥,于腋中线髂嵴上1 cm处穿刺10 mm Trocar,通过气腹管充入CO2,压力维持在12~15 mmHg,置入腹腔镜,直视下将腹膜推向腹侧,退出镜头,置入自制乳胶气囊,注气300 ml,维持3 min,取出气囊直视下分别于腋前线肋缘下、腋后线肋缘下穿刺5 mm、10 mm Trocar,置入相应器械,建立后腹腔间隙。(2)肾上腺上动脉的处理:观察后腹腔重要解剖标志腰大肌,用LigaSure沿腰大肌表面游离,纵行打开肾筋膜,直至膈肌脚(图1),此时可见明显呈梳状的来自膈下动脉分支的肾上腺上动脉(图2),因血管管径0.5~2.0 mm[4],可直接用LigaSure结扎切断肾上腺上动脉。(3)肾上腺中动脉及下动脉的处理:通过观察搏动寻及肾动脉,紧贴肾动脉及肾上极内侧缘夹角向深面游离(图3),在肾上腺下内侧与肾动脉、腹主动脉间用LigaSure大把钳夹扇形致密结缔组织(内含肾上腺中动脉及下动脉,管径分别为1.0~1.5 mm、1.0~2.0 mm[4])。(4)肾上腺中央静脉的处理:在多年的临床实践中我们发现,通过肾动脉与肾脏内侧缘所形成的“中央静脉三角”能较容易地寻找到中央静脉,即中央静脉通常与肾脏内侧缘、肾动脉所成的夹角所对的边平行,部分病例可能存在变异[5],术前或术中识别并处理这些变异可有效减少出血,术中应仔细分辨副肾动脉或肾动脉早发分支,以减少分支动脉损伤的发生。右侧:于右侧“中央静脉三角”范围内经过肾上腺下内侧与肾动脉间继续向内游离,可达腔静脉后外侧层面,沿腔静脉表面向上游离,至接近膈肌腔静脉孔下约0.5 cm可寻及右侧中央静脉汇入腔静脉处,用Hem-o-lok夹闭中央静脉,用剪刀离断,因右侧中央静脉较短,因此游离、结扎时应特别谨慎(图4)。左侧:在肾上腺下内侧与肾动脉间深面相对固定位置寻及较长的中央静脉或根据“中央静脉三角”原则由肾动脉及肾脏内侧缘所形成的夹角稍向外向深面的膈肌表面游离即可,寻找到中央静脉,用Hem-o-lok夹闭,用剪刀离断(图5)。(5)肾脏与肾上腺重合面的处理:肾脏、肾上腺间用LigaSure游离,到达肾前融合筋膜层面,将肾上腺与肾脏重叠部分分离(图6),从而将肾上腺完全切除(图7)。(6)标本的取出:将切除的肾上腺放入标本袋取出,经腋后线Trocar孔留置腹膜后引流管,关闭切口。
1.4 术后处理 术后常规预防性应用抗生素1 d,1~2 d拔除腹膜后引流管,鼓励患者早期下床活动,并根据患者食欲早期安排进食。术前诊断嗜铬细胞瘤或原发性醛固酮增多症的患者,观察血压或电解质变化,并对症处理;术前诊断皮质醇增多症的患者,补充激素治疗;术后1~2 d安排出院。
1.5 术后随访 术后第3、6、12个月门诊复查,1年后每年复查1次,检查血压、电解质、肾上腺激素及腹部B超。
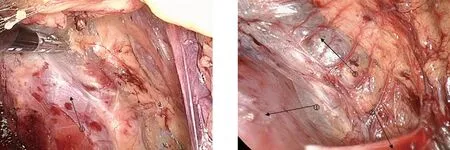
图1 以腰大肌为标志纵行切开肾周筋膜图2 暴露肾上腺上动脉并结扎
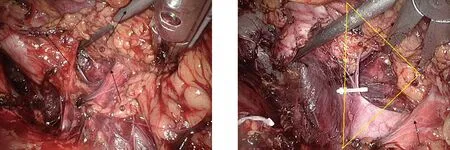
图3 游离肾动脉与肾上腺间结缔组织 图4 右侧“中央静脉三角”

图5 左侧“中央静脉三角”图6 游离肾上腺与肾脏重合面
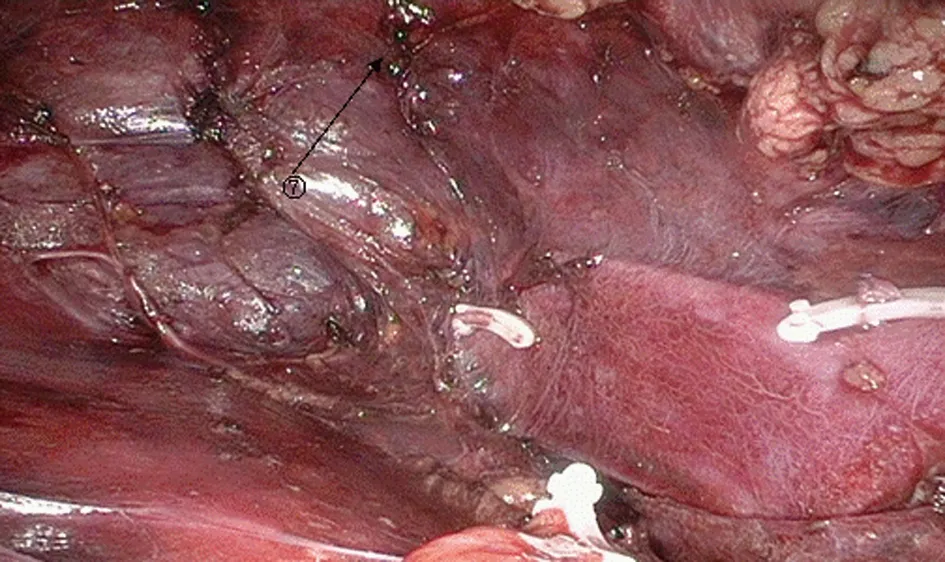
图7 完整切除肾上腺
备注:①腰大肌;②肾动脉;③梳状血管(肾上腺上动脉);④肾上腺;⑤肾脏;⑥中央静脉;⑦腹膜
2 结 果
178例手术获得成功,1例巨大肾上腺髓样脂肪瘤患者,因术中破裂出血改行开放手术;手术时间12~68 min,平均(30.2±10.3) min;出血量10~110 ml,平均(20.6±12.7) ml;术后住院1.5~3.9 d,平均(2.3±0.8) d;术中出现腹膜损伤2例,用Hem-o-lok夹闭。术后病理示:肾上腺皮质腺瘤115例,嗜铬细胞瘤37例,节细胞神经纤维瘤5例,皮质增生3例,成熟畸胎瘤2例,髓样脂肪瘤15例,肺癌肾上腺转移2例。术后患者均获随访,未见肿瘤复发及转移。
3 讨 论
对于需要手术切除的肾上腺肿瘤,自Gagner等[1]1992年报道腹腔镜下肾上腺切除术以来,经过多年的临床实践对比,与开放手术相比,腹腔镜手术具有以下优势[6-9]:(1)较低的并发症发生率;(2)术中失血少;(3)切口疼痛较小;(4)减少患者对麻醉剂的要求;(5)患者能尽早恢复活动与饮食;(6)缩短住院时间;(7)降低整体成本。因此腹腔镜手术已取代开放手术成为大多数肾上腺肿瘤治疗的金标准[10]。
腹腔镜肾上腺切除术的途径包括经腹、经腹膜后、经胸、经胸腹等。与经腹入路相比,经腹膜后入路不经过腹腔,减少了腹部并发症的发生,对于有腹部手术史的患者更加适用。研究[11-12]证实,经后腹腔途径较经腹途径减少了术后疼痛、缩短了住院时间,而手术时间相当。
国内最常用的手术方法为经腹膜后腹腔镜肾上腺切除术,尤以张旭[2-3]的“解剖性后腹腔镜肾上腺切除术的手术方法和技巧”应用最为广泛,即打开肾周筋膜后在三层相对无血管分离层面进行分离,第一分离层面为前层肾筋膜与肾周脂肪囊,第二分离层面为后层肾筋膜与肾周脂肪囊,第三分离层面为肾上腺底部脂肪囊与肾上极,最后分离肾上腺静脉并结扎离断,完全游离肾上腺并取出。在临床实践中我们发现此方法虽然实用,但也存在不足之处,表现在游离面大、受肾上极弧度及肾周脂肪的干扰较大,尤其肥胖患者增加了寻找肾上腺肿瘤的难度;因受到角度影响或肾周脂肪肥厚,处理中央静脉时通常比较困难,增加了中央静脉撕裂出血的可能性等[13];这种手术方法的特点是通过“相对无血管层面”游离肾上腺,这就有可能忽略或漏扎肾上腺血管,对于嗜铬细胞瘤等表面血管丰富或体积较大的肿瘤会造成不必要的出血。
为提高手术的精准度,减少不必要的组织损伤,我们所设计的手术方案为首先游离并结扎肾上腺动脉、中央静脉,进而达到在尽量减少出血的情况下完全游离肾上腺的目的。因此首先我们要理解肾上腺的血管分布及相对无血管区才能更好的驾驭肾上腺切除术。肾上腺上动脉来自膈下动脉的分支,管径0.5~2.0 mm[4],位于肾上腺的后面内上方,上动脉及其周围脂肪组织向上牵引固定肾上腺,这也是肾上腺的解剖定位标志之一;肾上腺中动脉及下动脉主要位于肾上腺下内方及内侧,管径分别为1.0~1.5 mm、1.0~2.0 mm[4];右侧中央静脉主要由肾上腺腹侧中部发出进入下腔静脉,而左侧中央静脉主要由肾上腺下内方发出进入肾静脉;肾上腺外周、前后面及底部与肾上极相邻处均为相对无血管区。
根据上述解剖特点,我们设计了以下手术路径与步骤:(1)打开肾周筋膜后,沿腰大肌表面游离并纵行打开肾筋膜,直至膈肌脚,沿肾上腺后方由外向内游离,可清晰显露膈下动脉及梳状肾上腺上动脉,离断肾上腺上动脉;(2)在肾上腺下内侧与肾动脉间离断肾上腺中、下动脉;(3)通过“中央静脉三角”寻找并离断中央静脉;(4)游离肾脏内侧缘与肾上腺重合面;(5)取出标本。与既往后腹腔镜肾上腺切除术相比,此方法具有以下特点:(1)手术视角:既往一般于腋中线髂前上棘2 cm甚至更上位置穿刺观察孔Trocar,导致手术过程需俯视手术视野,更容易失去参考标记;改进术式一般于腋中线髂前上棘1 cm处穿刺观察孔Trocar,平视下直接寻找肾上腺血管并处理,更符合人体视角;(2)肾上腺动脉血供的处理:既往通过三个相对无血管层面游离肾上腺,忽略肾上腺动脉的处理,容易漏扎肾上腺动脉导致出血,尤其肿瘤血供较丰富的患者,出血几率更高;而本方法主动离断肾上腺上、中、下动脉,减少了出血的几率;(3)此方法无需游离腹膜后脂肪,减少了出血的几率、缩短了手术时间;(4)肾上极的处理:既往需将肾上极完整游离,而此方法无需游离整个肾上极;(5)中央静脉的处理:既往手术最后处理中央静脉,受角度或肾周脂肪肥厚的影响,处理中央静脉时通常较困难,增加了中央静脉撕裂出血的可能;本方法根据“中央静脉三角”关系较早、准确地显露并离断中央静脉,操作更加直接,减少了中央静脉撕裂出血的几率;(6)肾上腺肿瘤的寻找:既往手术需完整游离肾上极脂肪才能完整暴露肾上腺,在瘤体较小或肥胖、脂肪较多的患者中寻找肿瘤较困难;此方法根据后腹腔镜下肾上腺的解剖特点及毗邻关系,无需寻找肾上腺,实现了“不寻找肾上腺的肾上腺切除”。总结见表1。
表1 两种手术方法的对比
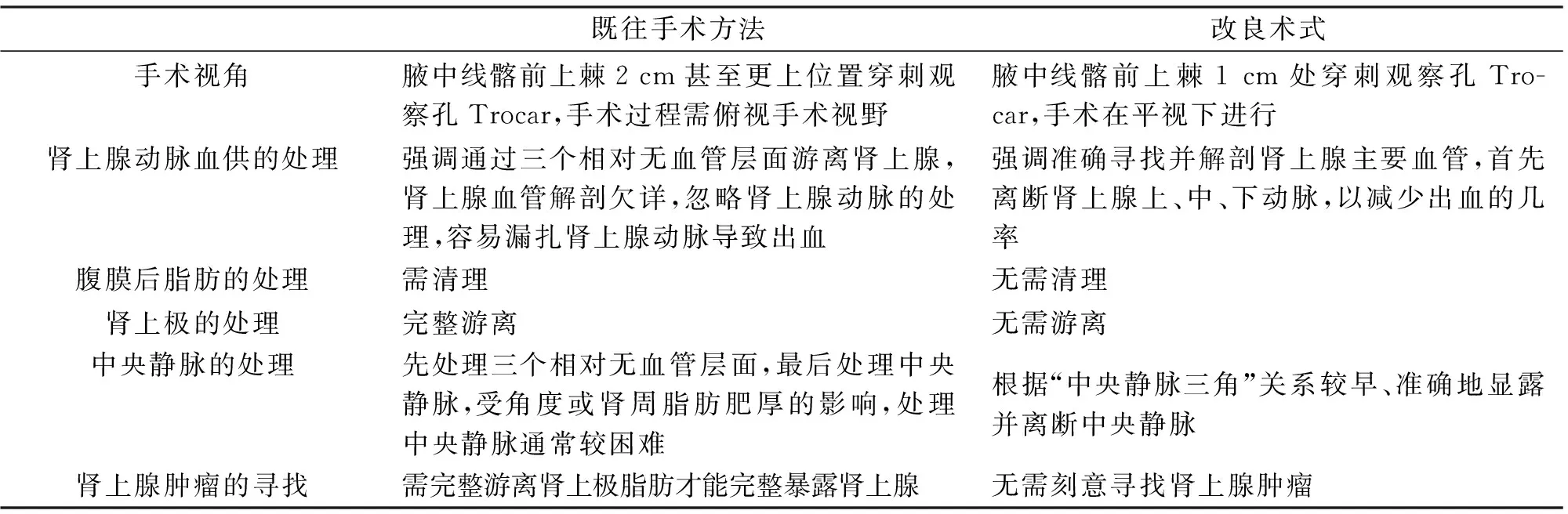
既往手术方法改良术式手术视角腋中线髂前上棘2cm甚至更上位置穿刺观察孔Trocar,手术过程需俯视手术视野腋中线髂前上棘1cm处穿刺观察孔Tro-car,手术在平视下进行肾上腺动脉血供的处理强调通过三个相对无血管层面游离肾上腺,肾上腺血管解剖欠详,忽略肾上腺动脉的处理,容易漏扎肾上腺动脉导致出血强调准确寻找并解剖肾上腺主要血管,首先离断肾上腺上、中、下动脉,以减少出血的几率腹膜后脂肪的处理需清理无需清理肾上极的处理完整游离无需游离中央静脉的处理先处理三个相对无血管层面,最后处理中央静脉,受角度或肾周脂肪肥厚的影响,处理中央静脉通常较困难根据“中央静脉三角”关系较早、准确地显露并离断中央静脉肾上腺肿瘤的寻找需完整游离肾上极脂肪才能完整暴露肾上腺无需刻意寻找肾上腺肿瘤
经过临床实践证明,基于肾上腺血管解剖的方法更加直接的处理肾上腺血供,减少了出血的几率,游离面较少,根据肾上腺的解剖关系不用刻意寻找肾上腺肿瘤,操作更加省时、简单,尤其应用于肾上腺较小肿瘤(<1 cm)、大肿瘤(>6 cm)、肥胖及肾上腺血供复杂的患者,优势更加明显。虽然部分肿瘤不用刻意分离就能很好的显露,但按照我们的方法首先控制肿瘤血供可明显减少出血及并发症的发生。
[1] Gagner M,Lacroix A,Bolté E.Laparoscopic adrenalectomy in Cushing's syndrome and pheochromocytoma[J].N Engl J Med,1992,327(14):1033.
[2] 张旭.解剖性后腹腔镜肾上腺切除术的手术方法和技巧[J].临床泌尿外科杂志,2007,22(8):561-564.
[3] Zhang X,Fu B,Lang B,et al.Technique of anatomical retroperitoneoscopic adrenalectomy with report of 800 cases[J].J Urol,2007,177(4):1254-1257.
[4] 刘欣,刘芳,李启华.肾上腺解剖学的研究进展[J].齐齐哈尔医学院学报,2008,29(13):1605-1606.
[5] 黄凯,王业华,顾晓,等.肾上腺血管的解剖特点及在腹腔镜手术中的临床应用[J].江苏医药,2014,40(23):2921-2922.
[6] 唐朝朋,周文泉,高建平.腹腔镜下肾上腺手术的研究进展[J].医学研究生学报,2012,25(12):1320-1324.
[7] Gupta PK,Natarajan B,Pallati PK,et al.Outcomes after laparoscopic adrenalectomy[J].Surg Endosc,2011,25(3):784-794.
[8] Tiberio GA,Solaini L,Arru L,et al.Factors influencing outcomes in laparoscopic adrenal surgery[J].Langenbecks Arch Surg,2013,398(5):735-743.
[9] Murphy MM,Witkowski ER,Ng SC,et al.Trends in adrenalectomy:a recent national review[J].Surg Endosc,2010,24(10):2518-2526.
[10] Smith CD,Weber CJ,Amerson JR.Laparoscopic adrenalectomy:new gold standard[J].World J Surg,1999,23(4):389-396.
[11] Lee CR,Walz MK,Park S,et al.A comparative study of the transperitoneal and posterior retroperitoneal approaches for laparoscopic adrenalectomy for adrenal tumors[J].Ann Surg Oncol,2012,19(8):2629-2634.
[12] Constantinides VA,Christakis I,Touska P,et al.Retroperitoneoscopic or laparoscopic adrenalectomy?A single-centre UK experience[J].Surg Endosc,2013,27(11):4147-4152.
[13] 徐振宇,周文泉,高建平,等.后腹腔镜肾癌根治术中保留肾上腺处置策略的研究[J].腹腔镜外科杂志,2012,17(7):519-522.
(英文编辑:黄 鑫)
A modified technique for retroperitoneal laparoscopic adrenalectomy based on adrenal vascular anatomy
ZHOUYu-lin1,TANGChao-peng2,XUZhen-yu2,etal.
1.DepartmentofUrology,theAffiliatedPeople’sHospitalofJiangsuUniversity,Zhenjiang212002,China;2.NanjingGeneralHospitalofPLANanjingMilitaryCommand
Objective:To investigate a modified technique for retroperitoneal laparoscopic adrenalectomy based on adrenal vascular anatomy.Methods:The clinical data of 179 patients (92 males and 87 females) with adrenal tumors from Dec.2013 to May 2015 were analyzed retrospectively.The average age was (47.8±9.8) years (ranging from 12 to 79).Ninety-one cases had left-located tumor and 88 cases had right-located tumor.The tumor diameter was (2.8±1.3) cm in average (ranging from 0.8 to 11.5 cm).All patients underwent retroperitoneal laparoscopic adrenalectomy according to the following protocol:(1)After the retroperitoneal working space was created,Gerota fascia was dissected near the diaphragm to the crura of diaphragm,then the superior suprarenal artery was exposed and coagulated.(2)To dissect the middle and inferior suprarenal artery,surgeons dissected along with the plane between the renal artery and the inner margin of upper pole of kidney in order to divide the connective tissues that contained middle and inferior adrenal artery.(3)Then central adrenal vein was dissected and ligated in the triangle consisting of renal artery,inner margin of kidney and central adrenal vein.(4)Dissection was made between kidney and adrenal gland till the prerenal fusion fascia level.(5) Finally,the tumor was extracted after the surrounding tissues were separated.Results:All surgeries were successful with one conversion to open surgery.The average operative time was (30.2±10.3) min (ranging from 12 to 68 min),and the mean blood loss was (20.6±12.7) ml (ranging from 10 to 110 ml).All patients were discharged from the hospital in 1.5 to 3.9 d after surgery,the average postoperative hospital stay was (2.3±0.8) d.Peritoneum perforation occurred in two cases in operation but no relapse or metastasis was found during the follow-up.Conclusions:This novel technique can dissect blood supply directly and reduce the risk of bleeding.Also,this novel technique has simplified separation plane and there is no need to find tumor during surgery based on adrenal gland anatomy,the operation is time-saving and simple.
Adrenal gland neoplasms;Adrenalectomy;Laparoscopy;Retroperitoneal approach;Dissection
1009-6612(2017)07-0481-05
10.13499/j.cnki.fqjwkzz.2017.07.481
周文泉,E-mail:shzwqzsl@163.com
周昱霖(1992—)男,江苏大学附属人民医院泌尿外科硕士研究生在读,主要从事泌尿外科的学习。
R736.6
A
2016-08-17)
