功能性消化不良患者抑郁状态与血清白介素6水平的相关性
2017-08-22刘洪娜苏少慧胡义亭王玉珍
刘洪娜,苏少慧,胡义亭,王玉珍
(1.河北医科大学 研究生学院, 河北 石家庄 050000;2.河北省人民医院 消化内一科, 河北 石家庄 050051)
·论著·
功能性消化不良患者抑郁状态与血清白介素6水平的相关性
刘洪娜1,2,苏少慧1,2,胡义亭2,王玉珍2
(1.河北医科大学 研究生学院, 河北 石家庄 050000;2.河北省人民医院 消化内一科, 河北 石家庄 050051)
目的 探讨精神心理因素引起血清白细胞介素6 (IL-6)水平变化及导致消化不良症状的可能机制。方法 选取汉密尔顿抑郁量表(HAMD)评分为轻中度抑郁(≥8且≤35分)的48例功能性消化不良(FD)患者为病例组,同期HAMD评分显示没有抑郁症状(<8分)的40例FD患者为对照组。测定所有患者血清IL-6水平,进行消化不良症状评分。结果 病例组血清IL-6水平、消化不良症状评分高于对照组(P<0.05);血清IL-6水平与HAMD评分、消化不良症状评分呈正相关(P<0.01);消化不良症状评分与HAMD评分呈正相关(P<0.01)。结论 精神心理因素在FD发病过程中起重要作用,患者抑郁程度越重,其血清IL-6水平越高,消化不良症状也越重。
消化不良;抑郁症;白细胞介素6
功能性消化不良(FD)是指起源于胃、十二指肠区域,具有上腹痛、上腹胀、早饱、恶心等症状,但缺乏任何引起上述症状的器质性、系统性或代谢疾病的一组临床综合征。流行病学统计显示,欧美国家中FD人群发病率达19%~41%,平均32%;国内为18%~45%,约占胃肠病专科门诊的50%[1]。以往研究认为其发病与胃肠动力障碍、内脏高敏感性、胃酸分泌过多、幽门螺杆菌感染、遗传易感性等因素相关,近年来随着生物-心理-社会医疗模式的发展,精神心理因素及脑肠轴功能失调、细胞因子等因素与FD发病的关系备受关注[2]。流行病学调查发现FD患者中抑郁症的发生率可高达57.0%~70.0%[3]。抑郁症患者经常以躯体症状,尤其是腹部不适、反酸烧心等胃肠道症状为主诉就诊于综合科室[4]。研究显示细胞因子介导的炎症反应可能是抑郁症的发病机制之一[5],血清白细胞介素6(IL-6)为促炎细胞因子,与抑郁症、胃肠功能有一定的相关性。然而,国内外对合并抑郁的FD患者IL-6水平变化相关报道较为少见。本研究通过对FD患者进行汉密顿抑郁量表(HAMD)评分,检测血清IL-6水平,探讨精神心理因素在FD发病过程中的作用以及伴抑郁的FD患者血清IL-6水平变化导致消化不良症状的可能机制及临床意义。
1 资料与方法
1.1 病例选择 2016年1-6月河北省人民医院消化科门诊及住院部FD患者88例,进行HAMD量表评分,HAMD评分≥8且≤35分的FD患者为病例组,共48例,其中男11例,女37例。年龄(59.02±8.96)岁,体重指数(BIM)(23.50±2.58)kg/m2;HAMD评分<8分的FD患者为对照组,共40例,其中男12例,女28例。年龄(59.20±8.52)岁,BMI(23.40±2.44)kg/m2,两组性别、年龄、BMI比较差异无统计学意义,具有可比性。
1.2 纳入及排除标准 纳入标准:(1)所有患者符合罗马Ⅲ关于FD的诊断标准[6]:①含有以下症状的一种或多种:上腹痛、上腹烧灼感、餐后饱胀和早饱;②呈持续反复发作的慢性过程:病程超过6个月,且近3个月症状持续(3个月内每个月症状持续大于3天);③以上症状在排便后仍不能缓解;④排除可以解释的代谢性、系统性及器质性病变。(2)符合中国精神障碍分类与诊断标准(CCMD-3)神经症中躯体形式障碍之胃肠紊乱的诊断标准。(3)经胃镜检查除外胃炎伴糜烂、溃疡、肿瘤等器质性病变。(4)近期查血、尿、便3大常规、生化全项、腹部超声结果正常者。(5)所有研究对象入组之前需签署知情同意书,能够配合完成HAMD量表及消化不良症状评分。排除标准:(1)伴有心、脑、肾、肝胆脾等严重系统性疾病者,如高血压、糖尿病、肝炎、甲状腺功能亢进症等。(2)其他严重精神心理疾病,近期服用抗抑郁药者。(3)妊娠期或哺乳期患者。(4)腹部手术史。(5)合并肠易激综合征者。
1.3HAMD评分HAMD评分总分<8分:正常,没有抑郁症状;总分8~20分:轻度抑郁;总分21~35分:中度抑郁;总分>35分:严重抑郁。
1.4IL-6水平检测 所有患者均空腹8~10小时,于清晨抽取静脉血5ml,收集于真空管,室温静置1~2小时后,3 000rm,离心15分钟,取上清,分装保存于-80 ℃冰箱备用,检测IL-6水平。
1.5 消化不良症状评分 对所有患者进行消化不良症状评分。主要症状包括餐后饱胀感、早饱感、上腹疼痛、食欲减退、嗳气。并以下列标准计分:0分:无症状;1分 :轻度,需稍加注意才感到症状,不影响日常生活 ;2分:中度,可自觉症状,尚不影响日常生活;3分:重度,经常发生,影响日常生活和工作。各项症状积分总和即为该患者的症状评分。
2 结 果
2.1 血清IL-6、HAMD评分、消化不良症状评分 病例组血清IL-6水平、HAMD评分、消化不良症状评分显著高于对照组,差异有统计学意义,见表1。
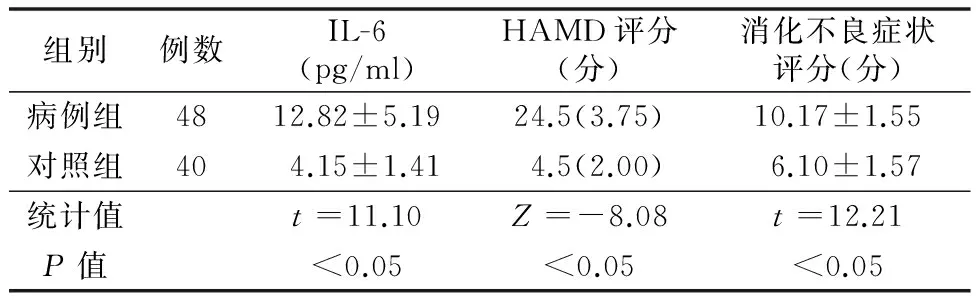
表1 两组血清IL-6、HAMD评分、消化不良症状评分比较
2.2 相关分析 病例组血清IL-6水平与HAMD评分、消化不良症状评分呈正相关;消化不良症状评分与HAMD评分呈正相关。见表2;图1~3。

表2 血清IL-6与消化不良症状评分、HAMD评分相关分析
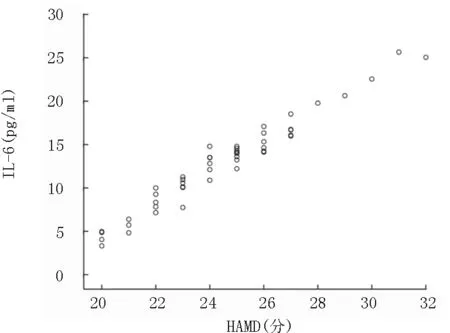
图1 血清IL-6与HAMD评分相关分析
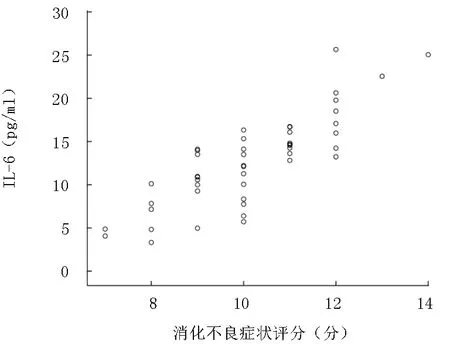
图2 血清IL-6与消化不良症状评分相关分析
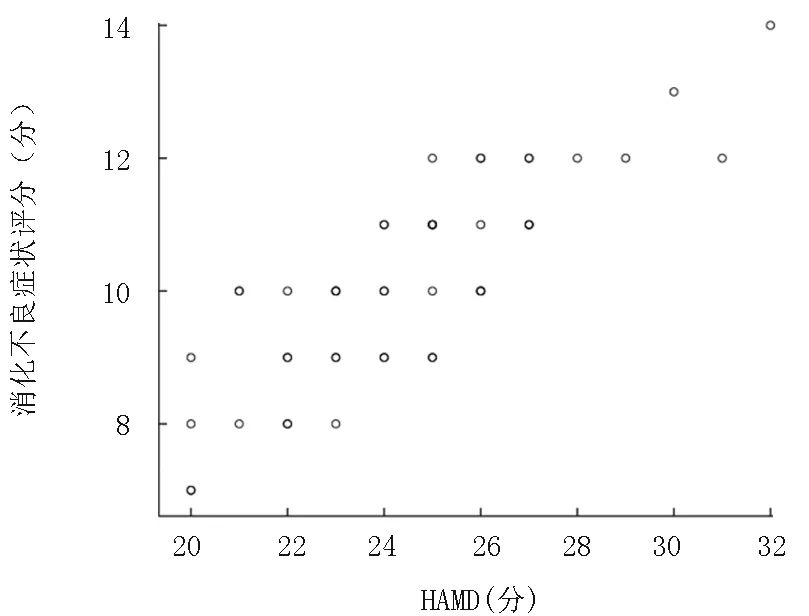
图3 消化不良症状评分与HAMD评分相关分析
3 讨 论
早在1884年Stiller曾提出“心因性消化不良”的概念,指出胃部不适患者中60%~70%可能存在“神经/心因性消化不良”[7]。FD是临床上的多发病、常见病,目前机制尚不清楚,其症状与胃肠动力障碍、内脏高敏感性相关,然而大部分患者应用促胃肠动力药和抑酸药治疗效果欠佳,尤其是对一些病情较重且反复的患者疗效甚微[8]。压力和抑郁与各种消化疾病相关,可能是功能性消化不良、肠易激综合症及胃癌的诱发因素[9]。2016年,罗马委员会在消化疾病周上提出了FD的新诊断标准-罗马Ⅳ,认为FD不应被视为单一的功能障碍,强调了脑和内脏的紧密联系并指出脑肠轴的重要性[10]。由此可见FD不单是一种胃肠动力障碍性疾病,而是一种与精神心理因素密切相关的心身疾病[4]。
研究显示,FD患者中有抑郁情绪的占42%。FD的临床表现可能是抑郁症患者的躯体化表现[11]。本研究显示,HAMD评分为轻中度抑郁的FD患者的消化不良症状评分与HAMD评分呈正相关,表明心理因素参与了FD的发生,心理测评可以一定程度上反映患者消化不良症状的严重程度,此结果与当前文献报道一致。现阶段,抑郁症的发病机制尚不清楚,Maes等[12]及Farré等[13]曾提出“抑郁症的炎症反应假说”,认为抑郁症是一种神经免疫紊乱性疾病。越来越多证据表明,抑郁症与免疫激活和炎症反应存在一定的相关性,细胞因子作为神经调质,在抑郁症的致病过程中具有重要作用[14-15]。有人提出环境因素,尤其是压力,可以使中枢神经系统微环境发生改变,释放的促炎细胞因子导致慢性神经炎症,影响神经递质代谢、神经内分泌功能和神经再生,进而影响抑郁状态[16]。荟萃分析得出结论:外周血IL-1β、IL-6、肿瘤坏死因子α(TNF-α)和C反应蛋白(CRP)是抑郁症患者最可靠的炎性生物标记物[17]。
胃肠道系统的运动和分泌受中枢神经、肠神经以及自主神经系统共同支配,易受到内外环境刺激的影响,是与精神心理相关性最强的系统。胃肠道的功能状态与精神心理状态关系密切[18]。脑肠轴将中枢神经系统与肠神经系统、内分泌系统、免疫系统连接起来,形成双向环路,对胃肠运动及功能进行调节[19]。精神心理应激可破坏边缘系统与下丘脑间的平衡,通过脑肠轴影响胃肠道功能及黏膜屏障完整性,同时患者胃肠道改变可反馈至大脑,对患者精神心理产生反向作用[20]。神经胃肠病学的发展揭示出精神心理因素、脑肠轴紊乱、消化道黏膜低度炎症与细胞因子在FD中起作用。心理应激通过大脑边缘系统和下丘脑使自主神经功能发生改变,激发下丘脑-垂体-肾上腺轴,导致神经内分泌、免疫功能失调[21]。由于下丘脑-垂体-肾上腺轴对内外环境刺激的高反应性,皮质激素合成增加,细胞因子水平升高,使机体处于“警戒”状态,诱发消化道发生低度黏膜炎症反应和免疫应答,造成黏膜屏障功能受损,诱导肠神经系统重塑,导致胃肠运动障碍和内脏高敏感性[22-23]。此外,肥大细胞参与了应激对胃肠运动的影响[20],心理应激可改变胃肠道免疫力, 特别是肥大细胞激活, 释放的5羟色胺、IL-6、组胺、白三烯等炎性介质,导致内脏感觉异常。综上所述,我们推测免疫细胞释放的炎症介质可介导胃肠动力改变和内脏敏感性增高[24]。
细胞因子不但在免疫炎症反应中起重要作用,而且具有广泛的生物学功能,如同神经递质和激素,是神经系统、内分泌系统和免疫系统间相互作用的重要物质,参与机体的内环境稳态及疾病的发生[25]。由炎性细胞释放的炎症因子可作用于肠神经系统、肠道平滑肌和Cajal间质细胞,影响胃肠道动力和内脏敏感性,导致消化不良[26]。研究显示FD患者的胃排空延迟与细胞因子释放有关[27]。IL-6是一种影响肾上腺应激反应和胃蠕动的非特异性炎性细胞因子,荟萃分析证实IL-6已成为抑郁症有效的生物学标志物,可反映抑郁严重程度[17]。IL-6分泌增加激活炎症过程是抑郁症潜在的病理基础。当人群暴露于各种抑郁相关的压力环境时,如童年虐待、低社会经济地位、消极的人际交往或父母离世等,IL-6水平会明显升高。与抑郁症的情感表现相比,IL-6可能与躯体症状的发展更相关。虽然IL-6通常被描述为一个促炎细胞因子,但更准确地应称为一个炎症应答细胞因子,IL-6的增多引起下丘脑-垂体-肾上腺轴及自主神经系统功能紊乱,诱发消化道黏膜的炎症反应和免疫应答,激活胃肠道黏膜下层的神经元,导致胃肠蠕动及分泌紊乱[28];也可使外周的感受器阈值变低,导致内脏高敏感性,进而引起消化道症状。高宏[29]研究显示,FD患者IL-6水平明显高于体检健康者,表明IL-6可能是引起FD的一大诱因,在FD的发病中发挥重要作用。本研究中伴抑郁的FD患者血清IL-6水平显著高于无抑郁的FD患者,IL-6水平与HAMD评分、消化不良症状评分呈正相关,推测IL-6不仅参与FD的发生,也可能与FD病情变化相关。抑郁可使IL-6水平进一步升高,加重消化不良症状,FD患者可能是由于精神心理因素引起的高血清IL-6水平导致消化不良症状。抑郁程度越重的患者,机体血清IL-6水平越高,IL-6作为神经内分泌免疫网络调控的中间介质,使胃肠蠕动、腺体分泌功能减弱,内脏的敏感性增高,出现消化不良症状。
总之,FD的发病机制复杂且多样,精神心理因素在FD的发病中起重要作用。临床医生应注意识别精神心理障碍,在给予常规治疗同时,注重精神心理治疗,包括认知行为治疗、心理疏导及抗焦虑、抑郁药物治疗等。采用心身结合的治疗方法,改善患者消化不良症状和不良情绪[30]。今后可通过增加样本,增加纵向研究,进一步探讨脑肠轴、血清IL-6在FD发病过程中的作用及相关机制。
[1] 杨昌妮,刘纯伦.精神心理因素与功能性消化不良的相关性研究进展[J].重庆医学, 2015, 44(15) :2129-2131.
[2]VanOudenhoveL,AzizQ.Recentinsightsoncentralprocessingandpsychologicalprocessesinfunctionalgastrointestinaldisorders[J].DigLiverDis, 2009, 41(11): 781-787.
[3]FilipovicBF,RandjelovicT,IlleT,etal.Anxiety,personalitytraitsandqualityoflifeinfunctionaldyspepsia-sufferingpatients[J].EurJInternMed, 2013, 24(1): 83-86.
[4] 王晓民,宁翠霞,员晓辉,等.功能性胃肠疾病与抑郁症的关系及治疗[J].中国医药导报, 2012, 9(16):32-34.
[5] 李红毛,叶萌.抑郁症发病机制的免疫学研究进展[J].中国免疫学杂志, 2016, 32(5): 760-763.
[6]DrossmanDA.ThefunctionalgastrointestinaldisordersandtheRomeIIIprocess[J].Gastroenterology, 2006, 130(5): 1377-1390.
[7]VanOudenhoveL,VandenbergheJ,DemyttenaereK,etal.Psychosocialfactors,psychiatricillnessandfunctionalgastrointestinaldisorders:ahistoricalperspective[J].Digestion, 2010, 82(4): 201-210.
[8] 王霞,陈玉龙.氟哌噻吨美利曲辛对伴抑郁的功能性消化不良患者疗效的多中心随机对照临床研究[J].中华消化杂志, 2013, 33(7): 446-450.
[9]LeeSP,SungIK,KimJH,etal.Theeffectofemotionalstressanddepressionontheprevalenceofdigestivediseases[J].JNeurogastroenterolMotil,2015, 21(2): 273-282.
[10]StanghelliniV,ChanFK,HaslerWL,etal.Gastroduodenaldisorders[J].Gastroenterology, 2016, 150(6): 1380-1392.
[11] 石鸿蓝.精神心理因素与功能性消化不良的相关性分析[J]. 世界临床医学, 2016, 10(7):71.
[12]MaesM.Evidenceforanimmuneresponseinmajordepression:areviewandhypothesis[J].ProgNeuropsychopharmacolBiolpsychiatry, 1995, 19 (1): 11-38.
[13]FarréR,VanheelH,VanuytselT,etal.Infunctionaldyspepsia,hypersensitivitytopostprandialdistentioncorrelateswithmeal-relatedsymptomseverity[J].Gastroenterology, 2013, 145(3): 566-573.
[14] 徐永君,盛慧,倪鑫.抑郁症发病机制研究进展[J].安徽医科大学学报,2012,47(3):323-326.
[15]MillerAH,RaisonCL.Theroleofinflammationindepression:fromevolutionaryimperativetomoderntreatmenttarget[J].NatRevImmunol. 2015, 16(1):22-34.
[16] 冯骁,高志涛,王辉.细胞因子诱导抑郁症的发病机制[J].医学综述, 2011, 17(21): 3234-3236.
[17]HowrenMB,LamkinDM,SulsJ.AssociationsofdepressionwithCreactiveprotein,IL-1,andIL-6 :ameta-analysis[J].PsychosomMed, 2009, 71(2):171-186.
[18]KoloskiNA,JonesM,KalantarJ,etal.Thebrain-gutpathwayinfunctionalgastrointestinaldisordersisbidirectional:a12-yearprospectivepopulation-basedstudy[J].Gut, 2012, 61(9): 1284-1290.
[19]HuangW,JiangSM,JiaL,etal.Effectofamitriptylineongastrointestinalfunctionandbrain-gutpeptides:adouble-blindtrial[J].WorldJGastroenterol,2013, 19(26): 4214-4220.
[20] 段丽萍.心理应激在功能性胃肠病发病中的潜在机制[J].中华消化杂志,2011, 31(6):361-363.
[21]OkumuraT,TannoS,OhhiraM.PrevalenceoffunctionaldyspepsiainanoutpatientclinicwithprimarycarephysiciansinJapan[J].JGastroenterol, 2010, 45(2): 187-194.
[22] 韩麦,段丽萍.功能性胃肠病与精神障碍共病的研究进展[J].中华医学杂志, 2010, 90(22) : 1580-1582.
[23]JonesMP,DilleyJB,DrossmanD,etal.Brain-gutconnectionsinfunctionalGIdisorders:anatomicandphysiologicrelationships[J].NeurogastroenterolMotil, 2006, 18(2): 99-103.
[24]BercikP,VerduEF,CollinsSM.Isirritablebowelsyndromealow-gradeinflammatoryboweldisease? [J].GastroenterolClinNorthAm, 2005, 34(2): 235-245.
[25] 张艳美.抑郁症与细胞因子[J].国外医学(精神病学分册), 2000, 27(2):122-124.
[26] 侯陈凤,陈建永,潘锋.功能性胃肠病与胃肠道黏膜炎症和免疫[J].浙江中西医结合杂志, 2014, 24(4): 379-381.
[27]TalleyNJ.Functionaldyspepsia:newinsightsintopathogenesisandtherapy[J].KoreanJInternMed, 2016, 31(3):444-456.
[28] 曾俊,唐亮.功能性消化不良患者血清白介素-6浓度与焦虑抑郁评分的相关性研究[J]. 临床和实验医学杂志, 2015, 14(3):207-209.
[29] 高宏.功能性消化不良患者血浆中NPSR1、CGRP及IL-6的表达水平及临床意义[J]. 中国医学前沿杂志(电子版),2016, 8(8):57-59.
[30]WilliamsM,BudavariA,OldenKW,etal.Psychosocialassessmentoffunctionalgastrointestinaldisordersinclinicalpractice[J].JClinGastroenterol, 2005, 39(10): 847-857.
Relationshipbetweenfunctionaldyspepsiawithdepressionandseruminterleukin6level
LiuHongna1,2,SuShaohui1,2,HuYiting2,WangYuzhen2
1.GraduateSchoolofHebeiMedicalUniversity,Shijiazhuang050000,China; 2.DepartmentofGastroenterology,HebeiGeneralHospital,Shijiazhuang050051,China
SuShaohui,Email:13613116257@163.com
ObjectiveToexplorethepossiblemechanismandclinicalsignificanceofseruminterleukin6 (IL-6)levelandthedigestivesymptomsinpatientscausedbythementalfactors.MethodsTotally48functionaldyspepsia(FD)patientswithHamiltonDepressionScale(HAMD)formild-to-moderatedepression(HAMD8points≤scores≤35points)wereselectedasthecasegroup.Meanwhile, 40FDpatientswithnodepressionsymptom(HAMDscores<8points)inthesameperiodwereselectedasthecontrolgroup.TheserumIL-6intwogroupsweremeasuredandtheindigestionsymptomwasscoredinthecasegroup.ResultsTheserumlevelofIL-6incasegroupwassignificantlyhigherthanthatofcontrolgroup(P<0.05).TheHAMDscoresandtheindigestionsymptomscoresincasegroupweresignificantlyhigherthanthoseofcontrolgroup(P<0.05).TheserumlevelofIL-6andHAMDscoreswerepositivelycorrelated(P<0.01).TheserumlevelofIL-6andtheindigestionsymptomscoreswerepositivelycorrelated(P<0.01).TheindigestionsymptomscoresandHAMDscoreswerepositivelycorrelatedincasegroup(P<0.01).ConclusionThementalfactorsplayimportantroleinthepathogenesisofFD.Themoredepressedpatientsare,thehighertheirserumIL-6are,andthemoreseveretheirdyspepticsymptomsare.
dyspepsia;depression;interleukin6
苏少慧,Email: 13613116257@163.com
R
A
1004-583X(2017)08-0699-04
10.3969/j.issn.1004-583X.2017.08.013
2017-04-24 编辑:王秋红
