HPLC同时测定祛痰止咳胶囊中3种活性成分含量
2017-08-22毛坤军黄平周慧云叶锡勇
毛坤军,黄平,周慧云,叶锡勇
(江西医学高等专科学校药学系,江西 上饶 334000)
HPLC同时测定祛痰止咳胶囊中3种活性成分含量
毛坤军,黄平,周慧云,叶锡勇
(江西医学高等专科学校药学系,江西 上饶 334000)
目的:建立祛痰止咳胶囊中阿魏酸、槲皮素、芹菜素3种活性成分的高效液相色谱法(HPLC)含量测定方法。方法:采用phenomonex®-C18色谱柱(4.6 mm×250 mm,5 μm),以甲醇(A)-0.1%的磷酸水溶液(B)为流动相,流速1.0 mL/min,柱温30℃,检测波长为360 nm。结果:阿魏酸、槲皮素、芹菜素在质量浓度分别为0.76~15.2,3.92~76.4,0.59~11.8 μg/mL范围内与峰面积呈良好的线性关系,加样回收率分别为98.48%,101.43%和99.08%。结论:本试验所建立的方法准确、可靠、重复性好,可为祛痰止咳胶囊的质量控制提供科学的依据。
高效液相色谱法;祛痰止咳胶囊;含量测定;质量控制
祛痰止咳胶囊是由《伤寒论》和《金匮要略》中的参夏汤与十枣汤化裁而来,属国家中药保护品种[1]。主要由党参、水半夏、芫花(醋制)、甘遂(醋制)、紫花杜鹃五味中药组成,具有健脾燥湿、祛痰止咳的功效;临床上主要用于慢性支气管炎及支气管炎合并肺气肿、肺源性心脏病所引起的痰多咳嗽、喘息等症[2]。据报道,芫花和紫花杜鹃作为处方中的君药和臣药,具有抗炎和镇咳祛痰作用,其主要化学成分均为黄酮类成分[3-4],且药效学研究表明黄酮类化合物为其镇咳祛痰的有效成分[5]。目前,祛痰止咳胶囊执行标准为《国家食品药品监督管理局国家药品标准》YBZ02962006-2009Z,其含量测定项下以党参中的阿魏酸为指标成分进行含量测定[6]。鉴于中药复方成分的多样性和复杂性,单一成分难以全面评价和控制药物的内在质量,且作为发挥药效的主要成分,黄酮类化合物还未见相关含量测定的研究报道。故本研究以党参中的阿魏酸、芫花中芹菜素和紫花杜鹃中的槲皮素为指标成分,建立祛痰止咳胶囊中该3种活性成分的HPLC含量测定方法,为进一步提高和完善祛痰止咳胶囊的质量标准提供科学的依据。
1 材料
1.1 仪器
Waters2695高效液相色谱仪:包括waters e2489检测器,Empower工作站(美国Waters公司);CPA225D型电子天平(德国赛多利斯);KQ-500DE型超声波清洗机(昆山市超声仪器有限公司);纯水仪(易普易达科技有限公司)。
1.2 试药
对照品:阿魏酸(批号:110773-201012)、芹菜素(批号:100756-201210)、槲皮素(批号:100081-201408)均购自中国药品生物制品检定所,纯度均≥98%;不同批次祛痰止咳胶囊(购自药店);色谱甲醇购自Merck公司;磷酸、分析甲醇为北京化工产品;水为去离子水。
2 方法与结果
2.1 色谱条件
phenomonex®-C18色 谱 柱(4.6 mm×250 mm,5 μm);流动相为甲醇(A)-0.1%的磷酸水溶液(B),梯度洗脱(0~20 min,30%~50%A;20~40 min,50%~60%A);体积流量1.0 mL/min,柱温30℃,检测波长360 nm,进样量均为10 μL。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取阿魏酸、槲皮素、芹菜素对照品适量,加甲醇制成质量浓度分别为15.2,76.4,11.8 μg/mL的混合对照品溶液,摇匀,即得。
2.2.2 供试品溶液的制备 取祛痰止咳胶囊10粒,混匀,研细,取约1.0 g,置锥形瓶中,加入80%甲醇25 mL,称重,超声处理30 min,称重,用80%甲醇补足减失的质量,摇匀,0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液的制备 根据处方制备缺党参、紫花杜鹃和芫花的阴性对照溶液。
2.3 方法学考察
2.3.1 专属性试验 分别精密吸取对照品、供试品、阴性对照溶液各10 μL,注入HPLC色谱仪,按“2.1”项下色谱条件分析,见图1。结果表明3种被测成分能达到完全分离。
2.3.2 线性关系考察 分别精密吸取“2.2.1”项下混合对照品溶液0.5,1.0,2.0,2.5,5.0,10.0 mL至10 mL容量瓶中,加甲醇定容至刻度。分别精密吸取10 μL注入HPLC分析,以峰面积Y对进样浓度X进行回归方程计算,结果见表1。
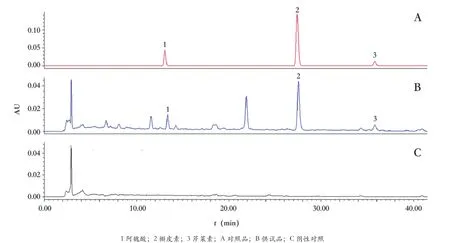
图1 专属性试验HPLC色谱图
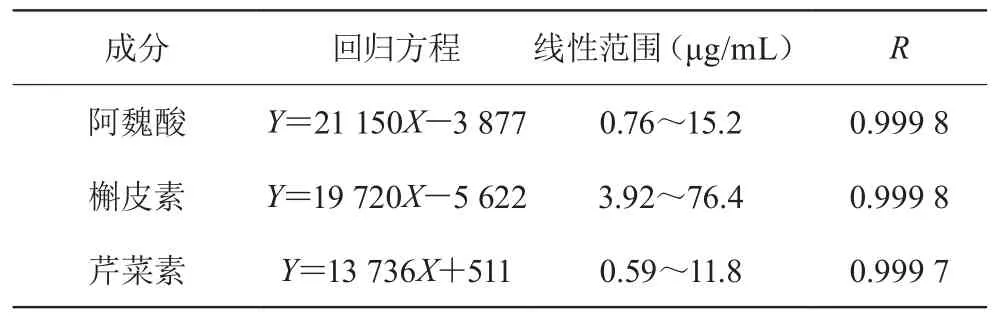
表1 3种被测成分的回归方程、线性范围和相关系数
2.3.3 精密度试验 精密吸取“2.2.1”项下混合对照品,按“2.1”项下色谱条件连续进样6次,记录峰面积并计算RSD。结果显示阿魏酸、槲皮素、芹菜素的RSD分别为1.22%,0.87%,1.88%。表明仪器精密度良好。
2.3.4 稳定性试验 取同一批号(151203)供试品溶液,按“2.1”项下色谱条件分别在0,2,4,6,8,12,24 h进样分析,记录峰面积并计算RSD。结果显示阿魏酸、槲皮素、芹菜素的RSD分别为2.04%,1.79%, 2.41%。表明供试品溶液24 h内稳定性良好。
2.3.5 重复性试验 取同一批号(151203)样品,按“2.2.2”项下方法平行制备6份供试品溶液,按“2.1”项下色谱条件分析,记录峰面积并计算RSD。结果显示阿魏酸、槲皮素、芹菜素的RSD分别为1.34%,0.89%,2.33%。表明方法重复性良好。
2.3.6 加样回收试验 取已知含量(151203)的样品6份,每份约0.5 g,按1∶1的比例加入对照品,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件分析,计算回收率,结果见表2。
2.3.7 样品含量测定 取不同批次样品约1.0 g,每个批次平均3份,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件分析,以外标法计算含量,结果见表3。
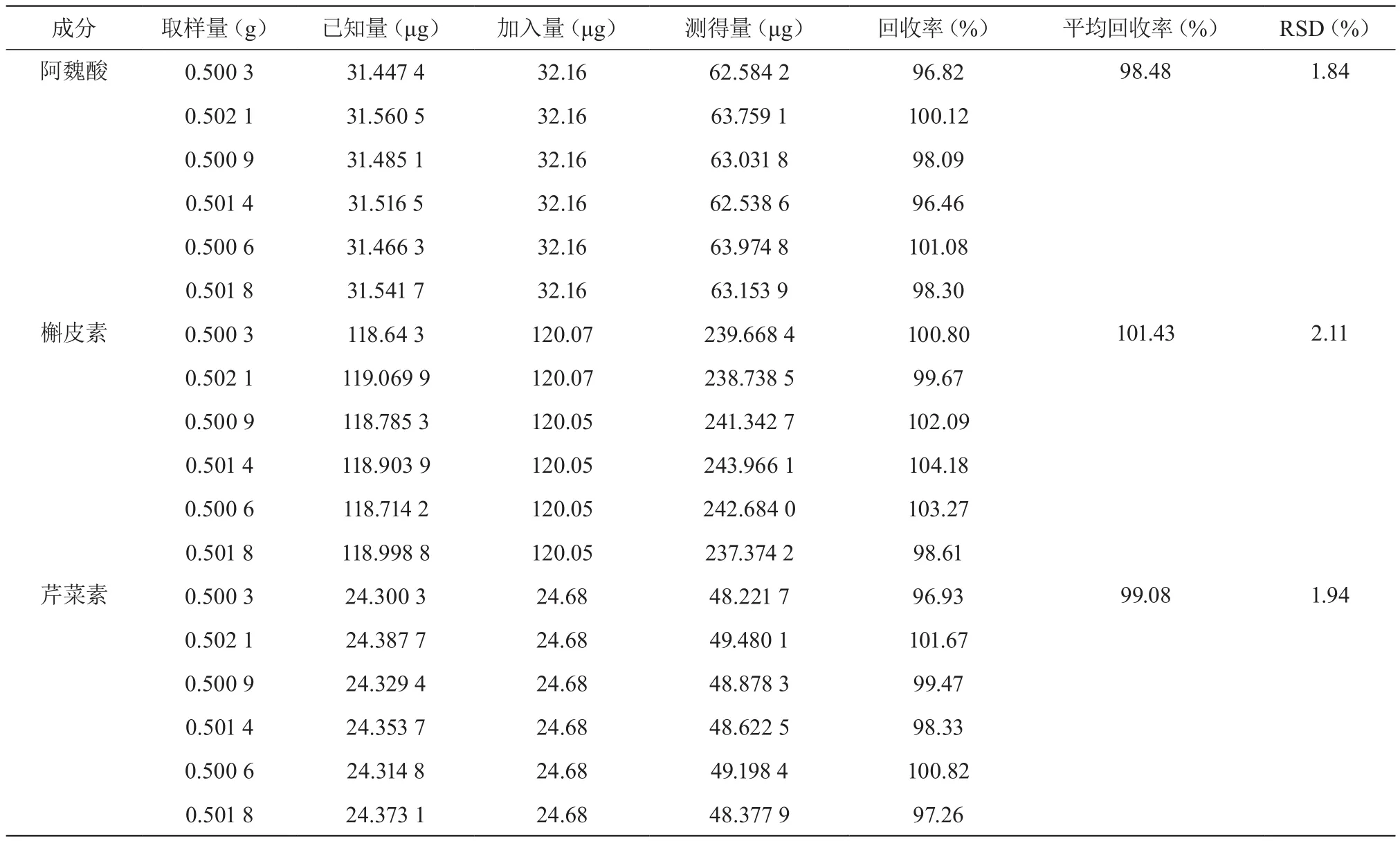
表2 加样回收率试验(n=6)

表3 样品含量测定结果
3 结语
3.1 提取条件的选择
采用单因素变量法对提取方法(超声、回流);提取溶剂(甲醇、乙醇);溶剂浓度(60%,80%,100%);提取时间(30,45,60 min);料液比(1∶10,1∶25,1∶50)进行考察,结果显示以25倍量80%甲醇超声提取30 min所得含量最佳。
3.2 流动相的选择
由于被测成分均显一定的酸性,故选择酸性系统洗脱,本试验考察了甲醇-0.1%磷酸水溶液和乙腈-0.1%磷酸水溶液;结果显示,甲醇分离效果优于乙腈,可能是乙腈洗脱效果较强,无法使每个被测成分与相邻色谱峰完全分离,且出于毒性、价格考虑,在环保和成本方面甲醇也更优于乙腈。故试验最终选择甲醇-0.1%磷酸水溶液进行测定。
3.3 检测波长的选择
据文献报道,阿魏酸最大紫外吸收波长为320 nm[7],槲皮素、芹菜素为360 nm[8]。本实验比较了两种波长下的吸收峰,结果发现在320 nm波长下有较多杂质峰,且槲皮素和芹菜素吸收相对较弱,故最终选择360 nm作为检测波长。
[1] 郭景仙,贺利军,林晓兰.祛痰止咳颗粒临床使用情况分析[J].医药导报,2007,26(6):678-681.
[2] 陈羽鹏,苏连彩,丘建芳,等.RH-HPLC法测定祛痰止咳颗粒中槲皮素的含量[J].中医药导报,2006,12(3):56-57.
[3] 李玲芝,宋少江,高品一.芫花的化学成分及药理作用研究进展[J].沈阳药科大学学报,2007,24(9):587-592.
[4] 栗建明,侯惠婵,隆颖.紫花杜鹃药材质量标准研究[J].今日药学,2011,21(4):229-231.
[5] 郑文燕,王晓东,彭维,等.祛痰止咳颗粒指纹图谱研究[J].中山大学学报:自然科学版,2011,50(3):98-101.
[6] 国家药典委员会.国家食品药品监督管理局国家药品标准[S].YBZ02962006-2009Z.
[7] 云学英,吴宁远,刘晓颖.蒙药耧斗菜中阿魏酸含量的高效液相色谱法测定[J].时珍国医国药,2015,26(3):589-590.
[8] 董爱文,朱春艳,卓琦.五爪龙外敷液中芹菜素与槲皮素的HPLC测定[J].天然产物研究与开发,2014,26(2):230-232,272.
本文编辑:鲁守琴
Simultaneous Determination of Contents of Three Active Components in Qutanzhike Capsules by HPLC
Mao Kun-jun, Huang Ping, Zhou Hui-yun, Ye Xi-yong
(Department of Pharmacy, Jiangxi Medical College, Jiangxi Shangrao 334000, China)
Objective:To develop a HPLC method for determination of three active constituents, i.e. ferulic acid, quercetin and apigenin in qutanzhike capsules. Methods:Phenomonex®-C18chromatographic column (4.6 mm×250 mm, 5 μm) was adopted serving methanol (A)-0.1%phosphoric acid (B) solution as mobile phase at a fow rate of 1.0 mL/min and a column temperature of 30℃. The detection wavelength was 360 nm. Results:The linear ranges of ferulic acid, quercetin and apigenin were 0.76~15.2, 3.92~76.4 and 0.59~1.8 μg/mL, while the average recovery rates were 98.48%, 101.43% and 99.08%, respectively. Conclusion:The developed method was accurate, reliable and reproducible, which provided a scientifc basis for the quality control of qutanzhike capsules.
HPLC; Qutanzhike Capsules; Content Determination; Quality Control
R284.1
A
10.3969/j.issn.2096-3327.2017.06.017
2017 - 03 - 05
毛坤军,男,硕士,助教。研究方向:药物质量标准研究。E-mail:737259639@qq.com
叶锡勇,男,学士,教授。研究方向:药物质量标准研究。E-mail:1962628419@qq.com
