益生菌治疗重症急性胰腺炎的随机对照试验Meta分析
2017-08-16王茂林冯碧敏王国俊
王茂林,陈 竹,冯碧敏,王国俊△
(1.西南医科大学附属医院药学部,四川泸州 646000; 2.西南医科大学药学院临床药学系,四川泸州 646000)
2016年度重庆市出版专项资金资助项目
·循证医学· doi:10.3969/j.issn.1671-8348.2017.19.024
益生菌治疗重症急性胰腺炎的随机对照试验Meta分析
王茂林1,2,陈 竹2,冯碧敏2,王国俊1,2△
(1.西南医科大学附属医院药学部,四川泸州 646000; 2.西南医科大学药学院临床药学系,四川泸州 646000)
目的 系统评价益生菌在重症急性胰腺炎(SAP)治疗中的安全性和有效性。方法 检索PubMed、Embase、Cochrane Library、Medline、中国生物医学文献服务数据库(CBM)、中文科技期刊数据库(VIP)、中国期刊全文数据库(CNKI)、万方学术期刊全文数据库,全面查找益生菌治疗SAP的临床随机对照试验(RCTs),采用Review Manager5.3软件进行统计分析。结果 共纳入12篇RCT研究,共910例患者,Meta分析结果显示:益生菌组与对照组在病死率[RR=0.97,95%CI(0.63,1.49),P=0.88]、多器官功能障碍发生率[RR=0.72,95%CI(0.49,1.06),P=0.10]及胰腺相关感染率[RR=0.76,95%CI(0.54,1.07),P=0.12]等方面比较,差异均无统计学意义;但两组住院时间[MD=-3.74,95%CI(-6.37,-1.12),P=0.005]及肠缺血坏死发生率[RR=11.39,95%CI(1.5,86.4),P=0.02]比较,差异均有统计学意义。结论 益生菌不能有效改善SAP患者的相关临床指标,同时会增加患者肠缺血坏死的发生风险,但可以缩短患者的住院时间。
益生菌;重症急性胰腺炎;Meta分析
急性胰腺炎(acute pancreatitis,AP)是指由多种病因引起胰酶激活,继以胰腺局部炎性反应为主要特征的一种临床常见的急腹症[1]。20%~25%的患者临床上病情重,出现局部或全身并发症、多器官功能衰竭,甚至危及生命,称为重症AP(severe acute pancreatitis,SAP)[2],其继发的胰腺坏死组织感染患者的病死率高达40%[3],肠道内菌群失调,肠黏膜屏障功能障碍和肠源性细菌易位被认为是导致胰腺坏死组织及胰周积液感染的主要原因[4]。故SAP患者肠道正常细菌微生态的维护,肠黏膜屏障功能的监测及肠源性细菌易位的预防成为近年研究的热点,益生菌的使用也成为研究热点之一,同时也存在极大的争议。2014年由Gou等[5]就益生菌在SAP治疗中的意义做了Meta分析,但其数据不全,漏收了Wang等[6]、李进等[7]的研究,存在局限性,之后又出现一些新的研究,因此有必要对益生菌治疗SAP的安全性和有效性重新进行评价,以期得到更可靠的循证依据,更好地为临床用药提供支持。
1 资料与方法
1.1 检索策略 根据中文关键词“益生菌、益生元”和“重症急性胰腺炎”检索中国生物医学文献服务数据库(CBM)、中国科技期刊数据库(VIP)、中国期刊全文数据库(CNKI)、万方学术期刊全文数据库;用英文关键词“severe acute pancreatitis、probiotics、prebiotics、 synbiotics”检索PubMed、Embase、Cochrane Library、Medline等数据库。检索时间均从建库到2016年5月。手工检索相关系统综述、病例分析等文献以作补充,文种不限。
1.2 纳入与排除标准 纳入标准:(1)文献类型,检索所有关于益生菌治疗SAP的随机对照试验(RCT);(2)研究对象,不限国籍、性别、年龄等,符合各国AP诊治指南明确诊断为SAP的患者,益生菌组和对照组的基线情况基本一致,具有可比性;(3)干预措施,益生菌组在常规治疗(包括禁食、胃肠减压、抑酸、抑制胰液分泌、维持水电解质平衡等治疗)和应用肠内营养(EN)液的基础上,加用益生菌治疗,对照组单纯采用常规治疗和应用EN液(未加用益生菌和其他药物);(4)结局指标,主要有病死率、多器官功能障碍、胰腺相关感染、肠缺血坏死、总感染率、并发症发生率、外科手术实施情况及平均住院时间等。排除标准:语种不是中英文且联系作者没有回复者或仅能查阅摘要;动物实验;综述; SCI或中文核心期刊目录未收录。
1.3 资料提取 两名评价员根据预先制定的纳入和排除标准独立地进行文献筛选和资料提取,如果出现争议则通过第3名评价员的讨论予以解决,无法获取的资料通过联系通信作者予以补充。提取资料内容:纳入研究的发表时间、样本量、干预措施、疗程、随机分配方法、盲法、分配方案隐藏、选择性报告及相关结局指标等。
1.4 质量评价 采用改良Jadad评分,同时根据Cochrane协作网偏倚风险评价工具和标准对纳入研究进行评价,所含指标:随机方法(randomization)、随机序列的产生(random sequence generation)、盲法(blinding)、分配隐藏(allocation concealment)、数据缺失(incomplete outcome date)、选择性报道结果(selective reporting)和其他偏倚。
1.5 统计学处理 效应量选择:根据Cochrane协作组提供的RevMan5.3软件,计数资料采用相对危险度(RR)及95%置信区间(95%CI);计量资料采用加权均数差(MD)及95%CI。异质性检验:采用χ2检验评价同类研究间的异质性,当I2≤50%,P≥0.10说明纳入文献间有同质性时,采用固定效应模型;若I2>50%,P<0.10研究间有异质性,采用亚组分析后仍有异质性,则使用随机效应模型合并统计量。
2 结 果
2.1 检索结果及文献质量评价结果 通过检索共得到460篇文献,查重后剩下171篇,阅读摘要除去与研究目的无关的78篇,只有摘要发表的6篇,综述、回顾性分析、个案报道等40篇,动物实验21篇,详细数据无法获得文献1篇,没有明确结局指标的文献1篇,进一步通读全篇,除去不是SCI、中文核心期刊及干预措施不符合条件的13篇, 最终入选12篇(图1)。所有研究均为RCT,其中1项研究[10]为多中心的RCT,4项研究[6,10,12-13]提及具体随机分组方法,6项研究[6,9,10,12-13,15]为双盲,5项研究[8-10,12-13]提及采用分配隐藏,纳入研究的质量评价见表1。该表得出了改良Jadad评分,同时得出Cochrane5.3评价风险偏移图表,见图2。
2.2 益生菌的使用情况 12项研究中有1项研究[13]的益生菌使用种类不清楚,2项研究[8,15]单独使用了一种菌株,其他研究使用了2种及以上的菌株组成的复合益生菌。见表2。

图1 文献检索、筛选流程和检索结果

图2 Cochrane 5.3风险偏移评估图
2.3 其他基线特征 纳入研究样本量为25~296例不等,共纳入SAP患者910例,其中益生菌组471例(益生菌联合EN液);对照组439例(EN液)。8项研究[6-7,10,12-14,16-17]诊断符合急性生理学与慢性健康状况(APACHE-Ⅱ)评分大于或等于8分;6项研究[6,8-10,12-13]诊断符合C反应蛋白(CRP)≥150 mg/L;4项研究[,8-10,14]诊断符合Glasgow评分大于或等于3分;2项研究[7,17]的诊断符合Ranson评分大于或等于3分;1项研究[15]的诊断符合改良Marshall评分大于或等于2分。综合12篇研究的原发病因主要有酒精性SAP、胆源性SAP、高脂血症性SAP及由暴饮暴食引起的SAP,以酒精性和胆源性SAP为主。
2.4 Meta分析结果
2.4.1 病死率 10项研究[6-14,17]报道了病死率(n=846),在Besselink等[10]的研究中益生菌组的病死率明显高于对照组,其他研究中益生菌组的病死率都未高于对照组。Meta分析结果显示:益生菌组与对照组的病死率比较,差异无统计学意义[RR=0.97,95%CI(0.63,1.49),P=0.88)],纳入研究间不存在异质性(I2=32%,P=0.15),因此采用固定效应模型分析,见图3A。

表1 纳入研究的质量评价表

续表1 纳入研究的质量评价表
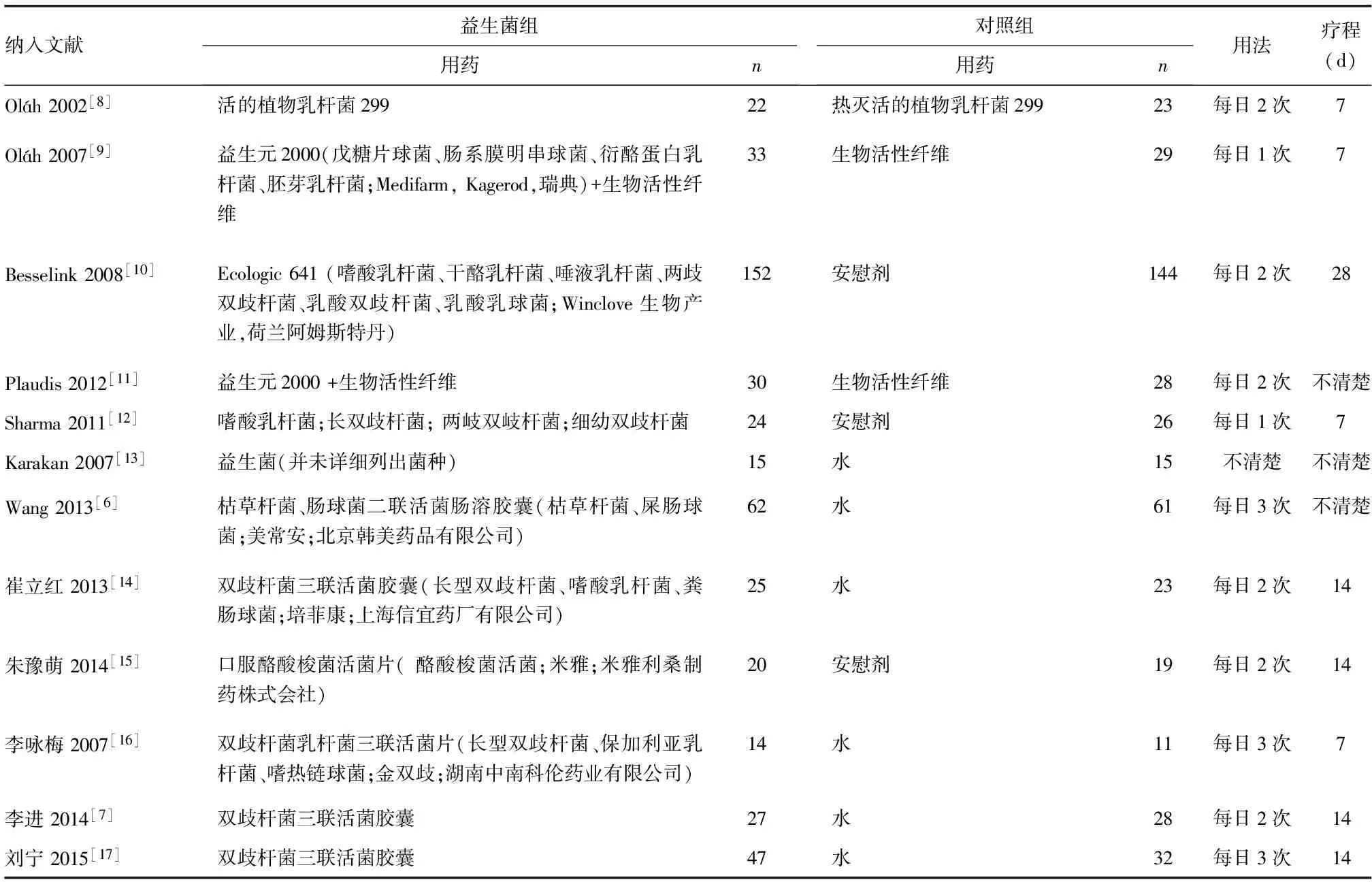
表2 各研究益生菌的使用情况
2.4.2 多器官功能障碍 7项研究[6,8-11,13,17]报道了多器官功能障碍的发生情况(n=693),其中在Besselink等[10]的研究中益生菌组18例,多器官功能障碍发生率为11.8%;对照组11例,发生率为7.6%,益生菌组的发生率明显高于对照组,其他研究中益生菌组多器官功能障碍的发生率都小于对照组。Meta分析结果显示:益生菌组与对照组多器官功能障碍发生率比较,差异无统计学意义[RR=0.72,95%CI(0.49,1.06),P=0.10],纳入研究间不存在异质性(I2=26%,P=0.23),采用固定效应模型分析,见图3B。
2.4.3 胰腺相关感染 8项研究[6-11,14-15]报道了胰腺相关感染的发生情况(n=726),其中在Besselink等[10]和朱豫萌等[15]的研究中益生菌组胰腺相关感染发生率高于对照组,其他研究中益生菌组的发生率均未超过对照组。Meta分析结果显示:益生菌组与对照组胰腺相关感染发生率比较,差异无统计学意义[RR=0.76,95%CI(0.54,1.07),P=0.12],纳入研究间不存在异质性(I2=23%,P=0.24),因此采用固定效应模型分析,见图3C。
2.4.4 总感染 5项研究[9-11,13,17]报道了总感染的发生情况(n=525),在Besselink等[10]的研究中益生菌组的总感染率高于对照组,其他研究中益生菌组总感染率均未超过对照组。Meta分析结果显示:益生菌组与对照组总感染率比较,差异无统计学意义[RR=0.82,95%CI(0.63,1.06),P=0.13],纳入研究间不存在异质性(I2=34%,P=0.19),因此采用固定效应模型分析,见图3D。
2.4.5 住院时间 7项研究[7,10,12-14,16-17]报道了住院时间(n=583),其中在李咏梅[16]的研究中,平均住院时间太长,而在Sharma等[12]的研究中,平均住院时间太短。Meta分析结果显示:益生菌组与对照组住院时间比较,差异有统计学意义[MD=-3.74,95%CI(-6.37,-1.12),P=0.005],纳入研究间存在异质性(I2=79%,P<0.01),探讨其原因可能是由各研究所纳入研究对象的基础生理状况,所采用的益生菌种类、用法用量,疗程等的不同而产生,因此采用随机效应模型分析,见图3E。
2.4.6 其他结局指标 在肠缺血坏死方面,2项研究[10,15]报道了肠缺血坏死的发生情况,益生菌组与对照组差异有统计学意义[RR=11.39,95%CI(1.5,86.4),P=0.02],纳入研究间不存在异质性(I2=23%,P=0.51);而在外科手术实施率、泌尿道感染和全身炎症反应综合征(SIRS)发生率比较,差异无统计学意义(P>0.05),见表3。
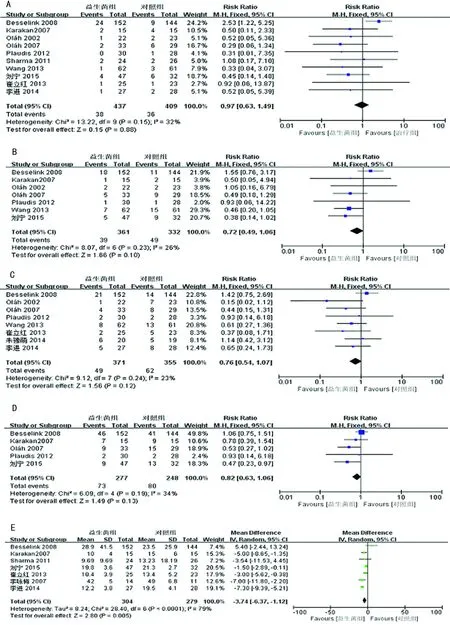
A:病率率;B:多器官功能障碍;C:胰腺相关感染;D:总感染;E:住院时间
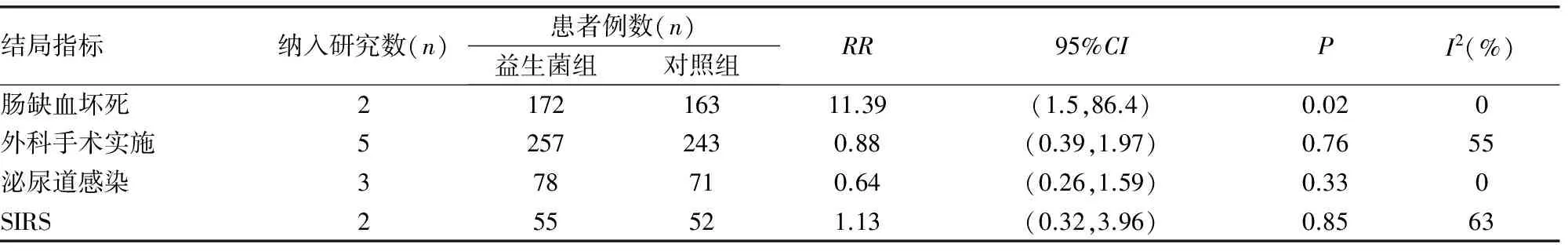
图3 益生菌组和对照组在病死率、多器官功能障碍、胰腺相关感染、总感染、住院时间的比较
3 讨 论
本研究系统评价了益生菌用于治疗SAP的安全性和有效性,结果表明:在SAP的治疗中益生菌对患者相关临床指标无明显影响,但可以缩短住院时间[MD=-3.74,95%CI(-6.37,-1.12),P=0.005],在纳入的7项研究[7,10,12-14,16-17]中,Besselink等[10]的研究表明益生菌组的平均住院时间明显长于对照组,该研究的质量较高,风险偏移较低,权重较大,其他研究益生菌组的住院时间都短于对照组,同时各研究之间异质性较大(I2=79%,P<0.01),其原因可能与各研究所纳入患者的基础生理状况,所用的益生菌种类、用法用量及疗程等的不同有关。而益生菌在治疗SAP的过程中增加了肠缺血坏死的发生率,有2项研究报道了肠缺血坏死的发生情况,纳入研究间无异质性(I2=23%,P=0.51)且益生菌组肠缺血坏死的发生率明显高于对照组[RR=11.39,95%CI(1.5,86.4),P=0.02][10,15],故临床上应该密切关注。
Meta分析为二次研究,其论证强度受到诸多因素的影响,因此存在一定的局限性:(1)纳入研究的基线特征中,多数患者原发病因不一致,所使用的益生菌种类、数量、用法用量、疗程等不尽相同。Sand等[18]研究表明,益生菌的疗效可能还与其菌群和剂量相关,肠道中有上百种菌群,不过只有一部分能表现出益生菌的疗效,这就造成一定的基线异质性。(2)纳入文献除了Besselink等[10]和Wang等[6]的研究样本量相对较大外,其余都属于小样本研究,7篇属于高质量文章,5篇质量相对较低,只有4篇明确提出了随机序列的产生方法,6篇采用了双盲且方法正确,因此存在实施偏倚和测量偏倚的可能;5篇采用了分配隐藏,所以存在选择性偏移的可能;有部分文献在结果指标和数据丢失上未进行报道,这对偏倚风险也会产生一定的影响。(3)部分结局指标的对照分析,所纳入的研究较少,有的仅有两项研究进行了报道,使得对Meta分析得出的结论需要持谨慎态度。(4)纳入的国内研究所占比例较大,患者的种族、身体质量、病情严重程度、生理情况等可能存在差异,临床应用时需根据患者的具体情况具体分析。由于纳入的研究有限,今后还需更多高质量的RCT研究对结论进行验证。
[1]王春友,李非,赵玉沛.急性胰腺炎诊治指南(2014)[J].浙江医学,2015,35(1):7-10.
[2]Munsell MA,Buscaglia JM.Acute pancreatitis[J].J Hosp Med,2010,5(4):241-250.
[3]Warshaw AL.Improving the treatment of necrotizing pancreatitis--a step up[J].N Engl J Med,2010,362(16):1535-1537.
[4]芦波,钱家鸣.重症急性胰腺炎病因及发病机制研究进展[J].中国实用外科杂志,2012,32(7):590-592.
[5]Gou S,Yang Z,Liu T,et al.Use of probiotics in the treatment of severe acute pancreatitis:a systematic review and meta-analysis of randomized controlled trials[J].Crit Care,2014,18(2):R57.
[6]Wang G,Wen J,Xu L,et al.Effect of enteral nutrition and ecoimmunonutrition on bacterial translocation and cytokine production in patients with severe acute pancreatitis[J].J Surg Res,2013,183(2):592-597.
[7]李进,王娟,徐艳琴.早期肠内营养加培菲康对重症急性胰腺炎患者血浆中炎症介质水平变化的效果[J].世界华人消化杂志,2014,22(36):5609-5614.
[8]Oláh A,Belágyi T,Issekutz A,et al.Randomized clinical trial of specific lactobacillus and fibre supplement to early enteral nutrition in patients with acute pancreatitis[J].Br J Surg,2002,89(9):1103-1107.
[9]Oláh A,Belágyi T,Pótó L,et al.Synbiotic control of inflammation and infection in severe acute pancreatitis:a prospective,randomized,double blind study[J].Hepatogastroenterology,2007,54(74):590-594.
[10]Besselink MG,van Santvoort HC,Buskens E,et al.Probiotic prophylaxis in predicted severe acute pancreatitis:a randomised,double-blind,placebo-controlled trial[J].Lancet,2008,371(9613):651-659.
[11]Plaudis H,Pupelis G,Zeiza K,et al.Early low volume oral synbiotic/prebiotic supplemented enteral stimulation of the gut in patients with severe acute pancreatitis:a prospective feasibility study[J].Acta Chir Belg,2012,112(2):131-138.
[12]Sharma B,Srivastava S,Singh N,et al.Role of probiotics on gut permeability and endotoxemia in patients with acute pancreatitis:a double-blind randomized controlled trial[J].J Clin Gastroenterol,2011,45(5):442-448.
[13]Karakan T,Ergun M,Dogan I,et al.Comparison of early enteral nutrition in severe acute pancreatitis with prebiotic fiber supplementation versus standard enteral solution:a prospective randomized double-blind study[J].World J Gastroenterol,2007,13(19):2733-2737.
[14]崔立红,王晓辉,彭丽华,等.早期肠内营养加微生态制剂对重症急性胰腺炎患者疗效的影响[J].中华危重病急救医学,2013,25(4):224-228.
[15]朱豫萌,林姝,党晓卫,等.益生菌在重度急性胰腺炎治疗中的作用[J].世界华人消化杂志,2014,22(32):5013-5017.
[16]李咏梅.益生菌辅助治疗重症急性胰腺炎14例[J].世界华人消化杂志,2007,15(3):302-304.
[17]刘宁,郭伟强,潘美云.早期联合应用肠内营养及益生菌辅助治疗重症急性胰腺炎的临床疗效[J].世界华人消化杂志,2015,23(36):875-5881.
[18]Sand J,Nordback I.Probiotics in severe acute pancreatitis[J].Lancet,2008,371(9613):634-635.
Probiotics in the treatment of severe acute pancreatitis:a Meta-analysis of randomized controlled trials
WangMaolin1,2,ChenZhu2,FengBimin2,WangGuojun1,2△
(1.DepartmentofPharmacy,theAffiliatedHospitalofSouthwestMedicalUniversity,Luzhou,Sichuan646000,China;2.DepartmentofClinicalPharmacy,CollegeofPharmacy,SouthwestMedicalUniversity,Luzhou,Sichuan646000,China)
Objective To systematically evaluate the safety and efficacy of probiotics in the treatment of severe acute pancreatitis (SAP).Methods The randomized controlled trials (RCTs) for studying probiotics in the treatment of SAP were retrieved from databases,including PubMed,Embase,Cochrane Library,Medline,Chinese Biomedical Literature Database (CBM),Chinese science and technology journal full-text database (VIP),China journal full-text database (CNKI),Wanfang academic journal full-text database.The methodological quality of included literatures was evaluated,and statistical analysis was performed via RevMan5.3 software.Results A total of 12 pieces of RCT literatures including 910 cases of patients with SAP were included.The results of meta analysis indicated that no statistically significant difference was found in the mortality [RR=0.97,95%CI(0.63,1.49),P=0.88],the incidence rate of multiple organ dysfunction [RR=0.72,95%CI(0.49,1.06),P=0.10] and the incidence rate of pancreas-related infections [RR=0.76,95%CI(0.54,1.07),P=0.12] between the probiotics group and the control group;while there were statistically significant differences in the length of hospital stay [MD=-3.74,95%CI(-6.37,-1.12),P=0.005] and the incidence rate of intestinal ischemia necrosis [RR=11.39,95%CI(1.5,86.4),P=0.02].Conclusion Probiotics could not improve clinical outcomes of patients with SAP,and may increase risk for intestinal ischemic necrosis.However,it could shorten the length of hospital stay.
probiotics;severe acute pancreatitis;Meta-analysis
2016年度重庆市出版专项资金资助项目
王茂林(1989-),药师,在读硕士,主要从事消化内科用药方面的研究。△
,E-mail:renren333@126.com。
2016年度重庆市出版专项资金资助项目
R576
A
1671-8348(2017)19-2672-05
2017-02-03
2017-04-08)
