HPLC波长切换法同时测定宝宝乐中四种成分的含量
2017-07-20张诚贤
沈 健,张诚贤
HPLC波长切换法同时测定宝宝乐中四种成分的含量
沈 健1,张诚贤2
目的 建立HPLC波长切换法同时测定宝宝乐中芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素的含量。方法 采用Venusil MP C18(250 mm×4.6 mm,5.0 μm),以乙腈-0.1%磷酸溶液为流动相,进行梯度洗脱,检测波长分别为230 nm(芍药内酯苷、芍药苷)和254 nm(毛蕊异黄酮葡萄糖苷、芒柄花素),流速0.9 mL/min,柱温30 ℃,进样量为10 μL。结果 芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素4个成分的质量浓度分别在4.18~83.60 μg/mL(r=0.999 8)、5.14~102.80 μg/mL(r=0.999 5)、5.60~112.00 μg/mL(r=0.999 9)、4.72~94.40 μg/mL(r=0.999 3)范围内与峰面积呈良好的线性关系;平均加样回收率及相应的RSD分别为99.66%(0.96%)、98.17%(1.39%)、97.00%(1.48%)、99.92%(0.58%);精密度良好,RSD≤1.06%;重复性良好,RSD≤1.69%。供试品溶液在室温条件下12 h内稳定,RSD≤1.12%。结论 所建立的方法灵敏度高、快速、专属性好、准确度高,为宝宝乐的质量控制提供了依据。
宝宝乐;芍药内酯苷;芍药苷;毛蕊异黄酮葡萄糖苷;芒柄花素;波长切换法;梯度洗脱
0 引言
宝宝乐由白芍、黄芪(蜜炙)、大枣、桂枝、干姜、山楂(炒)、六神曲(焦)、麦芽等8味中药材加工而成的中成药颗粒剂,具有温中补虚、和里缓急、开胃消食的功效,白芍[1]为方中君药,味苦、酸,微寒,养血敛阴,柔肝止痛,平肝阳,其主要成分为氧化芍药苷、芍药内酯苷和芍药苷;黄芪[1]味甘性微温,补齐固表,托疮生肌,毛蕊异黄酮葡萄糖苷和芒柄花素为黄芪的有效成分。宝宝乐主要用于脾胃虚寒、脘腹隐痛、喜温喜按、胃纳不香、食少便溏等症状的治疗。
宝宝乐标准收载于《卫生部颁药品标准》中药成方制剂第七册,是一种儿童常用药物,服用方便,其现行标准仅规定了制法、性状及冲剂的通则检查项,对所含成分未进行定量检测研究[2],也未检索到对该制剂多组分进行定量测定的文献报道,难以全面有效地控制本品的质量。多指标控制能更好地反映中成药的质量,本文对白芍的指标性成分芍药内酯苷、芍药苷,黄芪的指标性成分毛蕊异黄酮葡萄糖苷、芒柄花素,采用HPLC波长切换法同时进行了测定,现报道如下。
1 仪器与试药
Agilent 1100系列四元梯度泵高效液相色谱仪[四元梯度泵、自动进样器、柱恒温箱、可变波长检测器(VWD)](美国安捷伦公司);BS423S型分析天平(北京赛多利斯仪器系统有限公司);KQ-500DE超声波清洗器(昆山超声仪器有限公司)。
毛蕊异黄酮葡萄糖苷对照品(111920-201505,含量97.1%)、芒柄花素对照品(111703-201504,含量100.0%)、芍药苷对照品(110736-201640,含量95.2%)来源于中国食品药品检定研究院;芍药内酯苷对照品(39011-90-0,含量98.0%)来源于上海纯优生物科技有限公司。宝宝乐(5 g/袋,批号:615010、615016、616011)来源于河南宛东药业有限公司;乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 采用Venusil MP C18(250 mm×4.6 mm,5.0 μm)色谱柱;流动相A:乙腈,流动相B:0.1%磷酸溶液,梯度洗脱(0~12 min,15.0%A;12~23 min,15.0%A→22.0%A;23~32 min,22.0%A→38.0%A;32~40 min,38.0%A→15.0%A);0~23 min时在230 nm[3]波长下检测芍药内酯苷和芍药苷,23~40 min在254 nm[4]波长下检测毛蕊异黄酮葡萄糖苷和芒柄花素。流速:0.9 mL/min;柱温:30 ℃;进样量10 μL。
2.2 溶液的制备
2.2.1 对照品溶液的制备 分别精密称取对照品芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素各适量,用甲醇分别制得芍药内酯苷0.418 mg/mL、芍药苷0.514 mg/mL、毛蕊异黄酮葡萄糖苷0.560 mg/mL、芒柄花素0.472 mg/mL单一成分的对照品储备溶液。再分别依次量取上述各对照品储备液2.5、5.0、1.0、2.5 mL,置同一个量瓶中,用甲醇稀释至50 mL,振摇均匀,即得试验用混合对照品溶液。
2.2.2 供试品溶液的制备 取宝宝乐适量,研细,取约1.0 g,精密称定,置50 mL量瓶中,加入甲醇45 mL,超声处理30 min,放冷,再用甲醇稀释至刻度,振摇均匀,过滤,取续滤液,即得。
2.2.3 阴性样品溶液的制备 按宝宝乐质量标准项下的处方工艺,分别制备不含白芍的阴性样品和不含黄芪的阴性样品,按“2.2.2”项下方法制成白芍阴性样品溶液和黄芪阴性样品溶液。
2.3 专属性考察 精密吸取“2.2.1~2.2.3”项下制备的4个溶液各适量,按上述色谱条件进行检测。试验结果表明,白芍阴性样品溶液和黄芪阴性样品溶液的色谱图中,在所测芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素4个成分对应的位置无干扰,分离度均符合要求,理论塔板数均>2 500,色谱图见图1。
2.4 线性范围考察 分别精密吸取“2.2.1”项下制备的对照品储备液各0.1、0.2、0.5、1.0、1.5、2.0 mL,置于6个10 mL容量瓶中,用甲醇稀释至刻度,振摇均匀,即得到6个系列浓度的混合对照品溶液,按照上述测定方法进行测定,采用质量浓度X作为横坐标,测得的峰面积Y作为纵坐标,进行线性回归,回归方程及线性范围如表1所示。
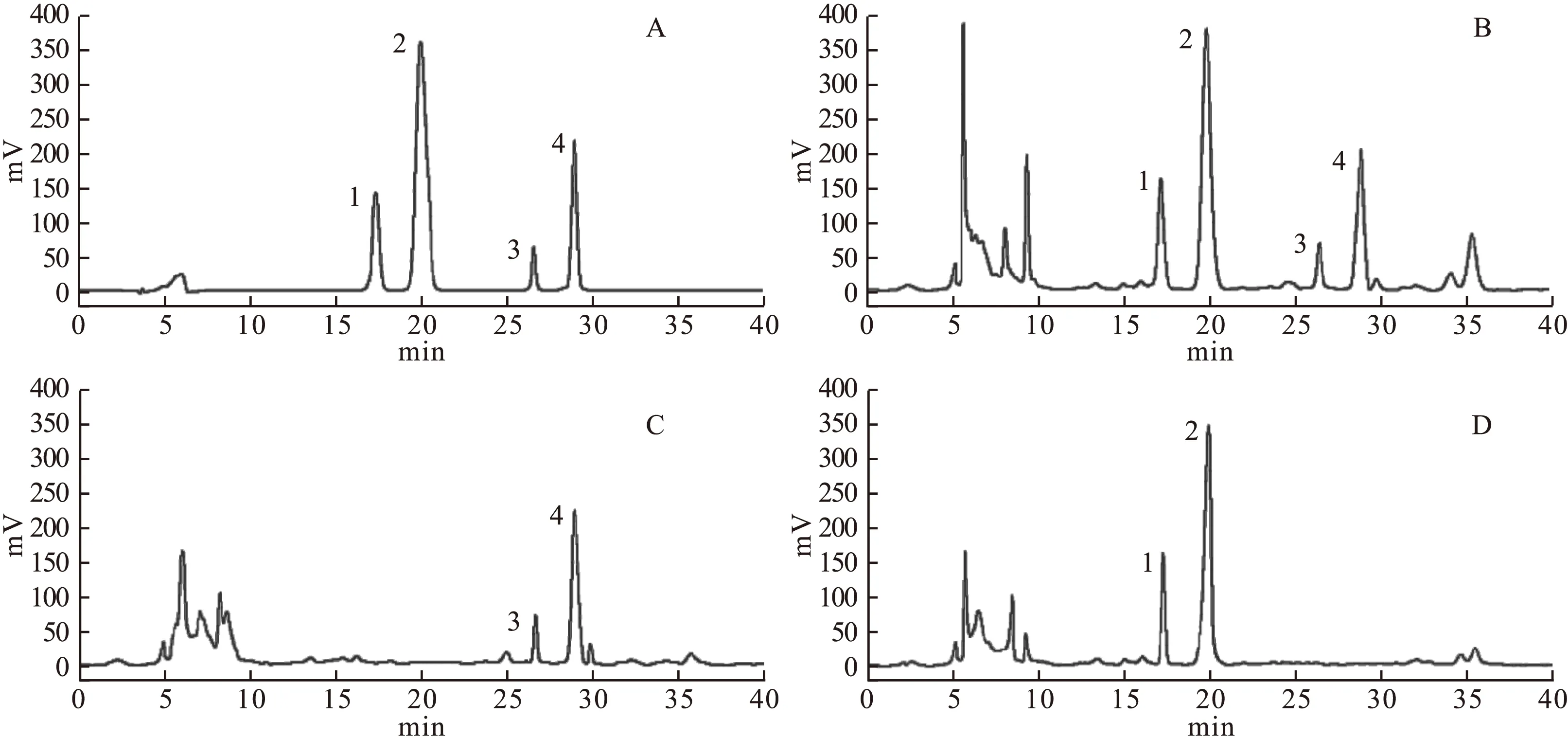
图1 色谱图

所测组分回归方程线性范围(μg/mL)r芍药内酯苷Y=6.5726×105X+417.94.18~83.600.9998芍药苷Y=9.1311×105X+181.25.14~102.800.9995毛蕊异黄酮葡萄糖苷Y=3.0413×105X-263.85.60~112.000.9999芒柄花素Y=7.0125×105X+448.04.72~94.400.9993
2.5 精密度考察 取混合对照品溶液,按“2.1”项下色谱条件测定,连续进样6次,记录峰面积,结果芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素峰面积的RSD(n=6)分别为0.92%、0.85%、1.06%和0.98%。
2.6 重复性考察 取宝宝乐样品(批号:615010)6份,按“2.2.2”项下制备方法制备供试品溶液,按“2.1”项下色谱条件进行测定,分别计算芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素的含量,并计算芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素含量的RSD,结果所测4个组分的RSD依次为1.42%、1.37%、1.69%和1.34%。
2.7 稳定性考察 取批号为615010宝宝乐样品的同一供试品溶液,室温下放置0、2、4、6、8、12 h,考察供试品溶液在室温下储存的稳定性,按“2.1”项下色谱条件测定芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素的峰面积值,结果其RSD分别为1.01%、0.96%、1.12%、1.07%。结果显示,供试品溶液自制备起,在室温下12 h内稳定。
2.8 加样回收率考察 取批号为615010的宝宝乐样品,研成细粉,取细粉6份,每份约0.5 g,精密称定,分置不同的50 mL量瓶中,精密加入上述制备的混合对照品溶液25 mL、甲醇20 mL,采用超声波超声处理30 min,放冷,用甲醇稀释至刻度,振摇均匀,过滤,即得加样回收样品试液。按“2.1”项下色谱条件及上述检测方法,计算芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素的回收率及RSD,结果其回收率分别为99.66%、98.17%、97.00%、99.92%,RSD分别为0.96%、1.39%、1.48%、0.58%。
2.9 样品测定 取3批宝宝乐,按“2.2.2”项下制备方法制备供试品溶液,按“2.1”项下色谱条件下进样测定,结果见表2。
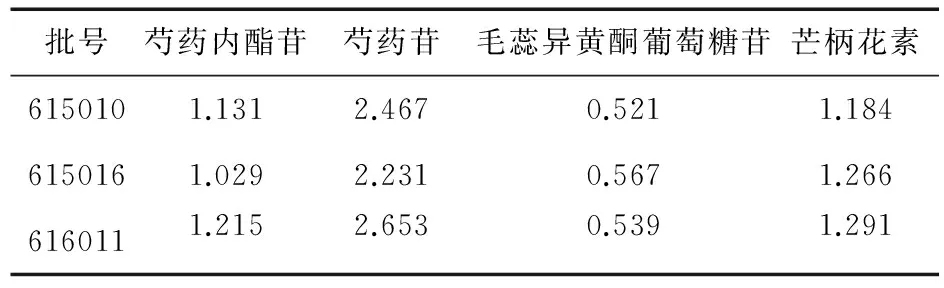
表2 含量测定结果(n=3,mg/g)
3 讨论
3.1 提取溶剂的选择 在实验过程中,笔者对不同的提取溶剂(50%甲醇、甲醇[5-6]、50%乙醇[7]、乙醇)进行了考察,以所测各组分芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素的提取率为指标,优选最佳的提取溶剂。结果以甲醇为提取溶剂时,所测4个组分的提取率最佳。
3.2 流动相的选择 本文分别考察了乙腈-水[4,8]、乙腈-0.2%乙酸溶液[9]、乙腈-0.02%磷酸溶液[5]、乙腈-0.1%磷酸溶液[10]等流动相体系,以所测各组分的分离效果、峰形等为指标,优选最佳的流动相体系。结果以乙腈-水为流动相体系梯度洗脱时,毛蕊异黄酮葡萄糖苷和芒柄花素能达到有效分离,但芍药内酯苷和芍药苷分离效果不佳;以乙腈-0.2%乙酸溶液为流动相体系梯度洗脱时,芍药内酯苷和芍药苷峰形较好,但芒柄花素与其他杂质峰达不到有效分离;以乙腈-0.02%磷酸溶液为流动相体系梯度洗脱时,毛蕊异黄酮葡萄糖苷峰形较差,存在拖尾现象;采用乙腈-0.1%磷酸溶液为流动相体系梯度洗脱时,基线较平稳,所测各组分峰形较好,均能达到有效分离,故选取乙腈-0.1%磷酸溶液按照文中的梯度洗脱程序对芍药内酯苷、芍药苷、毛蕊异黄酮葡萄糖苷和芒柄花素同时进行测定。
4 小结
本研究表明,本文所建立的HPLC波长切换联合梯度洗脱法,操作简便、准确,重复性好,能够有效控制宝宝乐的质量,确保临床用药的安全性和疗效的一致性,为进一步完善宝宝乐的质量标准提供了有力的数据支持。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:105,302-303.
[2] 中华人民共和国卫生部药典委员会.卫生部颁药品标准(中药成方制剂第七册)[S].北京:人民卫生出版社,1993:103.
[3] 李伟铭,赵月然,杨燕云,等.HPLC波长切换法同时测定白芍饮片中9个成分的含量[J].药物分析杂志,2011,31(12):2208-2212.
[4] 梁瑾,刘小花,任远,等.HPLC-DAD-ELSD法同时测定黄芪中5个成分的含量[J].药物分析杂志,2013,33(2):210-213.
[5] 欧金梅,吴德玲,金传山,等.HPLC法同时测定白芍总苷中4种单萜苷的含量[J].中药材,2013,36(3):423-425.
[6] 纪松岗,李翔,娄子洋,等.高效液相色谱法测定黄芪中毛蕊异黄酮苷和芒柄花素的含量[J].第二军医大学学报,2006,27(1):81-84.
[7] 刘金环,杨玉琴,丁秦,等.HPLC法同时测定白芍药材中芍药内酯苷和芍药苷的含量[J].河南中医,2013,33(10):1796-1797.
[8] 王晓辉,刘涛,李清,等.高效液相色谱法同时测定黄芪中的五种异黄酮类成分[J].色谱,2006,24(5):486-488.
[9] 陆小云,楚楚,颜继忠.超高效液相色谱法同时测定白芍中芍药苷和芍药内酯苷的含量[J].中南药学,2012,10(2):98-100.
[10]杜伟锋,胡淑珍,吴芳,等.不同等级杭白芍中3个有效成分的考察[J].中成药,2014,36(2):358-362.
Simultaneous determination of the content of four constituents in Baobaole by HPLC wavelength switching method
SHEN Jian1,ZHANG Cheng-xian2
(1.Huzhou Central Hospital,Huzhou 313000,China;2.Huzhou Institute for Food and Drug Control,Huzhou 313000,China)
Objective To develop an HPLC wavelength switching method for simultaneous determination of the content of alibiflorin,paeoniflorin,calycosin7-O-β-D-glucopyranoside and formononetin in Baobaole.Methods The Venusil MP C18(250 mm×4.6 mm,5.0 μm)chromatographic column was adopted;the mobile phase was acetonitrile-0.1% phosphoric acid solution with gradient elution,at a flow rate of 0.9 mL/min.The detection wavelengths were 230 nm(determination of alibiflorin and paeoniflorin),and 254 nm(determination of calycosin7-O-β-D-glucopyranoside and formononetin).The column temperature was set at 30 ℃,and the sample quantity was 10 μL.Results The concentration of alibiflorin,paeoniflorin,calycosin7-O-β-D-glucopyranoside and formononetin was respectively 4.18~83.60 μg/mL(r=0.999 8),5.14~102.80 μg/mL(r=0.999 5),5.60~112.00 μg/mL(r=0.999 9) and 4.72~94.40 μg/mL(r=0.999 3).The average recoveries and the correspondingRSDwere 99.66%(0.96%),98.17%(1.39%),97.00%(1.48%) and 99.92%(0.58%),respectively.The precision was good,RSD≤1.06%;the repeatability was goodRSD≤1.69%.Test solution was stable at room temperature within 12 h,RSD≤1.12%.Conclusion The established method is rapid,with high sensitivity,good specificity and high accuracy,which can be applied to the quality control of Baobaole.
Baobaole;Alibiflorin;Paeoniflorin;Calycosin7-O-β-D-glucopyranoside;Formononetin;Wavelength switching method;Gradient elution
2016-09-30
1.湖州市中心医院,浙江 湖州 313000;2.湖州市食品药品检验研究院,浙江 湖州 313000
10.14053/j.cnki.ppcr.201705021
