α-蒎烯环氧化反应的研究
2017-07-19张海东封禄田冮芷毓吴海璇郭彦彪
张海东, 封禄田, 冮芷毓, 吴海璇, 郭彦彪
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
α-蒎烯环氧化反应的研究
张海东, 封禄田, 冮芷毓, 吴海璇, 郭彦彪
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
以α-蒎烯为主要原料,双氧水经浓缩后再和冰乙酸反应制得过氧乙酸,用自制的过氧乙酸氧化α-蒎烯,高选择性地制备2,3-环氧蒎烷.通过体系预冷至-15 ℃的方法,容易控制反应温度,确定适宜的反应条件为:m(无水碳酸钠)∶m(α-蒎烯)=0.7,m(过氧乙酸)∶m(α-蒎烯)=3,氯仿为溶剂,在15 ℃下反应6 h.在此条件下,α-蒎烯的转化率达到99 %,2,3-环氧蒎烷的选择性达到95 %.
α-蒎烯; 2,3-环氧蒎烷;α-龙脑烯醛
2,3-环氧蒎烷作为合成香料的重要中间体,受到广泛关注,如利用2,3-环氧蒎烷可以合成龙脑烯醛.它又是合成檀香系列香料的主要原料,龙脑烯醛通过与丁酮发生羟醛缩合,加成,还原等步骤就可以合成檀香210[1],聚檀香醇[2-3]等一系列名贵的檀香系列香料[4].因此研究 2,3-环氧蒎烷的合成方法,对檀香香料化学有较大的理论价值和现实意义.
α-蒎烯生成2,3-环氧蒎烷的方法主要有两类:过氧酸环氧化法和过氧化氢环氧化法[5].其中过氧酸环氧化法,原料易得,过程简单,转化率和选择性较高.用过氧乙酸氧化α-蒎烯的反应方程式为:
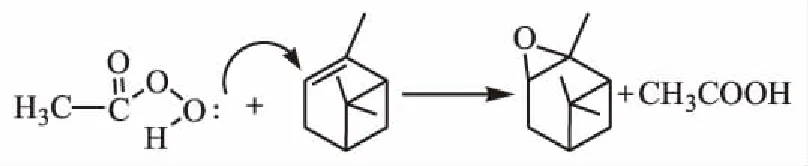
钟旭东[6]等人选择质量分数为40 %过氧乙酸作为环氧化剂,2,3-环氧蒎烷的选择性达到90 %以上,但需加入相转移催化剂,否则环氧蒎烷的选择性只能达到55 %~60 %.但加入的相转移催化剂沸点较高,体系乳化程度也很高,为分液分离带来困难;2013年徐徐[7]等人在反应温度为0~10 ℃,滴加浓度为2.0 mol/L过氧乙酸的条件下合成2,3-环氧蒎烷,α-蒎烯转化率为99 %以上,2,3-环氧蒎烷的选择性大于95 %,但实验发现反应初期放热特别剧烈,从0 ℃很容易就升温到20 ℃以上,不易控制.本文实验采用反应体系预冷至-15 ℃后加入过氧乙酸的方法,高选择性地合成了2,3-环氧蒎烷,反应过程方便控制,利于扩大生产规模.
1 实验部分
1.1 主要仪器与药品
安捷伦6820气相色谱仪,Nicolet 380 FT-IR红外光谱仪,予华仪器有限公司DFY-5L/40恒温低温反应浴,上海精科仪器有限公司WYA2S数显阿贝折射仪.
过氧化氢(质量分数30 %),α-蒎烯(质量分数95 %);冰乙酸(AR),浓硫酸(AR),无水碳酸钠(AR),无水硫酸镁(AR),丙酮、丁酮、氯仿、乙酸乙酯、甲苯均为分析纯.
1.2 过氧乙酸的制备及处理
采用文献[8]中方法浓缩过氧化氢,得到质量分数约为80 %的过氧化氢.然后冰乙酸、过氧化氢按照物质的量2∶1混合,加入总质量2 %的浓硫酸,常温下搅拌1 h,静置过夜,即得1.9~2.6 mol/L的过氧乙酸.在过氧乙酸中边搅拌边加无水乙酸钠中和至pH值为6~7后备用.
1.3 2,3-环氧蒎烷的制备
2 结果与分析
2.1 环氧化温度的影响
由于反应初始体系升温很快,所以尝试先把环境温度降至-15 ℃,再开始加入规定量的过氧乙酸,10~15 min滴加完毕;然后升温保持体系在一定温度,考察此温度对反应的影响,结果如图1所示.其他实验条件为:α-蒎烯21 g,无水碳酸钠17 g,氯仿37 mL,过氧乙酸90 g,反应8 h.
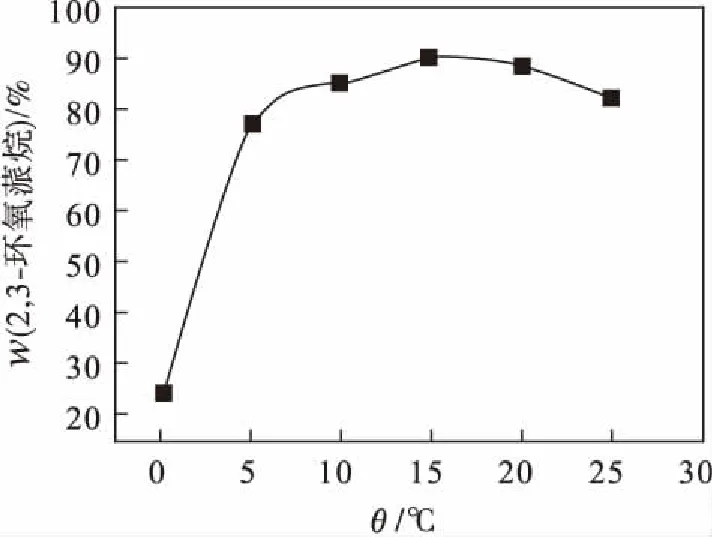
图1 环氧化温度的影响
由图1可以看出:温度低于15 ℃时,2,3-环氧蒎烷的质量分数随着温度的升高而不断增加,但由于2,3-环氧蒎烷分子结构既有三元环又有四元环,化学性质活泼,当温度超过15 ℃时,容易开环生成较多的副产物,影响2,3-环氧蒎烷的质量分数,故15 ℃为适宜反应温度.
2.2 环氧化时间的影响
在反应温度15 ℃的条件下考察反应时间对反应的影响,结果如图2所示.其他实验条件为:α-蒎烯21 g,无水碳酸钠17 g,氯仿37 mL,过氧乙酸90 g.由图2可以看出:反应时间小于6 h时,2,3-环氧蒎烷质量分数逐渐增加,因为低于6 h原料还未反应充分;大于6 h后,由于物料反应完全,使2,3-环氧蒎烷质量分数基本不变,故6 h为适宜反应时间.
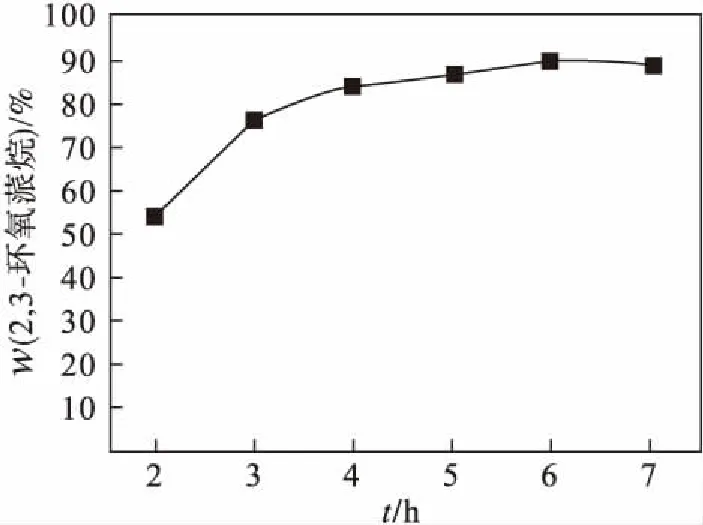
图2 环氧化时间的影响
2.3 缚酸剂无水碳酸钠用量的影响
控制反应温度为15 ℃,反应时间为6 h,在此条件下考察无水碳酸钠用量对反应的影响,结果如图3所示.其他实验条件为:α-蒎烯21 g,氯仿37 mL,过氧乙酸90 g.由图3可以看出:前期2,3-环氧蒎烷的质量分数随无水碳酸钠质量的增加而增加;后期基本不变,当无水碳酸钠质量为14.7 g,即与α-蒎烯质量比在0.7∶1时,目标产物质量分数达到最大值.无水碳酸钠虽不直接参与反应,但它在反应过程中起着重要的作用.首先,反应初期无水碳酸钠除具有缚酸剂的功能外还可能有结合体系中水的作用,从而使体系过氧乙酸增浓,所以初期2,3-环氧蒎烷生成速率很大.其次,由于反应生成醋酸,反应液中H+浓度升高,若不使用无水碳酸钠中和,会使环氧键发生开环副反应.因此,适宜的缚酸剂无水碳酸钠用量为14.7 g.
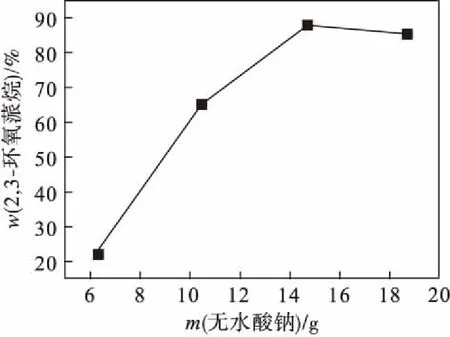
图3 缚酸剂无水碳酸钠用量对反应的影响
2.4 环氧化剂用量的影响
在α-蒎烯21 g,氯仿37 mL,反应温度15 ℃,反应时间6 h,无水碳酸钠15 g的条件下,考察环氧化剂过氧乙酸的用量对反应的影响,结果如图4所示.由图4可以看出:当过氧乙酸溶液质量为63 g时,过氧乙酸会使α-蒎烯完全环氧化.再增加过氧乙酸溶液用量,基本无变化.所以,过氧乙酸溶液质量为63 g时,2,3-环氧蒎烷的质量分数达到最高.
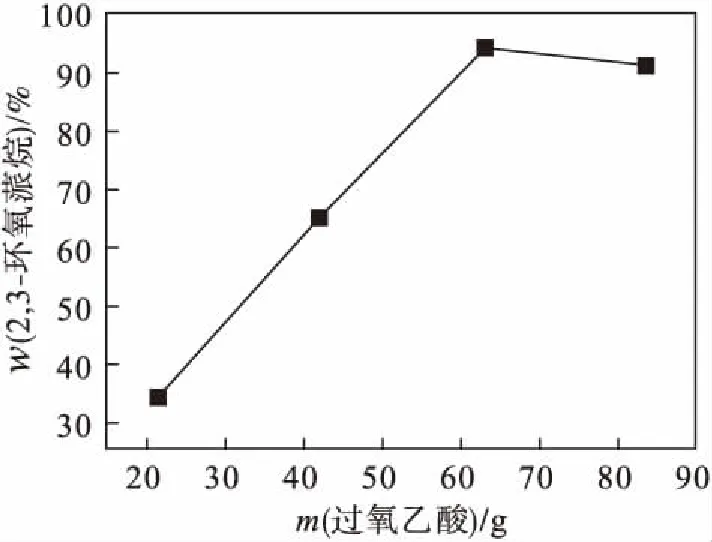
图4 环氧化剂用量对反应的影响
2.5 溶剂种类的影响
在α-蒎烯21 g,溶剂37 mL,反应温度15 ℃,反应时间6 h,无水碳酸钠15 g,过氧乙酸63 g的条件下,考察溶剂丙酮,氯仿,丁酮,乙酸乙酯,甲苯对反应的影响,结果见表1.由表1可以看出:氯仿、乙酸乙酯、甲苯做溶剂时,2,3-环氧蒎烷的选择性都达到了94 %以上,但乙酸乙酯,甲苯做溶剂时,蒎烯的转化率不高;丙酮,丁酮做溶剂时选择性,转化率都不高.
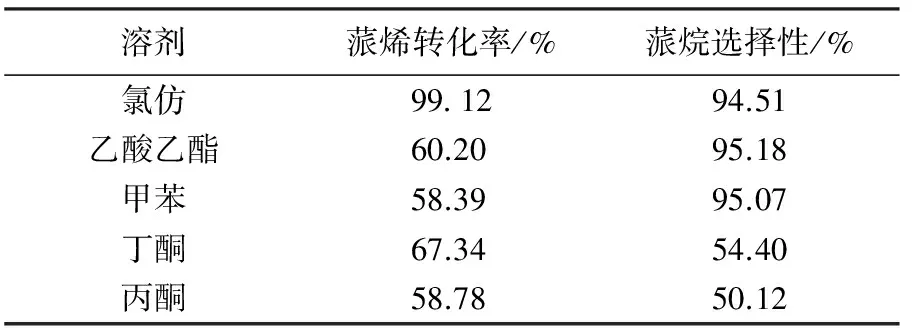
表1 溶剂种类对反应的影响
2.6 气相色谱(GC)及红外光谱分析
气相色谱(GC)分析条件为:色谱柱型号SE-52;进样温度260 ℃;检测器温度330 ℃;柱温80 ℃并保持1 min,然后以8 ℃/min的速度升温至220 ℃,再在220 ℃保持1 min.
在α-蒎烯21 g,氯仿37 mL,反应温度15 ℃,反应时间6 h,无水碳酸钠15 g,过氧乙酸63 g的条件下,反应结果的气相色谱图和红外光谱图如图5、图6所示.
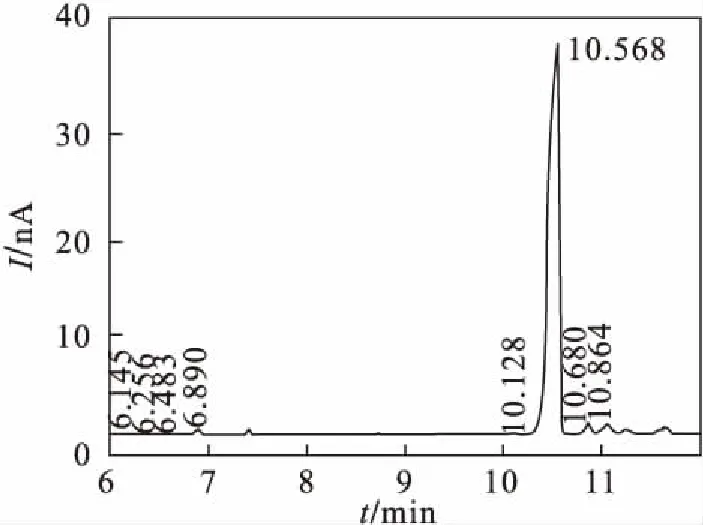
图5 2,3-环氧蒎烷的气相色谱
通过与标准样品对照表明:保留时间6.890 min是未反应α-蒎烯,保留时间10.568 min是生成的2,3-环氧蒎烷,10.864 min是副产物龙脑烯醛,其他小杂峰是所用原料本身和生成的副产物.经面积归一化法计算,α-蒎烯的转化率为99.12 %,2,3-环氧蒎烷的选择性为94.51 %.
红外光谱(IR)操作方法:将干燥的溴化钾(AR)粉末(约100 mg,粒度200目)装入模具内,在压片机上压制成片,再将样品涂在溴化钾晶片上.
与文献[9]值对比在红外谱图中波数838.97 cm-1处为环氧基的对称伸缩振动吸收峰,1 265.94 cm-1处为环氧基的不对称伸缩振动吸收峰,1 376.69 cm-1处为偕二甲基的振动吸收峰,2 918.29 cm-1处为六元环中CH2的不对称伸缩振动吸收峰,3 446.19 cm-1和1 646.65 cm-1处为溴化钾吸收空气中的水的吸收峰,1 731.67 cm-1是生成的副产物龙脑烯醛的羰基伸缩振动吸收峰,在3 000~3 100 cm-1未见α-蒎烯的==C—H的伸缩振动吸收峰.

图6 2,3-环氧蒎烷的红外光谱
3 结 论
本文采用自制的过氧乙酸氧化α-蒎烯,高选择性地制备了2,3-环氧蒎烷,得出结论:
(1) 由于初期环氧化反应速率快,温度急剧升高,不易控制,故应先将体系温度预冷至-15 ℃后再滴加过氧乙酸,容易控制体系的反应温度.
(2)m(无水碳酸钠)∶m(α-蒎烯)=0.7,m(过氧乙酸)∶m(α-蒎烯)=3,采用氯仿为溶剂,在15 ℃下反应6 h,可以高选择性地制备2,3-环氧蒎烷.
(3) 气相色谱(GC)及红外光谱分析表明上述条件下α-蒎烯转化率达到99 %,2,3-环氧蒎烷的选择性达到95 %.
[1] 蒋雁峰,裴雁,李菊仁.α-蒎烯合成香料研究进展[J].湖南化工,1999,29(4):4-6.
[2] 章平毅,戴辉,陆欢,等.聚檀香醇的合成方法:CN101723804A[P].2010-06-09.
[3] CASTRO J M,LINARES-PALOMINO P J,SALIDO S,et al.Synthesis of Polysantol®and Related Sandalwood-type Odorants Using Magnesiumα-Bromoketone Enolates[J].Tetrahedron Letters,2004,45(12):2619-2622.
[4] 俞忠华,周作良,吴卫,等.2,3-环氧蒎烷的合成[J].江西科学,2012,30(4):448-449.
[5] 付朝晖,刘图强,陈金珠,等.环氧蒎烷的合成研究与分析[J].江西林业科技,2004(6):28-30.
[6] 钟旭东,程芝.蒎烯环氧化及其产物的催化异构化反应的研究[J].林产化学与工业,1993,13(3):177-186.
[7] 徐徐,刘兵,唐年华,等.α-蒎烯高选择性环氧化合成2,3-环氧蒎烷的研究[J].南京林业大学学报(自然科学版),2013,37(1):96-100.
[8] 于国庆.高浓度过氧乙酸的实验室制备方法[J].天津化工,2012,26(4):42.
[9] 刘艳清,汪洪武,冯长根.α-蒎烯环氧化制备2,3-环氧蒎烷的研究[J].化学试剂,2002,24(2):120.
The Study for Epoxidation ofα-Pinene
ZHANG Hai-dong, FENG Lu-tian, GANG Zhi-yu, WU Hai-xuan, GUO Yan-biao
(Shenyang University of Chemical Technology, Shenyang 110142, China)
Peracetic acid was synthesized by reaction of acetic acid with pre-concentrated hydrogen peroxide.Then the self-madeperacetic acid was used to oxidizeα-pinene to synthesize 2,3-epoxypinane with high selectivity.The reactions were easier to control by precooling the system to 15 ℃.At the condition ofm(Na2CO3)∶m(α-pinene)=0.7,m(CH3CHOOOH)∶m(α-pinene)=3,chloroform as the solvent,15 ℃,6 h,the conversion rate ofα-pinene was above 99 %,and the selectivity of 2,3-epoxypinane was about 95 %.
α-pinene; 2,3-epoxypinane;α-campholenic aldehyde
2014-11-26
张海东(1989-),男,山东菏泽人,硕士研究生在读,主要从事精细化学品合成的研究.
封禄田(1961-),男,辽宁抚顺人,教授,博士,主要从事精细化工领域的研究.
2095-2198(2017)01-0020-04
10.3969/j.issn.2095-2198.2017.01.004
TQ655
A
