Cu-Si合金的高温氧化行为
2017-07-19张顺科付广艳
张顺科, 苏 勇, 付广艳, 刘 群
(1.沈阳化工大学 能源与动力工程学院, 辽宁 沈阳 110142;2.贵州工程应用技术学院 毕节市煤磷化工工程技术中心, 贵州 毕节 551700)
Cu-Si合金的高温氧化行为
张顺科1,2, 苏 勇1, 付广艳1, 刘 群1
(1.沈阳化工大学 能源与动力工程学院, 辽宁 沈阳 110142;2.贵州工程应用技术学院 毕节市煤磷化工工程技术中心, 贵州 毕节 551700)
通过氧化动力学曲线的测定以及对氧化膜形貌和构成的分析,研究Cu-0.6Si和Cu-3.6Si 合金在800 ℃、0.1MPa纯氧气条件下的高温氧化行为.结果表明:两合金氧化24 h后形成的氧化膜结构依次为CuO,Cu2O,Cu2O和SiO2的混合氧化物,均未形成连续的SiO2氧化膜.随着Si含量的提高,合金氧化膜内层SiO2含量明显提高,这有利于通过限制合金元素和氧的扩散提高合金的氧化抗力.Cu-3.6Si合金较Cu-0.6Si合金氧化膜内孔洞减少,致密度增加,这得益于SiO2对合金氧化膜内孔洞的补偿.SiO2对Cu较大的PBR值是两种合金氧化膜容易开裂的重要原因.
Cu-Si合金; 高温氧化; 氧化膜; 腐蚀
铜合金在导电和导热等诸多方面有着优良的性能[1].近些年来,铜硅复合材料在锂离子电池中的成功应用[2-4],又为铜合金的研究提供了新的思路.因此,随着科技的发展,铜合金越来越广泛地应用于工程领域.
向Cu合金中添加Al、Cr和Si,可期待提高其耐蚀性特别是耐氧化性能[5].Ogbuji[6]研究了Cu-Cr合金的恒温和循环氧化行为,发现随着Cr含量的增加,合金的氧化抗力增强,其氧化增重主要来源于Cr氧化物未完全覆盖合金基体时的氧化初期阶段,同时发现此阶段随着Cr含量的增加而变短.曹博[7]利用RBS等分析测试手段分别研究了在退火前后磁控溅射及离化团簇束沉积Cu薄膜与不同Si衬底之间的扩散和界面反应,并对扩散系数进行了估算.袁孚胜[8]采用铸锭冶金法制备了Cu-Si-Ni合金,通过多种方法研究了不同加工工艺和热处理方法对合金力学性能、导电性能及其组织结构的影响,并研究了它们的变化规律,从理论上进行了分析和解释.另外,有很多学者在改善Cu合金高温氧化性能方面进行了大量研究[9-11].
本文采用电弧熔炼方法制备了Cu-0.6Si和Cu-3.6Si合金,并研究它们在800 ℃纯氧气中的氧化行为,探讨了Si的添加对Cu-Si合金高温氧化行为的影响规 律,为改善Cu合金的耐蚀性能提供了理论依据.
1 实验方法
采用质量分数分别为99.8 %和99.9 %的Cu和Si(其中Cu和Si的主要杂质及其含量见表1和表2)按质量配比,将总质量为45 g的两种单质在真空非自耗电弧炉中通过电磁搅拌反复熔炼制成Cu-0.6Si和Cu-3.6Si合金.根据Cu-Si合金相图[12],两种成分的合金均为单相固溶体.利用线切割将合金锭切割成表面积约为150 mm2的片状试样,表面用800#砂纸处理,顶端打孔(φ≈1 mm),并清洁待用.
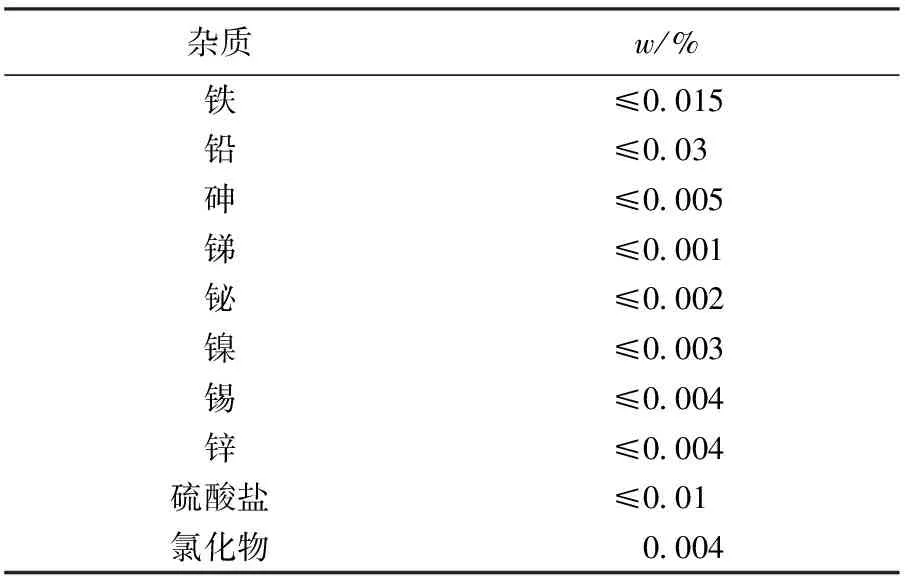
表1 Cu的主要杂质及其含量
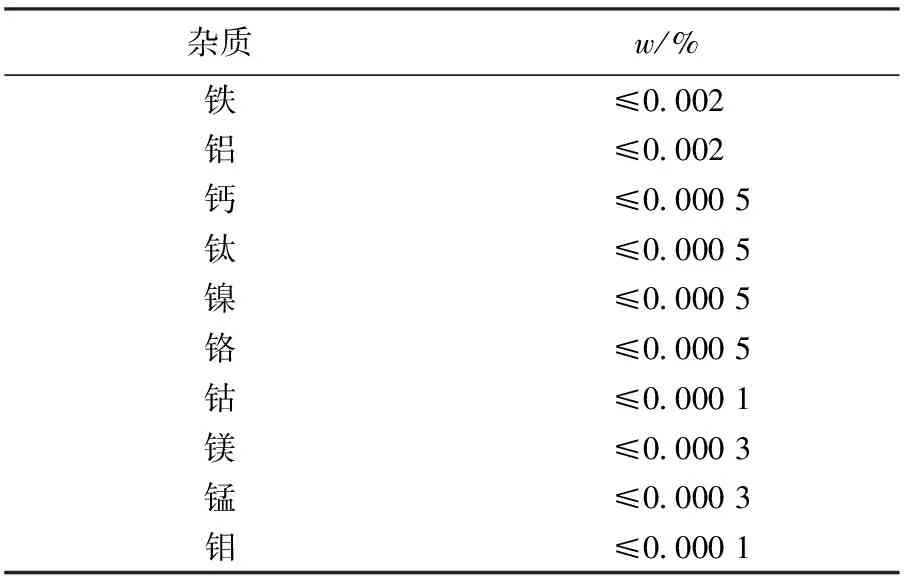
表2 Si的主要杂质及其含量
恒温氧化实验在Zry-2P型综合热分析仪中进行,具体实验条件:0.1 MPa流动的纯O2,温度800 ℃,氧化时间24 h.利用带有能谱的扫描电子显微镜(SEM/EDX),对两种成分合金氧化后的样品进行比较分析.
2 实验结果
2.1 氧化动力学曲线分析
图1为两种合金在800 ℃纯O2中氧化24 h的氧化动力学分析.图1(a)为合金单位面积氧化质量增量与时间的关系,由图1(a)可知:随着时间的增加两种合金的氧化速率逐渐降低,Cu-3.6Si 合金的氧化质量增量明显小于Cu-0.6Si 合金,表明随着Si含量的增加,合金的高温氧化抗力明显提高.另外,从图1(a)中还可以看出:Cu-3.6Si合金的氧化动力学规律不明显,而Cu-0.6Si合金的动力学曲线基本符合抛物线规律.图1(b)为Cu-0.6Si 合金单位面积氧化质量增量平方与时间的关系,计算表明其抛物线速率常数为4.40×10-9(g2·cm-4·s-1).

图1 Cu-Si合金在800 ℃纯O2中的氧化动力学曲线
2.2 氧化膜的结构与成分
图2和图3分别为Cu-0.6Si和Cu-3.6Si合金在800 ℃纯O2中氧化24 h后氧化膜的断面形貌和部分选区的能谱图.从图2(a)可以看出:Cu-0.6Si合金基体与氧化膜界面处形成了连续较宽的裂纹,如图中箭头所示,但从动力学曲线[图1(a)]的单调性看,这些裂纹产生于SEM样品的制备过程.不考虑裂纹宽度,氧化膜厚度约为280 μm.另外,在氧化膜内部形成了较多的孔洞,如图中矩形框内所示.这些孔洞降低了氧化膜的稳定性及其对基体的粘附性.图2(b)~(d)分别为图2(a)中A、B、C三点的能谱分析,表明氧化膜的最外层为CuO,其次为Cu2O.随着氧分压的减少,内层形成了混合氧化物Cu2O和SiO2.另外根据图2(d)中的能谱分析及图2(a) 的氧化膜形貌,可以判断Cu-0.6Si合金在该实验条件下发生了内氧化,在靠近氧化膜/基体的交界处,Si含量较高.
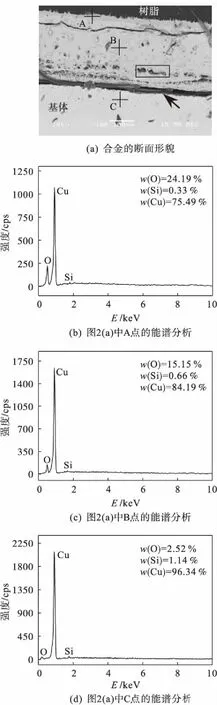
图2 800 ℃纯O2中氧化24 h后Cu-0.6Si合金氧化膜的断面形貌和部分选区的EDX分析
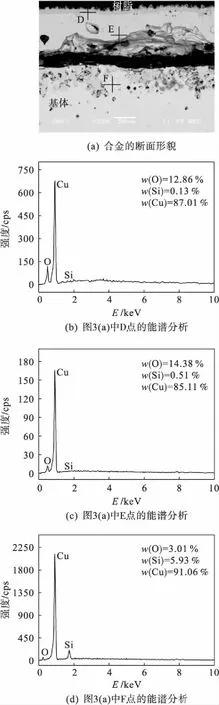
图3 800 ℃纯O2中氧化24 h后Cu-3.6Si合金氧化膜的断面形貌和部分选区的EDX分析
通过对Cu-3.6Si合金氧化膜断面形貌[图3(a)]和能谱分析[图3(b)~(d)]可知:Cu-3.6Si 合金形成的氧化膜结构类似于Cu-0.6Si合金,氧化膜的结构从内到外仍依次为CuO,Cu2O,Cu2O和SiO2的混合氧化物.但氧化膜中的孔洞较Cu-0.6Si更少,氧化膜更加致密,并且氧化膜内层Si含量明显增加,说明较Cu-0.6Si合金,Cu-3.6Si合金氧化膜内层生成了更多的SiO2.比较Cu-0.6Si和Cu-3.6Si合金氧化膜厚度,Cu-0.6Si 合金(280 μm)>Cu-3.6Si 合金(100 μm),这与氧化动力学曲线[图1(a)]显示的规律相一致.根据图中氧化膜形貌,两种合金氧化膜的粘附性均较差,并且均未形成连续的具有保护性的SiO2氧化膜,但Cu-3.6Si合金的氧化质量增量较Cu-0.6Si有明显的降低.
3 讨 论
从热力学上看,在实验温度下,SiO2生成的自由能低于Cu2O、CuO[13-14],SiO2的稳定性大于Cu2O、CuO,因而Si优先氧化生成SiO2.但是从动力学角度看,SiO2的生长速率较慢,故而被生长速率较快的Cu2O和CuO所覆盖[15],因此自外及内随着氧分压的降低氧化膜中依次包含了CuO和Cu2O[16],最内层生成了SiO2和Cu2O的混合氧化物.本研究中两合金表面均未形成连续的SiO2氧化膜,这可能与合金较低的Si含量有关[17].虽然如此,Cu-3.6Si合金氧化膜内层的Si含量较Cu-0.6Si合金明显增大,这增大了SiO2在氧化膜内层的含量,从而一定程度上限制了合金元素和氧的扩散,有利于合金氧化抗力的提高.
图2和图3表明Cu-0.6Si和Cu-3.6Si合金氧化膜孔洞多,粘附性较差.根据Pilling与Bedworth[18]提出的理论,氧化膜的致密性取决于氧化物分子与金属原子的体积比(PBR).当PBR≈1时,可形成具有保护性的完整连续的氧化膜;若PBR较小,则氧化物生长太慢,无法完全覆盖金属表面;若PBR较大,则氧化物生长太快,容易使氧化膜因应力积累过大而开裂与剥落.其计算方法如下:
PBR=Vox/VM
(1)
其中:VM和Vox分别为合金元素及其氧化物的摩尔体积,根据文献[18],Si的PBR值为1.72,记为:
PBRSiO2/Si=VSiO2/VSi=1.72
(2)
在本研究中,由于Cu为溶剂元素,SiO2应在氧化膜内层生成,因此应主要考虑SiO2对Cu的PBR.其计算方法如下:
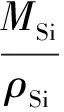
(3)

(4)
式中:VSi为Si原子的摩尔体积;VCu为Cu原子的摩尔体积;M和ρ分别为元素的摩尔质量和元素单质密度,取MSi=28 g/mol,MCu=64 g/mol,ρSi=2.33 g/cm3,ρCu=8.92 g/cm3.经计算,Cu-Si 合金表面SiO2氧化膜的PBR值约为2.9,故SiO2氧化膜在形成过程中容易开裂,无法形成完整连续的SiO2氧化膜.
Cu-0.6Si和Cu-3.6Si合金,在基体和氧化膜的交界处存在较多孔洞,这来源于Cu2+扩散留下的阳离子空位的聚集.但Cu-3.6Si合金氧化膜中的孔洞明显减少,氧化膜更加致密,这可能与Cu-3.6Si合金中有更多的SiO2形成并填补了Cu2+空位有关[19].氧化膜致密度的增加,有利于阻止氧和金属元素的扩散,提高合金的氧化抗力.
4 结 论
(1) 在800 ℃,Cu-0.6Si和Cu-3.6Si合金氧化膜的构成自外及内依次为CuO,Cu2O,Cu2O和SiO2的混合氧化物.
(2) 随着Si含量的增加,Cu-Si合金氧化膜内层SiO2含量增加,有利于通过限制合金元素和氧的扩散提高合金的氧化抗力.同时,由于SiO2对合金氧化膜内孔洞的补偿,Cu-3.6Si合金较Cu-0.6Si合金氧化膜内孔洞减少,致密度增加.
(3) 实验条件下各合金均未形成连续的SiO2氧化膜,这与合金较低的Si含量和SiO2对Cu合金较大的PBR值引起的氧化膜内应力积聚有关.
[1] 宋金龙,魏国武,郭泰清,等.10Cr1Cu耐蚀电焊管的生产工艺研究[J].钢铁,1993,28(3):30-33.
[2] 王茜,贾梦秋.化学镀铜法制备硅铜复合材料及其在锂离子电池中的应用[J].过程工程学报,2011,11(4):689-694.
[3] POLAT D B,KELES O,AMINE K.Well-aligned,Ordered,Nanocolumnar,Cu-Si Thin Film as Anode Material for Lithium-ion Batteries[J].Journal of Power Sources,2014,270:238-247.
[4] POLAT B D,KELES O.Multi-layered Cu/Si Nanorods and Its Use for Lithium Ion Batteries[J].Journal of Alloys and Compounds,2015,622:418-425.
[5] 李远士.几种金属材料的高温氧化、氯化腐蚀[D].大连:大连理工大学,2001:3-12.
[6] OGBUJI L U.Oxidation Behavior of Cu-Cr Environmental Barrier Coatings on Cu-8Cr-4Nb[J].Surface and Coatings Technology,2005,197(2):327-335.
[7] 曹博.铜硅体系的扩散和界面反应[D].兰州:兰州大学,2008:1-9.
[8] 袁孚胜.新型铜硅合金材料的制备及组织性能的研究[D].赣州:江西理工大学,2009:14-15.
[9] NIU Y,WANG S Y,GESMUNDO F.High-temperature Scaling of Cu-Al and Cu-Cr-Al Alloys:An Example of a Non-classical Third-Element Effect[J].Oxidation of Metals,2006,65(5):285-306.
[10]FU G Y,NIU Y,GESMUNDO F.Microstructural Effects on the High Temperature Oxidation of Two-phase Cu-Cr Alloys in 1 atm O2[J].Corrosion Science,2003,45(3):559-574.
[11]LI Y S,NIU Y,FU G Y,et al.Effect of Grain Size Reduction on High Temperature Oxidation of Binary Two-phase Alloys[J].Transactions of Nonferrous Metals Society of China,2001,11(5):644-648.
[12]SUFRYD K,PONWEISER N,RIANI P,et al.Experimental Investigation of the Cu-Si Phase Diagram atx(Cu)>0.72[J].Intermetallics,2011,19(10):1479-1488.
[13]李美栓.金属的高温腐蚀 [M].北京:冶金工业出版社,2001:5.
[14]朱日彰,何业东,齐慧滨.高温腐蚀及耐高温腐蚀材料 [M].上海:上海科学技术出版社,1995:28.
[15]MITRASINOVIC A M,UTIGARD T A.Trace Elements Distribution in Cu-Si Alloys[J].Chemical Physics Letters,2011,515(1/3):72-77.
[16]ZHANG D F,MORRAL J E,BRODY H D.Measurements for Cu and Si Diffusivities in Al-Cu-Si Alloys by Diffusion Couples[J].Materials Science and Engineering A,2007,447(1/2):217-221.
[17]王海涛.复合氧化膜对铁基高温合金抗氧化性能影响与机理研究[D].济南:山东大学,2010:7-11.
[18]PILLING N B,BEDWORTH R E.The Oxidation of Metal in High Temperature[J].Journal of Institute of Metals,1923,29:529-530.
[19]卢亚轩,高景海,刘万生,等.Ce对Ni-Cr-Cu合金抗氧化性的影响[J].中国腐蚀与防护学报,1982,2(2):21-28.
High-temperature Oxidation Behavior of Cu-Si Alloys
ZHANG Shun-ke1,2, SU Yong1, FU Guang-yan1, LIU Qun1
(1.Shenyang University of Chemical Technology, Shenyang 110142, China;2.Guizhou University of Engineering Science, Bijie 551700, China)
By means of the measurements of oxidation kinetic curves and the analysis on compositions and morphologies of oxide scales,the high-temperature oxidation behavior of Cu-0.6Si and Cu-3.6Si alloys at 800 ℃ in 0.1 MPa flowing pure O2has been investigated.Results show that the oxide scales of the two alloys consist of CuO,Cu2O and complex oxides of Cu2O and SiO2from outside to inside after 24 h oxidation,and no continuous layers of SiO2are formed.The SiO2content in the inner layers of oxide scales increases with the Si content,which is beneficial to improving the oxidation resistance of the alloys by hindering the diffusion of alloying elements and oxygen.Benefited from the compensation of SiO2for holes in oxide scales,the oxide scales formed on Cu-3.6Si alloy have less holes and larger density than Cu-0.6Si alloy.The biggerPBRof SiO2to Cu is the important reason for the fact that the oxide scales on the alloys are easy to crack.
Cu-Si alloy; high-temperature oxidation; oxide scale; corrosion
2014-12-03
贵州省高等学校创新能力提升计划(黔教合协同创新字[2014]08)
张顺科(1989-),男,河北张家口人,硕士研究生在读,国家奖学金获得者,主要从事材料的制备与耐蚀性的研究.
苏勇(1979-),男,山东临沂人,副教授,博士,主要从事材料的腐蚀与防护、显微组织控制及对性能影响的研究.
2095-2198(2017)01-0072-05
10.3969/j.issn.2095-2198.2017.01.013
TG172
A
