“无机化学”教学难点的梳理与辨析
2017-07-07张一兵李俏
张一兵, 李俏
(上饶师范学院 化学与环境科学学院,江西 上饶 334001)
“无机化学”教学难点的梳理与辨析
张一兵, 李俏
(上饶师范学院 化学与环境科学学院,江西 上饶 334001)
针对“无机化学”课程特点和大一新生的具体情况,从三个方面对“无机化学”中基本概念和基本理论部分的教学难点进行了深层次的梳理与辨析,以期达到提高学生的学习兴趣和效果的目的。
无机化学;教学难点;梳理;辨析;大学新生
“无机化学”是我校化学专业大一新生的专业课,由于是第一学年开设(第一学期“无机化学”上册内容为:基本概念与基本理论部分,第二学期“无机化学”下册:元素化学及配合物等内容)。长年的教学中所遇到的问题主要有如下几个方面:一是扩招后大学新生基础普遍薄弱,相当部分的学生中学化学知识还没有过关;二是新生适应大学学习生活的能力差,角色变换慢;三是对于现在的学生而言教学内容相对多,课时相对少;四是大环境下高校对学生要求低,要求保证有一定的毕业率和学位授予率,即要减小挂科率,导致学生学习动力不足,竞争意识弱。经过多年的“无机化学”教学,笔者对历届学生的学习情况进行了较长时间的比较与思考,现就扩招下的学生所显现的“无机化学”上册中基本概念与基本理论部分的教学难点进行梳理辨析(注:扩招前学生有的可能并不觉得是难点),以期帮助学生提高学习兴趣,少走弯路,提高学习效率,为后续专业课程夯实基础。
目前我们采用武汉大学等学校编写的“无机化学”作为主要教材[1],本文大致依照此教材上册中的教学内容的主要编排次序即物质的状态、原子结构、化学键与分子结构、化学热力学初步、化学反应速率、化学平衡、溶液、电解质溶液、氧化还原反应,进行讲述,不足之处敬请专家同行批评指正。旨在抛砖引玉,共同上好“无机化学”这门课。
1 原子结构部分
原子结构与分子结构是“无机化学”最重要也是最难学的两章。由于原子与分子看不见摸不着,属于微观世界,大一新学生普遍觉得原子结构这章内容抽象难懂,不易掌握。那么人们是如何知道原子的核外电子运动及排布的呢?讲解的方法可先给学生梳理一条由宏观到微观、由粗到细、由现象(化学性质)到本质(物质结构)脉络(如图1),让学生先有感性认识再到理性掌握,沿着图1的走向进行反向学习。

图1 原子结构讲解反向示意图
由图1学生就很快理解为什么教材中要先从氢原子(最简单的单电子原子)光谱入手,由易到难、由表及里进行渐进阐述。讲解本章内容要格外注意帮助学生建立微观粒子与宏观物质的运动方式截然不同,前者的运动具有波粒二象性(符合测不准原理),其运动行为不能套用宏观物质运动的经典力学公式——牛顿定理,而要用统计学的观点,以薛定谔方程来描述。
本章节另一个难点是四个量子数,即主量子数n、副量子数或角量子数l、磁量子数m、自旋量子数ms。除了帮助学生理解并掌握4个量子数的物理意义外,更重要的要掌握各量子数的功用。如图2所示,n、l决定多电子原子的电子的能量(其中H原子的电子能量仅由n决定);n、l、m决定电子的空间运动状态,即原子轨道、波函数;n、l、m、ms决定电子在原子核外的运动状态。我们把原子“轨道” 叫做电子的空间运动状态,把既有一定空间运动状态又有一定自旋状态的电子称作具有一定运动状态的电子。训练学生必须具备通过关联4个量子数数值计算各电子层中可能有的电子运动状态数的能力。
多电子原子的核外电子的排布要遵守三个原理及一个补充规则(俗称三把半钥匙):能量最低原理、保里不相容原理、洪特规则及其一个补充规则(全充满、半充满、或全空规则)。其中学生最难掌握并应用的是能量最低原理,因为必须掌握原子轨道的近似能级序,而大多数人往往是死记硬背。如何让学生能轻而易举的掌握原子轨道的近似能级序呢,笔者采用了如图3的方法帮助学生。
图3的形式是二叠V形,即一个大V字母内套一个小V字母,再配上口诀进行讲解,学生感觉形象易懂,效果很好。如果万一忘记了,还可结合我国著名化学家徐光宪将原子轨道的能级近似计算公式对能级进行排序:(1)对于基态原子:n+0.7l;(2)对于基态阳离子:n+0.4l。
图3的能量最低原理的能级序口诀:1,22,33,434,545,6456,7567,s开始,p结尾, f靠s,d靠p。口诀释义:1(1s),22(2s2p),33(3s3p),434(4s3d4p),545(5s4d5p),6456(6s4f5d6p),(7s5f6d7p)。图3将能级组、能级组内各原子轨道、元素周期表的分区、各周期的元素数目等知识有机地联系起来了。

图2 四个量子数的功用
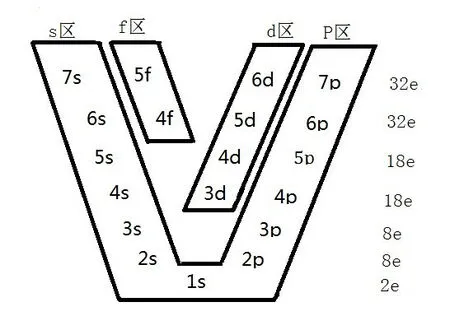
图3 原子轨道的近似能级序
2 分子结构部分
分子结构与化学键是“无机化学”最重要也最难学的另一章。相邻原子间通过强烈的作用力(即化学键)形成了分子。由于各原子的性质不同,形成了三类不同的化学键即离子键、共价键和金属键。其中通过共价键形成的物质最广泛。为此有关共价键的理论也最多,到目前为止主要有4个,分别是现代价键理论(即电子配对理论简称VB法)、杂化轨道理论、分子轨道理论(简称MO法)、价层电子对互斥理论(简称VSEPR理论)。杂化轨道理论应用相对更为普遍。各理论的功用各有千秋,通过列表(表1),便于学生掌握。
多原子共价分子ABn的极性与其键的极性和分子的空间构型(即形状)相关。如何教授学生准确快速把握共价型分子的空间构型,是教学的相对难点。为此笔者将相关知识联系起来梳理成表2,期望有事半功倍之效。表2中的等性杂化,笔者认为教材说的不够全面,应符合3个条件:(1)组成中心原子A杂化轨道的原子轨道的成分及能量均相同;(2)中心原子A无孤对电子对;(3)中心原子A与相同的端原子B或配位原子B形成键。上述条件如果有一个不符合即为不等性杂化,如BeCl2、BCl3、PCl5、SCl6等是等性杂化,而PCl3、H2O、CH3Cl等是不等性杂化。

表1 四大共价键理论的功用比较

表2 共价键及其形成分子的极性关系
杂化轨道理论在解释分子的空间构型时非常好用,应用广泛,尤其为后续的“有机化学”运用更多。为此,笔者有意识地对这部分内容与VSEPR理论进行对应比较教学(表3),便于学生消除这方面的难点。
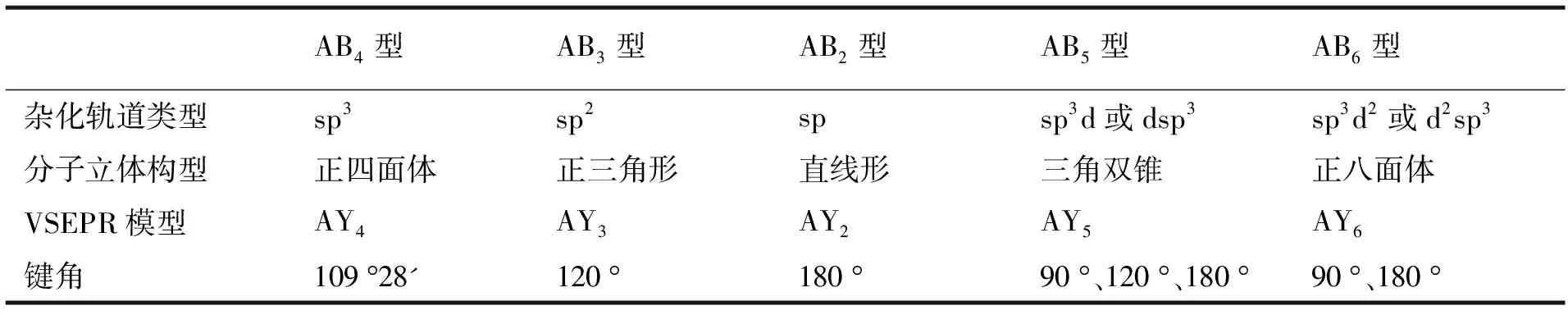
表3 几类典型的等性杂化轨道形成的完美分子构型
分子间作用力即范德华力的作用范围及产生原因是学生难以掌握的教学难点,为此笔者对此部分教学内容进行了梳理并总结列于表4,以利于学生的概念澄清,牢固掌握。从表4可知,色散力存在于一切分子之中,而取向力只存在于具有固有偶极的极性分子之间。

表4 分子间作用力作用范围及产生原因
化学键(原子间作用力)与分子间作用力(包括特殊形式的范德华力—氢键)的产生原因、产生对象、作用力大小以及力的特征等知识,有的学生也往往不易掌握,鉴于此,将它们进行了梳理比较分析,如表5,让学生一目了然,能快速准确地理解并掌握。
需要指出的是,氢键的本性到底是什么,目前说法不一。有的说是静电引力,因为高电负性的F或O或N与H结合形成共价型分子HY,使得H几乎成为质子,此时的H呈现强电正性,易与另一个分子HY中的Y原子即F或O或N接近,产生静电吸引作用,结果形成氢键,表5暂时采用这一说法;有的说是共价键,因为它具有饱和性和方向性的特征,但键的数值太小,没有达到化学键范围,所以又不合理;有的以作用力大小为依据,认为氢键是特殊形式的分子间作用力,但让人不信服的是它又有饱和性与方向性的共价键特征。
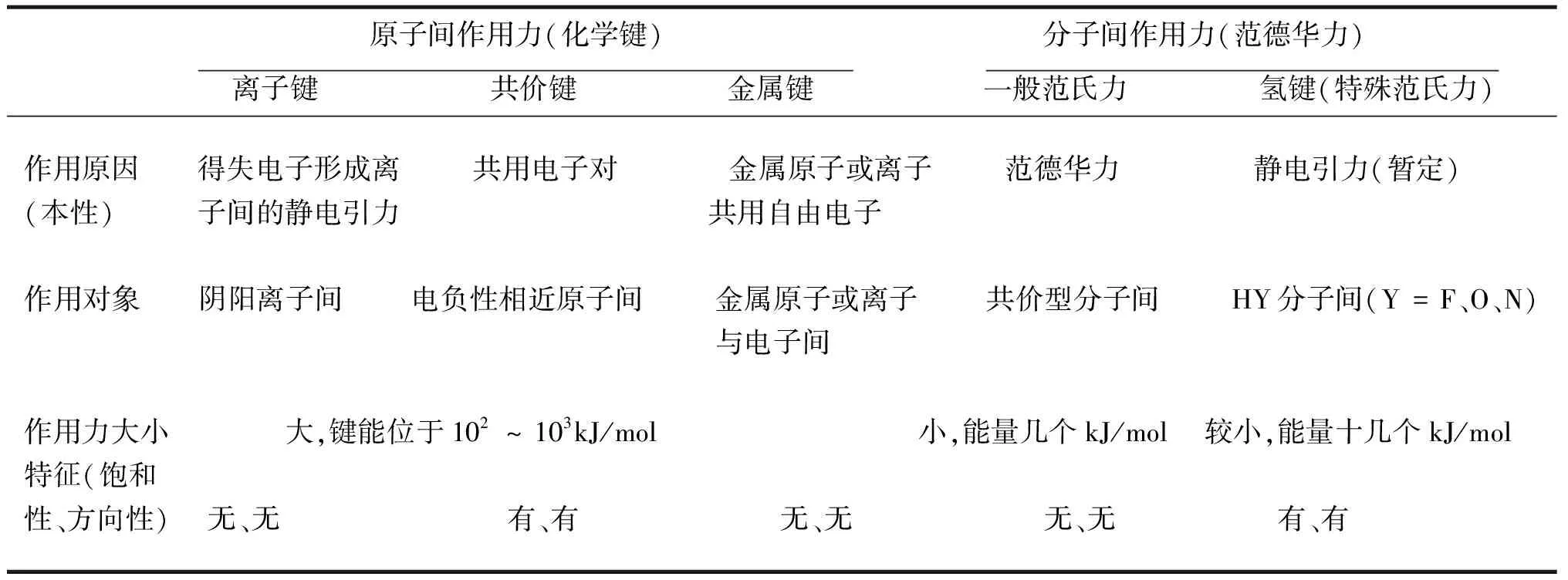
表5 原子间力与分子间力之比较
由化学键或分子间作用力形成的分子,其晶体往往不同,目前分为4类。为此将4种晶体的性质等知识进行综合比较得表6,目的是让学生便于厘清与掌握。

表6 四种晶体的性质比较
3 其它章节部分
除了上述最重要的两章有较多的难点外,其它章节相对更为容易些。梳理一下主要有如下难点。
3.1 化学热力学初步
状态函数的概念等知识是本章的重要内容,由于运用盖斯定律的函数必须是状态函数,所以学生要分清哪些是状态函数,哪些是非状态函数。状态函数主要有:P、V、U、H、S、G等,非状态函数有:W、Q等。注意教授学生状态函数的集合(和、差、积、商)也是状态函数[2],即U、H、S和G等也是状态函数。在U、U、H、H、S、S、G、G中,只有S有绝对值,U、H、G则没有。还要特别提醒S、S与H、G单位的异同。
要教会学生注意对大学化学中热力学的“标准状态”和中学化学中的“标准状况”这两个概念区分(见表7)。前者条件指的是:处于标准压力1.01×105Pa下的状态称为标准状态;后者要同时指明压力与温度即在标准压力101.325 kPa和273.15 K(即0 ℃)条件下为标准状况。

表7 “标准状态”与“标准状况”的比较
关于为何规定白磷的标准摩尔生成热为0的原因,一些学生弄不明白,为此要进行特别讲解。标准摩尔生成热定义是[2]:“在标准压力1.01×105Pa和指定温度下,由最稳定的单质生成1 mol该物质的等压热效应”。并规定在标准状态下最稳定单质的生成热为0,常用的是298 K的数据。但是,红磷化学性质比白磷稳定,为什么规定白磷作标准摩尔生成热为0而不是用红磷(红磷的为负值)呢?其原因是[2]:(1)到目前为止,人们对白磷的结构研究相对更为成熟。研究表明,在固态、液态和673 K以下的气态下,白磷均以P4分子形式存在,P4为正四面体,其键能、键角等参数业已确定;红磷的结构现在尚未弄清楚;(2)白磷的存在相对更为普遍。人们从磷酸盐中提取磷蒸气迅速导入水中冷却,结果总是得到白磷而不是其它同素异性体如红磷、黑磷等。白磷长期放置或在673 K密闭加热数小时才转化成红磷;将白磷高压下或常压用汞作催化剂加热方能得到黑磷;(3)白磷的化学性质相对更为活泼。所涉及白磷的化学反应比红磷或黑磷多的多。综上所述,人为规定白磷的标准生成热为0并用以进行相关计算,则显得更方便、更实用。长期的教学经验及实践表明,讲述标准生成热定义时,将白磷作为特例作出说明,有利于学生理解最稳定单质及标准生成热等概念,学会处理矛盾的普遍性与特殊性的关系,更加理解知识是为人类生产生活服务的。
3.2 溶液
溶液这章除了大纲要求掌握的基本知识外,要提示学生注意胶体溶液与高分子溶液的异同点,不然就会混淆不清,表8是为此所做的梳理、分析比较。

表8 胶体溶液与高分子溶液的性质比较
3.3 电解质溶液
有的学生对四大酸碱理论概念及优缺点分不清楚,老师应该对此讲透(表9)。四大酸碱理论包括酸碱电离理论、酸碱质子理论、酸碱电子理论、软硬酸碱理论(严格上算不上理论,只是经验规则,它以酸碱电子理论为基础。教材将此理论安排在下册的配合物一章,为了知识的综合归类,利于学生对比掌握,故提前在此讲解)。其中软硬酸碱理论是学生最难掌握的。

表9 四个酸碱理论的比较
软硬酸碱[4-5]将酸、碱分为“硬” “软”两种。“硬”指具有较高电荷密度、较小半径的微粒(原子、离子、分子),它们具有较大的“电荷密度/粒子半径”的比值;“软”是具有较低电荷密度、较大半径的微粒,即具有较小 “电荷密度/粒子半径” 的比值。“硬” 微粒的变形性(可极化性)较小,但极性较大;“软”粒子的变形性(可极化性)较大,但极性较小。为此软硬酸碱的概念如下(主要应用于配合物):
硬酸:正电荷数、体积小、变形性小,即对外层电子抓得紧的中心原子。如: H+、Li+、Na+、Fe3+、Cr3+,等。
软酸:正电荷数低、体积大、变形性大,即对外层电子抓得松的中心原子;如Hg2+、Ag+、Cu+、Cd2+,等。
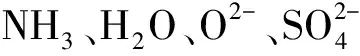

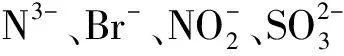
硬酸和硬碱相互作用力主要是静电引力,软酸和软碱相互作用力则以共价键为主。该理论的酸碱结合的口诀是:软亲软,硬亲硬,软硬结合不稳定。
4 结语
针对性地对“无机化学”上册的主要难点进行梳理与辨析,学生觉得这些难点知识掌握起来更容易了,结果增加了他们对无机化学的学习兴趣,提升了学习动力,变畏难为主动学习,收到了良好的教学效果。
[1] 武汉大学,吉林大学,等.无机化学:上册[M].3版.北京:高等教育出版社,1994.
[2] 徐祖耀,李麟.材料热力学[M].4版.北京:科学出版社,2005.
[3]吴国庆.无机化学[M].4版.北京:高等教育出版社,2002:229-230.
[4] PEARSON R G.Hard and soft acids and bases HSAB.1.Fundamental principles[J].Journal of Chemical Education,1968,45(9):581-587.
[5] PEARSON R G.Hard and soft acids and bases HSAB.2.Underlying theories[J].Journal of Chemical Education,1968,45(10):643-648.
Differentiating and Analyzing on the Teaching Difficulties ofInorganicChemistry
ZHANG Yibing, LI Qiao
(School of Chemistry and Environmental Science, Shangrao Normal University, Shangrao Jiangxi 334001, China)
According to both the characteristics of theinorganicchemistryand the specific circumstances of college freshman, this paper gives a deep differentiating and analyzing on the teaching difficulties of basic concepts and basic theory ininorganicchemistryfrom three aspects, in order to improve the students' learning interest and effect.
inorganicchemistry; teaching difficulties; differentiating and analyzing; college freshman
2017-02-20
江西省教育厅教改课题(JXJG-16-16-3);江西省精品课程资助项目(赣教高字〔2011〕74号) ;江西省精品资源共享课程资助项目(赣教高字〔2015〕79号)
张一兵(1963-),男,江西上饶人,教授,硕士,主要从事无机化学与无机材料研究。 E-mail:srxbzyb@163.com
O456
A
1004-2237(2017)03-0090-06
10.3969/j.issn.1004-2237.2017.03.018
