浅谈电极反应式中的书写方法
2017-06-05湖北省襄阳市第九中学441000
湖北省襄阳市第九中学(441000)
王 琼●
浅谈电极反应式中的书写方法
湖北省襄阳市第九中学(441000)
王 琼●
电化学知识是历年高考化学试题中的必考知识点,在倡导“绿色环保”、“节能高效、科学和谐发展”的社会情景下,能源问题日益受到重视,作为能量转化的主要理论之一——电化学(原电池和电解池),无疑就成为高考命题的热点.,而其中电极反应方程式的知识已成为近几年能力测评的重要内容之一,那么,如何准确书写电化学的电极反应式呢?根据这些年的教学经验浅谈几点认识.
一、共存原则

例1 银制器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去.则该反应的负极反应方程式为____,反应的正极反应方程式为____,总反应方程式为____.
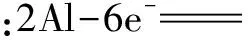
二、加减原则
两极反应式相加得到反应的总方程式.

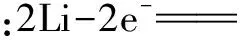
若能写出已知电池反应的总方程式,可以减去较易写出的电极反应式,从而得到较难写出的电极反应式.
例3 在乙醇燃料电池(电解质为KOH)中,通入正极物质的化学式为____;正极的电极反应式为____;乙醇在____极发生了____反应(还原或氧化);负极的电极反应式为:____.
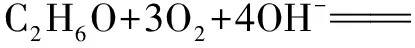
整理即得:
三、守恒原则
无论是原电池还是电解池两极反应都是氧化还原反应,先通过分析反应物和生成物及它们元素之间化合价的变化判断谁发生氧化反应谁发生还原反应,从而可判断出正负极或阴阳极及得失电子数.两极方程式都遵守原子守恒和电荷守恒,两极得失电子数目守恒,这样书写电极方程式就不会出现错误了.

解决此类题目,方法可能多种多样,但万变不离其宗,只需抓住以上本质,以不变应万变!
G632
B
1008-0333(2017)13-0089-01
