1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的合成
2017-06-01高志博
高 志 博
(南京三面体化工科技有限公司,江苏 南京,211100)
1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的合成
高 志 博
(南京三面体化工科技有限公司,江苏 南京,211100)
为减少最终产品的生产成本,改进和简化工艺条件,提高中间产物的收率,以邻叔丁基苯酚为原料,经一次加料氧化碘代,硫酸二甲酯甲基化,乌尔曼C-N偶联合成了1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮。讨论了原料配比对2-叔丁基-4,6-二碘苯酚、1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响,及反应温度对最终产品收率和性状的影响,并用1H-NMR确定了1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的结构。结果表明,得到的1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮总收率为60.15%,与已有文献报道的相比,基本相当,更易工业化。
化学合成;1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮;乌尔曼C-N偶联;邻叔丁基苯酚
1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮是一种精细化工及医药中间体,是合成Dasabuvir(达萨布韦)[1]及其衍生物,ABT-072[2]等药物的关键中间体。Dasabuvir(达萨布韦)及其衍生物和ABT-072是一类新型抑制丙型肝炎病毒非-核苷NS5B聚合酶抑制剂[1~7],具有广阔的临床应用前景,使得1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮成为有重要合成意义的有机中间体。
1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的合成报道较少,合成路线主要有2种,一种是先以邻叔丁基苯酚为原料经用稀硝酸硝化,ICl碘代,三甲基硅重氮甲烷甲基化,Fe粉氯化铵还原硝基,与(E)-3-甲氧基丙烯酰基异氰酸酯酰胺化,H2SO4催化成环合成1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮[2,7]。此法路线长,操作条件相对苛刻,总收率较低,产生较难处理的废酸和铁泥,有些反应试剂较复杂不易购得,不宜进行工业化生产。
另一种路线,也以邻叔丁基苯酚为原料,经分4次加料,并用Na2S2O3去除过量碘的氧化碘代,碱性碘甲烷甲基化,氩气条件下的乌尔曼C-N偶联合成1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮[2,7]。此法路线短,反应条件温和,总收率较高,所用试剂基本都简单易得,有进行工业化生产的可行性,但碘甲烷价格贵,沸点低易挥发而损失和造成操作环境恶化及空气污染。
基于2种路线的优缺点,为了使合成方法更靠近工业制法,本次研究采用第二种路线为基础的合成方法:以邻叔丁基苯酚为原料,以KI/NaClO为碘化剂组合一次性加料进行氧化碘代并用NaHSO3去除过量碘,选用价格低廉、活性高的硫酸二甲酯作为甲基化试剂,廉价氮气做保护气的乌尔曼C-N偶联,合成1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮(图1),探讨原料配比、反应温度等反应条件对反应收率的影响。

图1 1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮合成路线
1 实验部分
1.1 试剂与仪器
试剂:邻叔丁基苯酚,NaOH,KI,质量分数0.10的 NaClO溶液,浓盐酸,NaHSO3,甲醇,丙酮,石油醚,NaCl,无水K3PO4,CuI,N-(2-氰基苯基)吡啶酰胺,DMSO,一水合醋酸铜,NH4Cl,乙酸乙酯,以上试剂系南京化学试剂厂生产的分析纯级试剂。硫酸二甲酯为蒸馏回收试剂,纯度96%。
仪器:DF-101S型集热式恒温加热磁力搅拌器(南京文科仪器科技有限公司生产),JJ-1型电动搅拌器(南京文科仪器科技有限公司生产),SHB-3型循环水真空泵(南京文科仪器科技有限公司生产),DZF-6020型真空烘箱(上海精宏实验设备有限公司生产),RE52-99型旋转蒸发器(上海亚荣生化仪器厂生产),Varian300型核磁分析仪(美国Varian公司生产)。
1.2 合成
1.2.1 2-叔丁基-4,6-二碘苯酚的合成 将48 g邻叔丁基苯酚溶解在400 mL甲醇中,用冰/盐浴冷却反应体系。在低温下搅拌加入固体NaOH,当全部溶解转化成相应的酚盐后,加入KI。当体系温度降至0 ℃以下,开始滴质量分数为0.10的NaClO溶液,保持反应体系温度升至不高于1 ℃。反应溶液颜色从浅黄绿色颜色变为淡冰茶颜色。滴加完NaClO溶液后,滴加15.5 mL质量分数为0.167的NaHSO3溶液,尽量20 min内滴完,保持体系温度不超过2 ℃。滴加约85 mL浓盐酸将反应混合物的pH调节到3,保持体系温度不超过3 ℃。过滤得到的浆液,用水洗涤湿滤饼至中性。尽可能抽干滤饼,在真空烘箱50 ℃下干燥8 h,得到粉褐色固体。

2 结果与讨论
2.1 2-叔丁基-4,6-二碘苯酚合成的讨论
2.1.1 加料方式对2-叔丁基-4,6-二碘苯酚收率的影响 在文献[2,7]中,NaI和NaClO溶液分次添加,操作较为繁琐。本次研究在n(KI)∶n(NaClO)∶n(邻叔丁基酚)为3∶2.1∶1的条件下,分别采用分次加料和一次加料的方式进行反应。结果表明,两种加料方式得到的实验结果相差不大(表1),为了简便操作,以后的试验均采用一次加料的方式进行。

表1 加料方式对2-叔丁基-4,6-二碘苯酚收率的影响
2.1.2 KI的用量对2-叔丁基-4,6-二碘苯酚收率的影响 碘代反应一般认为按亲电取代机理进行,碘化剂的实质是NaClO氧化生成I2异裂产生的碘正离子进攻苯环。本反应NaClO溶液为滴加,KI始终过量,过量KI溶于水后电离出的碘负离子可与生成的碘形成三碘负离子,促进反应的进行。异裂产生的碘负离子,又被NaClO再次氧化成碘,这样可使碘循环利用。本反应的KI,NaClO,邻叔丁基酚理论摩尔比为2∶2∶1,而在文献[2,7]中,NaI用量是邻叔丁基苯酚的3倍,相对理论量过量过多,造成原料浪费和成本增加。考虑到NaClO易分解的理化性质,应适当过量。本次研究采用n(NaClO)∶n(邻叔丁基酚)为2.1∶1的实验条件,在原文献报道的基础上减少KI用量,并采用一次加料方式寻找适宜的KI用量。结果表明,随着KI用量的减少,2-叔丁基-4,6-二碘苯酚的收率没有发生明显的变化(表2)。综合考虑收率和制备成本,KI用量为邻叔丁基苯酚摩尔量的2.1倍较为适宜,收率为95.2%,较文献[2,7]中的93%有所提高。
2.2 1-叔丁基-3,5-二碘-2-甲氧基苯合成的讨论
2.2.1 硫酸二甲酯的用量对1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响 本次研究只考虑利用硫酸二甲酯上的一个甲基,本反应2-叔丁基-4,6-二碘苯酚与硫酸二甲酯理论上的摩尔比为1∶1,根据硫酸二甲酯的理化性质,其在50 ℃以上或者碱水中易迅速分解成硫酸和甲醇,考虑到硫酸二甲酯在反应过程中的损失,硫酸二甲酯应适当过量。本次研究在n(NaOH)∶n(2-叔丁基-4,6-二碘苯酚)为1.5∶1的条件下,室温反应5 h,考察硫酸二甲酯的用量对1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响。结果表明,当n(硫酸二甲酯)∶n(2-叔丁基-4,6-二碘苯酚)小于1.2∶1时,由于硫酸二甲酯的缓慢分解,使得原料2-叔丁基-4,6-二碘苯酚的转化率不高,收率偏低(表3)。当n(硫酸二甲酯)∶n(2-叔丁基-4,6-二碘苯酚)为1.2∶1时,1-叔丁基-3,5-二碘-2-甲氧基苯的收率达到最高水平,继续增加硫酸二甲酯的用量,1-叔丁基-3,5-二碘-2-甲氧基苯收率呈现小程度下降的趋势,原因是:在反应过程中硫酸二甲酯的用量增加,缓慢分解中产生的硫酸呈酸性,它会中和过量的NaOH,改变了体系的碱性环境,故1-叔丁基-3,5-二碘-2-甲氧基苯收率会呈现小程度下降的现象。由实验结果确定较好硫酸二甲酯用量是2-叔丁基-4,6-二碘苯酚摩尔量的1.2倍。

表2 KI用量对2-叔丁基-4,6-二碘苯酚收率的影响

表3 硫酸二甲酯用量对1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响
2.2.2 NaOH的用量对1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响 因甲基化的反应体系要求为碱性,NaOH用量要稍多于硫酸二甲酯。利用上一步得到较好的n(硫酸二甲酯)∶n(2-叔丁基-4,6-二碘苯酚)为1.2∶1,室温反应5 h的条件下,考察氢氧化钾用量对反应的影响。实验结果表明,在相同的实验条件下,随着碱试剂NaOH与2-叔丁基-4,6-二碘苯酚摩尔比的增加,1-叔丁基-3,5-二碘-2-甲氧基苯的收率先上升后变化不大(表4)。造成这种现象的原因,从反应过程中推测,因为碱试剂在本反应中的作用,一是与2-叔丁基-4,6-二碘苯酚作用形成酚钠,二是保证体系的偏碱性环境,以保证甲基化反应高效的进行。所以当NaOH用量较少时,其被反应过程中不断生产的偏酸性物质消耗,无法保证反应体系的碱性环境,1-叔丁基-3,5-二碘-2-甲氧基苯的收率较低;当NaOH用量过多时,体系pH值过高,此时酚钠更容易形成,同时硫酸二甲酯分解速度加快,并达到平衡,使1-叔丁基-3,5-二碘-2-甲氧基苯收率变化不大,由实验结果确定较佳的n(NaOH)∶n(2-叔丁基-4,6-二碘苯酚)为1.4∶1,1-叔丁基-3,5-二碘-2-甲氧基苯收率为99.5%,稍好于碘甲烷甲基化方法(99%)[2,7]。
2.3 反应温度对1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮收率和产品性状的影响
乌尔曼C-N偶联常用的反应温度是80~110 ℃,反应时应保持体系无水无氧。本次研究选用CuI作催化剂,N-(2-氰基苯基)吡啶酰胺作配体,K3PO4作为与CuI相匹配的碱[8],在n(尿嘧啶)∶n(K3PO4)∶n(CuI)∶n[N-(2-氰基苯基)吡啶酰胺]∶n(1-叔丁基-3,5-二碘-2-甲氧基苯)为1.2∶2.1∶0.1∶0.12∶1,通入N2惰化1 h后,加入CuI,反应体系加热到一定温度,保持24 h的反应条件,考察反应温度对1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4 (1H,3H)-二酮收率和产品性状的影响。结果表明,适当升高体系反应温度,可以提高1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的收率(表5)。当温度超过80 ℃时,体系的副反应增加,1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4 (1H,3H)-二酮收率变低,同时反应体系的颜色由墨绿色逐渐变成深棕色,产品颜色也逐渐变深,甚至状态发生了改变,由粉末状固体变成粘性固体。由实验结果确定较佳的反应温度是80 ℃,1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的收率为63.5%,与文献[2,7]中报道的收率(61%~70%)相当。

表4 NaOH用量对1-叔丁基-3,5-二碘-2-甲氧基苯收率的影响
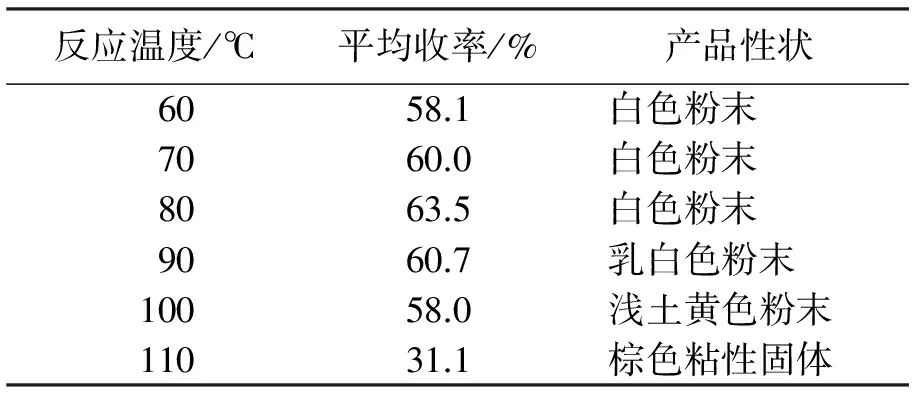
表5 反应温度对1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮收率及产品性状的影响
3 结 论
通过多次实验得到了1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮产品合成的较好实验条件。
氧化碘代:n(KI)∶n(NaClO)∶n(邻叔丁基酚)为2.1∶2.1∶1,2-叔丁基-4,6-二碘苯酚收率为95.2%。采用一次性KI/NaClO碘化剂组合加料方式,简化了原有的加料操作,减少了价格较贵原料KI的用量,降低了原料成本,反应收率较已有文献报道的收率有所提高。用NaHSO3做还原剂除过量的碘,避免过量的Na2S2O3在酸性条件下产生固体硫磺杂质。
甲基化:n(NaOH)∶n(硫酸二甲酯)∶n(2-叔丁基-4,6-二碘苯酚)为1.4∶1.2∶1,室温反应5 h,1-叔丁基-3,5-二碘-2-甲氧基收率为99.5%。用价格廉价且低挥发的硫酸二甲酯做甲基化试剂代替碘甲烷,改善操作环境,室温条件下反应节省能源,收率较文献收率稍有提高。
乌尔曼C-N偶联:n(K3PO4)∶n(CuI)∶n[N-(2-氰基苯基)吡啶酰胺]∶n(1-叔丁基-3,5-二碘-2-甲氧基苯)为1.2∶2.1∶0.1∶0.12∶1,通入N2惰化1 h后。加入CuI,反应体系加热到80 ℃,保持24 h,1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的收率为63.5%,总收率为60.15%。通过1H-NMR谱图可以确定出产品1-(3-叔丁基-5-碘-4-甲氧基苯基)嘧啶-2,4(1H,3H)-二酮的结构。产品收率与已有文献报道的相当。此步反应底物尿嘧啶反应活性较低,以致反应收率较低,以后仍需寻找更优的反应条件,以进一步提高产品的收率。
该工艺具有反应过程简单、操作方便、原料成本低、能耗少,产品收率高,更易于工业化的特点。
[1] Reviriego C.Dasabuvir:RNA-directed RNA polymerase (NS5B) inhibitor Treatment of hepatitis C virus infection[J].Drugs of the Future,2014,39(1):7-13.
[2] Califano C J,Napier J J,Becker L C,et al.Process for preparing antiviral compounds:US9216952B2[P].2015-12-22.
[3] Poordad F,Lawitz E,DeJesus E,et al.ABT-072 or ABT-333 combined with pegylated interferon/ribavirin after 3-day monotherapy in HCV genotype 1 (GT1)-infected treatment-naive subjects: 12-week sustained virologic response (SVR12) and safety results[J].Journal of Hepatology,2012,56(Suppl 2):S478.
[4] Krueger A C,Randolph J T,DeGoey D A,et al.Aryl uracil inhibitors of hepatitis C virus NS5B polymerase: Synthesis and characterization of analogs with a fused 5,6-bicyclic ring motif[J].Bioorganic & Medicinal Chemistry Letters,2013,23:3 487-3 490.
[5] Stedman C A.Current prospects for interferon-free treatment of hepatitis C in 2012[J].Journal of Gastroenterology and Hepatology,2013,28(1):38-45.
[6] Dennis J,Leonard J,Levien L T,et al.Ombitasvir/Paritaprevir/Ritonavir and Dasabuvir[J].Hosp Pharm,2015,50(5):396-412.
[7] Wagner R,Tufano M D,Stewart K D,et al.Uracil or thymine derivative for treating hepatitis C:CN101801935,CN102746239,EP2222646,JP2010539186,US2012213733,WO2009039127[P].2010-08-11.
[8] Strieter E R,Blackmond D G,Buchwald S L.The role of chelating diamine ligands in the goldberg reaction: A kinetic study on the copper-catalyzed amidation of aryl iodides[J].Journal of the American Chemical Society,2005,127(12):4 120-4 121.
(责任编辑:朱宝昌)
Preparation and Synthesis of 1-(3-tert-butyl-5-iodo-4-methoxyphenyl)pyrinidine-2,4(1H,3H)-dione
GAO Zhibo
(Nanjing Trihedron Chemical Technology Co., Ltd., Nanjing Jiangsu, 211100, China)
The objective of this paper was to reduce the production cost of the final product, simplify the process conditions and improve the yield of intermediate product. Taking 2-tert-butyl phenol as the raw materials, 1-(3-tert-Butyl-5-iodo-4-methoxyphenyl)pyrinidine-2,4(1H,3H)-dione was synthesized via one-time charging oxidation iodination, methylation by dimethyl sulfate and ullman C-N coupling. The ratio of the raw materials on the impact of 2-tert-butyl-4,6-diiodo-phenol and 1-tert-butyl-3,5-diiodo-2-methoxybenzene yields, and reaction temperature on the influence of finally product yield and properties were also discussed. The structure of 1-(3-tert-Butyl-5-iodo-4-methoxyphenyl)pyrinidine-2,4(1H,3H)-dione was determined by1H-NMR. The results showed that the total yield of 1-(3-tert-butyl-5-iodo-4-methoxyphenyl) pyrinidine-2,4(1H,3H)-dione might reach 60.15%, which was very near to the reference document and easy to industrialize for large scale.
chemical synthesis; 1-(3-tert-butyl-5-iodo-4-methoxyphenyl)pyrinidine-2,4(1H,3H)-dione; Ullman C-N coupling; 2-tert-butyl phenol
10.3969/J.ISSN.1672-7983.2017.01.008
2017-02-23
O625
A
1672-7983(2017)01-0039-05
高志博(1983-),男,中级工程师,硕士。主要研究方向:精细化学品的合成。
