不同取代的2'-羟基查尔酮类化合物的抑菌活性测定与分析
2017-06-01武圆圆张建平赵永光
赵 莹,武圆圆,张建平,赵永光
(河北科技师范学院化学工程学院,河北 秦皇岛,066600)
不同取代的2'-羟基查尔酮类化合物的抑菌活性测定与分析
赵 莹,武圆圆,张建平,赵永光
(河北科技师范学院化学工程学院,河北 秦皇岛,066600)
为确定查尔酮类化合物的抑菌活性,合成了5种2′-羟基查尔酮类化合物,分别为N,N-二甲氨基-2′-羟基查尔酮,4-甲氧基-2′-羟基查尔酮,3-羟基-2′-羟基查尔酮,4-氯-2′-羟基查尔酮和2-氯-2′-羟基查尔酮。采用滤纸片扩散法测定分析了这些查尔酮类化合物对大肠杆菌和金黄色葡萄球菌的体外抑菌效果,同时考察了培养基和药液不同配比条件下的抑菌活性。结果表明,N,N-二甲氨基-2′-羟基查尔酮和4-甲氧基-2′-羟基查尔酮对大肠杆菌均有较好的抑菌性能,当药液浓度分别为12.50 mg·L-1和6.25 mg·L-1时抑菌环直径分别为21.26 mm和18.24 mm,分别比对照2′-羟基查尔酮的抑菌环直径提高了48.1%和61.4%;而3-羟基-2′-羟基查尔酮的抑菌性能次之,4-氯-2′-羟基查尔酮和2-氯-2′-羟基查尔酮的抑菌性能较差。而对金黄色葡萄球菌的抑菌效果以N,N-二甲氨基-2′-羟基查尔酮为最好,当药液浓度为25.00 mg·L-1时抑菌环直径为29.40 mm,比对照2′-羟基查尔酮的抑菌环直径提高了57.9%,其它4种查尔酮抑菌效果较差。查尔酮A环不同位置连有不同基团时抑菌活性有着明显的差异,4-N,N-二甲氨基-2′-羟基查尔酮对大肠杆菌和金黄色葡萄球菌抑菌性能均最强。
2′-羟基查尔酮;抑菌活性;大肠杆菌;金黄色葡萄球菌
查尔酮学名为二苯基丙烯酮,是广泛存在于自然界的一种类黄酮化合物,可以从植物的不同部位中提取得到,是合成某些黄酮类化合物的重要中间体[1~5]。查尔酮具有较大的分子柔性,能与不同的受体相结合,因而具有广泛的生物活性,如抗菌、抗氧化、抗炎、抗病毒、抗肿瘤等[6~12]。正是由于查尔酮拥有如此多的生物活性,在食品、医学等很多行业已得到了广泛的应用,其发展前景广阔[13,14]。
2′-羟基查尔酮则是在查尔酮B环的邻位上有一羟基取代基,在2′-羟基查尔酮的A环上常会存在不同的基团,因存在的基团在某种程度上影响着2′-羟基查尔酮上的电子分布,所以不同取代的2′-羟基查尔酮的生物活性存在差异。笔者合成了5种2′-羟基查尔酮类化合物,采用滤纸片扩散法测定分析了对大肠杆菌和金黄色葡萄球菌的体外抑菌效果,同时考察了培养基和药液不同配比条件下的抑菌活性。为其在更多行业得到更加广泛的应用提供一定的理论基础。
1 材料与方法
1.1 仪器和试剂
JA2003N型分析天平(上海良平仪器仪表有限公司生产),XT22CM型高压蒸汽灭菌锅(沈阳市铝制品厂生产),250B智能生化培养箱(江苏省金坛市医疗仪器厂生产),IS09001游标卡尺(哈尔滨量具刃具集团有限责任公司生产)。
2-羟基苯乙酮、苯甲醛、2-氯苯甲醛、4-氯苯甲醛、3-羟基苯甲醛、4-甲氧基苯甲醛、N,N-二甲氨基苯甲醛(阿拉丁试剂有限公司生产)。
供试菌:大肠杆菌和金黄色葡萄球菌(引自河北科技师范学院微生物实验室)。
NB培养基:牛肉膏5.0 g,蛋白胨10.0 g,NaCl 5.0 g,琼脂20.0 g,蒸馏水1 000 mL,pH 7.0~7.2。
1.2 方法
1.2.1 2′-羟基查尔酮的合成 参照文献[15]方法合成2-氯-2′-羟基查尔酮,4-氯-2′-羟基查尔酮,3-羟基-2′-羟基查尔酮,4-甲氧基-2′-羟基查尔酮和4-N,N-二甲氨基-2′-羟基查尔酮,同时合成了2′-羟基查尔酮为对照(图1)。
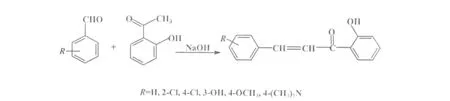
图1 不同取代的2′-羟基查尔酮的合成
1.2.2 2′-羟基查尔酮的抗菌活性测定方法 采用斜面接种技术制备菌种,将接好菌种的斜面培养基在37 ℃培养箱中培养24~36 h,而后放入4℃冰箱保存备用。细菌接到NB培养基上,37 ℃培养24 h。
采用二倍稀释法[16~18]将合成的不同取代的2′-羟基查尔酮用体积分数为0.95的乙醇稀释成5个质量浓度梯度,分别为100.00,50.00,25.00,12.50,6.25 mg·L-1。
用5 mL不同质量浓度的2′-羟基查尔酮溶液分别浸泡直径为6 mm的药敏纸片12 h,用体积分数为0.95的乙醇溶液进行对照试验。取出后真空干燥,高压蒸汽灭菌后,在-20 ℃的冰箱中保存。
用接种环分别取大肠杆菌和金黄色葡萄球菌1~2环,接入装有无菌水的灭菌试管中,充分混匀,制成菌悬液。
采用滤纸片扩散法测定抗菌活性。无菌操作倒入已融化的培养基15~20 mL,摇匀,使其凝固成平板;滴入0.2 mL的菌悬液,将药敏纸片平铺于已涂布菌液的平板上,37 ℃下培养24~36 h;双重实验,用游标卡尺测量抑菌圈直径。
1.2.3 培养基和药液不同配比条件下的抑菌活性测定 按照V(NB培养基)∶V(查尔酮药液)分别为10∶1,7∶1,5∶1,4∶1,3∶1,2∶1,1∶1进行配比,观察细菌生长从有到无的过程,从而确定培养基和原药液的适合配比为4∶1和3∶1。进一步将V(NB培养基)∶V(查尔酮药液)=4∶1的药液稀释浓度依次为20.00,10.00,5.00,2.50,1.25,0 mg·L-1,而将V((NB培养基)∶V((查尔酮药液)=3∶1的药液稀释浓度依次为25.00,12.50,6.25,3.12,1.56,0 mg·L-1。
在上述12种不同质量浓度查尔酮药液的培养基中分别接入0.1 mL大肠杆菌和金黄色葡萄球菌的菌悬液,观察细菌生长情况,记录不长菌时的最低抑菌质量浓度。
2 结果与分析
2.1 不同取代的2′-羟基查尔酮的抑菌活性
不同取代的2′-羟基查尔酮药液对大肠杆菌和金黄色葡萄球菌均有一定的抑菌活性,且随着药液浓度的升高,抑菌活性呈现增强的趋势;但不同的查尔酮药液的抑菌能力差异明显(表1,表2)。
4-N,N-二甲氨基-2′-羟基查尔酮在所试的各个质量浓度下对大肠杆菌和金黄色葡萄球菌都表现出极大的抑菌作用,显著高于对照。当药液质量浓度为12.50 mg·L-1时对大肠杆菌的抑菌环直径达到21.26 mm,比对照2′-羟基查尔酮的抑菌环直径提高幅度高达48.1%;同样地,当药液质量浓度为25.00 mg·L-1时对金黄色葡萄球菌的抑菌环直径达到29.40 mm,比对照2′-羟基查尔酮的抑菌环直径提高幅度更是高达57.9%。
4-甲氧基-2′-羟基查尔酮药液各质量浓度下对大肠杆菌均表现抑菌且显著高于对照,当质量浓度为6.25 mg·L-1时抑菌环直径已达到18.24 mm,较对照提高了61.4%。但4-甲氧基-2′-羟基查尔酮药液对金黄色葡萄球菌的抑菌作用没有表现出明显的规律,或高或低质量浓度均没有抑菌能力,只有在药液质量浓度为25.00,12.50 mg·L-1时才表现出一定的抑菌活性。
然而,2-氯-2′-羟基查尔酮药液对大肠杆菌和金黄色葡萄球菌抑菌活性均较差,在所有质量浓度下抑菌环直径均显著低于对照的抑菌环直径。特别是药液质量浓度为12.50 mg·L-1时对大肠杆菌的抑菌环直径只有7.35 mm,比对照降低了48.8%;而药液质量浓度为25.00 mg·L-1时对金黄色葡萄球菌的抑菌环直径也只有12.56 mm,比对照降低了32.5%。
此外,4-氯-2′-羟基查尔酮和3-羟基-2′-羟基查尔酮药液对大肠杆菌和金黄色葡萄球菌的抑菌作用没有一定的规律,但整体而言抑菌能力较差。

表1 不同质量浓度的查尔酮溶液对大肠杆菌的抑菌环大小比较 mm
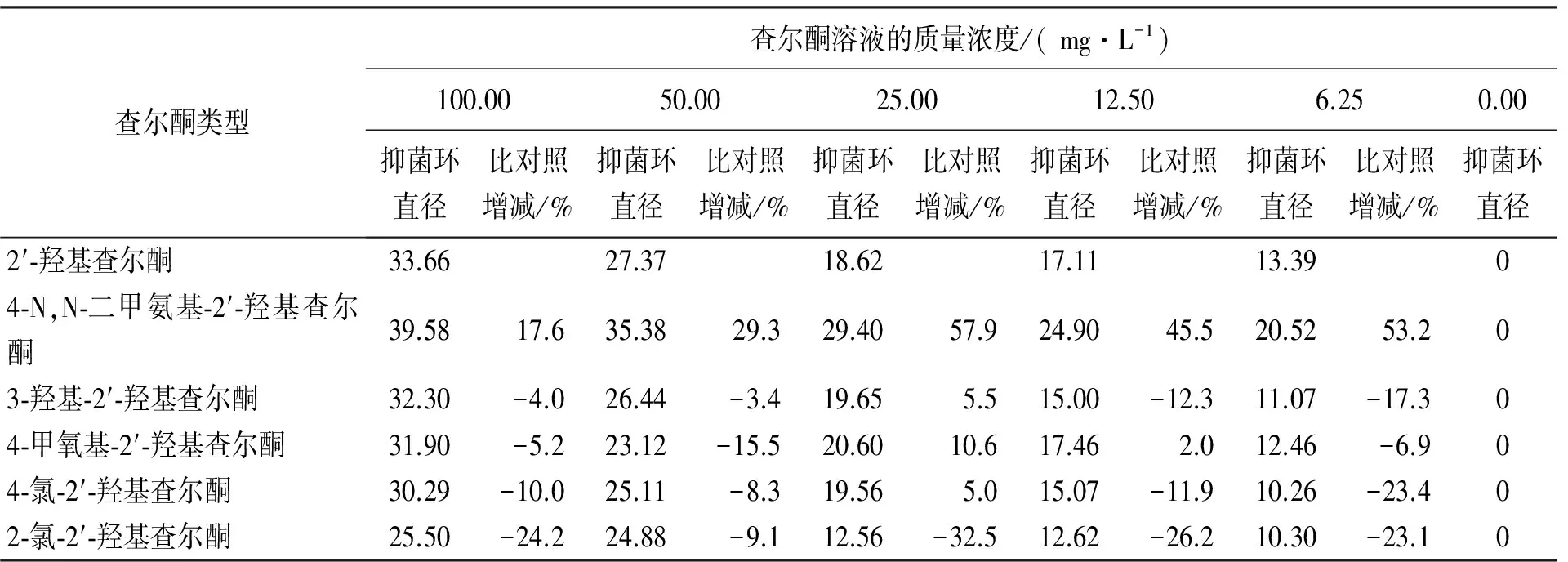
表2 不同质量浓度的查尔酮溶液对金黄色葡萄球菌的抑菌环大小比较 mm
2.2 不同取代的2′-羟基查尔酮结构与抑菌活性关系分析
不同取代2′-羟基查尔酮,不管是连有甲氨基还是甲氧基基团的化合物均对大肠杆菌和金黄色葡萄球菌有着抑制作用,但抑菌性能有一定的差异(表3)。
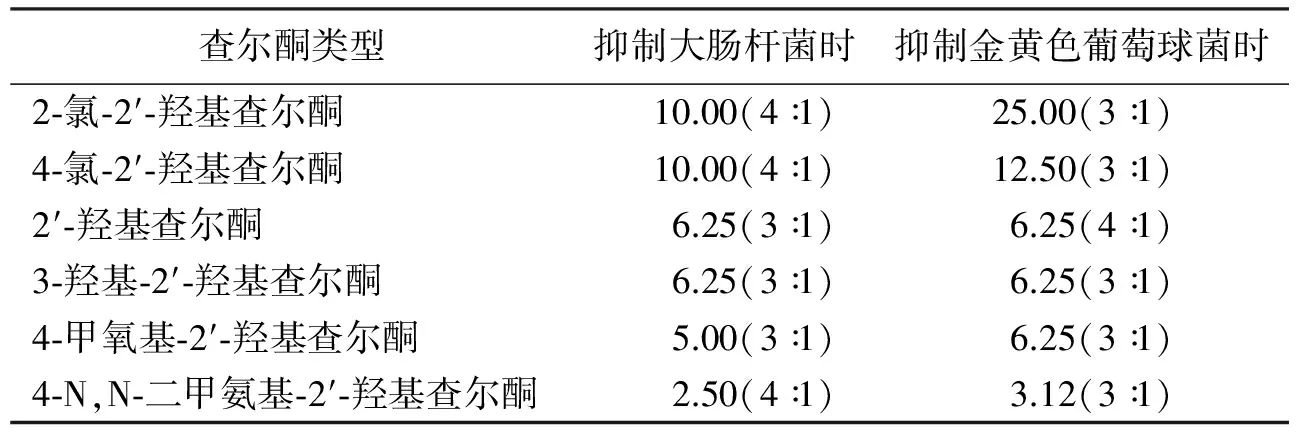
表3 不同取代的2′-羟基查尔酮的最低抑菌质量浓度及V(NB培养基)∶V(查尔酮药液) mg·L-1
当V(NB培养基)∶V(查尔酮溶液)=4∶1时,4-N,N-二甲氨基-2′-羟基查尔酮对大肠杆菌的最低抑菌浓度只需要2.50 mg·L-1;同样地,当V(NB培养基)∶V(查尔酮溶液)=3∶1时,对金黄色葡萄球菌的最低抑菌浓度也只需要3.12 mg·L-1。
在V(NB培养基)∶V(查尔酮溶液)为3∶1或4∶1条件下,对大肠杆菌和金黄色葡萄球菌的最低抑菌质量浓度从小到大顺序依次为:4-N,N-二甲氨基-2′-羟基查尔酮,4-甲氧基-2′-羟基查尔酮,3-羟基-2′-羟基查尔酮,4-氯-2′-羟基查尔酮,2-氯-2′-羟基查尔酮。这也是不同取代的2′-羟基查尔酮类化合物抑菌活性从大到小的顺序。
由此可见,与2′-羟基查尔酮相比,当查尔酮的A环连有—N(CH3)2或者—OCH3时,抑菌活性增强。其中对位取代基对其抑菌活性影响更大,4-N,N-二甲氨基-2′-羟基查尔酮对大肠杆菌和金黄色葡萄球菌抑菌能力最强。而当查尔酮的A环连有卤原子或者—OH时,抑菌活性减弱,但不同位置的取代对其抗菌活性影响不大。
3 结论与讨论
羟基查尔酮的抗菌活性受到了广泛的关注,但其较低的水溶性和中等的抗菌效价使它的应用受到了限制。
本次研究以邻羟基苯乙酮和不同取代的苯甲醛为原料合成了5种2′-羟基查尔酮类化合物,研究了2′-羟基查尔酮对大肠杆菌和金黄色葡萄球菌的抑菌活性。不同类型的2′-羟基查尔酮药液对同一细菌的抑菌性不同;同一药液对不同细菌的抑菌性也不相同。不管是连有卤素、羟基还有甲氧基基团的化合物均对大肠杆菌和金黄色葡萄球菌有着抑制作用,但抑菌性能有一定的差异。查尔酮的A环连有—OCH3或—(CH3)2N时,抑菌活性增强,其中对位取代基对其抑菌活性影响最明显,而卤原子使得查尔酮的抑菌活性变弱。N,N-二甲氨基-2′-羟基查尔酮和4-甲氧基-2′-羟基查尔酮对大肠杆菌有较好的抑菌性能,药液质量浓度为100.00 mg·L-1时抑菌环直径分别为37.08 mm和36.54 mm;而N,N-二甲氨基-2′-羟基查尔酮对金黄色葡萄球菌的抑菌性较好,当药液质量浓度为100.00 mg·L-1时抑菌环直径为39.58 mm。
查尔酮类化合物化学结构简单,合成也比较容易,以此为先导化合物对其结构进行优化和改造,研究其结构和活性之间的关系,有望研究开发出高效、低毒安全的新型抑菌剂。
[1] 陈欣华,王曼曼,宁鸿珍,等.明日叶中查尔酮三种提取方法的比较研究[J].食品工业,2014,35(6):91-94.
[2] 宁鸿珍,陈欣华,王曼曼,等.超声波辅助提取明日叶查尔酮的工艺优化[J].食品研究与开发,2014,35(8):34-37.
[3] 丁存宝,刘海燕,李桂秋,等.月季果黄酮的提取及抑菌作用研究[J].食品工业,2012(1):107-110.
[4] 西力扎提·阿不来提,杨旭超,木合布力·阿不力孜,等.胀果甘草全草中甘草查尔酮A的鉴定研究[J].安徽农业科学,2015,43(26):64-66.
[5] 胡栋宝,周文兵,张福鹏,等.昆仑雪菊中2个查尔酮化合物抗氧化活性构效关系[J].安徽农业科学,2017,45(1):94-96.
[6] 方线文,周丽珍,成昭,等.含氮芥基查尔酮类衍生物的合成、晶体结构及抗肿瘤活性[J].有机化学,2013,33(3):523-529.
[7] 李湘洲,郭远良,旷春桃,等.查尔酮的结构修饰及抗癌、抗炎活性研究进展[J].中南林业科技大学学报,2011,31(2):95-99.
[8] Dimmock J R,Elias D W,Beazely M A,et al.Bioactivities of chalcones[J]. Current Medicinal Chemistry,1999,6(12):1 125-1 149.
[9] Yu L,Zhang F,Hu Z,et al.Novel prenylated bichalcone and chalcone fromHumuluslupulusand their quinone reductase induction activities[J].Fitoterapia,2014,93(4):115-120.
[10] 旷春桃,李湘洲,郭远良,等,查尔酮衍生物的合成及其抗菌和抗氧化活性研究[J].中国科技论文,2013,8(9):862-864.
[11] 姜成,申晓慧,李春丰,等.仙人掌提取物抑菌作用的研究[J].内蒙古农业科技,2013(3):38-39.
[12] 尹璐,胡仁火,丘日光,等.7种中草药醇提取物抑菌杀菌作用的研究[J].安徽农业科学,2014,42(28):9 722-9 724.
[13] 孙朝霞,侯思宇,郭彬,等.苦荞查尔酮合成酶基因序列特征及分子进化分析[J].分子植物育种,2014,12(4):772-779.
[14] 冉芳,王爱华,袁萱,等.甘草查尔酮B诱导小鼠黑色素瘤细胞凋亡作用[J].中国实验方剂学杂志,2013,19(9):220-224.
[15] 齐秀霖,杨航,陈炳阳,等.2′-羟基查尔酮的合成工艺研究[J].第二军医大学学报,2010,31(5):572-573.
[16] 刘晓军,刘铀,陈绍红,等.构树叶提取物抑菌活性的初步观察[J].中国实验方剂学杂志,2013,19(19):283-286.
[17] 柳慧贞,高前欣,阙松宇,等.黄条金刚竹叶提取物抑菌活性研究[J].安徽农业科学,2013,41(4):1 730-1 731, 1 733.
[18] 田珈源,罗青春,梁华忠,等.查尔酮类似化合物的合成及其抑菌活性研究[J].安徽农业科学,2011,39(27):16 551-16 553,16 556.
[19] Lopez S N,Castelli M V,Zacchino S A,et al.In vitra antifungal evaluation and structure-activity relationships of a new series of chalcone derivatives and synthetic analogues, with inhibitory properties against polymers of the fungal cell wall[J].Bioorgnic & Medicinal Chemistry,2001,9(8):1 999-2 013.
(责任编辑:朱宝昌,陈于和)
Evaluation of Antibacterial Activities of Different Substituted 2′-hydroxy Chalcone Compounds
ZHAO Ying, WU Yuanyuan, ZHANG Jianping, ZHAO Yongguang
(College of Chemistry Engineering, Hebei Normal University of Science & Technology,Qinhuangdao Hebei, 066600, China)
In order to determine the antibacterial activities of chalcones, five 2′-hydroxychalcones-based compounds were synthesized, including N,N-dimethylamino-2′-hydroxychalcone, 4-methoxy-2′-hydroxychalcone, 3-hydroxy-2′-hydroxychalcone, 4-chloride-2′-hydroxychalcone and 2-chloro-2′-hydroxychalcone. Antibacterial effects of those compounds onEscherichiacoliandStaphylococcusaureuswere mainly studied using the filter paper diffusion method. Meanwhile, the antibacterial activities were also discussed with different ratios of the culture medium and medicine liquids. The results showed that the N,N-dimethylamino-2′-hydroxychalcone and 4-methoxy-2′-hydroxychalcone had good antibacterial properties onEscherichiacoli. When the solution concentration were 12.50 mg·L-1and 6.25 mg·L-1, the antibacterial zone diameters reached 21.26 mm and 18.24 mm, respectively, which increased 48.1% and 61.4% over that of 2′-hydroxychalcone, the check. 3-hydroxy-2′-hydroxychalcone, 4-chloro-2′-hydroxychalcone and 2-chloro-2′-hydroxychalcone were a little worse. Futhermore, The antibacterial effect of N, N- dimethylamino -2′-hydroxychalcone onStaphylococcusaureuswas the strongest among these compounds. When the solution concentration was 25.00 mg·L-1, the antibacterial zone diameter was as large as 29.40 mm, which incresed 57.9% over that of the check. However, the other four chalcones expressed low antibacterial activities. There were significant differences in the antibacterial activity of chalcones with different groups of A rings in different positions, and 4-N,N-dimethylamino-2′-hydroxychalcone had the strongest antibacterial activities on bothEscherichiacoliandStaphylococcusaureus.
2′-hydroxy chalcone; antibacterial activity;Escherichiacoli;Staphylococcusaureus
10.3969/J.ISSN.1672-7983.2017.01.012
河北省高等学校科学技术研究青年基金项目(项目编号:QN20131095)部分内容。
2016-12-30
R914.5
A
1672-7983(2017)01-0059-05
赵莹(1979-),女,硕士,讲师。主要研究方向:有机合成。
