心肌致密化不全合并弥漫性冠状动脉右室瘘1例
2017-05-16张志芳陈轶维傅立军张玉奇
戴 柯 张志芳 陈轶维 李 奋 傅立军 张玉奇
·论著·
心肌致密化不全合并弥漫性冠状动脉右室瘘1例
戴 柯 张志芳 陈轶维 李 奋 傅立军 张玉奇
目的 探讨心肌致密化不全合并弥漫性冠状动脉瘘的临床特点及诊断方法。方法 报告1例心肌致密化不全合并弥漫性冠状动脉右室瘘患儿,回顾其临床症状、辅助检查结果和治疗方案。在国外数据库(Pubmed、OVID和Elsevier)和国内数据库(万方和维普)中检索心肌致密化不全合并冠状动脉瘘和心肌病合并冠状动脉瘘病例的文献,检索时间为建库至2017年3月30日。总结此类病例的临床表现、诊断和治疗。结果 本文患儿为6月龄女婴,因“胃纳差伴盗汗2周”于2013年10月12日在上海交通大学医学院附属上海儿童医学中心心内科就诊。二维超声心动图显示,左心室增大伴左室致密化不全、左右冠状动脉扩张、右心室内心肌窦状间隙持续状态、二尖瓣中度返流、心室收缩功能低下等。心导管造影及冠状动脉造影检查显示,右冠状动脉及左前降支弥漫性微小右心室瘘、二尖瓣返流、左心室增大。予地高辛、速尿、安体舒通后患儿症状稍好转。国外数据库中检索到2例心肌致密化不全合并冠状动脉左室瘘的成年病例,以进行性呼吸困难和心前区疼痛为主要临床表现,心肌缺血表现更明显,诊断主要依靠二维超声心动图及心导管造影和冠状动脉造影检查,缺乏有效治疗手段;有部分心肌病合并心肌致密化不全患者接受选择性冠状动脉瘘介入封堵术的尝试。结论 心肌致密化不全合并冠状动脉瘘是一类罕见的先天性心脏发育异常疾病,婴儿临床症状主要为纳差、盗汗等心功能不全的表现,确诊主要依靠二维超声心动图以及心导管造影、冠脉造影检查,目前尚缺乏有效治疗手段,以强心、利尿、扩血管改善心功能治疗为主。
心肌致密化不全; 弥漫性冠状动脉右室瘘; 心肌病
1 病例资料
患儿女,6月龄,因“胃纳差伴盗汗2周”于2013年10月12日至上海交通大学医学院附属上海儿童医学中心(我院)住院接受治疗。
患儿出生后42 d体检时发现有心脏杂音,于当地医院进行二维超声心动图检查,提示卵圆孔未闭、心肌病变可能,未行处理。入我院前2周出现胃纳差,每日喂奶5~6次,每次奶量90~100 mL,偶有吃吃停停现象,平素汗多。病程中患儿精神一般,无气促、水肿,尿量正常。
患儿系G1P1,足月顺产,无窒息抢救史,出生体重3 600 g。父母均体健,否认近亲结婚,否认遗传性病史。家族成员无类似病史。
体格检查:患儿神志清,精神反应一般,能抬头、独坐;面容未见异常,营养发育一般;两肺呼吸音粗,未及干、湿啰音。心律齐,心率120·min-1,心音稍低,胸骨左缘3~4肋间可闻及2级收缩中晚期吹风样杂音。全腹软,肝肋下2.5 cm,剑突下未及,质地软,无压痛。脾肋下未及。神经系统检查未见异常。
实验室检查:肌酸激酶94 U·L-1,肌酸激酶同工酶21 U·L-1,快速肌钙蛋白T 202(正常值<50 )ng·L-1,N端B型利钠肽原15 375(正常值0~100)pg·mL-1。血常规、凝血酶原时间、活化部分凝血活酶时间、肝功能和肾功能检查均未见异常。
影像学检查:X线胸部正位片示,两肺纹理增多,心影增大。心电图示,左心室增大、ST-T段改变。超声心动图(图1)示,左心室增大伴左室致密化不全,左、右冠状动脉扩张,右心室内心肌窦状间隙持续状态,二尖瓣中度返流,心室收缩功能低下。心导管造影和冠状动脉造影(图2)示,右冠状动脉和左前降支弥漫性微小右心室瘘,二尖瓣返流,左心室增大。
根据患儿纳差、多汗的临床症状结合心脏彩超和血管造影结果,考虑诊断为心肌致密化不全、弥漫性冠状动脉右心室瘘和心功能不全。予每日公斤体重地高辛10 μg、速尿7.5 mg、安体舒通7.5 mg强心、利尿和改善心功能,磷酸肌酸营养心肌。1周后每日喂奶6~7次,每次进奶量130~150 mL,肝脏肋下1.5 cm,予以出院,嘱出院后继续口服地高辛、速尿和安体舒通等药物,门诊随访。出院后1个月和6个月时电话随访,患儿每日总奶量1 000~1 200 mL。出院后8个月时患儿因呼吸道感染和心功能不全在外院住院治疗,家属放弃治疗死亡。
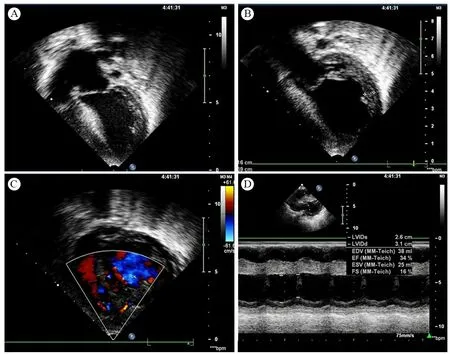
图1 患儿二维超声心动图
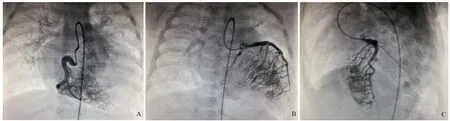
图2 患儿冠状动脉造影
2 讨论
1984年Engberding等[1]首次报道孤立的心肌致密化不全,1995年WHO和国际心脏病学联盟将本病定为未分类心肌病[2],2006年美国心脏学会将其划归为原发性遗传性心肌病的一种类型[3]。心肌致密化不全是由于胚胎发育过程中心肌致密化过程停止所致。正常情况下,胚胎发育第4~8周,疏松的肌小梁逐渐紧密压合,心室肌壁形成,窦状间隙演变成毛细血管网,成为冠状动脉循环的一部分。如果此过程发生异常,心肌保留在原始状态,即出现心肌致密化不全,可同时伴有窦状间隙开放,即临床所见冠状动脉心室瘘。目前的研究认为,心肌致密化不全有家族遗传可能,12%~47%的患者可有家族史[4]。Klassassen等[5]研究认为其发病可能与a-dystrobrevin、Cypber/ZASP、强直性肌营养不良蛋白激酶DMPK、抗肌萎缩蛋白、线粒体DNA和LMNA等基因突变有关。2013年,中华医学会儿科学分会心血管学组建议,对可疑心肌致密化不全家族遗传病例检测包括MYH7、ACTC、TPM1、MYBPC、TNNT2、FKBP-12和SCN5A在内的15种相关基因[6]。
本文患儿女,6月龄,因“胃纳差伴盗汗2周”入院,经二维超声心动图和冠状动脉造影确诊为心肌致密化不全合并多发弥漫性冠状动脉右心室瘘。检索国外Pubmed、OVID和Elsevier数据库,检索时间为建库至2017年3月30日,检索词为“cardiomyopathy and coronary artery fistula”,2篇文献明确报道了2例心肌致密化不全合并冠状动脉左室瘘的成人病例[7,8],1篇报道描述了1例肥厚性心肌病合并弥漫性冠状动脉右室瘘[9]。检索国内万方数据库及维普数据库,检索时间为建库至2017年3月30日,检索词为“心肌病或心肌致密化不全合并冠状动脉瘘”,未检索到相关文献。国外报道的2例心肌致密化不全合并冠状动脉左室瘘病例中,1例为67岁美国男性,因进行性呼吸困难伴心前区疼痛3个月就诊,二维超声心动图和血管造影检查示左心室致密化不全及弥漫性冠状动脉左室瘘。1例为46岁德国女性,因“呼吸困难”就诊,二维超声心动图证实心肌致密化不全,冠脉造影检查多发性左冠状动脉左室瘘[8]。1例肥厚性心肌病合并弥漫性冠状动脉右室瘘病例为6岁德国籍男孩,因“反复晕厥”入院,考虑存在严重心肌缺血及阿斯综合征,接受了选择性冠状动脉瘘封堵术,并植入了心律转复除颤器[9]。考虑到弥漫性冠脉瘘合并心肌致密化不全可因冠脉窃血及后续心肌病的原因导致心功能不全,在患者的长期预后中出现恶性心律失常的概率较大,因此植入心律转复除颤器也许是一个预防心律失常导致猝死的手段,但手术时机和针对婴幼儿的手术方法仍值得探索。
孤立性心肌致密化不全可有心功能不全、心律失常等多种临床表现。当心肌致密化不全合并冠状动脉瘘时,心肌缺血及心室肌病变所造成的心功能不全症状更为明显。瘘管分流使冠状动脉内血流减少,心室舒张期冠状动脉灌注压下降,造成冠脉窃血现象,影响心肌血供,最终导致心肌缺血、心肌收缩功能下降。此外,心肌致密化不全所引起的心室肌异常松弛和心室充盈受限,导致心肌舒张功能不全。心功能不全在小婴儿往往表现为喂奶烦躁不安、面色苍白、盗汗等。本文患儿出生后早期并无明显纳差、盗汗、喂养困难等表现,系因婴儿出生早期活动量小、氧耗低,心功能不全表现不明显。国外同类型成人病例发病时间明显晚于国内,可能与冠脉窃血量及患者自身耐受情况有关,患者具有的呼吸困难表现更像是冠心病的表现,可能与长期冠脉窃血导致心肌缺血、缺氧有关。
总结国外报道及本文共3例心肌致密化不全合并冠状动脉瘘的辅助检查结果,心电图可表现为心脏缺血,具体如ST段下移或者T波变化等;临床确诊主要依靠二维超声心动图及心导管造影检查(包括冠状动脉造影)。目前,二维超声心动图被认为是心肌致密化不全最简单易行的检查手段。Jenni等[10]总结并提出5条二维超声心动图诊断心肌致密化不全的标准:①心室腔内可见多发性粗大的肌小梁和深陷其中的隐窝所构成的网状结构;②非致密的心内膜层和致密的心外膜层之比儿童>1.4,成人>2;③彩色多普勒超声显示窦状间隙开放,并有低速血流与心腔相通;④受累心室腔增大,运动减弱,心肌收缩及舒张功能减低;⑤排除其他先天性或获得性心脏病。本文患儿及文献[7,8]报道的病例均符合上述诊断标准的前4条。冠状动脉瘘诊断主要依赖于冠状动脉造影,可明确冠状动脉走向、引流部位、瘘口大小、瘘口近心端冠状动脉分支的分布情况等。
心肌致密化不全合并冠状动脉瘘的的治疗,主要包括针对心功能不全的强心、利尿和扩血管治疗和针对冠状动脉瘘的手术或介入封堵治疗。文献[7,8]报道的2例均未提及治疗及患者转归。本文患儿年仅6月龄,且合并弥漫多发性冠状动脉右室瘘,不适合进行介入或手术治疗,故给予口服地高辛、利尿剂以改善心功能为主。患儿出院后临床症状稍改善,但缺乏影像学随访资料。
综上所述,心肌致密化不全合并弥漫性冠状动脉右室瘘是一类罕见的先天性心脏发育异常性疾病。婴儿临床症状主要表现为纳差、盗汗等心功能不全。临床确诊主要依靠二维超声心动图和心脏导管造影检查。目前尚缺乏有效的临床根治手段,主要以强心、利尿和扩血管等对症治疗为主。
[1]Engberding R, Bender F. Identification of a rare congenital anomaly of the myocardium by two-dimensional echocardiography: persistence of isolated myocardial sinusoids. Am J Cardiol, 1984, 53 (11): 1733-1734
[2]Richardson P, McKenna W, Bristow M, et al. Report of the 1995 World Health Organization/International Society and Federation of Cardiology Task Force on the Definition and Classification of cardiomyopathies. Circulation, 1996, 93(5): 841-842
[3]Maron BJ, Towbin JA, Thiene G, et al. Contemporary definitions and classification of the cardiomyopathies: an American Heart Association Scientific Statement from the Council on Clinical Cardiology, Heart Failure and Transplantation Committee; Quality of Care and Outcomes Research and Functional Genomics and Translational Biology Interdisciplinary Working Groups; and Council on Epidemiology and Prevention. Circulation, 2006, 113(14): 1807-1816
[4]杨思源,陈叔宝. 小儿心脏病学. 第4版. 北京:人民卫生出版社, 2012
[5]Klaassen S, Probst S, Oechslin E, et al. Mutations insarcomere protein genes in left ventricular noncompaction. Circulation, 2008, 117(22): 2893-2901
[6]中华医学会儿科学分会心血管学组,中华儿科杂志编辑委员会. 儿童心肌病基因检测建议. 中华儿科杂志,2013, 51(8):595-597
[7]Dias V, Cabral S, Vieira M, et al. Noncompaction cardiomyopathy and multiple coronary arterioventricular fistulae: 1 or 2 distinct disease entities? J Am Coll Cardiol, 2011, 57(25): e377
[8]Wilhelm J, Heinroth K, Stoevesandt D, et al. Non-compaction cardiomyopathy with diffuse left coronary artery fistulae as a rare cause of congestive heart failure. Eur Heart J, 2013, 34(1): 12
[9]Caputo S, Capozzi G, Santoro G, et al. Multiple right coronary artery fistulae in a patient with diffuse hypertrophic cardiomyopathy: a case report. J Am Soc Echocardiogr, 2005, 18(8): 884
[10]Jenni R, Oechslin E, Schneider J, et al. Echocardiographic and pathoanatomical characteristics of isolated left ventricular non-compaction: a step towards classification as a distinct cardiomyopathy. Heart, 2001, 86(6): 666-671
(本文编辑:孙晋枫)
Noncompaction cardiomyopathy complicated with multiple coronary artery-to-right ventricle fistula in one child
DAIKe,ZHANGZhi-fang,CHENYi-wei,LIFen,FULi-jun,ZHANGYu-qi
(DepartmentofCardiology,ShanghaiChildren'sMedicalCenteraffiliatedtoShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai200127,China)
Corresponding Author: ZHANG Zhi-fang, E-mail:zzftjh@hotmail.com
ObjectiveTo study the clinical features of a girl with noncompaction cardiomyopathy complicated with multiple coronary artery-to-right ventricle fistula and review the literatures. MethodsClinical symptoms and assistant examinations such as electrocardiogram, echocardiography and cardiac catheter of the case diagnosed as noncompaction cardiomyopathy complicated with multiple coronary artery-to-right ventricle fistula were reviewed. Two cases of noncompaction cardiomyopathy complicated with coronary artery to ventricle fistula and part of patients with cardiomyopathy complicated with coronary artery to ventricle fistula reported since 2003 were also reviewed in the study. Results(1)A 6 month girl with poor appetite and night sweat was admitted to our hospital. Transthoracic echocardiography revealed a moderately impaired left ventricular contractility (ejection fraction 34% calculated according to Simpson's rule) and hypertrabeculation of the left ventricular latero-apical region with a maximal ratio of noncompacted to compacted myocardium as 2.5, supporting the diagnosis of noncompaction cardiomyopathy. The color Doppler and contrast echocardiogram showed an unusually evident diastolic flow within the compacted layer of the myocardium. The coronary angiography showed the right ventricle was opaque after left and right coronary injections, disclosing multiple coronary right ventricular fistulae. The patient accepted digoxin, furosemidum, spironolactone treatment and the clinical symptom was improved. (2)Retrospective review of the literatures showed two cases of noncompaction cardiomyopathy complicated with coronary artery to ventricle fistula. These patients were adults and showed symptoms as dyspnea and angina pectoris. Doctors made a definite diagnosis through the examination of echocardiography and coronary angiography. One case of cardiomyopathy complicated with coronary artery to ventricle fistula accepted implantable cardioverter defibrillatror because of syncope.ConclusionNoncompaction cardiomyopathy associated with multiple coronary artery-to-right ventricle fistulas is one of the rare disease. The clinical symptoms mainly focus on congestive heart failure such as poor appetite and night sweat in infant. The echocardiography and coronary angiography is helpful to make a diagnosis. The medicine such as digitalis, diuretic and angiotensin converting enzyme inhibitors can be used to improve symptoms.
Noncompaction cardiomyopathy; Multiple coronary artery-to-right ventricle fistula; Cardiomyopathy
上海交通大学医学院附属上海儿童医学中心 上海,200127
张志芳,E-mail:zzftjh@hotmail.com
10.3969/j.issn.1673-5501.2017.02.013
2017-02-17
2017-04-13)
