不同水解方式对乳清浓缩蛋白水解产物结合钙量的影响
2017-05-15
(东北农业大学食品学院,哈尔滨150030)
不同水解方式对乳清浓缩蛋白水解产物结合钙量的影响
王楠楠,徐红华,夏行昊,董世荣,谢明明
(东北农业大学食品学院,哈尔滨150030)
研究了酸水解和酶水解两种不同水解方式对乳清浓缩蛋白(WPC)水解产物与钙离子结合量的影响。结果表明,采取不同水解方式水解乳清浓缩蛋白,水解产物与钙离子结合能力不同,当酸水解与酶水解达到相同水解度时,酸水解比酶水解水解产物结合的钙量高;就酶水解而言,胰蛋白酶比枯草杆菌中性蛋白酶水解产物结合的钙量低。这一结果说明:乳清浓缩蛋白在酸水解形成纳米纤维的过程中会生成能够与钙离子结合的基团,与酶水解相比其钙结合量更高可能与WPC纳米纤维自身特殊结构有关。
乳清浓缩蛋白;水解;钙
0 引言
随着社会的发展,人们对健康要求日益提升,据相关调查显示,我国居民每日钙摄入量仅为推荐量的50%左右,补钙问题逐渐受到人们的重视[1]。目前的补钙产品是将钙嵌合在氨基酸中间,直接通过肠道黏膜吸收,有效提高钙的吸收利用率[2-3]。生物代谢试验表明低聚肽较氨基酸与钙的结合产物更易被人体吸收利用[4-5],乳清蛋白水解肽常作为补钙产品中的主要低聚肽成分[6]。传统的酸碱水解方式在酸、碱存在下可控制性差且对氨基酸残基均有破坏作用,效果明显逊于酶水解制备乳清蛋白水解肽[7]。本课题通过比较不同水解方式对乳清蛋白水解产物结合钙量的影响,为乳清蛋白复合产品的生产和开发提供新的契机。
1 实验
1.1材料
原料:乳清浓缩蛋白(WPC-80)。
试剂:枯草杆菌碱性蛋白酶(180 000 U/g),胰蛋白酶(250 U/g),硼酸,氧化镧(纯度为99.99%),盐酸,氢氧化钠,浓硫酸,氯化钙,甲基红,溴甲酚绿,硫酸铜,硫酸钾,高氯酸,硝酸。
1.2仪器与设备
GL-21M型离心机,DK-98-ⅡA电热恒温水浴锅,pHS-3C型精密pH计,AL204型分析天平,HYP-314型多功能快速消化器,KDN-102C半自动定氮仪,PEAA800原子吸收分光光度计,磁力搅拌恒温水浴锅。
1.3方法
1.3.1 原料的制备
参考王晶[8]的方法并加以改进。准确称取乳清浓缩蛋白7.9 g,完全溶解于去离子水中并定容至100 mL,盐酸(6 mol/L和1 mol/L)调pH值至2.0,于19 000 g(4℃)下离心30 min,吸取中层清液消化定氮并稀释样品终质量分数为3%,4℃冰箱保存。
1.3.2 蛋白质质量分数测定
蛋白质质量分数测定采用凯氏定氮法[9]并加以改进。将0.2 g硫酸铜、6.0 g硫酸钾、2 mL待测样品及12 mL浓硫酸依次放入消化管中,打开机器开关,待消化管内液体呈蓝绿色澄清透明后消化结束,样品冷却至室温后,移入100 mL容量瓶中摇匀并移取10 mL于定氮管中,锥形瓶中加入15 mL硼酸和5滴的甲基红-溴甲酚绿混合指示剂放在蒸馏出口处,当锥形瓶中液体体积达到150 mL时在计时1 min,用0.05 mol/L盐酸滴定,同时做空白。计算公式为

式中:0.014为1 mL盐酸标准溶液相当于氮的质量(g);X为蛋白质质量分数(%);v1为样品消耗标准盐酸溶液的体积(mL);v0为空白消耗标准盐酸溶液的体积(mL);c为标准盐酸溶液的质量浓度(mol/L);F为氮换算为蛋白质的系数;m为样品质量或体积(g或mL)。
1.3.3 蛋白质的水解
(1)酸水解。取1.3.1中的溶液50 mL于烧杯中,调其pH至2.0后密封,90℃下分别水浴0、2、5、8、10 h,加热到指定时间后立即取出样品,冷却至室温,用0.2 mol/L盐酸滴定,当其pH恢复至2.0时记下消耗盐酸体积,利用公式计算水解度。
(2)酶水解(胰蛋白酶和枯草杆菌中性蛋白酶)。取1.3.1中的溶液50 mL于烧杯中,调pH值至7.0后置于40℃的磁力搅拌恒温水浴锅中,用浓度为0.2 mol/ L的氢氧化钠滴定保持溶液pH值为7.0不变,向样品中加入一定量的蛋白酶,待酶液完全溶解1 min后开始计时,在水解过程中通过不断滴加氢氧化钠保持溶液pH值不变,在达到与pH值为2.0,加热0,2,5,8,10 h相同水解度时,立即取出样品,90℃灭酶活15 min,同时记下消耗碱液量及反应时间。
1.3.4 水解度(DH)的测定
水解度的测定采用pH-stat法[10],其计算公式为

1.3.5 添加氯化钙
将质量分数为0.5%的氯化钙溶液加入到1.3.3的蛋白质水解液中,搅拌均匀室温下反应30 min后将溶液分别移入透析袋中,透析12 h并每隔1 h换一次水,结束后测定钙结合量。
1.3.6 钙结合量的测定
钙结合量的测定采用原子吸收光谱法法并加以改进[11]。设定测定参数:灯电流:9 mA,波长422.7 nm,狭缝2.4 nm,空气流量15 min/L,乙炔流量2.4 min/L,首先稀释钙标准溶液的质量浓度分别为0.5,1.0,1.5,2.0,2.5μg/mL;按照设定测定参数和钙标准溶液质量浓度,依次测定空白、钙标准溶液以及待测样品溶液吸光值,根据钙标准溶液做出以钙质量浓度为横坐标,吸光值为纵坐标的钙标准曲线,通过待测样品的吸光值确定其钙质量浓度,计算钙结合量。
1.4统计分析
实验数据采用 SPSS16.0统计分析软件中One-way ANOVO方法进行方差分析,对F检验达显著水平(P<0.05)的因子进行LSD法多重比较。数据均以平均值±标准差表示(n=3)。
2 结果与分析
2.1酸水解
由图1可以看出,乳清浓缩蛋白在pH值为2.0(90℃)条件下,随着加热时间的延长,水解度不断增大。这一结果说明乳清浓缩蛋白在形成纳米纤维的过程中,时刻伴随着水解反应的发生,而且加热时间越长肽键数目断裂越多。

图1 乳清浓缩蛋白酸水解水解度随时间的变化
2.2酶水解
由图2可以看出,在pH值为7.0(40℃)条件下,用胰蛋白酶和枯草杆菌中性蛋白酶分别水解乳清浓缩蛋白,达到同一水解度时,胰蛋白酶比枯草杆菌中性蛋白酶反应的时间长,说明胰蛋白酶比枯草杆菌中性蛋白酶水解的速率慢。有相关文献报道[7],枯草杆菌中性蛋白酶比胰蛋白酶作用底物更加广泛,因此其反应速率更快,在达到相同水解度时,单位时间内肽键断裂的数目更多,生成更多的肽和氨基酸。
2.3钙结合量的测定

图2 比较相同水解度下酶反应速率
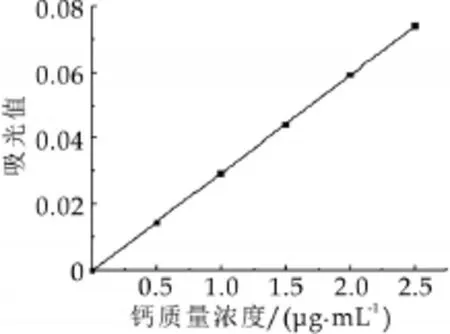
图3 钙标准曲线

图4 比较不同水解方式钙结合量
由图3可以看出,酸水解和酶水解的钙结合量随着水解度的增大而增大;相同水解度下,酸水解的钙结合量大于酶水解的钙结合量;就酶水解而言,枯草杆菌中性蛋白酶钙结合量大于胰蛋白酶钙结合量。能够与钙离子结合的基团主要有羧基、氨基和羰基,随着水解度的增大,肽键断裂更多且有更多游离氨基和羧基生成,因此酸水解和酶水解的钙结合量随着水解度的增大不断增大,其中酸水解、枯草杆菌中性蛋白酶、胰蛋白酶的钙结合量分别是水解前的8.64,7.50和7.66倍。乳清浓缩蛋白的酸水解即形成乳清浓缩蛋白纳米纤维的过程,不仅发生了肽键的断裂,而且在很大程度上是蛋白质结构的变化,最终在加热10h时形成了具有特殊三维立体网状结构的纳米纤维聚合物,这种结构有序、稳定,钙离子与其结合一方面是通过暴露的氨基酸残基,另一方面可能是通过吸附或者镶嵌在纤维结构内部的方式,所以钙结合量大于酶水解的钙结合量;由于枯草杆菌中性蛋白酶作用底物较胰蛋白酶广泛,因此达到相同水解度时,肽键断裂程度更大,钙结合量更多。
3 结论
通过对本课题的研究可知采取不同水解方式(酸水解和酶水解)水解乳清浓缩蛋白,水解产物与钙离子的结合能力不同,而且当酸水解与酶水解在相同水解度下,酸水解的水解产物与钙离子结合量明显高于酶水解水解产物与钙离子结合量;就酶水解而言,胰蛋白酶比枯草杆菌中性蛋白酶水解产物结合的钙量低。这一结果说明乳清浓缩蛋白纳米纤维具有结合钙离子的能力,而且在一定程度上与钙离子的结合量大于酶水解水解产物与钙离子的结合量,可能是由于WPC纳米纤维自身特殊结构导致的。
[1]葛可佑.中国居民膳食钙摄入量普遍低下[C].钙与妇女和儿童健康研讨会论文集,京,2001.
[2]曾敏莉,周远大.钙制剂的现状及发展趋势[J].儿科药学杂志,2004,8 (6):30-31.
[3]菅景颖.胶原多肽螯合钙的制备及其壮骨、骨质疏松防治作用研究[D].河北农业大学,2007.
[4]王阶标,李秀玲,王学生,等.活性钙在大鼠体内吸收利用率的研究[J].华北煤炭医学院学报,1999,(5):388-390.
[5]曾敏莉,周远大.钙制剂的现状及发展趋势[J].儿科药学杂志,2004,8 (6):30-31.
[6]赵丽娜,汪少芸.乳清蛋白-钙的螯合复合物制备及性质研究.2009.
[7]曹建,师俊玲.食品酶学.郑州:郑州大学出版社,2011.2.
[8]王晶.乳清浓缩蛋白纳米纤维的制备及其性质研究.2013.
[9]中华人民共和国卫生部.GB/T5009.46-2003乳与乳制品卫生标准的分析方法[S].
[10]中华人民共和国卫生部.GB/T5413.7-1997婴幼儿配方食品和乳粉灰分的测定[S].
[11]中华人民共和国卫生部.GB5413.21-2010婴幼儿食品和乳品中钙、铁、锌、钠、钾、镁、铜和锰的测定[S].
Effect of different hydrolysis ways on amounts of calcium combined with whey protein concentrate hydrolysates
WANG Nannan,XU Honghua,XIA Xinghao,DONG Shirong,XIE Mingming
(College of Food Science,Northeast Agricultural University,Harbin,150030,China)
The effect ofboth acid hydrolysis(pH=2.0)and enzyme hydrolysis(trypsin and bacillus subtilis neutralprotease)on amounts of cal⁃cium combined with whey protein concentrate(WPC)hydrolysates were investigated in this paper.The results showed that the ability of cal⁃cium combined with hydrosates was different when whey protein concentrate was hydrolyzed by two different hydrolysis ways.Compared with enzyme hydrolysis,the amounts of calcium combined with acid hydrolysis hydrosates were higher at the same degree of hydrolysis.In terms of enzymatic hydrolysis,trypsin hydrolysates had more calcium combined than bacillus subtilis neutral protease.The amounts of calci⁃um in combination with whey protein concentrate hydrolysates were higher in the process of acid hydrolysis than enzymatic hydrolysis,it may be associated with whey protein concentrate nanofribrilformed with a specialstructure and generated some groups combining with calci⁃um.
whey protein concentrate;hydrolysis;calcium
Q936
A
1001-2230(2017)04-0014-03
2016-10-31
国家自然基金项目(No.31471682)。
王楠楠(1991-),女,硕士,研究方向为食品科学。
徐红华
