过氧化氢检测用新型BODIPY探针的设计合成与性能
2017-05-07李保生陈建波
李保生, 陈建波, 孙 杰
(1. 西南科技大学材料科学与工程学院, 四川 绵阳 621010; 2. 中国工程物理研究院化工材料研究所, 四川 绵阳 621999)
1 引 言
早在19世纪,过氧化爆炸物如三过氧化三丙酮(TATP)、六亚甲基三过氧化二胺(HMTD)就被合成出来,由于其冲击感度高、稳定性低、挥发性高等缺点,很少被用于军事领域和民用工程[1]。然而,过氧化爆炸物具有原料易得、制备简单及爆炸威力大[2-3]等特点易被广泛用于恐怖爆炸袭击,如1994年的以色列驻英大使馆爆炸案、2005年的伦敦地铁爆炸案[4]及2015年的“11.13”巴黎恐怖爆炸袭击等。爆炸物的分析检测是预防恐怖爆炸袭击的重要手段[5],然而过氧化爆炸物既没有紫外吸收又没有荧光发射,且其化学结构同时缺乏硝基和芳香烃基,致使其分析检测面临极大的挑战[3]。目前,过氧化爆炸物的检测方法主要有电化学法[6],比色法[7],荧光法[8]等,其中基于荧光法的分子探针具有灵敏度高、选择性好、操作简单、易于携带等优点,是爆炸物检测领域的发展趋势之一[9]。
过氧化爆炸物含有不稳定的过氧化基团(—O—O—),易光解产生过氧化氢(H2O2)。另外,H2O2也是合成过氧化爆炸物的必要原料。因此,通过对H2O2的分析检测可实现对过氧化爆炸物的有效监测与预警。当前,研究人员常以苯基硼酸酯作为H2O2的识别基团,结合不同的荧光团组成荧光探针检测过氧化爆炸物[10]。在识别基团方面,日本东京大学Nagano[11]教授指出苯基硼酸酯识别过程易受NO干扰,可见硝基爆炸物光解NO会影响传统识别基团的检测可靠性。在荧光团方面,过氧化爆炸物光解H2O2的检测过程要求荧光团具有较高的光稳定性,然而美国加州大学Trogler教授报道的荧光素类荧光团的光稳定性较差[12],难以满足检测要求。二氟化硼二吡咯甲烷(BODIPY)[13]具有极好的光化学稳定性、较高的荧光量子产率和摩尔消光系数,已被广泛应用于生物标记、发光材料及化学传感等领域。遗憾的是,传统的识别基团如苯基硼酸酯却不易调控BODIPY对H2O2的荧光响应,以至于目前仍未见报道BODIPY荧光探针用于检测过氧化爆炸物。因此,针对过氧化爆炸物(H2O2)的分析检测,发展具备高选择性、高灵敏度与光稳定性的新型荧光探针具有十分紧迫的现实需求。
本研究以苯偶酰为识别基团,BODIPY为荧光团,设计合成得到对H2O2具有荧光增强响应的新型探针4-(4-硝基苯偶酰基)-氟硼二吡咯甲烷(BD-3)(见图1),并表征其化学结构、考察其光谱性质、探讨其检测性能。BD-3自身仅有微弱荧光,当与H2O2反应后可实现基于光致诱导电子转移(d-PET)原理的荧光增强响应,发射出强烈的绿色荧光。此外,新型探针还表现出了优异的检测性能包括好的光稳定性和高的选择性,可满足复杂环境条件下过氧化爆炸物的现场检测需求。
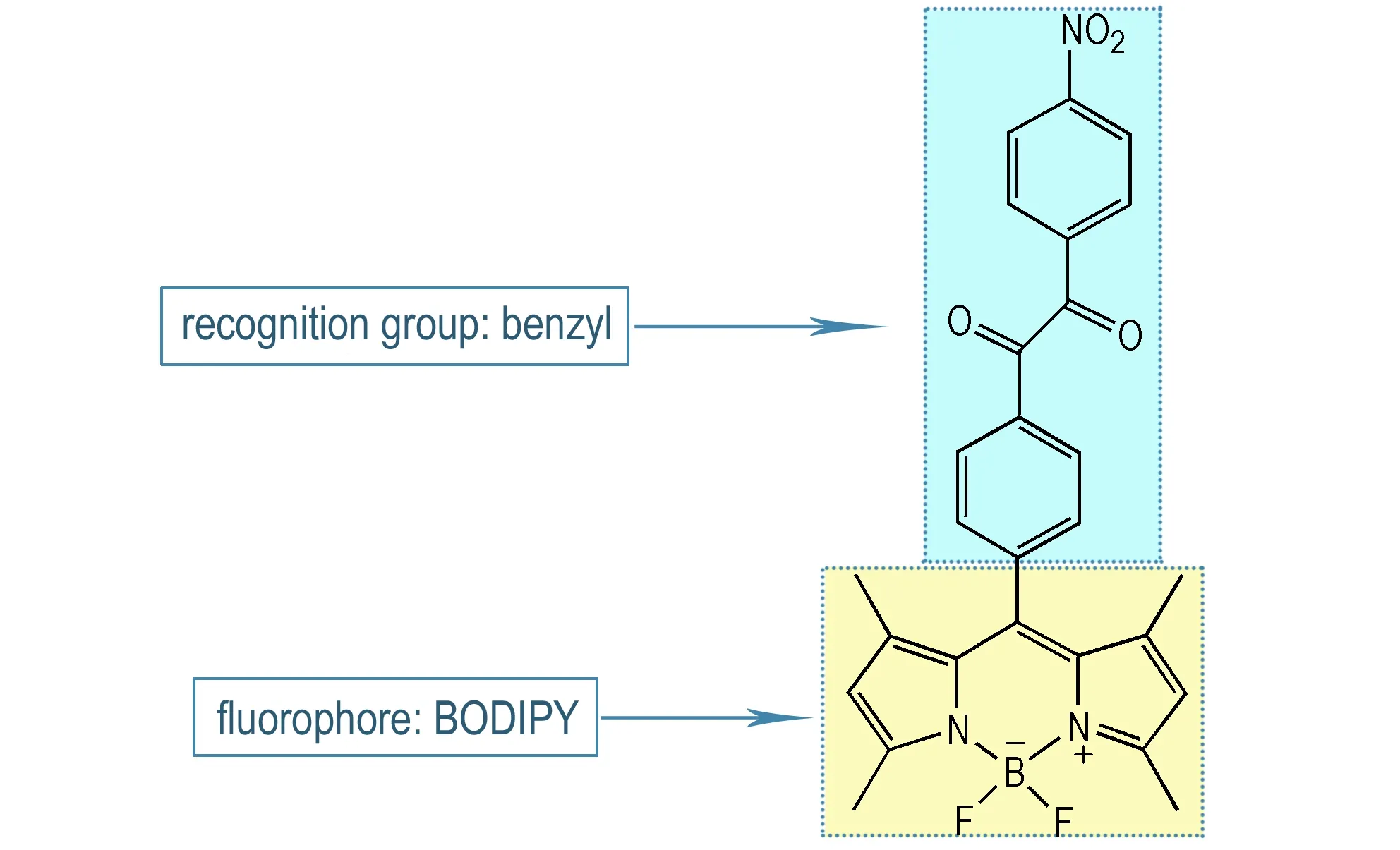
图1新型荧光探针BD-3的化学结构
Fig.1Chemical structure of new fluorescence probe (BD-3)
2 实验部分
2.1 实验仪器
LS-55荧光分光度计(美国PerkinElmer公司); Cary 100紫外-可见分光光度计(美国Varian公司); MicrOTOF QⅡ高分辨质谱仪(德国Bruker公司); Avance Ⅲ 600 MHz核磁共振仪(美国Bruker公司); Gnnie 2T漩涡混合器(美国Vortex公司); S220-K多参数测试仪(梅特勒-托利多仪器上海有限公司); ME204电子天平(梅特勒-托利多仪器上海有限公司); DF-1集热式磁力恒温搅拌器(江苏金坛市江南仪器厂); RE-3000旋转蒸发器(上海亚荣生化仪器厂); WFH-203B暗箱式三用紫外分析仪(上海精科实业有限公司); ENF-260C手提式管式紫外线灯(美国Spectronics公司); S300-H超声波发生器(德国Elma公司); FD115鼓风干燥器(德国Binder公司); VD23真空干燥箱(德国Binder公司)。
2.2 实验试剂
碘化亚铜、氯化铵、氯化钠、碳酸氢钠、三乙胺、三氟化硼乙醚、无水四氢呋喃、柱层析硅胶(100~200目)均为分析纯,购自上海晶纯生化科技股份有限公司; 2,4-二甲基吡咯,分析纯,购自浙江嘉兴玛雅试剂有限公司; 1-乙炔基-4-硝基苯、4-碘苯甲酰氯、碘化钯均为分析纯,购自北京百灵威科技有限公司; 双(三苯基膦)二氯化钯,分析纯,购自Sigma-Aldrich(上海)贸易有限公司; 薄层层析硅胶板购自乳山太阳干燥剂有限公司; 二氯甲烷、环己烷、乙酸乙酯、无水硫酸钠、石英砂均为分析纯,购自国药化学试剂有限公司。其他试剂均为分析纯,水为去离子水。
2.3 探针4-(4-硝基苯偶酰基)-氟硼二吡咯甲烷(BD-3)的合成
2.3.1 4-碘-氟硼二吡咯甲烷(BD-1)的合成
在氩气保护下,将2,4-二甲基吡咯(0.7 mL,6.71 mmol)滴加到含有4-碘苯甲酰氯(0.7 g,2.63 mmol)的无水二氯甲烷溶液(150 mL)中,室温搅拌72 h; 然后依次加入三乙胺(2.2 mL,15.75 mmol)和三氟化硼乙醚(2.68 mL,20.79 mmol),室温搅拌24 h; 混合溶液用饱和碳酸氢钠溶液(60 mL × 3)清洗,并用二氯甲烷萃取有机层用无水硫酸钠干燥; 旋转蒸干除去溶剂,经硅胶柱层析(淋洗剂: 环己烷/乙酸乙酯=4/1)纯化得到BD-1棕色粉末361.2 mg,产率30.59%。
1H NMR (600 MHz, CDCl3)δ: 7.82 (dd,J=26.4, 8.2 Hz, 2H), 7.05 (d,J=8.2 Hz, 2H), 5.99 (s, 2H), 2.55 (s, 6H), 1.42 (s, 6H);13C NMR(151 MHz, CDCl3)δ: 155.89, 142.92, 140.07, 138.35, 134.57, 131.14, 129.96, 121.44, 94.74, 14.66; HRMS (ESI): calcd for [M-H] 449.0498; found 449.0491。
2.3.2 4-(4-硝基苯乙炔基)-氟硼二吡咯甲烷(BD-2)的合成
在氩气保护下,BD-1(100 mg,0.22 mmol)与对硝基苯乙炔(80 mg,0.54 mmol)溶解在无水四氢呋喃(10 mL)中,依次加入双(三苯基膦)二氯化钯(PdCl2(PPh3)2)(10 mg,0.02 mmol)、碘化亚铜(CuI)(5 mg,0.03 mmol)、三乙胺(1 mL)作催化剂,60 ℃下反应10 h; 旋转蒸干溶剂,经硅胶柱层析(淋洗剂: 二氯甲烷/环己烷=3/2)纯化得到BD-2橙黄色粉末58.8 mg,产率56.51%。
1H NMR (600 MHz, CDCl3)δ: 8.30~8.25 (m, 2H), 7.76~7.68 (m, 4H), 7.37 (d,J=8.0 Hz, 2H), 6.03 (s, 2H), 2.59 (s, 6H), 1.45 (s, 6H);13C NMR (151 MHz, CDCl3)δ: 154.95, 146.23, 141.85, 139.33, 135.06, 131.54, 131.34, 130.08, 128.71, 127.48, 122.73, 121.95, 120.46, 92.66, 87.74, 13.58; HRMS (ESI): calcd for [M-H] 468.1695; found 468.1688。
2.3.3 4-(4-硝基苯偶酰基)-氟硼二吡咯甲烷(BD-3)的合成
在氩气保护下,BD-2(60 mg,0.13 mmol)溶解在DMSO(3 mL)中,加入碘化钯(PdI2)(5 mg,0.014 mmol)作催化剂,140 ℃下反应4 h; 冷却至室温,用20 mL水稀释,再用60 mL(20 mL × 3)的乙酸乙酯萃取,收集有机层并用饱和氯化铵溶液清洗,然后用无水硫酸钠干燥。旋转蒸干溶剂,经硅胶柱层析(淋洗剂: 二氯甲烷/环己烷 = 3/1)纯化得到BD-3深红色粉末27 mg,产率42.18%。
1H NMR (600 MHz, CDCl3)δ: 8.27 (d,J=7.0 Hz, 2H), 7.72 (dd,J=12.0, 11.2 Hz, 4H), 7.37 (d,J=8.2 Hz, 2H), 6.07 (s, 2H), 2.58 (s, 6H), 1.46 (s, 6H);13C NMR (151 MHz, CDCl3)δ: 191.58 (s), 191.23 (s), 156.50, 151.31, 142.64, 142.52, 139.11, 137.12, 132.72, 131.15, 130.74, 130.67, 129.40, 124.21, 121.75, 14.68; HRMS (ESI): calcd for [M-H] 500.1593; found 500.1597。
2.4 探针BD-3的光谱性能测试
紫外光谱测定使用1 cm比色池,使用Varian carry 100紫外-可见吸收光谱仪测定200~800 nm波长范围的紫外吸收波长与吸收光谱。荧光光谱测定使用1 cm石英池,在PerkinElmer LS-55荧光分光度仪上测定200~800 nm波长范围的激发、发射光谱与荧光强度。测试介质选用缓冲溶液-乙腈混合液(V/V为8/2,pH=7.0),缓冲溶液为磷酸氢二钠-柠檬酸缓冲液。在浓度为1.0 μmol·L-1的探针溶液中加入一定浓度的H2O2标准溶液,在室温下反应30 min后进行光谱实验。
2.5 探针BD-3的光稳定性测试
用波长为365 nm的紫外光连续照射荧光探针溶液及其H2O2衍生产物溶液,然后每隔20 min测定荧光强度,激发波长为500 nm,激发和发射狭缝分别为12.0/0.0。
2.6 探针BD-3的选择性测试
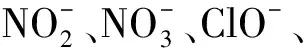
2.7 探针BD-3的灵敏度测试
在浓度为1.0 μmol·L-1的探针溶液中分别加入浓度为0~10 mmol·L-1的H2O2溶液室温反应60 min,然后于PerkinElmer LS-55荧光分光度仪测定上述各衍生溶液的荧光强度及荧光光谱,激发波长为500 nm,激发和发射狭缝分别为12.0/0.0。
检测限(LOD)计算公式为:
LOD=3σ/κ
(1)
式中,σ为空白样品的标准偏差;κ为标准工作曲线的斜率。
3 结果与讨论
3.1 新型探针的设计与合成
过氧化爆炸物含有不稳定的过氧化基团(—O—O—),易光解产生H2O2,其检测过程要求荧光探针具备更高的光稳定性。BODIPY具有好的光化学稳定性,可用作新型探针的荧光团。苯偶酰基可与H2O2高选择性反应,且不受硝基爆炸物NO的影响,可作为新型探针的识别基团。此外,在苯偶酰上引入特定官能化基团,通过与H2O2反应前后引起BODIPY共轭体系电子云分布的变化,进而有望实现对BODIPY的荧光增强调控。基于上述设计思路,以对硝基苯偶酰基作为识别基团,BODIPY作荧光团,以4-碘苯甲酰氯和2,4-二甲基吡咯为起始原料,经过一系列有机合成反应,制备了一种对H2O2具有荧光增强响应的新型探针BD-3,具体合成路线如Scheme 1所示。
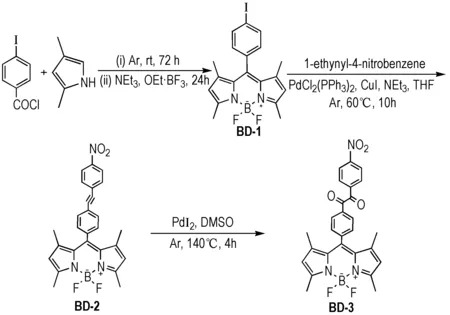
Scheme1Synthesis strategy of new fluorescence probe (BD-3)
3.2 新型探针的光谱性质
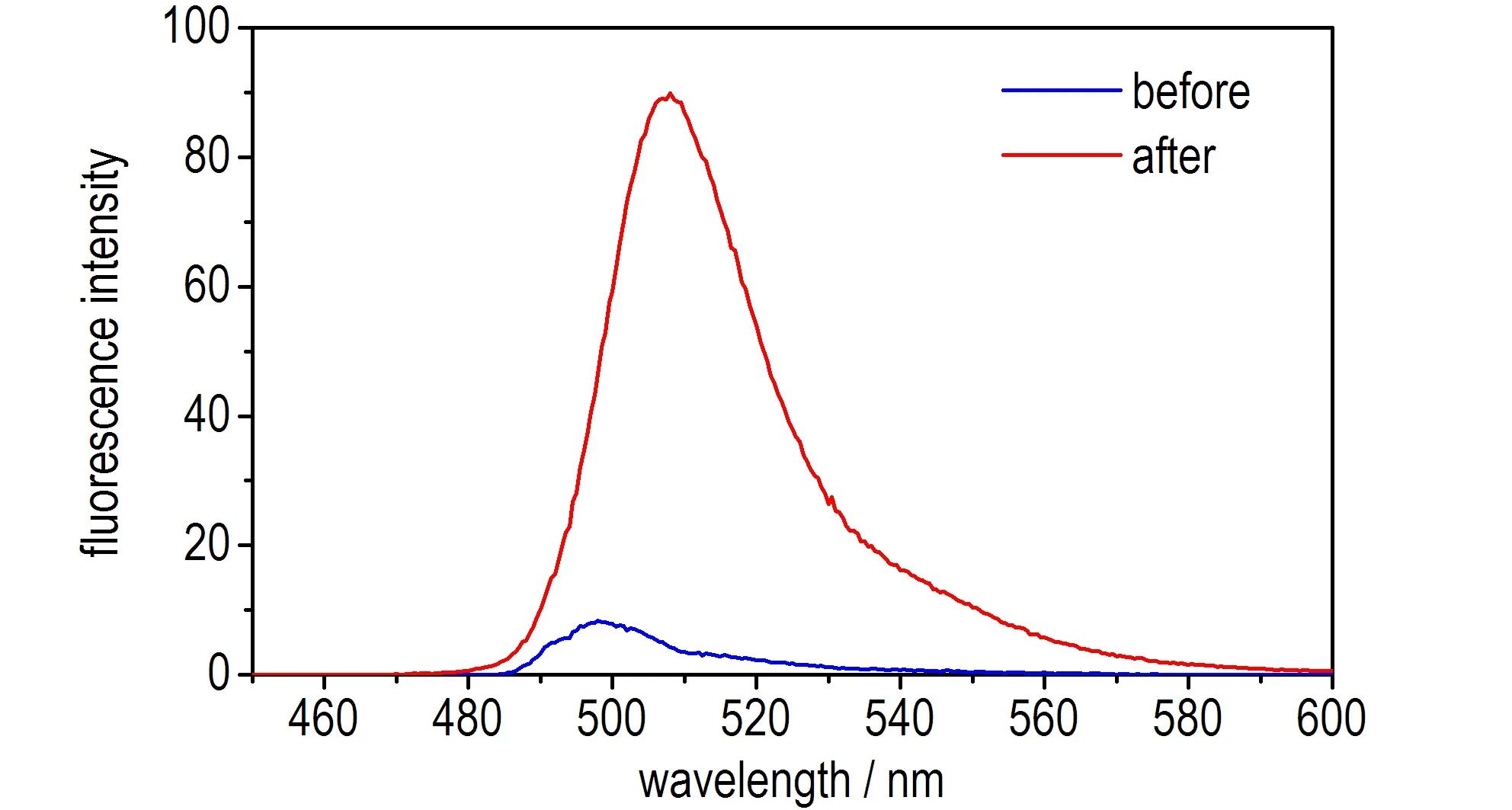
实验考察了1.0 μmol·L-1的探针溶液加入10 mmol·L-1H2O2响应前后的紫外吸收光谱和荧光发射光谱,具体如图2所示。在未加入H2O2之前,探针在紫外吸收光谱的最大吸收峰为500 nm,摩尔消光系数(ε)为6.68×104L·mol-1·cm-1,其荧光发射光谱的最大发射峰在508 nm处,且荧光强度非常弱。在加入H2O2充分反应之后,探针最大的紫外吸收峰仍在500 nm(ε=6.9×104L·mol-1·cm-1),且吸光度变化不大,其最大荧光发射峰仍在508 nm,荧光强度增强11倍,并发射出强烈的绿色荧光。
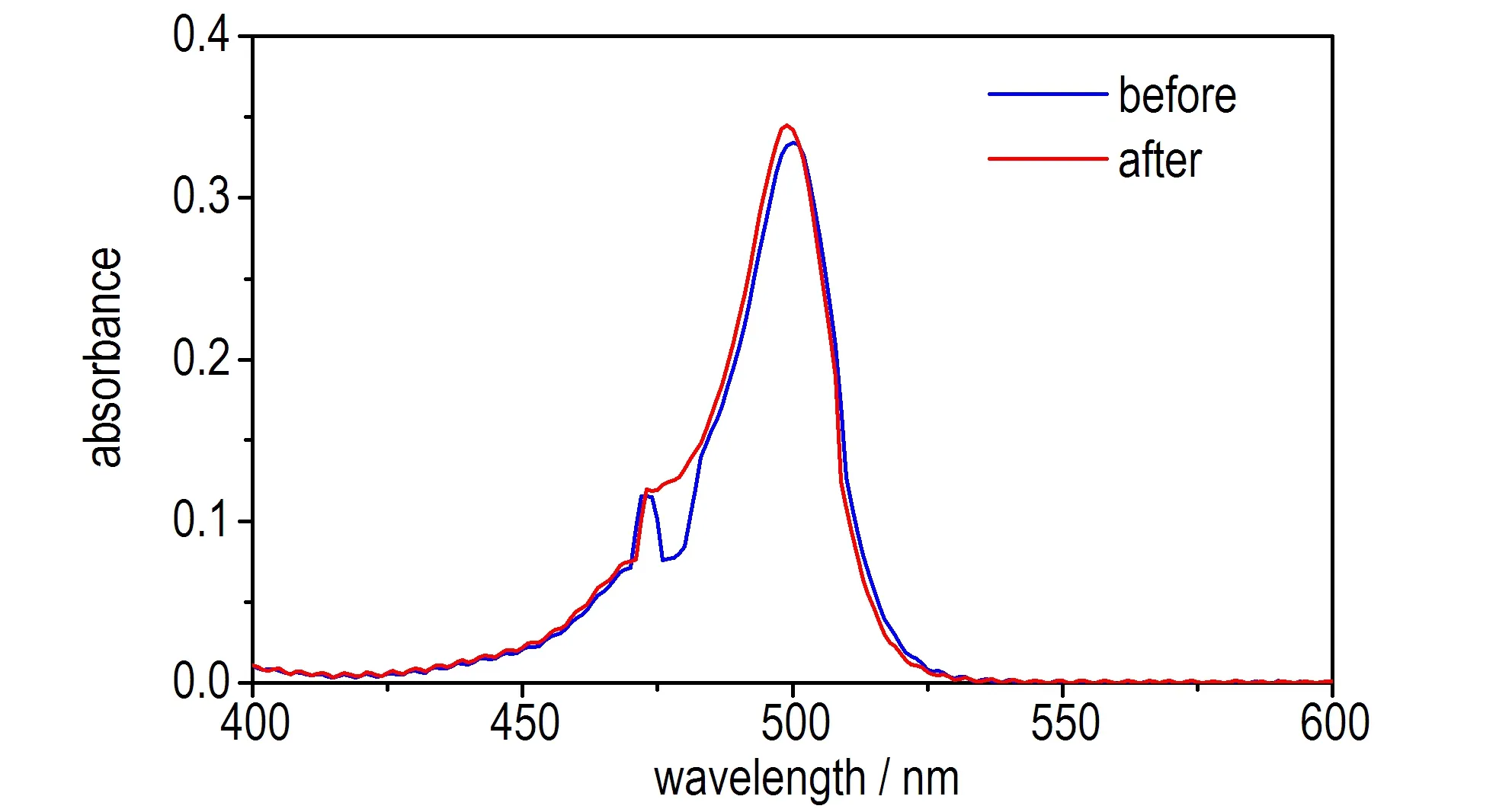
a. UV absorption spectrum
b. fluorescence emission spectrum
图2BD-3响应H2O2前后的紫外吸收光谱和荧光发射光谱
Fig.2The UV absorption spectrum and fluorescence emission spectrum of BD-3 before and after reaction with H2O2
3.3 探针响应H2O2的荧光增强机理
通过紫外吸收光谱和荧光发射光谱研究发现探针BD-3与H2O2之间发生了不可逆的化学反应,其反应机理如图3所示。由于苯偶酰基团含有强吸电子的硝基,有效增强了苯偶酰基团的电负性,使得BODIPY上的电子云分布向苯偶酰基团转移,发生氧化型的光致诱导电子转移(d-PET)机理,从而使探针的强荧光受到抑制,仅展示出微弱的荧光。当加入H2O2后,探针与H2O2发生Baeyer-Villiger反应,使苯偶酰转变为苯甲酸酐,苯甲酸酐再进一步被水解为苯甲酸[11]。这一过程导致强吸电子的硝基基团随苯偶酰基一起脱离BODIPY,BODIPY自身的荧光得以恢复,从而发射出强的绿色荧光,实现对H2O2的荧光增强响应[14-15]。
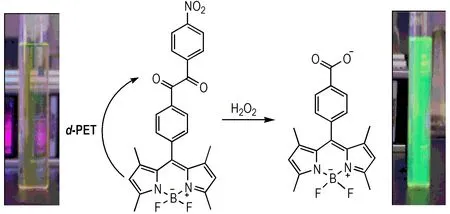
图3新型荧光探针响应H2O2的机理
Fig.3Reaction mechanism of new fluorescence probe for H2O2
3.4 新型探针的光稳定性研究
过氧化爆炸物的检测过程需要对爆炸物进行光解产生H2O2,要求荧光探针及其衍生产物具有良好的光稳定性。实验研究了在波长为365 nm的紫外光连续照射下荧光探针溶液及其H2O2衍生产物溶液的荧光变化情况,如图4所示。光照20 min后,探针BD-3溶液的荧光强度未发生明显变化,其H2O2衍生产物溶液的荧光强度仅减小了2%; 光照40 min后,探针BD-3溶液的荧光强度基本保持不变,其H2O2衍生产物溶液的荧光强度仅减小了4%; 光照90 min后,探针BD-3溶液的荧光强度仅增加了6%,其H2O2衍生产物溶液的荧光强度仍维持在94%以上。因此,本研究的新型探针具有较好的光稳定性,能满足过氧化爆炸物的检测过程对探针光稳定性的要求。
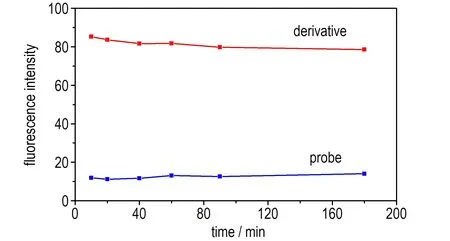
图4BD-3及其H2O2衍生溶液在连续光照下的荧光强度变化
Fig.4Fluorescence intensities of BD-3 and its H2O2derivative solution under continuous illumination
3.5 新型探针的选择性分析
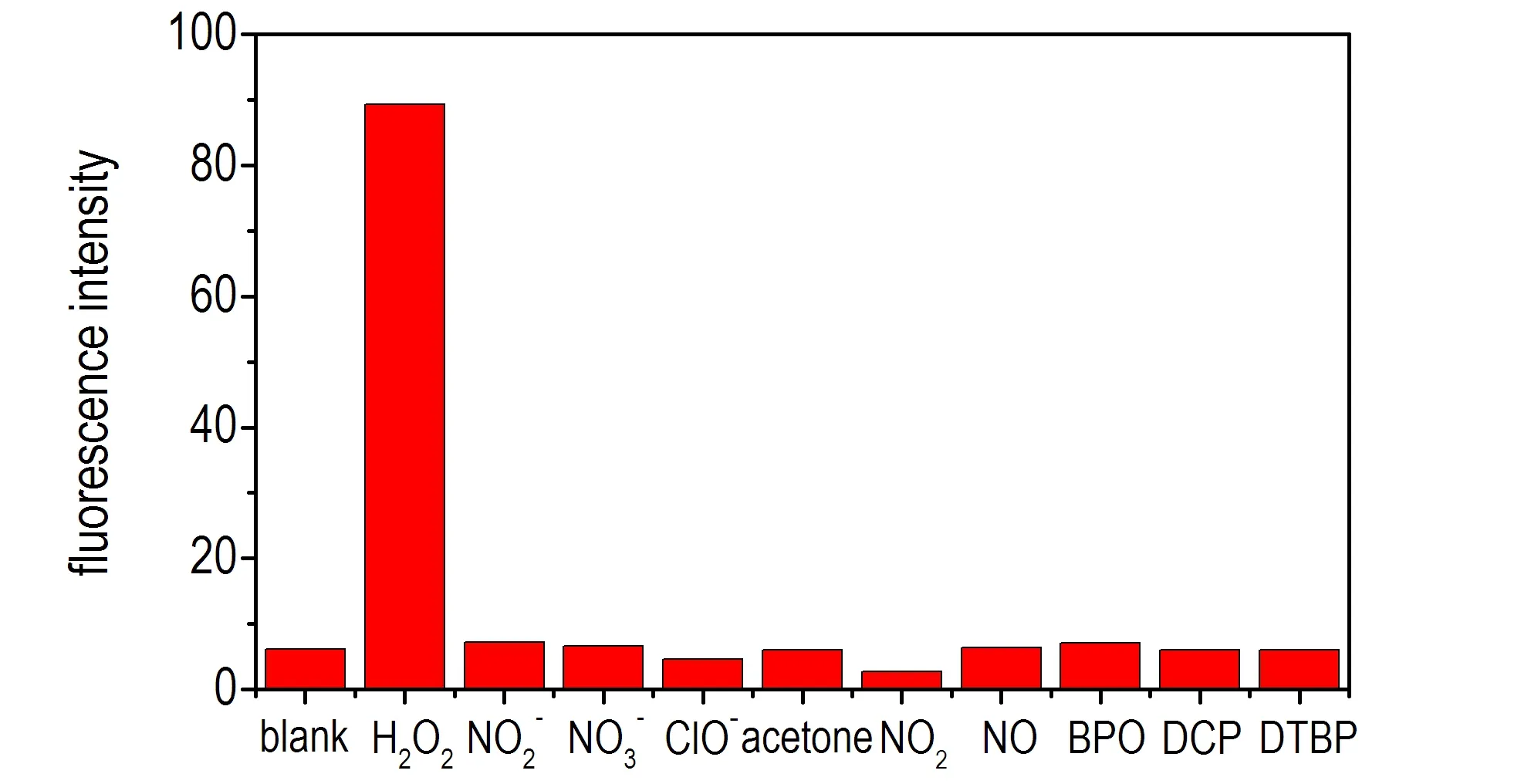
图5BD-3在不同干扰物存在下的荧光强度变化
Fig.5Fluorescence intensities of BD-3 in the presence of different interferences
3.6 新型探针的工作曲线及灵敏度
实验进一步考察了1.0 μmol·L-1的新型探针溶液响应不同浓度的H2O2(0~10 mmol·L-1)的荧光发射光谱及标准工作曲线,具体如图6所示。随着H2O2浓度的增加,荧光强度不断增强且在H2O2浓度达到5.0 mmol·L-1之后趋于稳定。在H2O2浓度为1.0×10-6~1.0×10-4mol·L-1的范围内,新型探针的荧光强度与H2O2的浓度呈现较好的线性关系,线性方程为Y=0.22185X+5.50365,R=0.9998。根据公式(1)可得出新型探针对H2O2的检出限(LOD)为0.9 μmol·L-1。
4 结 论
(1)以苯偶酰作为识别基团,并以光稳定性好的BODIPY作荧光团,首次设计合成了一种对H2O2具有荧光增强响应的BODIPY探针BD-3,BD-3的最大吸收和发射波长分别为500 nm和508 nm,摩尔吸光系数ε为6.68×104L·mol-1·cm-1。
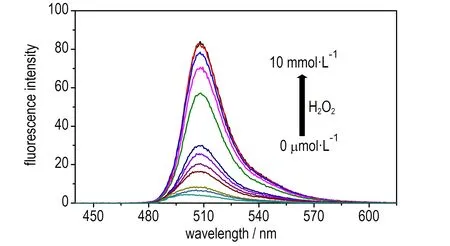
a. fluorescence emission spectrum of probe BD-3 after reacting with various concentrations of H2O2
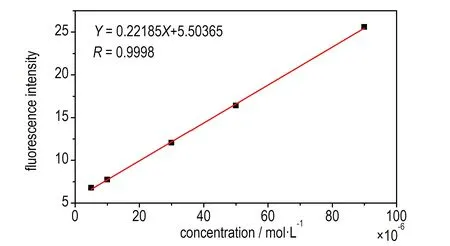
b. the standard curve
图6新型荧光探针BD-3与不同浓度H2O2响应的荧光发射光谱和标准工作曲线
Fig.6Fluorescence emission spectrum of BD-3 reacting with various concentrations of H2O2and the standard curve
(2)BD-3自身仅有微弱荧光,当与H2O2反应后,基于光诱导电子转移机理(PET机理)发射出较强的绿色荧光,荧光强度增强约11倍,并且裸眼可视。新型BD-3对H2O2呈现出较好的线性响应,线性范围为1.0×10-6~1.0 × 10-4mol·L-1,相关系数R为0.9998,检出限为0.9 μmol·L-1。
(3)新型BD-3对H2O2的检测具有很好的光稳定性,当紫外光连续照射90 min后,新型BD-3响应H2O2的荧光强度仍维持其初始值的94%以上。此外,新型BD-3对H2O2还展现出了高的选择性,检测过程不受其他过氧化物、硝基爆炸物及其降解产物NO的影响。因此,新型荧光探针BD-3可应用于过氧化爆炸物的现场检测。
参考文献:
[1] Dubnikova F, Karloff R, Along J, et al. Decomposition of triacetone triperoxide is an entropic explosion[J].JournaloftheAmericanChemicalSociety, 2005, 127(4): 1146-1159.
[2] Schulte-Ladbeck R, Vogel M, Karst U. Recent methods for the determination of peroxide-based explosives[J].AnalyticalandBioanalyticalChemistry, 2006, 386: 559-565.
[3] Burks R M, Hage D S.Current trends in the detection of peroxide-based explosives[J].AnalyticalandBioanalyticalChemistry, 2009, 395(2): 301-313.
[4] 伍星, 孙玉友. TATP检测的研究进展[J]. 刑事技术, 2010(6): 33-35.
WU Xing, SUN Yu-you. Advance in analysis of TATP[J].ForensicScienceandTechnology, 2010(6): 33-35.
[5] 熊鹰, 刘勇, 刘学涌, 等. 9-乙炔基-9-羟基蒽酮结构和荧光性能的理论研究[J]. 含能材料, 2011, 19(2): 189-193.
XIONG Ying, LIU Yong, LIU Xue-yong, et al. Theoretical study on structure and fluorescence properties of 9-ethynyl-9-hydroxyanthrone[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2011, 19(2): 189-193.
[6] Wang J. Electrochemical sensing of explosives[J].Electroanalysis, 2007, 19(4): 415-423.
[7] Schulte-Ladbeck R, Kolla P, Karst U.A field test for the detection of peroxide-based explosives[J].Analyst, 2002, 127(9): 1152-1154.
[8] Meaney M S, McGuffin V L. Luminescence-based methods for sensing and detection of explosives[J].AnalyticalandBioanalyticalChemistry, 2008, 391(7): 2557-2276.
[9] 王仕辰, 居佳, 艾文涛, 等. 炔基三苯胺的合成及其光谱性质[J]. 含能材料, 2015, 23(9): 892-897.
WANG Shi-chen, JU Jia, AI Wen-tao, et al. Synthesis and spectral properties of alkynyl substituted triphenylamines[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2015, 23(9): 892-897.
[10] 李震宇, 李静, 杜吕佩, 等. 硼酸及硼酸酯类过氧化氢荧光探针的最新研究进展[J]. 中国科学: 化学, 2012, 42(12): 1683-1693.
LI Zhen-yu, LI Jing, DU Lü-pei, et al. Recent advances in the boric acid/boronate-based fluorescent probes for detection of hydrogen peroxide[J].ScientiaSinicaChimica, 2012, 42(12): 1683-1693.
[11] Abo M, Urano Y, Hanaoka K, et al. Development of a highly sensitive fluorescence probe for hydrogen peroxide[J].JournaloftheAmericanChemicalSociety, 2011, 133: 10629-10637.
[12] Sanchez J C, Trogler W C. Polymerization of a boronate-functionalized fluorophore by double transesterification : applications to fluorescence detection of hydrogen peroxide vapor[J].JournalofMaterialsChemistry, 2008, 18(42): 5134-5141.
[13] Boens N, Leen V, Dehaen W. Fluorescent indicators based on BODIPY[J].ChemicalSocietyReviews, 2012, 41: 1130-1172.
[14] Abo M, Minakami R, Miyano K, et al. Visualization of phagosomal hydrogen peroxide production by a novel fluorescent probe that is localized via SNAP-tag labeling[J].AnalyticalChemistry, 2014, 86: 5983-5990.
[15] Zhang K M, Dou W, Li P X, et al. A coumarin-based two-photon probe for hydrogen peroxide[J].BiosensorsandBioelectronics,2015, 64: 542-546.
