纳米ZnO/LDPE食品包装膜及食品模拟物中ZnO含量的测定
2017-04-26史迎春胡长鹰黄金宇
史迎春,胡长鹰,黄金宇
1(暨南大学 包装工程研究所,广东 珠海,519070) 2(暨南大学,食品科学与工程系,广东 广州,510632) 3(广东普通高校产品包装与物流重点实验室,广东 珠海,519070) 4(广东出入境检验检疫局检验检疫技术中心,广东 广州,510623)
纳米ZnO/LDPE食品包装膜及食品模拟物中ZnO含量的测定
史迎春1,胡长鹰2,3*,黄金宇4
1(暨南大学 包装工程研究所,广东 珠海,519070) 2(暨南大学,食品科学与工程系,广东 广州,510632) 3(广东普通高校产品包装与物流重点实验室,广东 珠海,519070) 4(广东出入境检验检疫局检验检疫技术中心,广东 广州,510623)
建立了微波消解/电感耦合等离子体原子发射光谱(inductively coupled plasma atomic emission spectrometer, ICP-AES)及电感耦合等离子质谱仪(inductively coupled plasma mass spectrometer, ICP-MS)对纳米氧化锌/低密度聚乙烯(纳米ZnO/LDPE)薄膜及食品模拟物中ZnO含量的检测方法。根据EU10/2011选择30 g/L乙酸及超纯水为食品模拟物,将纳米ZnO/LDPE薄膜在40 ℃下浸泡10 d,测定食品模拟物中的ZnO含量。结果表明:Zn在0.03~100 μg/L及0.1~5 mg/L的浓度范围内线性关系良好,相关系数不低于0.999 8,在低、中、高3个水平进行加标实验,加标回收率在91.2%~110.2%之间,相对标准偏差(RSD,n=6)为0.3% ~6.8%,方法在消解液、30 g/L乙酸及超纯水的检出限(LOD)分别为0.015 mg/L,0.03 mg/L及0.03 μg/L,方法的定量限(LOQ)分别为0.05 mg/L,0.1 mg/L及0.1 μg/L,方法精密度好,灵敏度高,定性定量准确。采用该方法测得,实验室3种自制纳米复合薄膜中ZnO含量分别为(4.71±0.19),(9.20±0.49)及(12.87±0.33) g/kg,在40 ℃ 10 d后,3%乙酸(w/v)食品模拟物中ZnO的含量分别为(2.35±0.02),(3.54±0.01)及(4.12±0.35)mg/kg,在水食品模拟物中ZnO的含量分别为(24.65±0.68),(24.80±1.25)及(45.85±0.32)μg/kg。
纳米氧化锌;低密度聚乙烯;微波消解;电感耦合等离子体原子发射光谱;电感耦合等离子质谱
纳米材料因其量子尺寸使纳米复合材料呈现出不同于普通聚合物复合材料的特性[1],改善了聚合物的强度,刚性和阻隔性等性质[2-3]。目前已有多种纳米复合材料应用于食品包装市场[4],纳米氧化锌(nano Zinc oxide, nano-ZnO)凭借自身优良的抗菌性能[5-6]成为近年复合包装薄膜的研究热点。但是纳米复合薄膜包装材料在与食品接触过程中可能会出现纳米物质向食品中的迁移而导致食品安全隐患[7-8]。美国食品药品监督管理局(FDA)认定氧化锌(Zinc oxide, ZnO)是安全的食品添加剂[9],但并没有提及纳米ZnO,欧盟塑料食品接触材料法规EU10/2011[10]也没有对纳米金属及其氧化物的特定迁移量(specific migration limit, SML)做出规定,只规定了金属元素Zn的SML为25 mg/kg。因此从食品安全角度考虑,尽管已有纳米ZnO复合包装薄膜的研究和应用,但纳米ZnO向食品的迁移研究还是十分必要。
目前,关于纳米ZnO食品包装材料的研究主要集中在生物基膜的研究[11-12],包括对其性能的改善以及其抑菌性能、抑菌机理等方面,对于聚合物基膜研究比较少[13-19]。目前纳米食品包装多用于包装非脂肪类食品[5],并且其他纳米金属复合材料(如,纳米Ag)的迁移研究集中在纳米金属向水基食品模拟物的迁移,对于纳米ZnO/聚合物食品包装材料及其迁移试验的研究比较少,纳米ZnO的检测方法也仍不完善。本文建立了纳米ZnO/LDPE包装材料膜及水基食品模拟物中ZnO的检测方法,根据欧盟标准EU10/2011[10]选取30 g/L乙酸及超纯水作为本实验的食品模拟物,为后面迁移规律及机制的研究作准备。
1 材料与方法
1.1 材料与试剂
粒径为(50±10) nm的纳米ZnO,钛酸脂偶联剂(上海瀚思化工有限公司),聚乙烯粒子(深圳塑料原料专店)。HNO3(分析纯)、H2O2(分析纯,≥30%)、乙酸(分析纯),广州东巨公司;蒸馏水;Zn 单元素标准溶液(1 000 μg/mL),深圳市时得佳科技有限公司。
配制的溶液:30 g/L乙酸溶液(称取30 g乙酸溶液于1 000 mL容量瓶内,用超纯水定容到刻度后摇匀);体积分数5%硝酸溶液(称量50 mL硝酸溶液于1 000 mL容量瓶内,用蒸馏水定容到刻度后摇匀)20 mg/L标准储备液(将Zn单元素标准溶液取2 mL于100 mL容量瓶内,用30 g/L乙酸定容到刻度后摇匀)。
1.2 仪器与设备
35型造粒机,科倍隆机械有限公司;FYC-25型小型吹膜机,金方圆机械制造有限公司;Thermo iCAP6500型电感耦合等离子体原子发射光谱仪,美国Thermo公司;8500型电感耦合等离子体质谱仪 美国Agilent公司;微波消化萃取仪,意大利Ethos Touch Control公司;HH-ZK4型水浴锅,巩义予华仪器;超纯水器 MILLI-Q,德国密理博公司。
1.3 方法
1.3.1 薄膜的制备
纳米ZnO/LDPE薄膜样品及其空白样品,自制于暨南大学包装工程实验室,3种薄膜中纳米ZnO的添加量分别为10 g/kg(样品1),20 g/kg(样品2),20 g/kg并添加0.1%钛酸脂偶联剂(样品3)。样品1,样品2及样品3按照相应含量的纳米ZnO、钛酸酯偶联剂与LDPE母粒充分混合后通过双螺杆挤出造粒机造粒,工作条件如下:造粒机料桶1区至料桶9区的加热温度分别为165、190、190、190、190、200、200、200及195 ℃,模头温度为190 ℃,螺杆转速从20 r/min逐渐增加到60 r/min,重复造粒2次。然后通过FYC-25型小型吹膜机进行吹塑成型,吹膜机进料端到模头的4段温度分别为170、175、175及190 ℃。空白LDPE薄膜无需经过二次造粒,直接通过双螺杆挤出造粒机造粒后,通过吹塑机吹塑成型。
1.3.2 样品处理
1.3.2.1 微波消解处理
将纳米ZnO/LDPE复合薄膜裁至1 cm×1 cm大小,使用电子天平称取约0.1 g (精确到0.001 g)薄膜碎片置于聚四氟乙烯消解罐中,向消解罐中添加5 mL硝酸及2 mL过氧化氢溶液后盖上内盖,将消解罐置于耐外压罐中拧紧螺帽,放入微波萃取仪中进行消解,微波消解程序如表1所示。

表1 微波消解程序
消解完成后,将消解液移至100 mL容量瓶内,并用超纯水定容,待ICP-AES检测。
1.3.2.2 湿法消解处理
将纳米ZnO/LDPE复合薄膜裁至1 cm×1 cm大小,使用电子天平称取约0.1 g(精确到0.001 g)置于平底烧瓶中,向平底烧瓶中放入5 mL硝酸及2 mL过氧化氢溶液后置于温度为220 ℃的电热板上进行消解,待溶液消解至不足1 mL后将溶液移至100 mL容量瓶内,使用超纯水进行定容,待ICP-AES检测。
1.3.3 仪器的检测条件
ICP-AES及ICP-MS的检测条件见表2。
1.3.4 标准溶液的配制与标准曲线的绘制
消解液标准溶液:分别取一定量的20 mg/L标准溶液储备液于25 mL容量瓶内,用体积分数5%硝酸配制成0、2、5、7、10及12 mg/L的标准工作液。

表2 ICP-AES及ICP-MS的检测条件
30 g/L乙酸标准溶液:分别取一定量的20 mg/L标准溶液储备液于25 mL容量瓶内,用30 g/L乙酸配制成0、0.2、0.5、1、2及5 mg/L的标准工作液。
水标准溶液:分别取一定量的20 mg/L标准溶液储备液于25 mL容量瓶内,用体积分数5%的硝酸溶液配制成0、5、10、20、500及100 μg/L的标准工作液。
1.3.5 试验方法
总含量的测定:采用ICP-AES测定1.3.1.1 中稀释后的消解液。
水基模拟物中ZnO的测定:根据EU10/2011[10]中规定,每0.6 dm2的塑料薄膜对应100 mL的食品模拟物,将纳米ZnO/LDPE薄膜裁至1 cm×1 cm大小,分别取9片裁好的薄膜放入15 mL的30 g/L乙酸食品模拟物中及超纯水,其中酸性模拟物30 g/L乙酸用来模拟酸性食物,超纯水用来模拟水性食物。40 ℃ 10 d的测试条件可涵盖各种不同时间冷藏和冷冻的储存条件,包括最长2 h、最高70 ℃的加热或最长15 min、最高100 ℃的加热。置于40 ℃下储存10 d后,取出酸性模拟物,使用ICP-AES测定30 g/L乙酸中ZnO浓度。取出水性模拟物,并向其滴入1 mL HNO3后,使用ICP-MS测定水中ZnO浓度。
1.6 计算
膜中纳米ZnO含量由式1求出。
(1)
式(1)中:mZn为ICP-AES测得样品中Zn的含量,g;m0为ICP-AES测得空白样品中Zn的含量,g;mZnO为纳米ZnO的含量,g。
纳米ZnO的迁移量由式2求出。
纳米ZnO的迁移量(mg/g)=Cfood simulant×V/mfood simulant
(2)
式2中:Cfood simulant为食品模拟物中纳米ZnO的浓度,mg/L;V为待测食品模拟物的体积,L;mfood simulant为食品模拟物的质量,g。
纳米ZnO的迁移率由式3求出。
纳米ZnO的迁移率/%=(Cfood simulant×V/mZnO)×100
(3)
式(3)中:Cfood simulant为食品模拟物中纳米ZnO的浓度,mg/L;V为待测食品模拟物的体积,L;mZnO为纳米ZnO的含量,g。
本文中数据处理采用Minitab17进行处理,数据比较采用T检验方法,取95%置信度,即当P<0.05时有2组数据有显著性差异。
2 结果与分析
2.1 样品前处理条件
目前常用于聚合物消解的有微波消解及湿法消解2种方法,本试验中对比微波消解法及湿法消解法,观察薄膜消解情况,1 h后湿法消解的平底烧瓶中,纳米ZnO/LDPE薄膜仍存在未消解部分,而在相同的时间内,微波消解法将薄膜消解得更加彻底,效率更高。
2.2 方法的标准曲线、检出限及定量限
Zn在消解液中对应的线性方程为y=574x+174,相关系数(R)为0.999 8。对试剂空白溶液连续测定11次,以其结果标准偏差值的3倍计算检出限为0.03 mg/L,以其结果标准偏差的10倍计算定量限为0.1 mg/L。
Zn在30 g/L乙酸中对应的线性方程为y=14 093x+1 094,相关系数(R)为0.999 9,锌的质量浓度在0.1~5 mg/L范围内成线性,检出限为0.015 mg/L,定量限为0.05 mg/L。
Zn在超纯水中对应的线性方程为y=4 390.8x+17 499,相关系数(R)为0.999 8,锌的质量浓度在0.03~100 μg/L范围内成线性,检出限为0.03 μg/L,定量限为0.10 μg/L。
其中30 g/L乙酸中的纳米ZnO通过ICP-AES测定,超纯水中纳米ZnO通过ICP-MS测定。ICP-MS方法的检出限和定量限明显低于ICP-AES的检出限与定量限(P<0.05),由于水中ZnO的迁出量低于ICP-AES的定量限故采用ICP-MS进行检测。
2.3 方法的回收率及精密度
分别向聚四氟乙烯罐中放置0.100 g(精确到0.001 g) 1 cm×1 cm的空白膜及2种食品模拟物中放置9片1 cm×1 cm空白膜,分别添加低、中、 高3个水平的标样,进行回收率和精密度实验,每个浓度重复测定6次,进行结果分析,结果如表3所示,计算得薄膜中Zn含量的加标回收率为91.2%~110.2%,相对标准偏差(RSD)为0.3%~6.8%,ICP-AES与ICP-MS在低、中、高3个浓度下的RSD有明显差异(P<0.05),ICP-AES及ICP-MS检测方法都具有良好的准确性。
2.4 薄膜及食品模拟物中ZnO的含量
利用该检测方法对实验室自制纳米ZnO/LDPE薄膜及食品模拟物中的ZnO的含量进行测定,每个样品设定3个平行样品,取平均值,检测结果如表4所示。3种不同样品膜中纳米ZnO的含量均低于添加量,主要是因为纳米材料粒径小、易吸附,在造粒与制膜的过程中吸附在造粒机与吹塑机的料筒中,造成纳米ZnO的损耗,因此在接下来的迁移研究中迁移率的计算应用此方法测得的添加量作为初始含量(C0)。样品3中纳米ZnO含量显著高于样品2中纳米ZnO含量(P<0.05)是由于样品3中钛酸酯偶联剂的加入,表明偶联剂一方面可以改善复合膜中纳米颗粒的分散性、提高无机材料的填充性[22],同时可能对迁移能力产生影响。纳米ZnO向酸性模拟物中的迁移量明显大于向水中的迁移量(P<0.05),这一结论与纳米Ag与纳米TiO2向食品模拟物中迁移研究相似[20],这是由于酸性食品模拟物中氢离子促进了纳米ZnO的迁移。由于3种样品的初始含量不同,故通过比较迁移率的大小来比较纳米ZnO的迁移能力,在40 ℃ 10 d的迁移条件下样品1,样品2及样品3向30 g/L乙酸中的迁移率分别为22%,20%及18%,向超纯水中的迁移率分别为0.3%,0.18%及0.18%。其中,样品1向酸性及水性模拟液的迁移率明显高于样品2,其原因和机理正在进一步研究。样品2及样品3向水性食品模拟物的迁移率并没有差异(P>0.05),但向酸性食品模拟物,样品2的迁移能力明显高于样品3(P<0.05),说明40 ℃ 10 d下,在水性模拟液中偶联剂的加入对于纳米ZnO的迁移并没有明显作用,在酸性模拟物中,偶联剂的加入降低了纳米ZnO的向酸性食品模拟物的迁移能力。
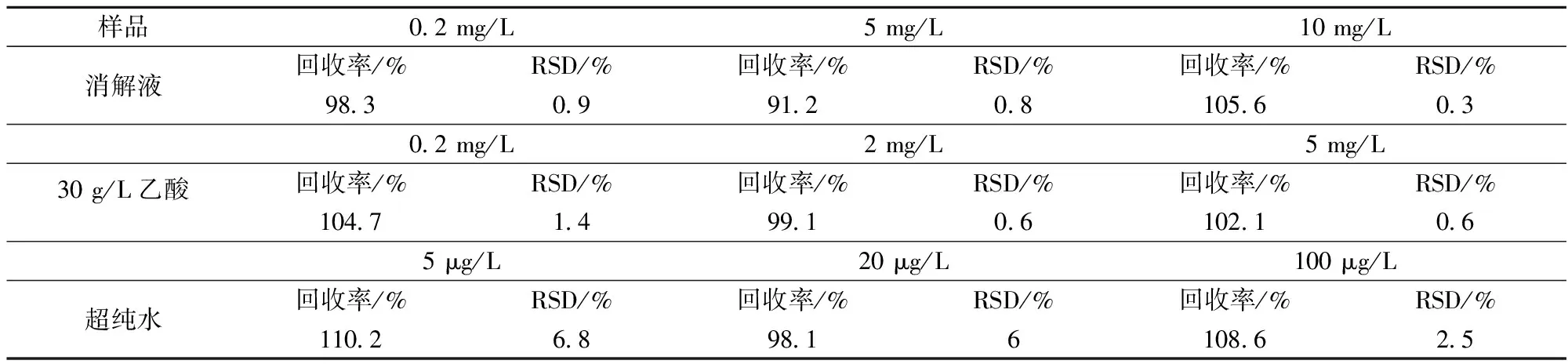
表3 Zn在食品模拟物及消解液中的加标回收和相对标准偏差(n=6)

表4 纳米ZnO/LDPE及食品模拟物中纳米ZnO的含量及其迁移率(n=6)
3 结论
(1)本文建立了纳米复合包装材料中ZnO的微波消解-ICP-AES检测方法及水性食品模拟物中ZnO的ICP-AES、ICP-MS检测方法,其中ICP-MS检测方法的检出限与定量限明显低于ICP-AES检测方法,适合于更加痕量ZnO的定量测定。(2)造粒及吹膜工艺会造成纳米ZnO的损失,偶联剂的加入改善了纳米颗粒的分散性,显著降低了纳米颗粒的损失,并且在40 ℃10 d的迁移条件下降低了纳米ZnO向酸性食品模拟物的迁移能力。(3)纳米ZnO在酸中迁移量明显高于在水中的迁移量,即纳米ZnO/LDPE薄膜包装酸性食品的安全隐患可能高于包装水性食品。这一检测方法的建立为后期研究纳米ZnO向食品中迁移的规律和机制打下了基础。
[1] 叶轻飏.纳米粒子改性LDPE薄膜的研制和保鲜性能研究[D].杭州:浙江大学,2014.
[2] LI B R, WANG X H, YAN M Y, et al. Preparation and characterization of nano-TiO2powder[J].Materials Chemistry and Physics, 2003,78(1):184-188.
[3] ESPITIA P J P, SOARES N F F, COIMBRA J S R, et al. Physical-mechanical and antimicrobial properties of nanocomposite films with pediocin and ZnO nanoparticles[J].Carbohydrate Polymer,2013,94(1):199-208.
[4] BUMBUDSANPHAROKE N, KO S.Nano-Food Packaging: An Overview of Market, Migration Research, and Safety Regulations[J].Journal of Food Science,2015,80(5):910-923.
[6] ARFAT Y A,BENJAKUL S,PRODPRAN T,et al. Properties and antimicrobial activity of fish protein isolate/fish skin gelatin film containing basil leaf essential oil and zinc oxide nanoparticles[J].Food Hydrocolloids,2014,41(20):265-273.
[7] MARAMBIOJONES C, HOEK E M V.A review of the antibacterial effects of silver nanomaterials and potential implications for human health and the environment [J].Journal of Nanoparticle Research,2010,12(5):1 531-1 551.
[8] 刘颖,陈春英. 纳米材料的安全性研究及其评价[J].科学通报,2011,56(2):119-125.
[9] Code of Fedcral Regulations Title 21 182.899[S].Federal Food and Drug Administration,2008.
[10] European Commission.2011. Commission Regulation (EU) No 1282/2011 of 28 November[S].Offcial Journal of the European Union,2011.
[11] AABDORREZA M N, CHENG L H, KARIM A A. Effects of plasticizers on thermal properties and heat sealability of sago starch films[J]. Food Hydrocolloids,2011,25(1):56-60.
[12] NAFCHI A M, NASSIRI R, SHEIBANI S, et al.Preparation and characterization of bionanocomposite films filled with nanorod-rich zinc oxide[J].Carbohydrate Polymers,2013,96(1):233-239.
[13] ELEN K, MURARIU M, PEETERS R,et al.Towards high-performance biopackaging: barrier and mechanical properties of dual-action polycaprolactone/zinc oxide nanocomposites[J].Polymers for Advanced Technologies, 2012,23(10):1 422-1 428.
[14] DIEZ-PASCUAL A M, DIEZ-VICENTE A L. ZnO-Reinforced Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) Bionanocomposites with Antimicrobial Function for Food Packaging[J].Acs Applied Materials and Interfaces,2014,6(12):9 822-9 834.
[15] ESPITIA P J P, SOARES N F F, COIMBRA J S R. Zinc oxide nanoparticles: synthesis, antimicrobial activity and food packaging applications[J].Food and Bioprocess Technology.2012,5(5):1 447-1 464.
[16] BRAYNER R,FERRARIILIOU R,BRIVOIS N,et al. Toxicological impact studies based onEscherichiacolibacteria in ultrafine ZnO nanoparticles colloidal medium[J].Nano Letters,2006,6(4):866-870.
[17] EMAMIFAR A,KADIVAR M,SHAHEDI M, et al. Effect of nanocomposite packaging containing Ag and ZnO on inactivation ofLactobacillusplantarumin orange juice[J].Food Control,2011,3(22):408-413.
[18] ESMAILZADEH H, SANGPOUR P, SHAHRAZ F.Effect of nanocomposite packaging containing ZnO on growth ofBacillussubtilisandEnterobacteraerogenes[J].Materials Science and Engineering:C,2016,58:1 058-1 063.
[19] PANEA B, RIPOLL G, GONZA′LEZ J, et al. Effect of nanocomposite packaging containing different proportions of ZnO and Ag on chicken breast meat quality[J].Journal of Food Engineering,2014,123(2):104-112.
[20] ECHEGOYEN Y,RODRGUEZS,NERN C.Nanoclay migration from food packaging materials[J].Food Additives and Contaminants, 2016,33(3):530-539.
[21] CUSHEN M, KERRY J, MORRIS M, et al. Silver migration from nanosilver and a commercially available zeolite filler polyethylene composites to food simulants[J].Food Additives and Contaminants,2014,31(6):1 132-1 140.
[22] 李红玲, 董斌, 韩延, 等. 钛酸酯偶联剂的偶联机理及研究进展[J].表面技术,2014,41(4):99-102.
Quantification of ZnO in nano ZnO /LDPE food packaging films and food simulant
SHI Ying-chun1,HU Chang-ying2,3*, HUANG Jin-yu4
1(Packaging Engineering Institute of Jina University, Zhuhai 519070, China) 2(Department of Food Science and Engineering of Jinan University, Guangzhou 510632, China) 3(Key Laboratory of Product Packaging and Logistics of Guangdong Higher Education Institutes, Zhuhai 519070, China) 4(Guangdong Inspection and Quarantine Technology Center, Guangzhou 510623, China)
Zinc oxide (ZnO) was determined in nano-zinc oxide food packaging and food simulants by microwave digestion with inductively coupled plasma atomic emission spectrometry (ICP-AES) and inductively coupled plasma mass spectrometry (ICP-MS). According to the European Union regulation (EU 10/2011), 3% acetic acid was chosen and ultrapure water was used as food simulants, the test was carried out at 40 ℃ for 10 days. The amount of ZnO in food simulant was analyzed by ICP-AES and ICP-MS. The results showed the calibration curve of Zn was linear in the range of 0.1-5 mg/L with correlation coefficients no less than 0.9998. The spiked recoveries at three spiked levels were in the range of 91.2%-110.2% with relative standard deviations (RSD) of 0.3%-6.8%. The limit of detection (LOD) was 0.015 mg/L, 0.03 mg/L and 0.03 μg/L respectively; the limit of quantitation (LOQ) was 0.05 mg/L, 0.1 mg/L and 0.1 μg/L respectively. This method was precise, highly sensitive and accurate. This method was applied in determination of nano ZnO amount in three types of film and result was (4.71±0.19) g/kg, (9.20±0.49) g/kg and 12.87±0.33 g/kg respectively. The amount of nano ZnO in 3% acetic acid food simulates at 40 ℃ for 10 days was (2.35±0.02) mg/kg, (3.54±0.01) mg/kg and (4.12±0.35) mg/kg respectively; the amount of nano ZnO in ultrapure water simulate at 40 ℃ for 10 days was (24.65±0.68) μg/kg,2(4.80±1.25) μg/kg and (45.85±0.32) μg/kg, respectively.
nano Zinc oxide (nano-ZnO); low density polyethylene (LDPE); microwave digestion; inductively coupled plasma atomic emission spectrometer (ICP-AES); inductively coupled plasma mass spectrometry (ICP-MS)
10.13995/j.cnki.11-1802/ts.201703040
硕士研究生(胡长鹰教授为通讯作者,E-mail:hucy 0000@sina.com)。
国家自然科学基金(31571762, 21277061);国家质检总局科技项目(2014IK078)
2016-07-08,改回日期:2016-08-31
