β-隐黄素纳米乳的制备及其稳定性研究
2017-04-26孙志高黄巧娟盛冉郝静梅
孙志高,黄巧娟,盛冉,郝静梅
(西南大学柑桔研究所,重庆 北碚,400712)
β-隐黄素纳米乳的制备及其稳定性研究
孙志高*,黄巧娟,盛冉,郝静梅
(西南大学柑桔研究所,重庆 北碚,400712)
以D-柠檬烯为油相,采用低能乳化法制备β-隐黄素纳米乳。对比研究了温度、光照对β-隐黄素纳米乳及β-隐黄素油溶液的影响,以及酸、碱、氧化剂和还原剂对β-隐黄素纳米乳的影响。结果发现:所制备的β-隐黄素纳米乳平均粒径为12.14 nm;β-隐黄素纳米乳比β-隐黄素油溶液更耐热、耐光;短时间强酸强碱环境对β-隐黄素纳米乳稳定性影响较小,但长时间的强酸条件会加速β-隐黄素的降解,而强碱条件会使β-隐黄素纳米乳变浑浊;高浓度的氧化剂会使β-隐黄素纳米乳有轻微降解,而还原剂对β-隐黄素纳米乳具有一定的保护作用。因此,β-隐黄素纳米乳比β-隐黄素油溶液具有更好的稳定性,但仍需避免长时间处于强酸强碱环境。
β-隐黄素;纳米乳;制备;稳定性
β-隐黄素为类胡萝卜素的一种,具有抗癌、抗氧化、预防骨质疏松、降低关节炎、改善脂质代谢、转化为VA等生理功能,在食品、医药、化妆品等行业具有广泛的应用前景[1]。在结构上,β-隐黄素为聚异戊二烯复合物,含有多烯双键及羟基等氧代基团,对光、热、氧及其他加工条件敏感,容易分解,难于稳定存在于产品之中[2]。此外,β-隐黄素为脂溶性色素,不溶于水,极大地限制了β-隐黄素的应用。如何提高β-隐黄素的生物利用度及其在各类产品中的稳定性、增加其水溶性等是拓宽β-隐黄素应用范围亟需解决的关键问题。
纳米乳是指平均粒径为10~100 nm的乳状液,具有粒径小、高透明度且动力学稳定等特点,常被应用于医药、化工等领域[3]。纳米乳能负载类胡萝卜素类色素,如β-胡萝卜素[4]、番茄红素[5-6]、辣椒红素[7]等,且所制备的类胡萝卜素纳米乳能有效地提高类胡萝卜素的生物利用度及稳定性[8-9]。然而,目前制备色素纳米乳时多采用有机溶剂溶解色素,所制备的纳米乳可能存在有机溶剂残留问题。因此,若能找到有机溶剂替代剂,并将其运用于纳米乳的制备中,对色素纳米乳的制备具有重要意义。D-柠檬烯是柑桔精油的主要成分,为一种单环单萜烯,具有抗癌、抗氧化等多种生理功能[10]。此外,D-柠檬烯具有较强的溶解能力,可以作为烷烃等有机溶剂的绿色替代剂,且具有安全性高、溶解效果好等优点[11-14]。研究表明,D-柠檬烯还可以作为油相,运用于纳米乳的制备中,制备出粒径小,且稳定性好的纳米乳[15]。本试验尝试以D-柠檬烯替代烷烃类试剂作为油相,溶解β-隐黄素,采用低能乳化法制备出安全性高、稳定性好的β-隐黄素纳米乳,以拓宽β-隐黄素的使用范围。
1 材料与方法
1.1 试验材料与试剂
β-隐黄素(纯度>90%)、D-柠檬烯(纯度>90%)、吐温-80、吐温-60、司班-20、司班-60、恒温水浴锅、双束可见-紫外分光光计、冷冻离心机、氯化钠、氢氧化钠、盐酸、双氧水、激光粒度仪(马尔文 Zetasizer Nano-ZS90)。
1.2 试验方法
1.2.1 表面活性剂的筛选
将吐温-60、吐温-80、司班-60和司班-20按照一定的比例配制成不同亲水亲油平衡(HLB)值的混合乳化剂,加入固定的油相(D-柠檬烯),将乳化剂和油相按一定比例混合后,用恒温磁力搅拌器使乳化剂和油相充分混合,并同时匀速滴加蒸馏水,观察纳米乳的形成情况。
1.2.2 β-隐黄素纳米乳的制备
参考李娅男[16]和KOMAIKO[17]等的制备方法,并稍作改进,制备空白纳米乳。将一定量的乳化剂及D-柠檬烯在小烧杯中混合均匀,并用滴管缓慢逐滴滴加蒸馏水,且确保每滴蒸馏水被充分搅拌和分散,待蒸馏水滴加完成后,再将制备的乳状液于恒温磁力搅拌器上充分搅拌直至纳米乳形成。
将一定量的β-隐黄素加入40 ℃水浴的D-柠檬烯中,搅拌均匀即得β-隐黄素油溶液。参照空白纳米乳的制备方法及合适配方制备β-隐黄素纳米乳。
1.2.3β-隐黄素纳米乳最大吸收波长的测定
吸取一定量制备好的β-隐黄素纳米乳(或空白纳米乳)于1 cm比色皿中,在紫外分光光度计上进行波长300~600 nm范围扫描,经图谱比较确定β-隐黄素纳米乳的最大吸收峰。
1.2.4 β-隐黄素纳米乳粒度测定
利用马尔文 Zetasizer Nano-ZS 90 激光粒度仪在 25℃下测量纳米乳粒径,设定平衡时间为 60 s、间隔时间为10 s、每次扫描 3 次,测平均值。
1.2.5 稳定性试验[5,18-19]
(1)离心试验:取乳状液10 mL于离心管中,设置转速为10 000 r/min,离心20 min,观察是否有色素上浮,若色素上浮则表明该乳状液并非是纳米乳,其稳定性较差。
(2)稀释稳定性试验:用蒸馏水与β-隐黄素纳米乳按一定比例稀释,观察稀释后的纳米乳溶液是否出现分层现象,若出现分层,则表明所制备的纳米乳稀释稳定性较差。
(3)温度的影响:制备同浓度的β-隐黄素纳米乳及β-隐黄素油溶液各100 mL,立即测其吸光度。取7份10 mL的纳米乳(或油溶液)分别置于50 mL锥形瓶中,将锥形瓶置于30 ℃、40 ℃、50 ℃、60 ℃、70 ℃、80 ℃和90 ℃的水浴锅中,每隔一段时间,测定样品的吸光度,计算β-隐黄素的残存率,其计算公式如下:
(1)
(4)光照的影响:制备2份50 mL相同浓度的β-隐黄素纳米乳及β-隐黄素油溶液,立即测其吸光度。取3份15 mL的纳米乳(或油溶液)分别置于50 mL锥形瓶中,将锥形瓶分别置于暗室、日光灯室、紫外灯室,每隔一段时间测定样品的吸光度,并计算β-隐黄素的残存率。
(5)酸碱的影响:制备β-隐黄素纳米乳,并将其分为5份,每份为9.5 mL,再向每份样品中滴加质量浓度分别为1.00%、2.00%、3.00%、4.00%和5.00%的HCl溶液0.5 mL,使得最终溶液中HCL质量浓度为0.05%、0.10%、0.15%、0.20%和0.25%;然后置于暗处,每隔2 h测定其吸光度。同时,用同样方法研究NaOH对β-隐黄素纳米乳的影响。
(6)氧化剂及还原剂的影响:选用H2O2作为氧化剂、Vc作为还原剂,将其配置成一定浓度,并加入到β-隐黄素纳米乳中,使氧化剂及还原剂的最终浓度为0.10%、0.50%、1.00%。
2 实验结果
2.1 表面活性剂的筛选
表1为不同表面活性剂制备空白纳米乳的情况。制备D-柠檬烯纳米乳较为理想的表面活性剂为吐温60/吐温80系列。在乳化的过程中,发现滴加一定量水相后会出现液晶相,若液晶相为无色透明状则表明该乳化剂易于形成纳米乳,反之若液晶相为白色(凝胶)则表明该乳化剂较难甚至不能形成纳米乳,故纳米乳的形成与该液晶相有较大的关联度。因从初步筛选表面活性剂时发现,用较多的吐温80更有利于纳米乳的形成,故后续实验选用100%的吐温80作为表面活性剂。

表1 表面活性剂的筛选
2.2 β-隐黄素纳米乳的制备
图1为利用马尔文激光粒度仪对制备好的β-隐黄素纳米乳进行粒度测定的情况。从图1中可以看出,β-隐黄素纳米乳粒径主要集中在10 nm左右,平均粒径为12.14 nm,测定结果表明平均粒径符合纳米乳要求。此外,制备的β-隐黄素纳米乳外观为透明状,黏度极低,符合纳米乳的表观特征。
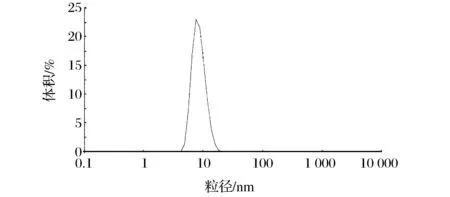
图1 β-隐黄素纳米乳的平均粒径Fig.1 Average particle size of β-cryptoxanthin nanoemulsion
2.3 β-隐黄素纳米乳稳定性实验
2.3.1 离心实验
本实验制备的β-隐黄素纳米乳经离心后,未观察到分层及絮凝现象,这表明所制备的β-隐黄素纳米乳较为稳定。
2.3.2 稀释稳定性
制备的β-隐黄素纳米乳能以任意比例与水混溶,未观察到油水分层现象,这证明所制备的β-隐黄素纳米乳具有良好的稀释稳定性。
2.3.3 最大吸收波长的确定
图2为β-隐黄素纳米乳及空白纳米乳的紫外扫描吸收峰。由图2可见,β-隐黄素纳米乳的最大吸收峰均为451 nm,与β-隐黄素标准品的最大吸收峰相同,且在此波长处空白纳米乳无吸收,这表明β-隐黄素纳米乳在此波长处检测时无吸收干扰,故选择451 nm为测定波长。

图2 纳米乳光谱扫描曲线Fig.2 spectral scanning curves of nanoemulsion
2.3.4 温度对β-隐黄素纳米乳及β-隐黄素油溶液的影响
图3为β-隐黄素纳米乳在不同温度下的变化。

图3 温度对β-隐黄素纳米乳的影响Fig.4 Effect of temperature on β-cryptoxanthinnanoemulsion
从图3中可以看出,低温对β-隐黄素纳米乳的影响较小,在温度低于70 ℃时随着加热时间的延长β-隐黄素纳米乳中的β-隐黄素几乎不会降解;温度为80 ℃时长时间加热β-隐黄素会有少量降解;当温度高于90 ℃时,受热时间越长其β-隐黄素降解越快。温度对β-隐黄素油溶液的影响很大,且出现溶液变浑浊的现象,这可能是高温使得油相D-柠檬烯挥发、β-隐黄素发生降解造成的。如表2所示,在90 ℃加热1 h后,β-隐黄素油溶液中β-隐黄素降解很明显,在加热2 h后,β-隐黄素几乎完全降解。在80 ℃加热3 h、70 ℃加热4 h后,β-隐黄素油溶液中β-隐黄素也几乎完全降解。此实验表明,β-隐黄素不耐高温,在长时间的高温条件下容易降解;β-隐黄素纳米乳的耐热性强于β-隐黄素油溶液。

表2 温度对β-隐黄素纳米乳及油溶液的影响
2.3.5 光照对β-隐黄素纳米乳及β-隐黄素油溶液的影响
从图4与图5可以看出,日光灯照射对β-隐黄素纳米乳及β-隐黄素油溶液的影响很小,在放置65 h后β-隐黄素几乎没有降解;但紫外灯照射对β-隐黄素纳米乳及其油溶液的影响较大,纳米乳置于紫外光20 h后β-隐黄素开始降解,在65 h后β-隐黄素残存率约为58%。从图5可以看出,紫外灯光对β-隐黄素油溶液的影响很大,在紫外灯下暴露6 h后,β-隐黄素油溶液中β-隐黄素开始降解,降解速度非常快,在暴露30 h后β-隐黄素几乎完全降解。由此可看出:日光灯对β-隐黄素纳米乳及β-隐黄素油溶液的影响较小,紫外灯光对两者影响较大,但纳米乳对β-隐黄素具有一定的保护作用。
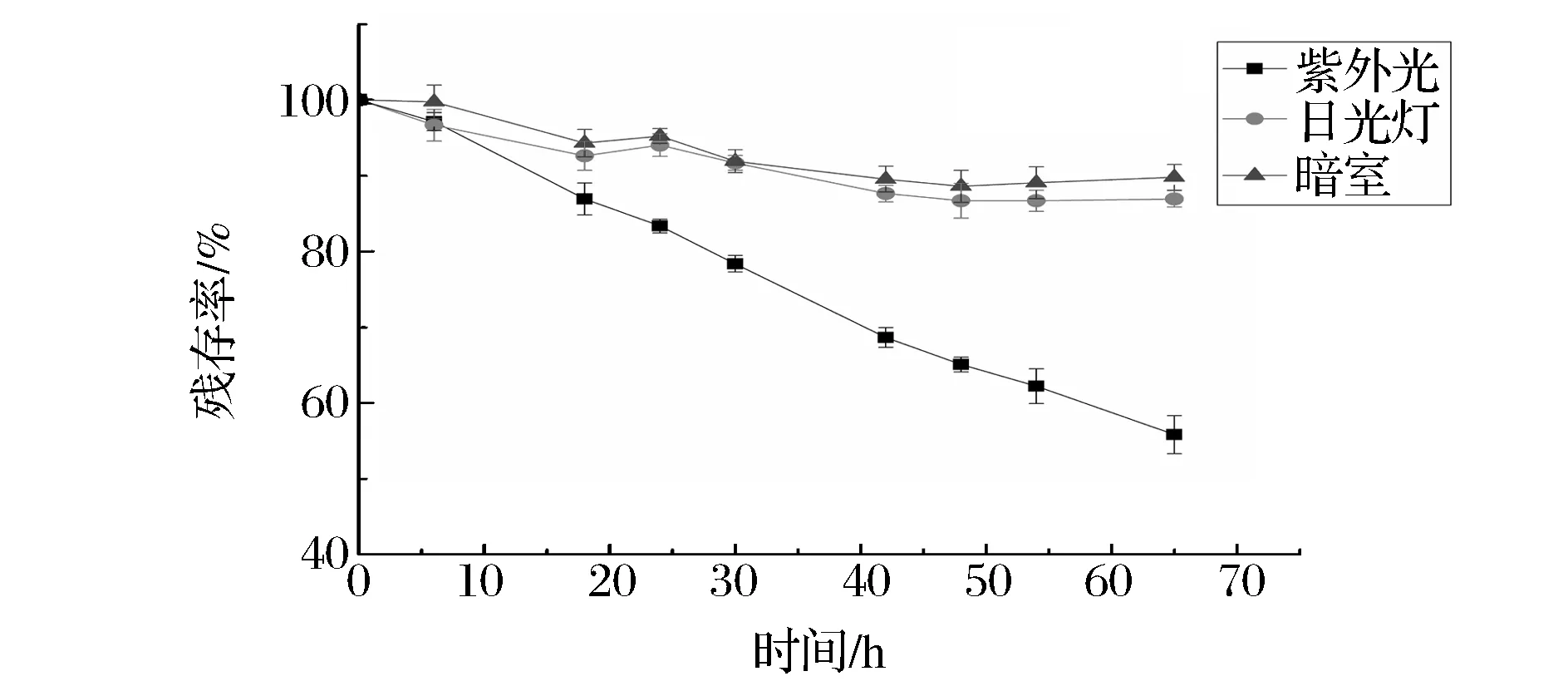
图4 光照对β-隐黄素纳米乳的影响Fig.4 Effect of light on β-cryptoxanthine nanoemulsion

图5 光照对β-隐黄素油溶液的影响Fig.5 Effect of light on β-cryptoxanthine oil solution
2.3.6 酸、碱对β-隐黄素纳米乳的影响
从图6可以看出,强酸和强碱对β-隐黄素纳米乳均具有一定的影响。随着酸浓度的增加和时间的延长,β-隐黄素逐渐降解,但降解速度较为缓慢,时间少于4 h时影响非常小。随着碱浓度的增大和时间的延长,β-隐黄素纳米乳发生一定的变化;在时间少于4 h时强碱对β-隐黄素几乎没有影响,但时间超过4 h后,加入浓度为0.10%以上强碱的纳米乳液开始出现轻微浑浊,可能是生成某种物质所致。因此,β-隐黄素纳米乳可以增强抗强酸和强碱的性能,但仍不宜长时间放置在强酸和强碱的环境中。
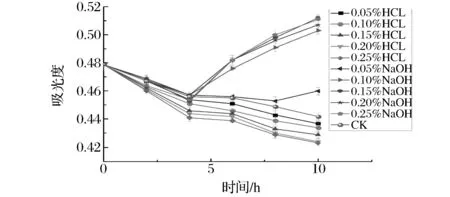
图6 酸碱对β-隐黄素纳米乳的影响Fig.6 Effect of acid and alkali onβ-cryptoxanthine nanoemulsion
2.3.7 氧化剂及还原剂对β-隐黄素纳米乳的影响
图7与图8为氧化剂和还原剂对β-隐黄素纳米乳的影响。从图7可以看出,氧化剂双氧水对β-隐黄素纳米乳具有一定的影响,随着双氧水浓度的增加,β-隐黄素会进行缓慢降解,即表明β-隐黄素纳米乳具有较强的耐氧化性。从图8可以看出,还原剂Vc对β-隐黄素纳米乳的稳定性影响很小,不同浓度的Vc对β-隐黄素纳米乳影响几乎无差异。与对照组相比,加入Vc的纳米乳β-隐黄素降解较低,即Vc对β-隐黄素纳米乳的稳定性起到增效作用,能减缓β-隐黄素的氧化。SASAKI等曾利用Vc来增加β-隐黄素水溶液的稳定性,并将其运用于食品和饮料中[20]。
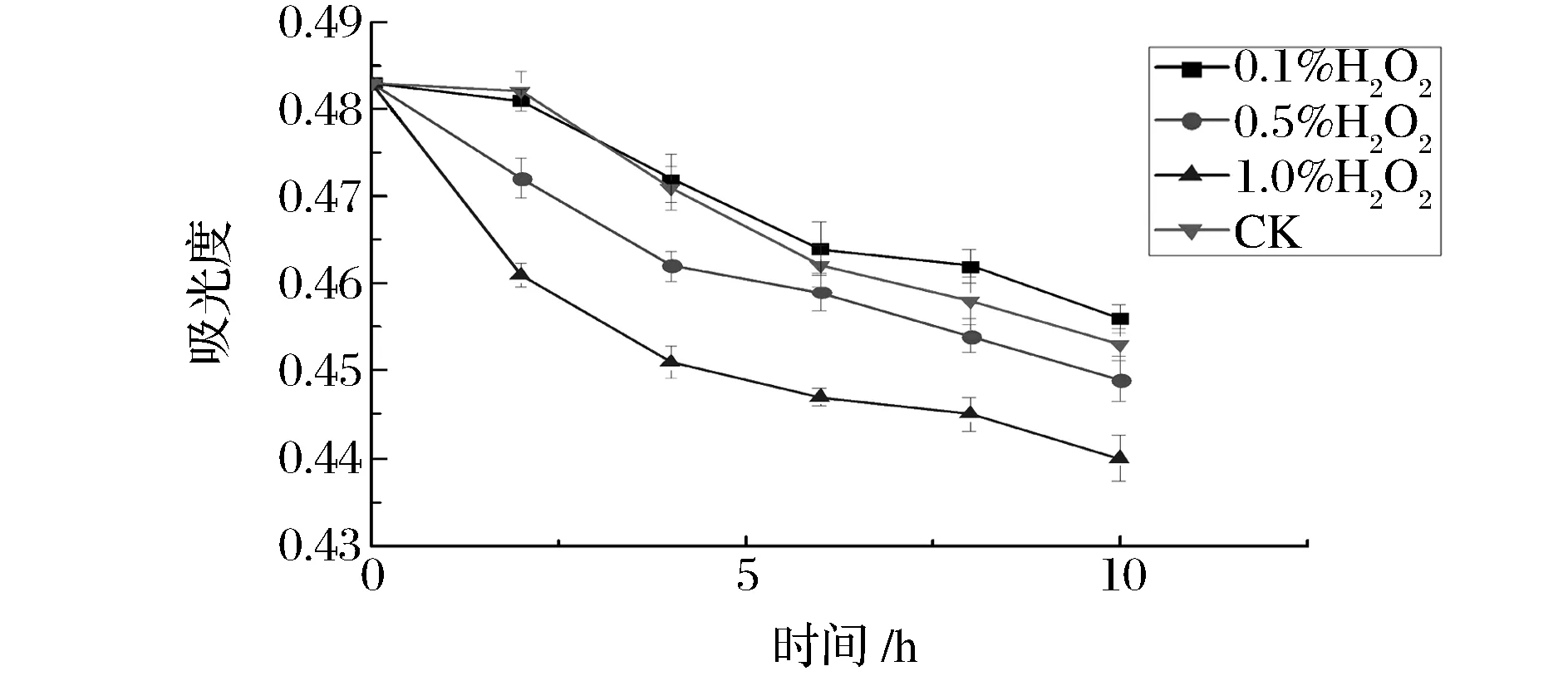
图7 氧化剂对β-隐黄素纳米乳的影响Fig.7 Effect of oxidanton β-cryptoxanthine nanoemulsion
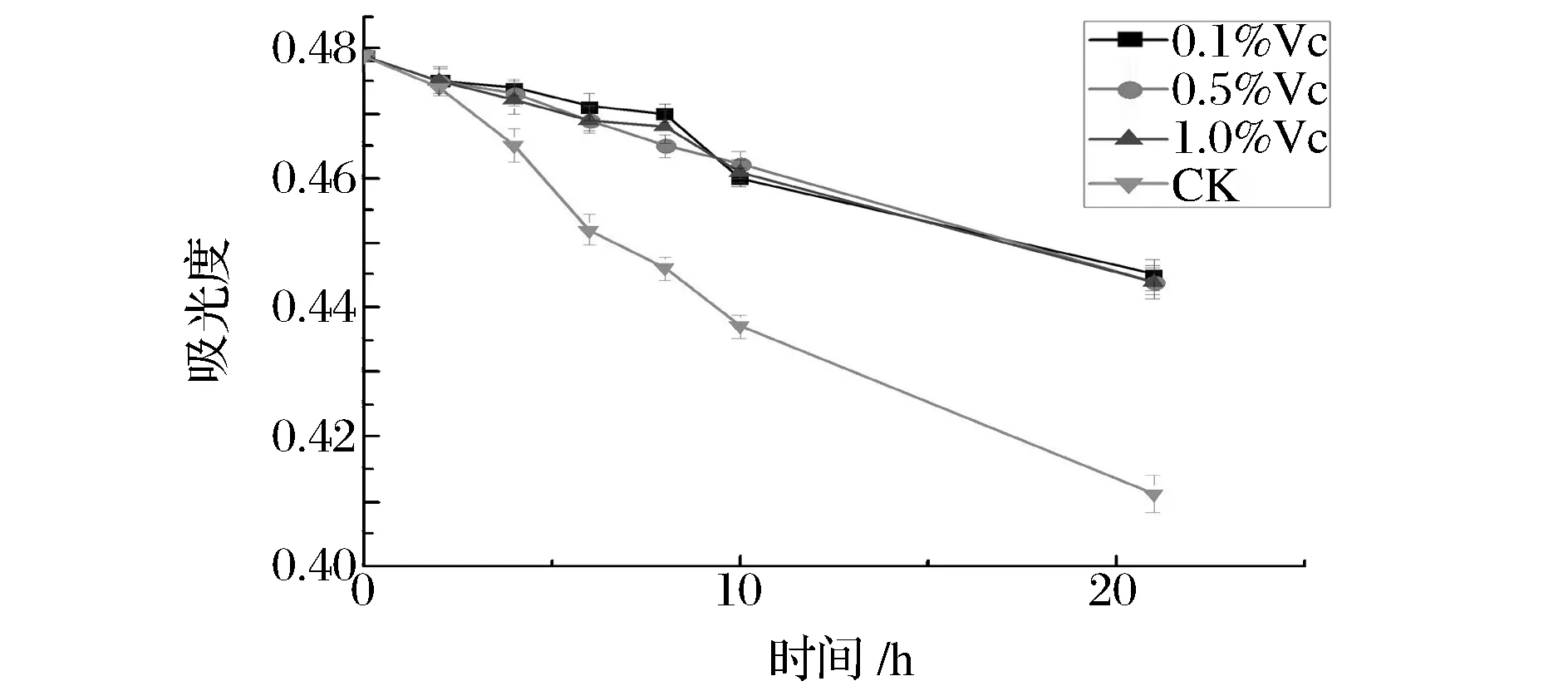
图8 还原剂对β-隐黄素纳米乳的影响Fig.8 Effect of reducer on β-cryptoxanthine nanoemulsion
3 结论
本试验利用D-柠檬烯溶解β-隐黄素制备了平均粒径为12.14 nm的β-隐黄素纳米乳,并对β-隐黄素纳米乳及β-隐黄素油溶液进行了稳定性试验。结果发现,温度对β-隐黄素纳米乳及β-隐黄素油溶液均有一定影响,与油溶液相比纳米乳对温度的耐受性更强,且不易发生化学反应,增强了β-隐黄素的稳定性。日光灯光对β-隐黄素纳米乳及油溶液的影响均较小,而紫外灯光对两者的影响均较大,且在30 h后β-隐黄素油溶液中色素几乎全部降解,而纳米乳对β-隐黄素具有较强的保护作用。β-隐黄素纳米乳能耐受一定的强酸强碱,且具有较强的耐氧化性。此外,还原剂Vc对β-β-隐黄素纳米乳具有一定的保护作用,可使其更加稳定。
因此,β-隐黄素纳米乳较β-隐黄素油溶液具有更好的稳定性;β-隐黄素纳米乳能以任意比例与水混溶,大大增强了β-隐黄素的水溶性。此外,为了增强β-隐黄素纳米乳的稳定性可在制备纳米乳时同时添加少量Vc;为了保持β-隐黄素的生物活性,β-隐黄素纳米乳应尽量避免长时间与强酸和强碱接触,并避免长时间处于高温及紫外灯照射环境。
[1] BURRI B J. Beta-cryptoxanthin as a source of vitamin A.[J]. Journal of the Science of Food & Agriculture, 2015,95(9):1 786-1 794.
[2] 李涛, 张慧, 张志忠,等. β-隐黄质的特性及其应用[J]. 中国食品添加剂, 2011(4):156-158.
[3] 陈风平, 刘晨光. 纳米乳研究进展[J]. 生物技术通报, 2013(12):43-48.
[4] 王大红. β-胡萝卜素乳剂的性状和稳定性的影响因素研究[D].武汉:华中农业大学,2006.
[5] 孙莹. 番茄红素纳米分散体的制备及稳定性研究[D].无锡:江南大学,2008.
[6] KIM S O, HA T V A,CHOI Y J, et al. Optimization of homogenization-evaporation process for lycopene nanoemulsion production and its beverage applications[J]. Journal of Food Science, 2014, 79(8): 1 604-1 610.
[7] 胡江良. 辣椒红色素提取脱辣及乳化研究[D].昆明:昆明理工大学,2008.
[8] SALVIA-TRUJILLO L,MCCLEMENTS D J. Improvement of β-carotene bioaccessibility from dietary supplements using excipient nanoemulsions[J]. Journal of Agricultural and Food Chemistry, 2016,64(22):4 639-4 647.
[9] HO N H,INBARAJ B S, CHEN B H. Utilization of microemulsions from rhinacanthus nasutus (L.) Kurz to improve carotenoid bioavailability[J]. Scientific Reports, 2016, 6:25426.
[10] 黄巧娟,孙志高,龙勇,等.D-柠檬烯抗癌机制的研究进展[J]. 食品科学,2015,36(7):240-244.
[11] FAURE K, BOUJU E, SUCHET P, et al. Use of limonene in countercurrent chromatography: a greenalkane substitute[J].Analytical Chemistry, 2013, 85(9): 4 644-4 650.
[12] CHWMAT S, TOMAO V, CHEMAT F. Limonene as Green Solvent for Extraction of Natural Products[M]//Green Solvents I. Springer Netherlands, 2012: 175-186.
[13] DEJOYE TANZI C, ABERT VIAN M, CHEMAT F. New procedure for extraction of algal lipids from wet biomass: A green clean and scalable process[J].Bioresource Technology, 2013, 134: 271-275.
[14] 黄巧娟, 黄林华, 孙志高,等. 柠檬烯的安全性研究进展[J]. 食品科学, 2015, 36 (15) : 277-281.
[15] OSTERTAG F, WEISS J, MCCLEMENTS D J. Low-energy formation of edible nanoemulsions: Factors influencing droplet size produced by emulsion phase inversion[J]. Journal of Colloid & Interface Science, 2012, 388(1):95-102.
[16] 李娅男.D-柠檬烯纳米乳的制备与应用研究[D]. 北京:北京化工大学, 2013.
[17] KOMAIKO J, MCCLEMENTS D J. Optimization of isothermal low-energy nanoemulsion formation: hydrocarbon oil, non-ionic surfactant, and water systems.[J]. Journal of Colloid & Interface Science, 2014, 425(7):59-66.
[18] 安红丽. 原花青素纳米乳的研制[D]. 杨凌:西北农林科技大学, 2007.
[19] 蒋国玲. 温州蜜柑皮β-隐黄素的提取、纯化及稳定性研究[D]. 重庆:西南大学, 2012.
[20] SASAKI T,TAKAYAMA K. Stabilized beta cryptoxanthin-containing water and the use thereof: US, US20120156333 A1[P]. 2012.
Preparation and stability of β-cryptoxanthin nanoemulsion
SUN Zhi-gao*,HUANG Qiao-juan,SHENG Ran,HAO Jing-mei
(Citrus Research Institute, Southwest University, Chongqing 400712, China)
Nanoemulsion of β-cryptoxanthin was prepared byD-limonene as oil phase. The effect of temperature and light on β-cryptoxanthin nanoemulsion and β-cryptoxanthin oil solution were compared. The effect of acid, alkali, oxidant, reducer to β-cryptoxanthin nanoemulsion was also studied. The results are: average particle size of β-cryptoxanthin nanoemulsion 12.14nm; β-cryptoxanthin nanoemulsion has better resistance of heat and light; acid and alkali has a little effect of β-cryptoxanthin nanoemulsion in short time; however strong acid accelerated β-cryptoxanthin degradation and strong alkali made β-cryptoxanthin nanoemulsion solution cloudy at long time. High concentration oxidant can cause slightly degradation while reducing agent has certain protection to β-cryptoxanthin nanoemulsion. So, β-cryptoxanthin nanoemulsion has better stability, and needs to avoid in strong acid and alkali.
β-cryptoxanthin; nanoemulsion; preparation; stability
10.13995/j.cnki.11-1802/ts.201703031
副研究员(本文通讯作者,E-mail:cpro@cric.cn)。
重庆市科技支撑示范工程项目(cstc2014fazktjcsf80034)
2016-06-28,改回日期:2016-08-19
