联合培美曲塞与联合紫杉醇的三线化疗方案治疗晚期乳腺癌的有效性和安全性比较
2017-04-26黄新恩
钱 婷, 黄新恩
(南京医科大学附属江苏省肿瘤研究所 江苏省肿瘤医院 化疗科, 江苏 南京, 210009)
联合培美曲塞与联合紫杉醇的三线化疗方案治疗晚期乳腺癌的有效性和安全性比较
钱 婷, 黄新恩
(南京医科大学附属江苏省肿瘤研究所 江苏省肿瘤医院 化疗科, 江苏 南京, 210009)
乳腺癌; 培美曲塞; 紫杉醇; 化疗; 安全性; 有效性
蒽环类或以紫衫为基础的化疗方案被认为是治疗Her-2阴性的晚期乳腺癌的一线方案[1-5]。培美曲塞作为多靶点的抗叶酸制剂,可抑制胸苷酸合酶、二氢叶酸还原酶(DHFR)和甘氨酰胺核苷酸转移酶(GARFT),并展现了其在多个肿瘤类型中的抗肿瘤活性[6-8]。本研究探讨联合培美曲塞的化疗方案与联合紫杉醇化疗方案治疗晚期乳腺癌三线化疗时的有效性与安全性,现报告如下。
1 资料与方法
1.1 一般资料
选取2009年1月—2016年2月109位晚期乳腺癌患者。所有患者在一线以及二线化疗后均复发。随机分为A组52例和B组57例,患者特征见表1。纳入标准: ① 病理诊断为晚期乳腺癌(ⅢB或Ⅳ), 一线以及二线化疗失败, KPS评分≥70分; ② 至少有一个转移部位; ③ 在治疗前签署知情同意书; ④ 心电图正常; ⑤ 白细胞≥4.0×109/L, 血红蛋白≥80 g/L, 血小板≥80×109/L; ⑥ ALT≤正常上限的2倍,胆红素≤正常上限,肌酐≤正常上限。排除标准: ① 不能忍受化疗; ② 同时患有其他肿瘤; ③ 产生了无法忍受的过敏反应。
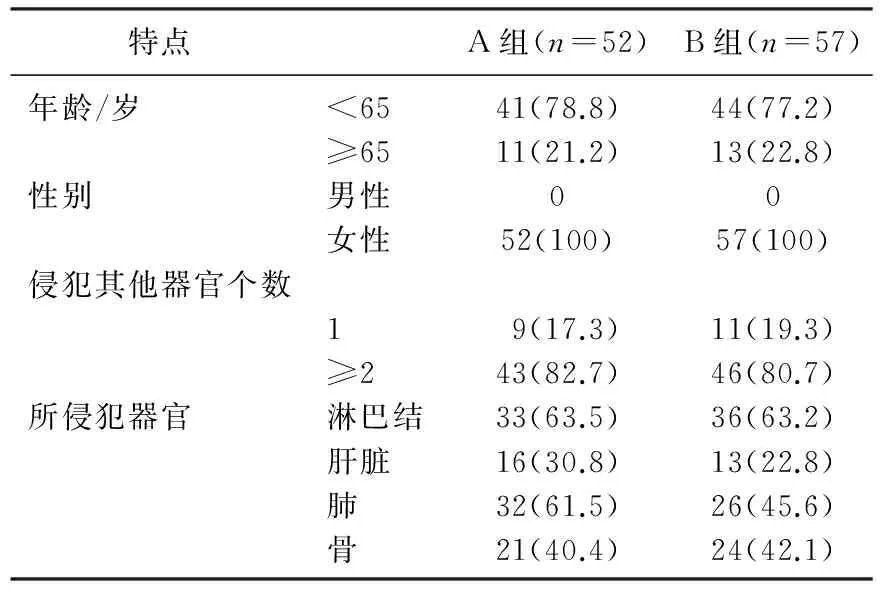
表1 2组患者一般资料比较
1.2 方法
A组:培美曲塞预处理参考相关文献[9], 预处理之后病人接受培美曲塞500 mg/m2和其他化疗药物,包括洛铂(卡铂)或表柔比星。B组:紫杉醇预处理参考相关文献[10],在预处理之后,患者接受135 mg/m2剂量的静脉滴注的紫杉醇化疗方案。2个周期化疗之后,采用CT评估病情变化,具体评价可参照RECIST标准,包括完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)。
2 结 果
A组疗效为CR 1例, PR 9例, SD 11例, PD 31例。B组疗效为CR 0例, PR 12例, SD 8例, PD 37例。A组疾病缓解率(CR+PR)为19.2%, B组为21.1%, 差异无统计学意义(P=0.903)。A组疾病控制率(CR+PR+SD)为40.4%, B组为35.1%, 差异无统计学意义(P=0.905)。所有患者的副反应均根据WHO分级标准评估。A组中22例患者有副反应,主要为骨髓抑制(30.8%), 13.4%患者发生肝肾功能损伤, 7.7%患者出现呕吐,无1例因副反应停止治疗。B组中41例患者出现副反应,包括36例骨髓抑制(6例患者达到3~4度), 26例肝肾损伤(45.6%), 25例呕吐(43.9%), 3例皮疹, 2例腹泻。未发生因副反应导致死亡的患者。2组副反应比较有显著差异(P=0.032)。见表2。
3 讨 论
紫杉醇被广泛用于晚期乳腺癌的治疗[11], 大多数患者在一线治疗之后,病情会继续进展,需要接受二线甚至三线化疗[12]。有研究[13]表明,胸苷酸合酶的肿瘤表达与培美曲塞的抗肿瘤活性存在关联,培美曲塞有比5-Fu更多的分子靶点,并且在治疗间皮瘤[14-17]、非小细胞肺癌[18-20]上有明确疗效。研究[21]表明以培美曲塞为基础的化疗方案在多种晚期肿瘤包括乳腺癌的治疗中有一定作用。
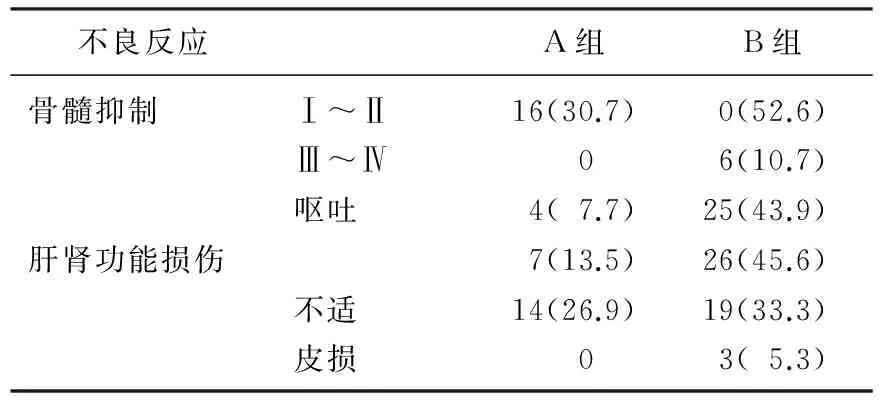
表2 2组不良反应比较[n(%)]
就不良反应来说, 2组均会出现粒细胞减少、恶心、呕吐、肝转氨酶增高等,并且B组的不良反应程度显著高于A组。但2组均无因无法耐受副反应而中途退出的患者。本研究比较了以培美曲塞为基础的化疗方案与以紫杉醇为基础的化疗方案在治疗晚期乳腺癌的差异,前者与后者有效性相似,安全性更高。除了化疗之外,内分泌治疗以及靶向治疗对于乳腺癌的治疗同样有效。
[1] Passant H, Borley A. Adjuvant treatment for breast cancer[J]. Surgery, 2013, 31: 37-40.
[2] Benson J R, Jatoi I. The global breast cancer burden[J]. Future Oncol, 2012, 8: 697-702.
[3] Swain S, Kim S, Cortes J, et al. 350 O-PR-Final overall survival (OS) analysis from the CLEOPATRA study of first-line (1 L) pertuzumab (Ptz), trastuzumab (T), and docetaxel (D) in patients (pts) with HER2-positive metastatic breast cancer (MBC)[J]. European Society for Medical Oncology, 2014: 312-321.
[4] Harris J R, Lippman M E, Morrow M, et al. Diseases of the Breast[M]. 4th ed. Philadelphia, PA: Lippincott-Raven Publishers, 2010: 877-919.
[5] Partridge A H, Rumble R B, Carey L A, et al. Chemotherapy and targeted therapy for women with human epidermal growth factor receptor 2-negative (or unknown) advanced breast cancer: American Society of Clinical Oncology Clinical Practice Guideline[J]. J Clin Oncol, 2014, 32: 3307-3329.
[6] Schilsky R L. Biochemical pharmacology of chemotherapeutic drugs used as radiation enhancers[J]. Semin Oncol, 1992, 19: 2-7.
[7] Adjei A A. Pemetrexed (Alimta): a novel multitargeted antifolate agent[J]. Expert Rev Anticancer Ther, 2003, 3: 145-156.
[8] Yamaguchi T, Nakanishi T, Hayashi M, et al. Efficacy and safety of cisplatin plus pemetrexed as a first-line treatment for Japanese patients with advanced non-squamous non-small-cell lung cancer-a retrospective analysis[J]. Gan To Kagaku Ryoho, 2015, 42: 183-187.
[9] Wu X Y, Huang X E, Cao J, et al. Efficacy of Bifidobacterium Tetragenous Viable Bacteria Tablets for Cancer Patients with Functional Constipation[J]. Asian Pac J Cancer Prev, 2014, 15(14): 5941-4.
[10] Szczepanowicz K, Bzowska M, Kruk T, et al. Pegylated polyelectrolyte nanoparticles containing paclitaxel as a promising candidate for drug carriers for passive targeting[J]. Colloids & Surfaces B Biointerfaces, 2016, 143: 463-471.
[11] Minish M. Jain, Smita U. Gupte, Shekhar G, et al. Paclitaxel injection concentrate for nanodispersion versus nab-paclitaxel in women with metastatic breast cancer: a multicenter, randomized, comparative phase Ⅱ/Ⅲ study[J]. Breast Cancer Res Treat, 2016, 156(1): 125-34.
[12] Liu J, Huang X E, Tian G Y, et al. Phase Ⅱ Study on Safety and Efficacy of Yadanzi (Javanica oil emulsion injection) Combined with Chemotherapy for Patients with Gastric Cancer[J]. Asian Pac J Cancer Prev, 2013, 14: 2009-12.
[13] Martin M. Clinical experience with pemetrexed in breast cancer[J]. Semin Oncol, 2006, 33: S15-8.
[14] Jackman D M. Current options for systemic therapy in mesothelioma[J]. Semin Thorac Cardiovasc Surg, 2009, 21: 154-8.
[15] Manegold C, Schmid-Bindert G, Pilz L R. Pemetrexed for the treatment of non-small-cell lung cancer[J]. Expert Rev Anticancer Ther, 2009, 9: 1195-209.
[16] Qian T, Huang X E. Study of Pemetrexed-based Chemotherapy for Patients with Locally Advanced or Metastatic Cancers[J]. Asian Pac J Cancer Prev, 2015, 16(11): 4791-5.
[17] 王文江. 新辅助化疗对晚期乳腺癌患者血浆microRNA及肿瘤相关指标的影响[J]. 海南医学院学报, 2015, 21(11): 1509-1511.
[18] 孙运坡, 应学翔, 何萍青. 不同分子亚型乳腺浸润性导管癌组织中Integrin β4、S100A4的表达及意义[J]. 实用临床医药杂志, 2015, 19(5): 28-31.
[19] 王琼, 贺玉娟, 冯俊明, 等. 乳腺导管癌中原位癌成分和浸润性成分的核分级及EGFR的表达与病理特点间的关系研究[J]. 华南国防医学杂志, 2015(6): 419-422.
[20] 彭月琴, 仲瑛, 岳雁娟. 彩色多普勒超声与钼靶X线对乳腺癌的诊断价值探讨[J]. 实用临床医药杂志, 2013, 17(A01): 86-87.
[21] 王星, 于艳红, 李彩娟. 彩色多普勒超声、MRI及其联合应用对小乳腺癌的诊断价值分析[J]. 黑龙江医药科学, 2015, 38(1): 64-65.
2017-01-20
黄新恩
R 737.9
A
1672-2353(2017)07-145-02
10.7619/jcmp.201707046
