酶法水解乳糖与热处理偶联对牛乳Maillard反应的影响
2017-04-25李思宁唐善虎毛濛兰
李思宁,唐善虎,*,胡 洋,毛濛兰,刘 媛
(1.西南民族大学生命科学与技术学院,四川 成都 610041;2.新希望乳业控股有限公司技术中心,四川 成都 610040)
酶法水解乳糖与热处理偶联对牛乳Maillard反应的影响
李思宁1,唐善虎1,*,胡 洋1,毛濛兰1,刘 媛2
(1.西南民族大学生命科学与技术学院,四川 成都 610041;2.新希望乳业控股有限公司技术中心,四川 成都 610040)
旨在探讨乳糖水解程度及热处理方法与Maillard反应的关系,鲜牛乳用中性乳糖酶处理获得不同水解程度的低乳糖牛乳,然后对牛乳进行不同的热处理,处理后的样本进行Maillard反应程度评价。采用葡萄糖氧化酶法测定不同水解时间的牛乳中葡萄糖质量浓度和乳糖水解率,用高效液相色谱法和紫外分光光度法分别测定水解后牛乳经不同热处理后的糠氨酸和5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)含量及牛乳褐变程度的OD值。结果表明,随着乳糖水解时间的延长,牛乳中的葡萄糖含量呈增加的趋势,葡萄糖质量浓度从0.00 mg/100 mL增加到1 721.33 mg/100 mL,但增加趋势逐渐变缓;乳糖水解率从0%增加到70.33%,水解时间2.0 h后的牛乳水解率达到了50%以上。糠氨酸含量呈上升的趋势(P<0.05),水解时间在3.0 h以上并经75 ℃、30 min热处理的牛乳,糠氨酸含量超过了190 mg/100 g pro;水解时间为0.5 h及以上并经75 ℃、15 s热处理的牛乳,糠氨酸含量超过了12 mg/100 g pro。生鲜牛乳和水解后经75 ℃、30 min热处理的牛乳,均未检测到5-HMF,水解后经75 ℃、15 s热处理的牛乳,随乳糖水解时间的延长,牛乳中5-HMF含量增加显著(P<0.05)。牛乳的褐变程度随乳糖水解时间显著增加(P<0.05),且乳糖酶水解后75 ℃、30 min热处理的牛乳的褐变程度明显高于75 ℃、15 s热处理的牛乳。本研究结果说明,乳糖经过酶水解后的牛乳,长时间热处理会加重乳Maillard反应,影响乳的蛋白质品质。
牛乳;乳糖水解;Maillard反应;糠氨酸;5-羟甲基糠醛
牛乳含有促进人类生长发育以及维持健康水平的必需营养成分,是一种重要的饮食资源[1]。但由于牛乳中的乳糖不能被乳糖不耐人群消化和吸收,极易引发乳糖不耐受现象,使牛乳资源的利用受到限制。因此,针对这些人群开发低乳糖牛乳,即牛乳中的乳糖经乳糖酶适度水解后生产的牛乳,是企业十分感兴趣的课题。然而,牛乳中的乳糖经水解后,生成半乳糖和葡萄糖,经过必要的热处理后更易发生Maillard反应,而造成牛乳营养价值和感官品质的降低[2-3]。因此,有必要研究热处理对酶法水解乳糖牛乳Maillard反应的影响。
通常认为,乳制品中的糠氨酸是乳糖与氨基酸、蛋白质在高温条件下发生Maillard反应的产物[4]。牛乳在加热过程中,氨基酸、蛋白质与乳糖通过Maillard反应生成ε-N-脱氧乳果糖基-L-赖氨酸,经酸水解生成更稳定的糠氨酸(ε-N-2-呋喃甲基-L-赖氨酸)[5]。以下一些研究报道表明:还原糖与蛋白质受热发生Maillard反应,也生成糠氨酸。Marconi等[6]报道了蜂王浆中糠氨酸的测定方法;周骁等[7]建立了高效液相色谱测定蜂花粉中糠氨酸的方法,此方法可作为标准方法评价蜂花粉的产品质量;牛猛[8]进行了全麦鲜湿面褐变机制及品质改良的研究,结果表明全麦湿面在常温(25 ℃左右)条件下保存时,其中可以检测到糠氨酸,随着保存温度从20 ℃逐渐升高到80 ℃,糠氨酸含量也逐渐增加。
Maillard反应机理复杂,糠氨酸只是初期反应的产物。5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)是由糖类化合物在高温或弱酸性条件下水解产生的一种呋喃类化合物,是Maillard反应的一种重要的中间产物,可用来监测热处理对牛乳色泽的影响效果[9]。通过测定糠氨酸及5-HMF含量来综合评价酶法水解乳糖与热处理结合对牛乳Maillard反应的影响。目前,关于牛乳Maillard反应相关的研究很多,基本上集中在对生乳、复原乳及超高温灭菌(ultra high temperature sterilization,UHT)乳中糠氨酸含量的测定及Maillard反应对乳制品品质的影响方面[10-14],而对于低乳糖牛乳Maillard反应的研究还较少。伍桃英等[15]以5-HMF作为考察指标,采用β-半乳糖苷酶水解牛乳至乳糖水解率超过90%,研究了几种褐变抑制剂对低乳糖乳褐变的抑制效果,结果表明Na2SO3、柠檬酸、NaHSO3、EDTA-2Na对低乳糖乳中5-HMF的抑制作用依次递减。常浩祥[16]以水解率达到70%以上的牦牛乳为对象,添加不同种类的抑制剂,测定5-HMF的含量来评价抑制剂的抑制效果。结果表明,将低乳糖牛乳在85 ℃加热10 min,除抗坏血酸对Maillard反应有促进作用外,VE、2,6-二叔丁基-4-甲基苯酚(butylated hydroxytoluene,BHT)、甲硫氨酸和半胱氨酸均能对低乳糖牦牛乳中Maillard反应具有抑制作用。目前鲜见有关牛乳中乳糖不同水解程度与牛乳Maillard反应之间关系的研究报道。本实验以中性乳糖酶处理牛乳获得不同水解程度的低乳糖牛乳,通过葡萄糖氧化酶法测定不同水解时间的牛乳中的葡萄糖质量浓度和乳糖水解率,使用高效液相色谱法(high performance liquid chromatography,HPLC)和紫外分光光度法测定乳糖水解后再经热处理的牛乳中糠氨酸和5-HMF的含量及牛乳的褐变程度,研究酶法水解乳糖与热处理对牛乳Maillard反应的影响,旨在探索牛乳中乳糖水解程度与热处理牛乳的Maillard反应之间的关系,以期为开发低乳糖牛乳产品提供科学依据。
1 材料与方法
1.1 材料与试剂
生鲜牛乳 新希望乳业控股有限公司。
中性乳糖酶(2 600 U/g) 荷兰皇家帝斯曼集团;葡萄糖测定试剂盒 北京普利莱基因技术有限公司;糠氨酸标准品(纯度>99%) 法国NeoMPS公司;5-HMF标准品(纯度>99%) 上海Aladdin公司;盐酸、乙醇、磷酸、六氰合铁酸钾、乙酸锌、甲醇、草酸(分析纯)、乙腈、甲醇(色谱纯) 成都市科龙化工试剂厂;三氟乙酸(色谱纯) 上海源叶生物科技有限公司;考马斯亮蓝G-250、标准牛血清白蛋白(分析纯)美国Sigma公司。
1.2 仪器与设备
1100高效液相色谱仪 美国安捷伦公司;快速乳成分分析仪 浙江大学食品科学与发酵工程研究所;恒温水浴锅 国华电器有限公司;DHP-9052电热恒温培养箱 上海齐欣科学仪器有限公司;紫外分光光度计翔艺仪器有限公司。
1.3 方法
1.3.1 实验设计
分别取9 份200 mL生鲜牛乳,在水浴锅中经过75 ℃、15 s预杀菌处理,冷却至40 ℃左右,分别添加0.8 g乳糖酶(添加量4‰),搅拌均匀。将9 份牛乳样品在40 ℃水浴中分别水解0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0 h,均取出10 mL牛乳,用于测定牛乳中的葡萄糖质量浓度和乳糖水解率。剩余每份牛乳(190 mL)平均分成两份,每份95 mL,9 个不同水解时间的牛乳为一组。第一组牛乳经75 ℃、30 min加热处理,第二组牛乳经75 ℃、15 s加热处理。两组热处理后的样品均冷却至25 ℃左右,测定样品糠氨酸、5-HMF含量及褐变程度。糠氨酸、5-HMF含量及褐变程度指标测定均以生鲜牛乳为对照。
1.3.2 指标测定
1.3.2.1 乳成分的测定
采用快速乳成分分析仪对原料乳的成分进行测定。
1.3.2.2 葡萄糖含量的测定
采用葡萄糖测定试剂盒和分光光度法测定乳糖水解后,产生的葡萄糖含量。按照操作说明,将葡萄糖标准品和待测样品在530 nm波长处测定OD值,根据标准曲线计算样品中葡萄糖的含量。
1.3.2.3 乳糖水解率的测定
根据1.3.2.2节测定的葡萄糖的质量浓度折算成乳糖后计算水解率(degree of hydrolysis,DH)[17]。其中,起始乳糖含量由乳成分分析仪测得,葡萄糖质量浓度由葡萄糖测定试剂盒测得。水解率计算公式如式(1)。

式中:342为乳糖的相对分子质量;180为葡萄糖的相对分子质量;ρ为葡萄糖质量浓度/(mg/100 mL);c为起始乳糖含量/(g/100 g)。
1.3.2.4 糠氨酸含量的测定
采用HPLC法测定牛乳中的糠氨酸,参照文献[13,18]方法,并做适当调整。
糠氨酸标准工作溶液的配制:将糠氨酸标准品用3 mol/L盐酸溶液配制成200 μg/mL的标准贮备液,贮存于4 ℃冰箱中。取0.1 mL标准贮备溶液,用3 mol/L盐酸定容至10 mL配制成2 μg/mL的糠氨酸标准工作溶液。
试样水解液的制备:吸取2.00 mL牛乳,置于水解管中,加入6 mL的10.6 mol/L盐酸溶液,混匀。向水解管中缓慢通入高纯度氮气1~2 min,密封试管。然后将其置于110 ℃的烘箱中水解24 h。水解结束后,将水解管从烘箱中取出,冷却后过滤,保留滤液供测定。
试样水解液中蛋白质含量的测定:采用考马斯亮蓝G-250法[19]测定蛋白质质量浓度。具体方法为:吸取1.0 mg/mL的标准牛血清白蛋白0.0、0.1、0.2、0.4、0.6、0.8、1.0 mL于7 支试管,补加蒸馏水至1.0 mL,在每支试管中加入4 mL考马斯亮蓝G-250试剂,混匀。2~5 min后,测定各样品在595 nm波长处的OD值,作出标准曲线。吸取0.2~0.8 mL样品溶液,补加蒸馏水至1.0 mL后,其余步骤同牛血清白蛋白,测定样品的OD值,并计算样品中的蛋白含量。
试样水解液中糠氨酸含量的测定:吸取0.5 mL过滤后的试样水解液于试管内,用3 mol/L盐酸溶液定容至3 mL,过0.45 μm滤膜,滤液用于HPLC测定。
色谱条件:色谱柱:Waters Symmetry C18色谱柱(4.6 mm×250 mm,5 μm);流动相:A为0.08%三氟乙酸,B为甲醇;紫外检测波长:280 nm;进样量:10 μL;柱温:35 ℃。梯度洗脱程序见表1。

表1 梯度洗脱程序Table 1 Gradient elution program for furosine
在测定时,首先将洗脱液A和B的混合液(50∶50),以1 mL/min的流速平衡色谱系统。并注入20~50 μL的3 mol/L盐酸溶液平衡色谱柱,以检测溶剂的纯度。每测定10 个样品后测定一次标准工作溶液,以校准仪器。
糠氨酸含量按式(2)计算。

式中:W为样品中每100 g蛋白质中糠氨酸的质量/(mg/100 g pro);ρ为样品水解液中糠氨酸的质量浓度/(μg/mL);d为测定时稀释倍数(d=6);ρ1为样品水解液中蛋白质质量浓度/(mg/mL)。
1.3.2.5 5-HMF含量的测定
采用HPLC法测定牛乳中的5-HMF,参照文献[20]方法,并做适当调整。
5-HMF标准溶液的配制:精确称取5-HMF标准品0.03 g,用10 mL甲醇溶解后,用水稀释定容至100 mL,得到300 μg/mL 5-HMF标准贮备液。取一定量5-HMF贮备液,用水稀释成质量浓度分别为0.00、0.10、0.50、1.00、1.50、2.00 μg/mL的5-HMF标准溶液。
样品溶液的制备:准确称取牛乳样品10.00 g,加入5 mL 0.15 mol/L草酸溶液,混合均匀。再加入92 g/L六氰合铁酸钾溶液3 mL和183 g/L乙酸锌溶液3 mL,振摇充分后静置10 min,用甲醇定容至50 mL,混匀、过滤,弃去固相,收集上清液,用0.45 µm滤膜过滤后进样。
色谱条件:色谱柱:Waters Symmetry C18色谱柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(体积比15∶85);紫外检测波长:280 nm;流速:1.0 mL/min;进样量:10 μL;柱温:30 ℃。
结果计算:样品中5-HMF的含量按式(3)计算,扣除空白。

式中:X为样品中5-HMF的含量/(mg/kg);Si为样品中5-HMF的峰面积;Ss为标准溶液中5-HMF的峰面积;ρs为标准工作液中5-HMF的质量浓度/(μg/mL);V为样品最终定容体积/mL;m为样品的取样质量/g。
1.3.2.6 紫外分光光度法测定牛乳的褐变程度
根据文献[21]的方法并稍作修改进行测定。取1 mL处理后的牛乳,用蒸馏水稀释200 倍,在420 nm波长处测定样品的OD值(以生鲜牛乳作为空白)。OD值越大,表明牛乳的褐变程度越剧烈。
1.4 数据处理
2 结果与分析
2.1 牛乳基本成分GB 19301—2010《食品安全国家标准 生乳》规定:蛋白质含量≥2.80 g/100 g,脂肪含量≥3.1 g/100 g,非脂乳固体含量≥8.1 g/100 g[22]。由表2可知,本实验所使用的牛乳满足国标对原料乳的质量要求。

表2 牛乳基本成分Table 2 Proximate composition of milk
2.2 不同水解时间牛乳中葡萄糖含量及乳糖水解率变化在530 nm波长处,以各标准管OD值为y轴,葡萄糖浓度为x轴,绘制出葡萄糖质量浓度的标准曲线,线性关系表示为y=0.018 3x+0.021 5,R2=0.999 6。通过该方法可准确测出样品中葡萄糖的含量。在不同水解时间,牛乳中葡萄糖含量及乳糖水解率变化见表3。随着水解时间的延长,牛乳中的葡萄糖含量一直在增加,这是由于在乳糖酶的作用下,牛乳中的乳糖水解生成了葡萄糖。水解时间在0.0~2.0 h,葡萄糖质量浓度增加速率较快,从0.00 mg/100 mL增加到了1 250.99 mg/100 mL,增加了1 250.99 mg/100 mL;水解时间在2.0~4.0 h,葡萄糖质量浓度增加速率减慢,从1 250.99 mg/100 mL上升到1 721.23 mg/100 mL,增加了470.24 mg/100 mL。这表明,随乳糖水解时间的延长,牛乳中的乳糖水解为葡萄糖的含量增加,但乳糖酶的水解效率下降。
随着乳糖水解时间的延长,牛乳中乳糖水解率(DH)呈上升的趋势。水解时间从0.0~4.0 h,乳糖水解率从0%增加到70.33%。高亚滨[23]认为,当牛乳中的乳糖降低50%后,就可以克服乳糖不耐症的问题。因此,乳糖水解时间为2.0 h及以后的牛乳满足了乳糖不耐症患者的需要。

表3 不同水解时间牛乳中葡萄糖含量及乳糖水解率变化Table 3 Changes in glucose content and hydrolysis degree of milk as a function of hydrolysis time
2.3 不同水解时间牛乳中糠氨酸变化
2.3.1 糠氨酸标准品色谱图
质量浓度为2 μg/mL糠氨酸标准工作溶液的色谱图见图1。从出峰情况可以看出,糠氨酸的保留时间为5.990 min。
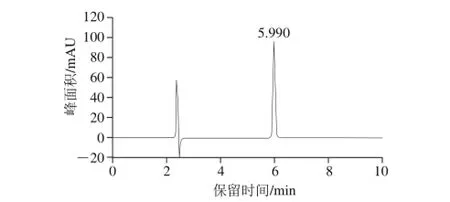
图1 糠氨酸标准品色谱图Fig. 1 HPLC chromatogram of furosine standard
2.3.2 不同水解时间的牛乳中糠氨酸含量
在乳糖酶作用下,牛乳水解0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0 h后,采用HPLC测定牛乳中糠氨酸的含量,结果见表4。
糠氨酸是Maillard反应产生的特定产物。近年来,糠氨酸常被用作判断食品受热程度的指标,在蛋类、谷物、乳制品、肉制品、中药口服液中均有应用[24]。由表4可知,随着乳糖酶水解时间的延长,牛乳中糠氨酸含量呈上升的趋势(P<0.05)。生鲜牛乳中糠氨酸含量为3.040 mg/100 g pro,符合生鲜乳糠氨酸含量3~5 mg/100 g pro的要求[13]。生鲜牛乳经75 ℃、15 s预杀菌处理,乳糖酶水解0 h,再经75 ℃、30 min热处理,其糠氨酸含量是同样条件下经75 ℃、15 s热处理牛乳的14 倍以上,表明牛乳经巴氏预杀菌后再经长时间热处理,糠氨酸含量会明显增加。NY/T 939—2005《巴氏杀菌乳和UHT灭菌乳中复原乳的鉴定》规定,巴氏杀菌乳中糠氨酸含量大于12 mg/100 g pro或UHT乳中糠氨酸含量大于190 mg/100 g pro,则鉴定为含有复原乳[5]。对于水解时间在3.0 h以上且经75 ℃、30 min热处理的牛乳,糠氨酸含量基本超过了190 mg/100 g pro,相当于含有复原乳的UHT杀菌乳。对于水解时间为0.5 h及以上并经75 ℃、15 s热处理的牛乳,糠氨酸含量超过了12 mg/100 g pro,相当于含有复原乳的巴氏杀菌乳。孙琦[25]测定了生鲜牛乳经75 ℃、15 s热处理后糠氨酸的含量,与生鲜牛乳相比,热处理后的牛乳糠氨酸含量有所增加,但不显著;但经超高温瞬时灭菌(137 ℃、4 s)后糠氨酸含量显著增加,超过了100 mg/100 g pro。
糠氨酸是牛乳加工过程中经Maillard反应使蛋白质和还原糖形成的特征产物之一。随着水解时间的延长,乳糖被乳糖酶水解生成葡萄糖和半乳糖的量增加,而还原性单糖更容易发生Maillard反应[26],表征Maillard反应程度加剧。
2.4 不同水解时间牛乳中5-HMF变化
2.4.1 5-HMF标准品色谱图及标准曲线
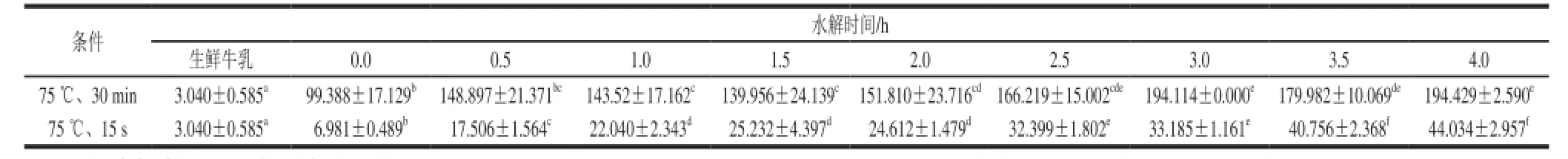
表4 不同水解时间牛乳中糠氨酸含量Table 4 Change in furosine content of milk as a function of hydrolysis time

表5 不同水解时间牛乳中5-HMF含量Table 5 Change in 5-HMF content of milk as a function of hydrolysis time
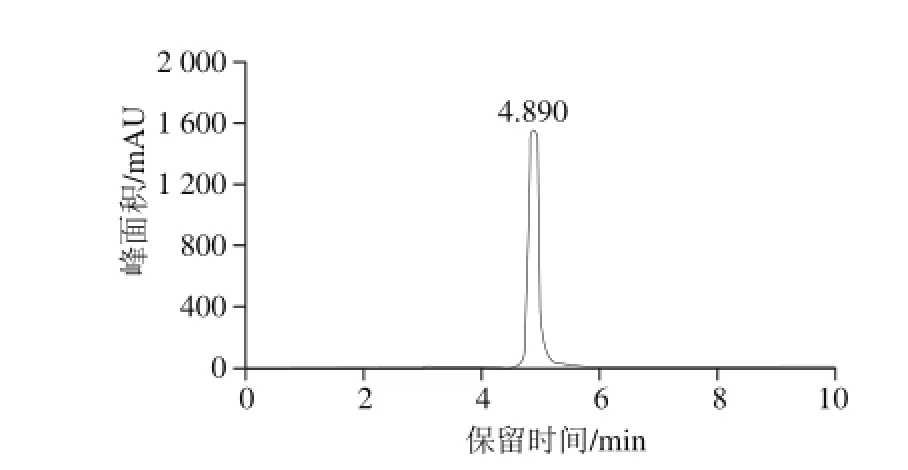
图2 5-HMF标准品色谱图Fig. 2 HPLC chromatogram of 5-HMF standard
质量浓度为2.00 μg/mL标准品的色谱图见图2。从出峰情况可以看出,保留时间为4.890 min。5-HMF标准工作曲线峰面积与质量浓度的线性关系表示为y=10 058x+35.482,R2=0.994 7。通过该方法可准确测出样品中5-HMF的含量。
2.4.2 不同水解时间的牛乳中5-HMF含量
在乳糖酶作用下,牛乳水解0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0 h后,采用HPLC测定牛乳中5-HMF的含量,结果见表5。
5-HMF是葡萄糖、果糖等单糖化合物在高温或弱酸性条件下脱水产生的酚醛类化合物,其为黑色,具有难闻气味,是引起食品风味和褐变的指标成分之一[27]。若5-HMF质量浓度偏高,表明加工过程中受到过度加热。由表5可知,生鲜牛乳和乳糖酶水解后经75 ℃、30 min热处理的牛乳,均未检测到5-HMF。这可能是因为牛乳经长时间热处理,牛乳中还原糖和氨基酸或蛋白质中的自由氨基缩合生成的Shiff碱经过一系列的反应而产生的Maillard中间产物5-HMF极不稳定,与多余的氨基化合物反应生成了褐色的含氮聚合物和共聚物[28-29],还可能是5-HMF发生异构化(裂解)反应,生成了小分子物质[30],因此未检测到5-HMF。对于75 ℃、15 s热处理的牛乳,随着乳糖水解时间的延长,牛乳中5-HMF含量呈上升的趋势(P<0.05),表明即使牛乳中的乳糖经乳糖酶水解成还原性单糖,巴氏杀菌处理(75 ℃、15 s)对牛乳的杀菌强度仍没有达到剧烈的程度,而使牛乳中检测不到5-HMF。2.5 不同水解时间牛乳的褐变程度变化
在乳糖酶作用下,牛乳水解0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0 h后,经75 ℃、30 min和75 ℃、15 s加热处理。采用分光光度法测定样品的褐变程度,其测定结果见图3。
褐变分为酶促褐变和非酶褐变。本实验中的牛乳经过巴氏杀菌处理,大部分酶已失活,主要考虑加工过程发生的非酶褐变(Maillard反应)。Maillard反应体系在420 nm波长处的紫外吸收大小与Maillard反应中间产物的形成有关[31]。由图3可知,随着乳糖酶水解时间的延长,牛乳的褐变程度呈显著上升的趋势(P<0.05),这表明,乳糖酶水解时间越长,Maillard反应程度越大,这是因为牛乳中的乳糖水解后,还原糖数量增加,更容易发生Maillard反应[16]。乳糖酶水解后75 ℃、30 min热处理的牛乳的褐变程度明显高于75 ℃、15 s热处理的牛乳,说明长时间热处理对牛乳Maillard反应的影响更剧烈。
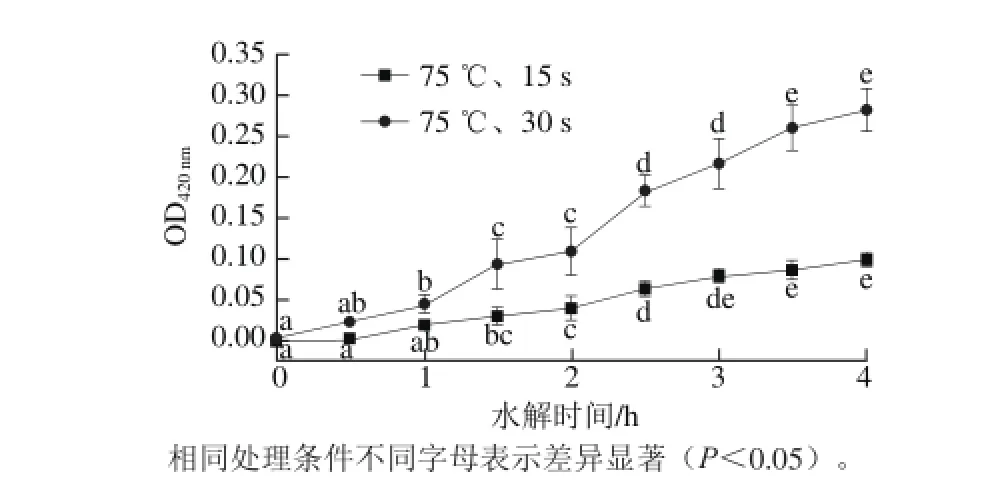
图3 不同水解时间牛乳褐变程度变化Fig. 3 Browning degree of milk during Maillard reaction as a function of hydrolysis time
3 结 论
采用中性乳糖酶对牛乳水解,并对牛乳进行热处理,获得以下结论:
测定不同水解时间牛乳中葡萄糖质量浓度和乳糖水解率表明,随着乳糖水解时间的延长,牛乳中葡萄糖含量呈增加的趋势,但这种趋势逐渐变缓。水解时间0.0~4.0 h,牛乳中的葡萄糖质量浓度从0.00 mg/100 mL增加到1 721.33 mg/100 mL;乳糖水解率从0%增加到70.33%,乳糖水解时间为2.0 h及以后的牛乳水解率达到了50%以上。
随着乳糖酶水解时间的延长,牛乳中糠氨酸含量呈上升的趋势。对于水解时间在3.0 h以上并经75 ℃、30 min热处理的牛乳,糠氨酸含量基本超过了190 mg/100 g pro,相当于含有复原乳的UHT杀菌乳。对于水解时间为0.5 h及以上并经75 ℃、15 s热处理的牛乳,糠氨酸含量超过了12 mg/100 g pro,相当于含有复原乳的巴氏杀菌乳。
生鲜牛乳和乳糖酶水解后经75 ℃、30 min热处理的牛乳,均未检测到5-HMF;而乳糖酶水解后经75 ℃、15 s热处理的牛乳,随着乳糖水解时间的延长,牛乳中5-HMF含量呈上升的趋势。
随着乳糖酶水解时间的延长,牛乳的褐变程度呈极显著上升的趋势,且乳糖酶水解后75 ℃、30 min热处理的牛乳的褐变程度明显高于75 ℃、15 s热处理的牛乳。长时间热处理对牛乳Maillard反应的影响更剧烈,影响乳的蛋白质品质。
[1] 王晓哲, 钱方, 曹迪, 等. 乳糖酶水解生产低乳糖牛乳工艺的优化[J]. 食品与机械, 2013, 29(2): 183-185. DOI:10.3969/j.issn.1003-5788.2013.02.044.
[2] ROY I, GUPTA M N. Lactose hydrolysis by Lactozym™immobilized on cellulose beads in batch and fl uidized bed modes[J]. Process Biochemistry, 2003, 39(3): 325-332. DOI:10.1016/S0032-9592(03)00086-4.
[3] CONTRERAS-CALDERÓN J, GUERRA-HERNÁNDEZ E, GARCÍA-VILLANOVA B. Utility of some indicators related to the Maillard browning reaction during processing of infant formulas[J]. Food Chemistry, 2009, 114(4): 1265-1270. DOI:10.1016/ j.foodchem.2008.11.004.
[4] 张宁. 液态乳生产工艺对糠氨酸含量的影响的初步研究[J]. 山东食品发酵, 2008(3): 19-21.
[5] 农业部. 巴氏杀菌乳和UHT灭菌乳中复原乳的鉴定: NY/T 939—2005[S]. 北京: 中国农业出版社, 2005: 2.
[6] MARCONI E, CABONI M F, MESSIA M C, et al. Furoaine: a suitable marker for assessing the freshness of royal jelly[J]. Journal Agricultural Food Chemistry, 2002, 50(10): 2825-2829.
[7] 周骁, 薛晓锋, 吴黎明, 等. 蜂花粉中糠氨酸的高效液相色谱测定方法[J]. 现代科学仪器, 2008(2): 90-92.
[8] 牛猛. 全麦鲜湿面褐变机制及品质改良的研究[D]. 无锡: 江南大学, 2014: 39-40.
[9] KEENEY M, BASSETTE R. Detection of intermediate compounds in the early stages of browning reaction in milk products[J]. Journal of Dairy Science, 1959, 42: 954-960. DOI:10.3168/jds.S0022-0302(59)90678-2.
[10] 王加启, 卜攀登, 于建国, 等. 生乳与UHT灭菌乳中糠氨酸含量及其测定方法研究[J]. 中国奶牛, 2005(6): 13-16. DOI:10.3969/ j.issn.1004-4264.2005.06.008.
[11] MENDOZA M R, OLANO A, VILLAMIEL M. Chemical indicators of heat treatment in fortif i ed and special milks[J]. Journal Agricultural Food Chemistry, 2005, 53: 2995-2999. DOI:10.1021/jf040406l.
[12] 杭锋, 郭本恒, 任璐, 等. 影响超高温灭菌纯牛乳糠氨酸含量的关键点分析及控制[J]. 食品工业科技, 2008, 29(11): 76-79.
[13] 迟骁玮. 乳品中糠氨酸定量分析及热处理对糠氨酸含量影响的研究[D]. 济南: 山东理工大学, 2012: 1-43.
[14] FERRER E, ALEGRIA A, COURTOIS G, et al. High-performance liquid chromatographic determination of Maillard compounds in storebrand and name-brand ultra-high-temperature-treated cow’s milk[J]. Journal of Chromatography A, 2000, 881: 599-606. DOI:10.1016/ S0021-9673(00)00218-1.
[15] 伍桃英, 陈云辉, 曾知音, 等. 高水解率低乳糖奶的褐变抑制研究[J].食品与机械, 2014, 30(5): 50-53; 71.
[16] 常浩祥. 牦牛乳源乳糖水解工艺及美拉德反应抑制剂的研究[J]. 食品工业科技, 2014, 35(13): 95-99.
[17] 付志军, 史玉东, 康小红, 等. 乳糖酶在生产低乳糖奶中的应用研究[J]. 食品研究与开发, 2008, 29(8): 48-52. DOI:10.3969/ j.issn.1005-6521.2008.08.014.
[18] 彭瑜, 陈坤, 徐锦忠, 等. 蜂王浆中糠氨酸含量测定及其对新鲜度的影响[J]. 中国蜂业, 2010, 61(1): 5-7. DOI:10.3969/ j.issn.0412-4367.2010.01.001.
[19] 冯昕, 王吉中, 尧俊英, 等. 考马斯亮蓝法测定乳与乳制品中蛋白质含量[J]. 粮食与食品工业, 2010, 17(3): 57-59. DOI:10.3969/ j.issn.1672-5026.2010.03.018.
[20] 吴榕, 孟瑾, 韩奕奕. 高效液相色谱法测定牛乳中的5-羟甲基糠醛[J].食品工业, 2006(4): 49-51.
[21] 黎婕, 陈中, 林伟峰, 等. 分光光度法分析柚子果肉汁的非酶褐变[J].食品工业科技, 2012, 33(21): 90-92; 95.
[22] 全国信息与文献标准化技术委员会. 食品安全国家标准 生乳: GB 19301—2010[S]. 北京: 中国标准出版社, 2010: 1-2.
[23] 高亚滨. 如何解决乳糖不耐症[J]. 中国乳品工业, 1997, 25(1): 38-40.
[24] 李沙, 郭栋, 王晓雯, 等. HPLC法检测分析温度对中药口服液品质的影响[J]. 中国酿造, 2015, 34(4): 30-34. DOI:10.11882/ j.issn.0254-5071.2015.04.008.
[25] 孙琦. 牛乳热加工特性及其盐类平衡的研究[D]. 北京: 中国农业科学院农产品加工研究所, 2012: 26-27.
[26] JING H, KITTS D D. Chemical and biochemical properties of caseinsugar Maillard reaction products[J]. Food and Chemical Toxicology, 2002, 40: 1007-1015. DOI:10.1016/S0278-6915(02)00070-4.
[27] 孔祥虹, 何小军, 何强, 等. 高效液相色谱法测定浓缩果汁及水果果糖中5-羟甲基糠醛[J]. 食品工业科技, 2012, 33(23): 314-315; 407.
[28] CAPUANO E, FERRIGNO A, ACAMPA I, et al. Characterization of Maillard reaction in bread crisps[J]. European Food Research and Technology, 2008, 228(2): 311-319. DOI:10.1007/s00217-008-0936-5.
[29] CAPUANO E, FERRIGNO A, ACAMPA I, et al. Effect of flour type on Maillard reaction and acrylamide formation during toasting of bread crisp model systems and mitigation strategies[J]. Food Research International, 2009, 42(9): 1295-1302. DOI:10.1016/ j.foodres.2009.03.018.
[30] 马志玲, 王延平, 吴京洪, 等. 乳及乳制品加工中的美拉德反应[J]. 中国乳品工业, 2002, 30(3): 8-10. DOI:10.3969/ j.issn.1001-2230.2002.03.003.
[31] LEE H S, NAGY S. Relationship of sugar degradation to detrimental changes in citrus juice quality[J]. Food Technology, 1998, 42: 91-97.
Effect of Enzymatic Hydrolysis of Lactose Combined with Heat Treatments on Maillard Reaction of Milk
LI Sining1, TANG Shanhu1,*, HU Yang1, MAO Menglan1, LIU Yuan2
(1. College of Life Science and Technology, Southwest University for Nationalities, Chengdu 610041, China; 2. Technology Center, New Hope Dairy Holding Co. Ltd., Chengdu 610040, China)
The objective of this study was to investigate the relationship between the hydrolysis degree of lactose combined with heat treatments and Maillard reaction in milk. Fresh milk was hydrolyzed with neutral lactase to obtain low-lactose milk with different hydrolysis degrees. Then, the products were treated by various heating methods and the degree of Maillard reaction was assessed. The glucose concentration and the hydrolysis degree of lactose in milk at different hydrolysis times were measured by the glucose oxidase method. Furosine and 5-hydroxymethylfurfural (5-HMF) contents and browning degree (OD values) were determined by using high-performance liquid phase chromatography (HPLC) and ultraviolet spectrophotometry, respectively. The results showed that the glucose content in milk was increased with prolonged time of lactose hydrolysis, and glucose concentration slowly increased from 0.00 to 1 721.33 mg /100 mL. Similarly, lactose hydrolysis percentage increased from 0% to 70.33%, reaching a level higher than 50% after 2.0 h heat treatment. Furosine content in milk showed a rising trend with extended heat treatment (P < 0.05). Milk subjected to hydrolysis for more than 3.0 h and then heat treatment at 75 ℃ for 30 min had a furosine content exceeding 190 mg/100 g protein, while hydrolysis for 0.5 h and longer followed by heat treatment at 75 ℃ for 15 s resulted in a furosine content more than 12 mg/100 g protein. 5-HMF was not detected in fresh milk or in milk hydrolyzed and heat treated at 75 ℃ for 30 min. The content of 5-HMF in hydrolyzed milk increased with the extension of hydrolysis time followed by heat treatment at 75 ℃ for 15 s (P < 0.05). Likewise, the browning degree signif i cantly increased with the extension of hydrolysis time (P < 0.05). Browning reaction in milk treated at 75 ℃ for 30 min was signif i cantly higher than that at 75 ℃ for 15 s. Therefore, enzymatic hydrolysis of lactose coupled with heat treatment can promote Maillard reaction and thus affect protein quality in milk.
10.7506/spkx1002-6630-201707020
TS252.4
A
1002-6630(2017)07-0122-07
2016-05-10
中央高校基本科研业务费专项资金项目(2015NZYQN35);四川省科技支撑计划项目(2014NZ0032)
李思宁(1988—),女,实验师,硕士,研究方向为食品加工与贮藏技术。E-mail:616906108@qq.com
*通信作者:唐善虎(1964—),男,教授,博士,研究方向为动物性食品加工及检测。E-mail:stang01@126.com
李思宁, 唐善虎, 胡洋, 等. 酶法水解乳糖与热处理偶联对牛乳Maillard反应的影响[J]. 食品科学, 2017, 38(7): 122-128. DOI:10.7506/spkx1002-6630-201707020. http://www.spkx.net.cn
LI Sining, TANG Shanhu, HU Yang, et al. Effect of enzymatic hydrolysis of lactose combined with heat treatments on Maillard reaction of milk[J]. Food Science, 2017, 38(7): 122-128. (in Chinese with English abstract)
10.7506/spkx1002-6630-201707020. http://www.spkx.net.cn
Key words:milk; lactose hydrolysis; Maillard reaction; furosine; 5-hydroxymethylfurfural
