腹腔镜左半结肠癌根治性切除术的手术体会
2017-04-20赵小军王元杰连彦军尤小兰程之逸南通大学附属泰州市人民医院江苏泰州225300
赵小军,王元杰,连彦军,尤小兰,程之逸(南通大学附属泰州市人民医院,江苏 泰州,225300)
腹腔镜左半结肠癌根治性切除术的手术体会
赵小军,王元杰,连彦军,尤小兰,程之逸
(南通大学附属泰州市人民医院,江苏 泰州,225300)
目的:探讨腹腔镜左半结肠癌根治性切除术的临床疗效及操作体会。方法:回顾分析2015年9月至2016年7 月11例患者行腹腔镜下标准左半结肠癌根治术的临床资料,采用五孔法中间入路,操作过程中严格遵循层面间隙内游离及结肠恶性肿瘤根治原则。结果:11例患者均顺利完成标准腹腔镜辅助左半结肠癌根治术,手术时间平均(142.25±35.26)min,术中出血量平均(21.53±8.76)ml,清扫淋巴结数量平均(18.45±4.28)枚,肛门排气时间平均(30.48±8.23)h,平均住院(10. 23±5.26)d。术后无切口愈合不良表现,术后出现肺部感染1例,腹腔感染1例,吻合口瘘1例,经营养支持、消炎、引流等保守治疗后痊愈,术后肠梗阻1例,保守治疗成功,术后1例发生腹腔内出血,再次行腹腔镜探查,发现为胰腺尾部创面边缘出血,行止血治疗。无围手术期死亡病例,患者均获随访,未发现切口肿瘤种植。结论:只要熟悉各个解剖层次,术中保持层面间隙内游离,避免过度牵拉,腹腔镜辅助左半结肠癌根治术是安全、有效的。
结肠肿瘤;结肠癌根治术;腹腔镜检查
腹腔镜辅助结肠癌手术因安全可靠、术后患者康复快,更具优势,已在临床得到广泛应用[1],也已成为结肠癌治疗指南推荐的术式之一。左半结肠在发育过程中融合层面较多,手术游离范围跨度大,涉及周围脏器多,手术难度相对较大。目前,关于腹腔镜左半结肠癌根治术的临床报道较少,临床研究也较少。2015年9月至2016年7月我们共开展腹腔镜下标准左半结肠癌根治术11例,现将体会报道如下。
1 资料与方法
1.1 临床资料 排除标准:(1)手术方式为非腹腔镜标准根治,同期行其他手术,肿瘤分期为Ⅳ期;(2)合并肠梗阻、穿孔、出血等需急诊处理;(3)行新辅助放、化疗及参与转化治疗;(4)心肺功能不佳。最终入组患者共11例,其中男7 例,女4例,55~74岁,平均(65.35±6.42)岁;TNM分期:Ⅰ期2例,Ⅱ期6例,Ⅲ期3例;细胞分化程度:高分化3例,中分化5例,低分化3例。术前患者均经CT、肠镜+病理证实为左半结肠癌。
1.2 手术方法 采用五孔法、中间入路行腹腔镜左半结肠癌根治术。气管插管全身麻醉后,患者取仰卧分腿位,头低脚高并向右侧倾斜15~20°,术者立于患者右侧,助手立于患者左侧,扶镜手立于患者两腿间,先经脐部穿刺10 mm Trocar作为观察孔,建立气腹,压力维持在10~12 mmHg。置入腹腔镜,初步探查腹盆腔,确定有无腹水,壁层腹膜有无肿瘤种植及腹内脏器有无转移。术者操作孔位置位于右侧腹直肌外侧缘,分别于脐上10 cm、脐下5 cm处穿刺5 mm、10 mm Trocar,左侧对应位置或稍偏外偏下穿刺两枚5 mm Trocar作为助手操作孔。仔细探查肿瘤及其对应淋巴引流区域肠系膜情况及脾脏下极粘连情况。为防止脾脏的损伤,一般对于有粘连的脾脏先行松解。对于中央区血管淋巴结的处理,一般患者采取腹主动脉分支血管的根部结扎+腹主动脉分支血管根部区域淋巴结清扫(高位血管结扎+高位淋巴结清扫),但合并糖尿病、血管粥样硬化、高血压、高血脂等患者采取腹主动脉分支血管的下级支根部结扎+腹主动脉分支血管根部区域淋巴结清扫(低位血管结扎+高位淋巴结清扫),以确保吻合口血供。两者手术操作步骤略有不同。以降结肠癌为例,高位血管结扎+高位淋巴结清扫:用超声刀于骶骨岬处切开乙状结肠右侧浆膜与后腹膜的融合线,并向头侧延伸切开腹主动脉右侧表面后腹膜,进入相连续的Toldt筋膜间隙与乙状结肠后间隙,充分向左侧拓展该层面,直至降结肠旁沟处脏层腹膜与壁层腹膜的交界线,在此过程中注意保护肾前筋膜的完整性,并于腹主动脉表面肠系膜下动脉根部断扎。于降结肠旁沟处切开脏层腹膜与壁层腹膜的交界线,使乙状结肠及降结肠中下段从腹后壁完全游离。沿腹主动脉表面继续向头侧切开后腹膜,直至胰腺下缘。继续于左侧Toldt筋膜间隙后方将降结肠向头侧游离,直至胰腺下缘,提起横结肠及游离的降结肠,于胰腺下缘切开降结肠系膜后层的Toldt筋膜,进入胰前间隙,继续向头侧游离,切开横结肠系膜前叶,进入网膜囊,于胰腺表面,以网膜囊及胰腺下方的Toldt筋膜间隙为引导,向右侧切开横结肠系膜前叶及Toldt筋膜,直至胰腺尾部(此过程于胰腺下缘切断肠系膜下静脉及可能存在的Riolan动脉弓)。外侧方离断膈结肠韧带,同时将结肠向尾侧及内侧牵引,于Toldt筋膜间隙层面内游离至胰腺下缘。上方分别提起胃大弯及横结肠,张紧胃结肠韧带,于胃窦体交界处横向切断胃结肠韧带,直至胰尾部,至此结肠脾曲游离。根据肿瘤具体位置于中结肠血管左侧裁剪横结肠系膜及对应部位的胃结肠韧带。提起乙状结肠,于直肠上端切断直肠系膜,裸化肠管,Endo-GIA切断直肠,辅助小切口切除左半结肠,经肛门将横结肠残端吻合于直肠上端。低位血管结扎+高位淋巴结清扫:腹腔组织的游离、淋巴结的清扫同高位结扎,主要区别在于腹主动脉前方分离出肠系膜下血管根部后,不进行离断,而是沿血管间隙内游离,暴露左结肠动脉、数支乙状结肠动脉及直肠上动脉,在保留直肠上动脉及1~2支下方的乙状结肠动脉基础上,根部离断左结肠动脉及上方的1~2支乙状结肠动脉,切除动脉支配的对应系膜及肠管,最后形成横结肠与乙状结肠的吻合。
2 结 果
11例患者均顺利完成标准腹腔镜辅助左半结肠癌根治手术,手术时间平均(142.25±35.26)min,术中出血量平均(21.53±8.76)ml,清扫淋巴结数量平均(18.45±4.28)枚,肛门排气时间平均(30.48± 8.23)h,平均住院(10.23±5.26)d。术后无切口愈合不良表现,术后出现肺部感染1例,腹腔感染1 例,吻合口瘘1例,经营养支持、消炎、引流等保守治疗后痊愈,术后肠梗阻1例,保守治疗成功,术后1例发生腹腔内出血,再次行腹腔镜探查,发现为胰腺尾部创面边缘出血,行止血治疗。无围手术期死亡病例,患者均获随访,未发现切口肿瘤种植。
3 讨 论
腹腔镜下标准左半结肠癌根治性切除术的切除范围同开腹手术,包括横结肠左侧、大网膜左侧、降结肠及乙状结肠大部、所切除肠管对应系膜,其适应证为横结肠左侧肿瘤、结肠脾曲肿瘤、降结肠肿瘤及乙状结肠上端肿瘤。虽然这些肿瘤的流行病学特征不同[2],肿瘤细胞的分子特性也各不相同[3],但对于手术方式、切除范围及手术质量控制的要求是相同的。因腹腔镜具有放大功能,使得镜下解剖层面的辨认更具优势,但因操作孔位置、器械的限制及肠管对周围组织的遮挡,游离结肠脾曲存在较大困难,这就要求术者与助手必须熟练配合,既要有手术的整体观,又要有局部组织的精细解剖能力。
3.1 左半结肠的筋膜解剖 胚胎学研究表明,降结肠系膜经过逆时针旋转其系膜后层与肾前筋膜融合[4],两者间原有的腹膜形成双层折叠,并在生长发育过程中逐渐演化为疏松结缔组织,形成所谓的融合筋膜,又名Toldt筋膜,它是一层疏松结缔组织构成的无成形结构的筋膜间隙,易于分离而不会损伤重要结构,而其后方的肾前筋膜是一层相对致密的膜性结构,也就成为腹腔镜下指引正确外科平面的重要结构。有观点认为肾前筋膜是胰体后方Treitz筋膜的延续外科平面,也就是说在游离左半结肠系膜后方时,向上容易进入胰后间隙,因此在胰腺下缘需及时切断结肠系膜后层,以便进入胰前间隙。横结肠系膜左侧附着于胰腺前方,其前叶与胰腺筋膜相延续,后叶于胰腺下缘与降结肠系膜前层相延续[5]。大网膜在发育过程中与横结肠融合,大网膜内层浆膜与横结肠系膜前叶相延续,外层与横结肠浆膜相延续。
3.2 术前肿瘤的定位与评估 术前肿瘤的定位与评估对治疗方案的选择具有较大意义。常见的术前肿瘤定位方法有肠镜定位、CT定位及肠镜下施金属夹后X线定位。不得已可术中使用肠镜定位,但会导致肠腔积气,影响手术操作空间。此外,术前CT评估很重要[6],首先可明确肠系膜下血管走行、变异、长度等重要信息,避免术中误损伤。其次,能明确肿瘤大小及与周围脏器关系。因CT不能显示肿瘤周围水肿带,因此CT检查结果好于实际情况,这在进展期肿瘤术前评估中应充分预计到。再次,提高整体观,术前可明确患者腹盆腔积液、区域淋巴结情况、肝脏内转移情况,甚至可初步评估腹膜转移情况。第四,可明确肿瘤供血血管,尤其横结肠左侧肿瘤,是左结肠血管供血为主还是结肠中血管左支供血为主,并指导中央组淋巴结的定位与清扫。
3.3 Toldt筋膜间隙的游离 从结肠脾曲以下左半结肠的系膜覆盖于左侧腹膜后,与肾前筋膜相隔于Toldt筋膜间隙。此段肠管的游离就是充分游离该筋膜间隙,内侧至腹主动脉表面,外侧至Toldt线,上方至胰腺下缘,下方至骶骨岬平面[7]。此筋膜间隙内无重要血管、神经,后方为相对致密的肾前筋膜。不论内侧入路抑或外侧入路,游离时需注意避免局部的过度深入,以防误入层次后因缺乏周围层次作为参照而不能及时纠正。具体操作中可用纱球钝性游离,能较好的避免损伤左半结肠系膜后层或肾前筋膜,见图1。
3.4 结肠脾曲游离 结肠脾曲的游离是左半结肠癌根治手术的关键所在。而辨认正确解剖层面是结肠脾曲游离的基础。结肠脾曲的游离包括三个部分,降结肠系膜上缘的切断、横结肠系膜根部的切断及胃结肠韧带的切断。因融合层面多、范围广,周围还有容易损伤的脾脏,因此,此处的游离是结肠癌根治的难点。历史上曾出现过多种手术入路:内侧入路、外侧入路、三路包抄、横向入路。其中三路包抄应用最为广泛,李国新教授团队[8]认为“三路包抄”的方法能较方便地完成结肠脾曲的游离。其最大的优点是将结肠脾曲游离分解成三步,脾曲的暴露通过3个单独层面给予增强,从而达到游离目的。其最大的困难在于左侧Toldt间隙与网膜囊的会师。原因为Toldt间隙与胰后间隙相延续,需切开结肠系膜后叶(Toldt筋膜间隙的浅层)才能进入胰前间隙,再切开胰前包膜或横结肠系膜前叶进入网膜囊,见图2、图3。横向入路法[5]先切断横结肠系膜后叶,进入胰前间隙,充分扩展胰腺前间隙后,切断胰腺后方下缘附着的筋膜,提前从上方进入左侧Toldt间隙,为后面的游离指引方向。这对于肥胖及胰腺显露不清的患者具有更显著的优势。
3.5 脾脏保护 保护脾脏的观念应贯彻于整个手术过程。引起脾脏损伤的主要原因是过度牵拉引起的脾脏包膜撕裂出血。这就要求术前我们应优先探查脾脏与结肠、网膜等有无粘连,切断粘连能较好的保护手术前期的脾脏出血。游离结肠脾曲时,牵拉力量应适度,避免暴力,在外侧方游离时尽早切断脾结肠韧带,沿胰腺下缘向外侧游离时应准确看到超声刀夹持组织及前方组织结构,否则及时更换路径。而于腹侧游离时,应尽可能全程看到脾脏,一能指引切线方向,二能避免损伤脾脏,见图4。
3.6 中央组淋巴结清扫与血管的保留 因左半结肠癌涉及的肿瘤位置不同,主要支配血管及淋巴回流区域也不相同,横结肠左侧肿瘤的主要供血血管为结肠中动脉左支,降结肠肿瘤主要血管为左结肠动脉,乙状结肠上端肿瘤的主要血管为乙状结肠动脉上1~2支。对于是否行结肠中血管或肠系膜下血管根部区域的淋巴结清扫,目前尚无统一意见。我们采用的方案是:如果为降结肠或乙状结肠上端肿瘤,则保留结肠中动脉左侧分支血管,根部断扎肠系膜下血管并清扫肠系膜下血管根部区域淋巴结。如果为横结肠左侧肿瘤,则保留乙状结肠血管下方1~2支及直肠上动脉,根部断扎结肠中血管+结肠中血管根部淋巴结清扫。如果患者合并高血压、糖尿病、高血脂、血管粥样硬化等血管条件不佳的情况,一般行腹主动脉分支血管的下级支根部结扎+腹主动脉分支血管根部区域淋巴结清扫,即结肠中动脉左侧分支根部断扎+结肠中动脉根部区域淋巴结清扫或左结肠血管及乙状结肠血管上方1~2支根部结扎+肠系膜下动脉根部区域淋巴结清扫,见图5。
3.7 输尿管与神经的保护 输尿管走行方向为由内上向外下,全程位于肾前筋膜后方。在输尿管跨过髂血管时位置明显变浅,可能会误以为直肠上动脉而予以牵拉、夹持,甚至离断。我们的经验是透过菲薄的肾前筋膜显露输尿管及生殖血管,这样就能避免灾难的发生。研究表明[9],上腹下丛的左、右侧束及束间交通支与肠系膜下动脉根部关系较密切。右侧束距离肠系膜下动脉根部较远,位于肾前筋膜下,只要分离层面正确,一般不会损伤。在左侧以左侧束降支为界,其近端,上腹下丛左侧束、肠系膜下丛、腹主动脉丛紧贴肠系膜下动脉根部左侧壁并相互延续,其远端左侧束走行于肾前筋膜下。但左侧束降支距离肠系膜下动脉起点的距离不恒定。这就表明游离时较易损伤上腹下丛左侧束,但如果能辨认左侧束降支,于其下方断扎肠系膜下动脉,则上腹下丛左侧束能受到保护。

图1 Toldt筋膜间隙的游离
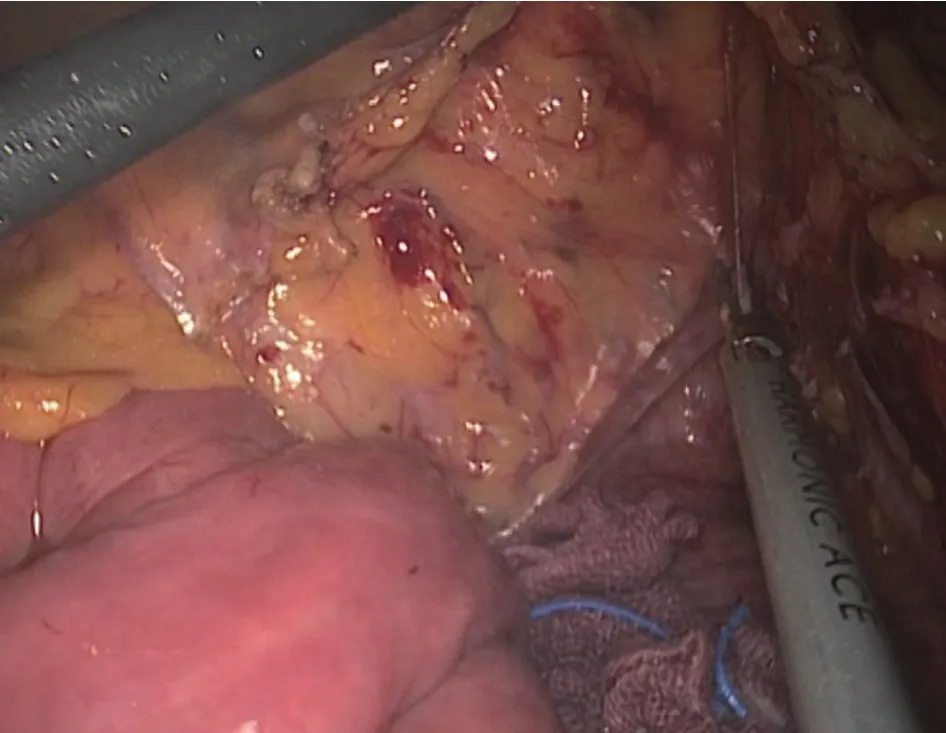
图2 在胰腺下缘切开Toldt筋膜,进入胰前间隙

图3 切开横结肠系膜前叶,进入网膜囊

图4 腹侧胃结肠韧带的游离

图5 低位血管结扎+高位淋巴结清扫
3.8 乙状结肠保留长度 左半结肠手术时游离较长肠管,而指南上也表明切除足够长度(超过10 cm)即可,导致部分病例保留较多乙状结肠甚至部分降结肠,而支配此段肠管的神经肠系膜下丛在肠系膜下动脉根部离断或肠系膜下动脉周围区域淋巴结清扫时已被切断,导致外源性去神经、交感神经破坏,肠管抑制运动受到影响,术后容易出现肠功能紊乱[10]。我们仅保留足够吻合长度的肠管,其余均切除。
3.9 辅助小切口位置 辅助小切口位置的常见选择:左下腹经腹直肌小切口,左侧腹经腹直肌小切口,下腹正中小切口。不论选取哪种切口,一般需兼顾以下方面:(1)损伤小;(2)美容效果好;(3)恶性肿瘤标本能完整取出;(4)满足消化道重建需要; (5)并发症少[11]。我们一般在横结肠游离、系膜裁剪较为满意时采用下腹部正中切口,损伤小,缝合快,甚至可在直视下完成吻合口浆肌层的加强缝合。而在横结肠左侧肿瘤手术时常采用左侧腹经腹直肌切口,更容易裁剪横结肠系膜、探查横结肠保留段血供情况。
总之,腹腔镜下左半结肠癌根治术的范围跨度较大,涉及周围脏器及筋膜层次较多,手术难度较大,但只要熟悉各解剖层次,保持正确层面的游离,避免过度牵拉加上手术团队间熟练配合,就能顺利完成。
[1] 赵平武,鲍峰,王东,等.腹腔镜结直肠癌根治术210例临床分析[J].腹腔镜外科杂志,2011,16(7):538-541.
[2] Lee GH,Malietzis G,Askari A,et al.Is right-sided colon cancer different to left-sided colorectal cancer?-A systematic review [J].Eur J Surg Oncol,2015,41(3):300-308.
[3] Missiaglia E,Jacobs B,D'Ario G,et al.Distal and proximal colon cancers differ in terms of molecular,pathological,and clinical features[J].Ann Oncol,2014,25(10):1995-2001.
[4] Gore RM,Balfe DM,Aizenstein RI,et al.The great escape:interfascial decompression planes of the retroperitoneum[J].AJR Am J Roentgenol,2000,175(2):363-370.
[5] 刁德昌,万进,王伟,等.横向入路法腹腔镜左半结肠癌根治术的临床应用[J].中华胃肠外科杂志,2015,18(10):1056-1058.
[6] 蔡恒烈,戎祯祥.腹腔镜左半结肠癌根治术前MSCT三维重建的临床价值[J].实用医学杂志,2015,31(5):788-790.
[7] 李国新,赵丽瑛.腹腔镜结直肠癌根治术解剖概要[J].中国实用外科杂志,2011,31(9):844-848.
[8] 耿岩,胡彦锋,余江,等.中间入路法腹腔镜辅助全结直肠切除的临床应用[J].中华胃肠外科杂志,2013,16(1):32-35.
[9] 杨晓飞,李国新,钟世镇,等.肠系膜下动脉根部自主神经保护的解剖学基础[J].中国临床解剖学杂志,2013,31(5): 497-500.
[10] Lee WY,Takahashi T,Pappas T,et al.Surgical autonomic denervation results in altered colonic motility:an explanation for low anterior resection syndrome?[J].Surgery,2008,143(6):778-783.
[11] 许景洪,李立志,黄文文,等.腹部腹腔镜手术后大块标本取出的切口并发症的多因素分析[J].中国微创外科杂志, 2014,14(9):792-795.
Surgical experience of laparoscopic left hemicolectomy for colon carcinoma
ZHAO Xiao-jun,WANG Yuan-jie,LIAN Yan-jun,et al.Department of Gastrointestinal Surgery,Taizhou People’s Hospital of Nantong University,Taizhou 225300,China
Objective:To explore the clinical effect and surgical experience of laparoscopic left hemicolectomy for colon carcinoma.Methods:The clinical data of 11 patients who underwent laparoscopic left hemicolectomy for colon carcinoma from Sep.2015 to Jul.2016 were retrospectively analyzed.Five-port method and medial approach was used.The standard of colonic radical resection for cancer and separation in the gap were strictly followed in the operation.Results:Eleven patients successfully underwent standard laparoscopic-assisted left hemicolectomy for colon carcinoma.The mean operation time was(142.25±35.26)min,the blood loss was(21.53 ±8.76)ml,the number of dissected lymph nodes was(18.45±4.28),the average time for flatus and hospital stay was(30.48±8.23) h and(10.23±5.26)d respectively.No poor healing of incision occurred.Postoperative complications included pulmonary infection(n =1),abdominal infection(n=1),anastomotic fistula(n=1),ileus(n=1)and abdominal cavity hemorrhage(n=1).Postoperative ileus was cured after conservative treatment.The patient with abdominal cavity hemorrhage underwent re-laparoscopic exploration and hemostasis because of hemorrhage at wound edge of pancreatic tail.The other complications were cured after conservative treatment such as nutrition support,anti-inflammation,drainage and so on.No death occurred in the perioperative period.No port-site recurrence was found during follow-up.Conclusions:Laparoscopic-assisted left hemicolectomy for colon carcinoma is safe and effective if surgeons are familiar with anatomical level,separate in gap and avoid excessive traction.
Colonic neoplasms;Radical operation for carcinoma of colon;Laparoscopy
R735.3+5
A
1009-6612(2017)04-0269-05
10.13499/j.cnki.fqjwkzz.2017.04.269
2016-09-19)
(英文编辑;杨庆芸)
赵小军(1980—)男,江苏省泰州市人民医院胃肠外科副主任医师,主要从事腹腔镜胃肠手术方面的研究。
