SOX和XELOX在进展期胃癌新辅助化疗中的临床疗效比较
2017-04-13张玉新左艳娇宋洪江薛英威
陈 力 张玉新 左艳娇 马 菲 宋洪江 薛英威
·临床应用·
SOX和XELOX在进展期胃癌新辅助化疗中的临床疗效比较
陈 力1张玉新1左艳娇1马 菲2宋洪江1薛英威1
目的探讨SOX和XELOX在进展期胃癌新辅助化疗中的临床疗效。方法 选取2011年2月1日—2015年10月1日我院行SOX和XELOX新辅助化疗的胃癌患者75例。分析两种方案临床分期、疗效评价、手术情况、术后病理、不良反应、生存分析等情况。结果 SOX和XELOX有效率分别为47.22%和41.03%。两组在CT疗效评价、有效率、疾病控制率方面比较,差异均不具有统计学意义(P>0.05);两组DFS、OS中位生存时间,差异均具有统计学意义(P<0.05)。结论 SOX和XELOX对进展期胃癌进行新辅助化疗均具有较高的安全性和有效性,XELOX远期疗效要优于SOX,改善患者预后。
新辅助化疗;进展期胃癌;有效率;无病生存时间;总生存时间
胃癌是最常见的恶性肿瘤之一,其病死率在全球恶性肿瘤中位居第二位[1]。胃癌早期不易发现,就诊时多数为进展期胃癌[2-3]。目前胃癌治疗仍以手术治疗为主,但我国胃癌患者的病情重且晚,即使行手术治疗,预后并不理想[4]。随着新辅助化疗的概念和理论的深入,明确指出该治疗方法可缩小肿瘤、降低临床分期、提高R0根治切除率,已成为肿瘤综合治疗的重要部分[5-6]。近年来新型化疗药物不断涌现,胃癌新辅助化疗的方案有很多种,而SOX(S-1 and oxaliplatin)方案和XELOX(Xeloda and oxaliplatin)方案在临床上最为常用[7-8]。尽管化疗方案有许多种,但迄今为止世界范围内尚未有公认的首选方案和标准,仍需进一步的探索[9]。本研究旨在分析这两种方案用于胃癌新辅助化疗的临床疗效及预后影响,以期为临床治疗提供一定的依据,现将结果报道如下。
1 资料与方法
1.1 一般资料
选取2011年2月1日—2015年10月1日于哈尔滨医科大学附属肿瘤医院胃肠外科确诊为进展期胃癌患者75例行新辅助化疗,术前均接受2~4个周期的SOX或XELOX化疗,并签署知情同意书。两组在年龄、性别、体重、BMI、饮水、进食速度、口味、胃区疼痛、腹胀腹痛、黑便等方面无统计学差异(P>0.05)(表1)。
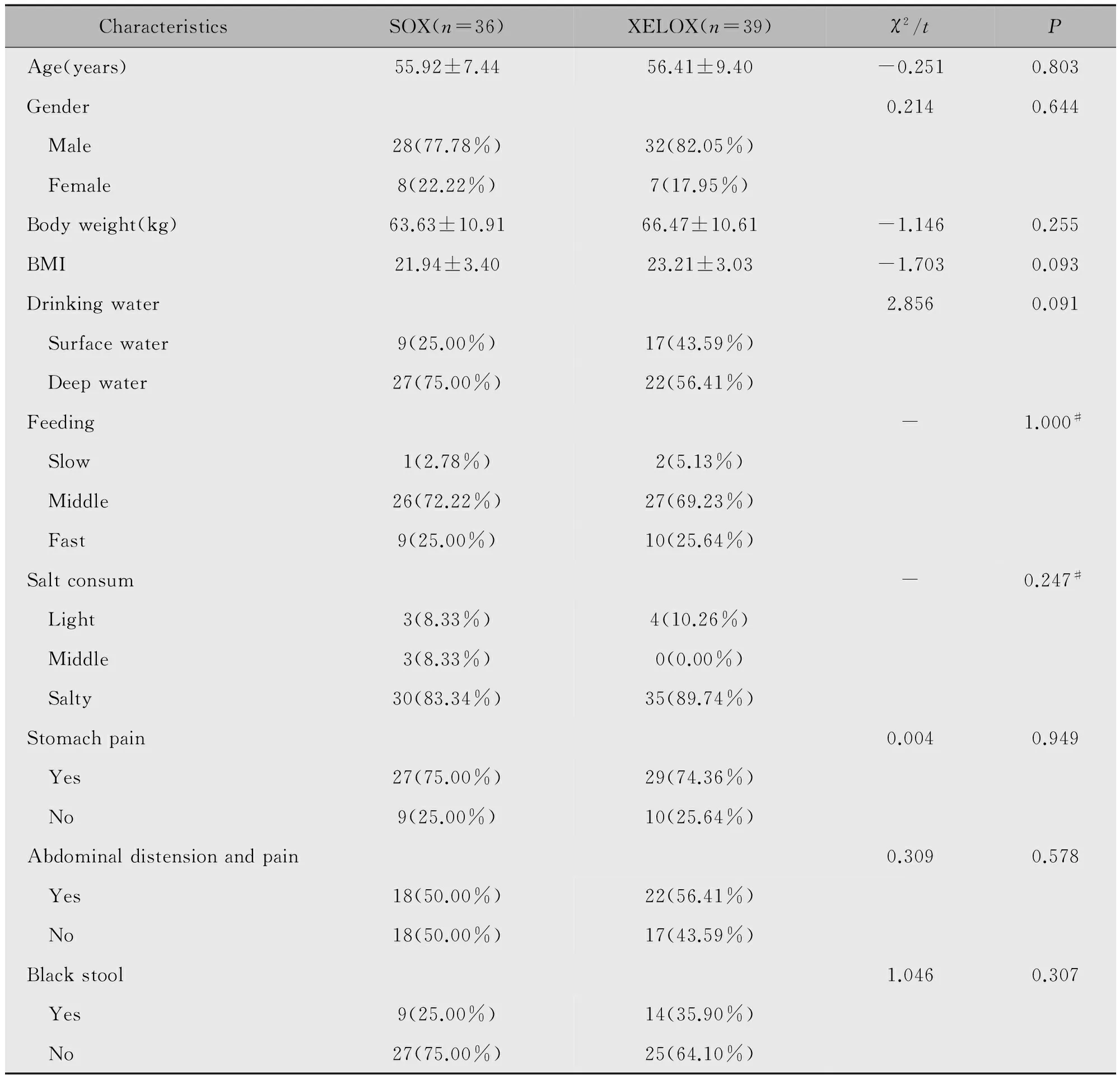
表1 SOX和XELOX方案患者一般临床资料Table 1 The comparison of the general clinical data between SOX group and XELOX group
Note:#Fisher exact test.
1.2 新辅助化疗标准
行胃镜检查,并经病理确诊为胃癌;入院前未进行相关治疗,包括放化疗、中医药治疗、免疫治疗等;心、肺、脑、肝、肾、骨髓等功能无明显异常,无手术、化疗禁忌;根据术后病理证实为进展期胃癌,以淋巴结转移、病灶浸润深度、周围脏器侵犯情况为准。
1.3 新辅助化疗方案
SOX方案:替吉奥胶囊(爱斯万)60 mg/次,2次/天,早晚餐后口服,第1~14天+注射用奥沙利铂200 mg 持续静脉滴注4小时,第1天,21天为一个周期。XELOX方案:卡培他滨片1 500 mg/次,2次/天,早晚餐后口服,第1~14天+注射用奥沙利铂200 mg持续静脉滴注4小时,第1天,21天为一个周期。
1.4 临床疗效评价
根据《日本胃癌处理规约》第14版中的标准进行疗效评价,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD),有效率为CR+PR,疾病控制率为CR+PR+SD。化疗2个周期行CT复查,评估化疗效果,化疗结束后1~2周进行手术。
1.5 CT TNM分期
根据《肿瘤学临床实践指南(中国版)》和国际抗癌联盟UICC第7版进行CT TNM分期[10]。淋巴结短径≥10 mm,或增强后CT值≥100 HU为转移阳性的评估标准[11]。
1.6 随访情况
术后1~2年每3~6个月随访1次,术后2~5年每6~12个月随访1次,5年后每年随访1次,直至死亡。
1.7 统计学方法
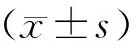
2 结果
2.1 SOX和XELOX方案CT T和N分期比较情况
SOX降期12(33.33%)人,不变23(63.89%)人,升期1(2.78%)人;XELOX降期17(43.59%)人,不变19(48.72%)人,升期3(7.69%)人。两组在化疗前T分期方面比较,差异具有统计学意义(P<0.05);在化疗前N分期、化疗后T分期及N分期方面比较,差异均不具有统计学意义(P>0.05)(表2)。
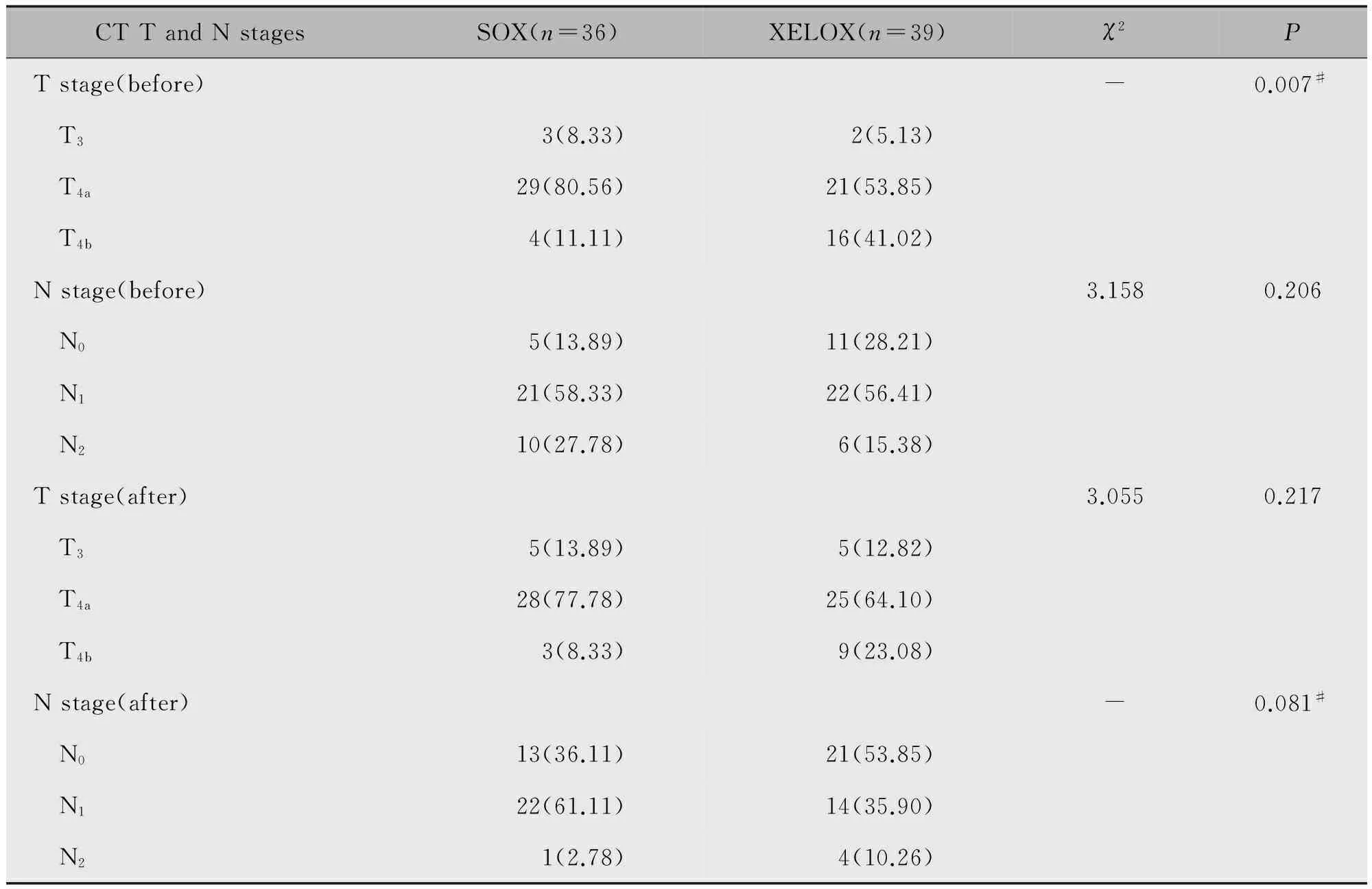
表2 SOX和XELOX方案CT T和N分期比较情况[n(%)]Table 2 The comparison of the CT T and N stage between SOX group and XELOX group[n(%)]
Note:#Fisher exact test.
2.2 两组临床疗效评价
SOX CR 0人,PR 17人,CR+PR为47.22%(17/36),CR+PR+SD为94.44%(34/36);XELOX CR 0人,PR 16人,CR+PR为41.03%(16/39),CR+PR+SD为97.44%(35/36)。两组在CT有效率、疾病控制率方面比较,差异均不具有统计学意义(P>0.05)。
2.3 SOX和XELOX方案手术情况比较
75例患者均行手术治疗。两组在根治情况、肿瘤大小、大体分型方面比较,差异均不具有统计学意义(P>0.05);在病变部位、胃切除范围方面相比较,差异均具有统计学意义(P<0.05)(表3)。
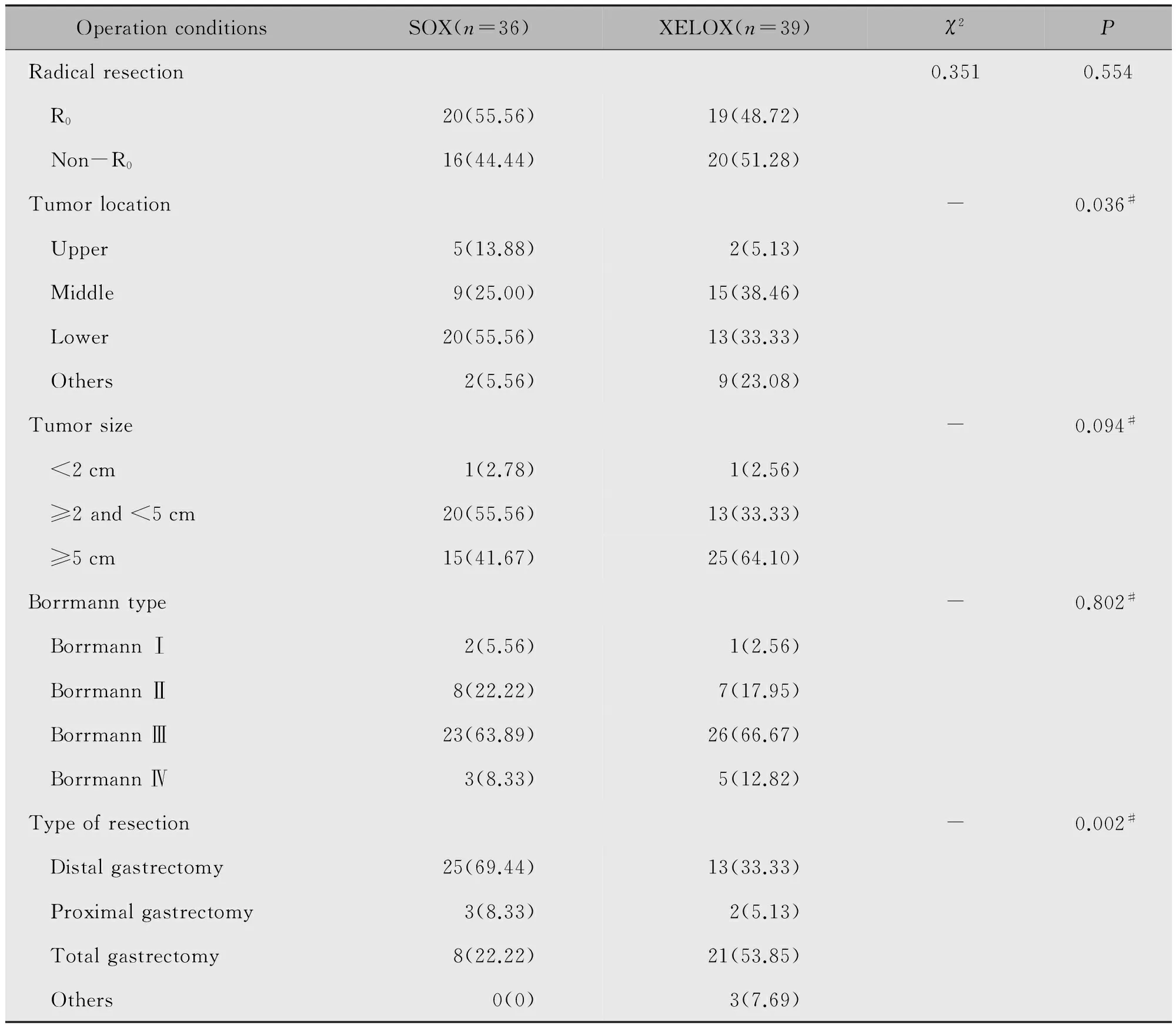
表3 SOX和XELOX方案手术情况比较[n(%)]Table 3 The comparison of operative condition between SOX group and XELOX group[n(%)]
Note:#Fisher exact test.
2.4 SOX和XELOX方案术后病理比较情况
4例病理完全缓解(pCR),其中SOX 3例,XELOX 1例。两组在N分期比较,差异均具有统计学意义(P<0.05);在T分期、M分期、组织学类型、分化程度方面比较,差异均不具有统计学意义(P>0.05)(表4)。
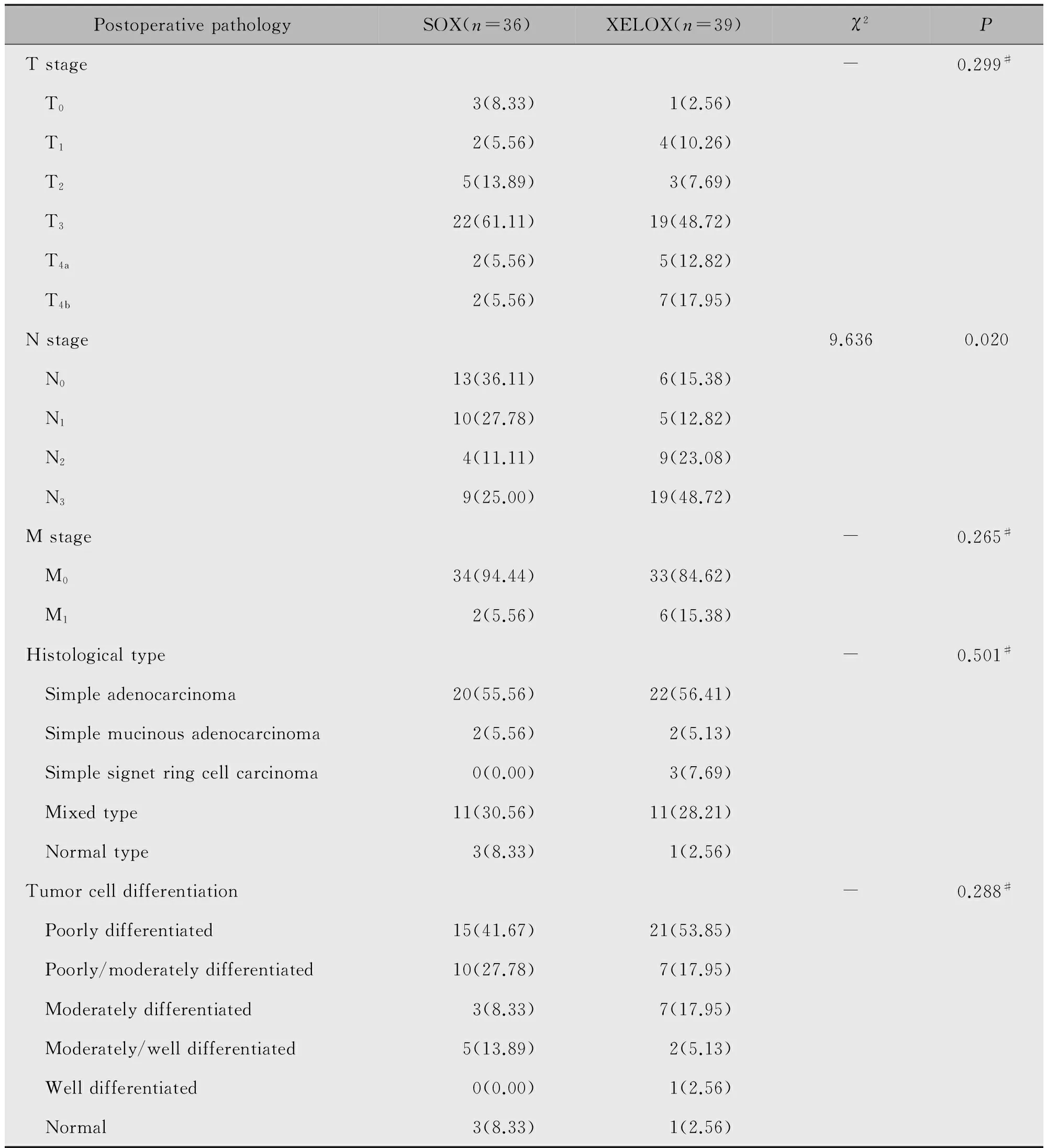
表4 SOX和XELOX方案术后病理比较情况[n(%)]Table 4 The comparison of postoperative pathology between SOX group and XELOX group[n(%)]
Note:#Fisher exact test.
2.5 SOX和XELOX方案化疗不良反应情况
SOX出现骨髓抑制4例、胃肠道反应3例;XELOX出现骨髓抑制4例、胃肠道反应8例。给予止吐和升白药物,症状均得到有效控制和缓解。住院期间无死亡患者发生。
2.6 SOX和XELOX方案生存情况比较
两组患者经2~4个周期新辅助化疗后行手术治疗,术后行2~6个周期化疗。化疗期间常规给予止吐药物治疗。末次随访时间为2016年7月1日,75例患者均行随访,其中有3例失访,随访率为96.00%(72/75)。两组DFS、OS的1年、3年、5年生存率相比较,差异均无统计学意义(P>0.05)(表5)。两组DFS、OS中位生存时间,差异均具有统计学意义(P<0.05)(图1-2)。
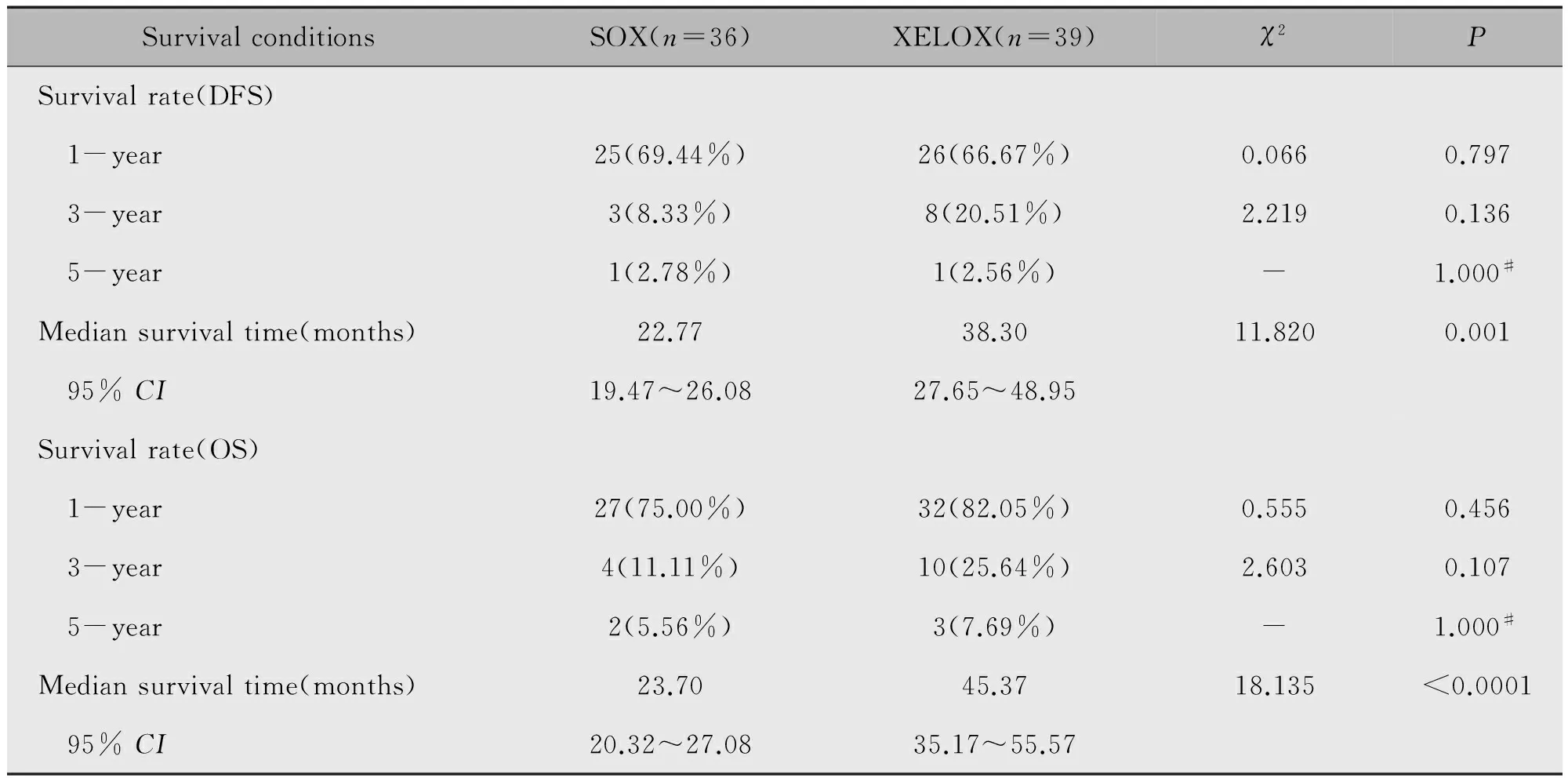
表5 SOX和XELOX方案生存情况比较Table 5 The comparisons of survival conditions between SOX group and XELOX group
Note:#Fisher exact test.
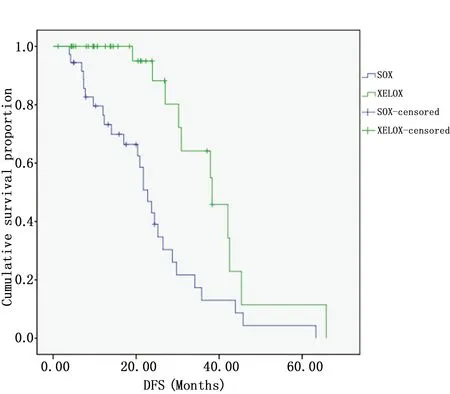
图1 SOX和XELOX方案无病生存时间曲线比较Figure 1 The comparisons of disease free survival curves between SOX group and XELOX group
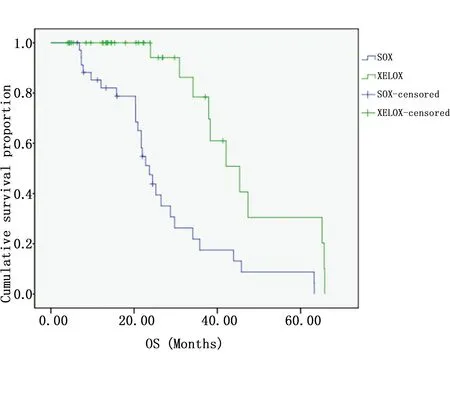
图2 SOX和XELOX方案总生存时间曲线比较Figure 2 The comparisons of overall survival curves between SOX group and XELOX group
3 讨论
日本ACTS-GC和韩国CLASSIC临床试验明确SOX和XELOX方案均具有较好的化疗效果,而被推荐为临床一线化疗方案[12-13]。SOX和XELOX区别在于前者应用替吉奥,后者应用卡培他滨。替吉奥属于第二代5-Fu类药物,其组成包括替加氟、吉美嘧啶、奥替拉西钾三种有效成分,可抑制二氢嘧啶脱氢酶活性,提高体内氟尿嘧啶药物浓度,减少氟尿嘧啶脱氧核苷酸的生成,使消化道的副作用降到较小程度[14]。替吉奥可单药口服,其临床不良反应小,患者一般较易接受。卡培他滨属于抗代谢氟嘧啶脱氧核苷氨基甲酸酯类药物,通过在体内转为氟尿嘧啶,提高其在体内的有效浓度而发挥对抗肿瘤细胞DNA的作用。
本研究发现两组化疗前T分期和N分期均以T4a和N1多见;化疗后T分期均以T4a多见,N分期SOX以N1多见,XELOX方案组以N0多见。术后病理T分期均以T3多见;N分期SOX以N0多见,XELOX以N3多见;其中有4例达到病理完全缓解(pCR)。T分期我们发现术后病理分期要低于CT分期,而在N分期上要高于CT分期。术前CT没有发现转移,而术后病理显示有6例发生转移,这也表明CT TNM分期具有一定的局限性[15]。Koizumi应用SOX有效率接近60%[16],李涛等[17]应用SOX可达69.5%,疾病控制率达97.6%。肖康等[18]应用XELOX有效率达82.5%,疾病控制率达95.0%。本研究结果显示,应用SOX和XELOX有效率分别为47.22%和41.03%;疾病控制率分别为94.44%和97.44%。临床有效率要低于这些学者的研究,疾病控制率大体一致。经新辅助化疗后肿瘤分期均有明显降低,SOX临床降期要低于XELOX(33.33%vs. 43.59%),XELOX临床降期要优于SOX。
新辅助化疗后共有39例行R0根治术,有效切除率达52.00%。研究表明[19-20],应用SOX方案R0根治切除率达81.3%,XELOX方案R0根治切除率达53%。本研究中,SOX和XELOX方案R0根治切除率分别为55.56%和48.72%。这可能与我们选择患者的病期较晚有关。术后我们进行2~6个周期化疗,化疗期间常规给予止吐药物治疗。分析两组的生存情况发现SOX方案DFS 1年、5年生存率要高于XELOX,而3年生存率要低于XELOX;SOX方案OS 1年、3年、5年生存率均低于XELOX。这与朱益平等[21]研究一致,而与李远军等[22]研究有差异。SOX方案DFS和OS的中位生存时间均低于XELOX(22.77vs. 38.30个月;23.70vs. 45.37个月),差异具有统计学意义。从生存曲线上可以看出,XELOX生存时间要长于SOX,远期疗效优于SOX。
综上所述,本研究发现XELOX新辅助化疗效果要优于SOX,术前行2~4个周期的化疗,根据患者缓解情况进行手术,SOX和XELOX均具有较高的安全性和有效性。但在临床治疗上,我们应根据患者的具体情况,而进行综合分析,采用个性化的治疗方案,从而使患者获得最大的治疗效益,以期提高生存时间和改善生活质量。
1 Rebecca LS,Kimberly DM,Ahmedin J,et al.Cancer Statistics,2015[J].CA Cancer J Clin,2015,65(1):5-29.
2 Strong VE,Wu AW,Selby LV,et al.Differences in gastric cancer survival between the U.S.and China[J].J Surg Oncol,2015,112(1):31-37.
3 Marrelli D,Polom K,de Manzoni G,et al.Multimodal treatment of gastric cancer in the west:where are we going?[J].World J Gastroenterol,2015,21(26):7954-7969.
4 Fontana E,Smyth EC.Novel targets in the treatment of advanced gastric cancer:a perspective review[J].Ther Adv Med Oncol,2016,8(2):113-125.
5 Tian SB,Yu JC,Kang WM,et al.Effect of neoadjuvant chemotherapy treatment on prognosis of patients with advanced gastric cancer:a retrospective study[J].Chin Med Sci J,2015,30(2):84-89.
6 Tao F,Bu ZD,Li ZY,et al.Neoadjuvant chemoradiation therapy for resectable esophago gastric adenocarcinoma:a meta-analysis of randomized clinical trials[J].BMC Cancer,2015,15:322-331.
7 Wang X,Wang ML,Zhou LY,et al.Randomized phaseⅡstudy comparing paclitaxel with S-1 vs.S-1 as first-line treatment in patients with advanced gastric cancer[J].Clin Transl Oncol,2013,15:836-842.
8 Bang YJ,Kim YW,Yang HK,et al.Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy(CLASSIC):a phase 3 open-label,randomised controlled trial[J].Lancet,2012,379(9813):315-321.
9 Knight G,Earle CC,Cosby R,et al.Neoadjuvant or adjuvant therapy for resectable gastric cancer:a systematic review and practice guideline for North America[J].Gastric Cancer,2013,16:28-40.
10 Ba-Ssalamah A,Prokop M,Uffnann M,et al.Dedicated multidetector CT of the stamach spectrum of diseases[J].Radio Graphics,2003,23(3):625-645.
11 Yoshikawa T,Tanabe K,Nishikawa K,et al.Accuracy of CT staging of locally advanced gastric cancer after neoadjuvant chemotherapy:cohort evaluation within a randomized phase II study[J].Ann Surg Oncol,2014,21(Suppl 3):385-389.
12 Oh SY,Kwon HC,Jeong SH,et al.A phase Ⅱ study of S-1 and oxaliplatin(SOX)combination chemotherapy as a first line therapy for patients with advanced gastric cancer[J].Invest New Drugs,2012,30(1):350-356.
13 Luo HY,Xu RH,Wang F,et al.Phase Ⅱ trial of XELOX as first-line treatment for patients with advanced gastric cancer[J].Chemotherapy,2010,56(2):94-100.
14 Aoyama T,Yoshikawa T,Watanabe T,et al.Safety and feasibility of S-1 adjuvant chemotherapy for gastric cancer in elderly patients[J].Gastric Cancer,2012,15(1):76-82.
15 Tang L,Li ZY,Li ZW,et al.Evaluating the response of gastric carcinomas to neoadjuvant chemotherapy using iodine concentration on spectral CT:a comparison with pathological regression[J].Clinical Radiology,2015,70:1198-1204.
16 Koizumi W,Takiuchi H,Tsuburaya Y,et al.PhaseⅡstudy of oxaliplatin plus S-1 as first-line treatment for advanced gastric cancer(G-SOX study)[J].Ann Oncol,2010,21(5):1001-1005.
17 李涛,冯道夫,梁美霞,等.进展期胃癌应用SOX方案新辅助化疗对肿瘤TNM分期的影响[J].世界华人消化杂志,2014,22(2):249-252.
18 肖康,戈伟.奥沙利铂联合卡培他滨的新辅助化疗治疗进展期胃癌的疗效及安全性[J].中国肿瘤临床与康复,2016,23(3):261-263.
19 靖昌庆,李乐平,王金中.XELOX和FOLFOX4新辅助化疗方案对不能手术切除的局部进展期胃癌的疗效比较[J].中华消化外科杂志,2010,9(6):430-433.
20 张剑军,郑志超,赵岩,等.FOLFOX、XELOX、SOX 方案用于局部进展期胃腺癌的疗效及安全性比较[J].山东医药,2014,54(33):44-45.
21 Zhu YP,Sheng LL,Wang L,et al.Clinical efficacy of oxaliplatin combined with capecitabine(XELOX)and oxaliplatin combined with S-1(SOX)on advanced gastric cancer[J].Cancer Res Prev Treat,2014,41(7):815-819.
22 李远军,邢娟,吴翰昌,等.奥沙利铂联合替吉奥(SOX)与奥沙利铂联合卡培他滨(XELOX)治疗中国进展期胃癌患者的Meta 分析[J].中国生化药物杂志,2015,5(35):57-60.
(收稿:2016-10-19)
The comparison of clinical efficacy of SOX and XELOX in the neoadjuvant chemotherapy for advanced gastric carcinoma
CHENLi1,ZHANGYuxin1,ZUOYanjiao1,MAFei2,SONGHongjiang1,XUEYingwei1
1.Department of Gastrointestinal Surgery,The Affiliated Tumor Hospital of Harbin Medical University,Harbin 150081,China;2.Department of Endoscopy,The Affiliated Tumor Hospital of Harbin Medical University
Objective To investigate the clinical efficacy of SOX and XELOX in neoadjuvant chemotherapy for advanced gastric carcinoma.Methods Seventy-five cases with advanced gastric carcinoma were selected from our hospital from Feb 1,2011 to Oct 1,2015.SOX and XELOX were used to these patients treatment.The relationship between SOX and XELOX with tumor stage,clinical curative effect evaluation,operation,postoperative pathology,adverse reaction,survival analysis with advanced gastric carcinoma had been analyzed retrospectively.Results The efficacy of SOX and XELOX were 47.22%,41.03%.Compared with the two groups,the CT curative effect evaluation,effective rate,disease control rate had no significant differences(P>0.05).The median survival time of DFS and OS were significant between the two groups(P<0.05).Conclusion The SOX and XELOX for neoadjuvant chemotherapy of advanced gastric carcinoma treatment is safety and effective,and the XELOX is better than SOX in terms of long-term effect,prognosis and clinical benefits.
Neoadjuvant chemotherapy;Advanced gastric carcinoma;Effective rate;Disease free survival;Overall survival
吴阶平基金科学技术部(320.6750.13105);黑龙江省教育厅面上项目(12541458)
1.哈尔滨医科大学附属肿瘤医院胃肠外科(哈尔滨 150081);2.哈尔滨医科大学附属肿瘤医院腔镜室
陈力,男,(1990-),硕士研究生,从事胃肠道肿瘤的临床与基础研究。
宋洪江,E-mail:hongjiangsong2015@163.com
R735.2
A
10.11904/j.issn.1002-3070.2017.01.005
