雷替曲塞联合奥沙利铂治疗中晚期原发性肝癌的临床研究
2017-04-06沈永奇黄军陈超庭斯韬王志祥谢华东孔祥应刘金娥韩朝稳
沈永奇,黄军,陈超庭,斯韬,王志祥,谢华东,孔祥应,刘金娥,韩朝稳
(1.广西医科大学附属柳铁中心医院肿瘤科,广西 柳州 545007;2.贵阳中医学院第三附属医院肿瘤科,贵州 都匀 558004;3.广西科技大学第二附属医院化疗二科,广西 柳州 545006;4.广西中医药大学第三附属医院肿瘤二科,广西 柳州 545001;5.广西中医药大学第三附属医院肿瘤一科,广西 柳州 545001;6.广西壮族自治区柳州市融水县人民医院肿瘤科,广西 柳州545300)
雷替曲塞联合奥沙利铂治疗中晚期原发性肝癌的临床研究
沈永奇1,黄军2,陈超庭3,斯韬4,王志祥5,谢华东6,孔祥应2,刘金娥1,韩朝稳1
(1.广西医科大学附属柳铁中心医院肿瘤科,广西 柳州 545007;2.贵阳中医学院第三附属医院肿瘤科,贵州 都匀 558004;3.广西科技大学第二附属医院化疗二科,广西 柳州 545006;4.广西中医药大学第三附属医院肿瘤二科,广西 柳州 545001;5.广西中医药大学第三附属医院肿瘤一科,广西 柳州 545001;6.广西壮族自治区柳州市融水县人民医院肿瘤科,广西 柳州545300)
目的:探讨雷替曲塞联合奥沙利铂(RALOX)应用于中晚期原发性肝癌(PLC)的疗效及药物毒性反应。方法:选取34例中晚期PLC患者为观察组,对其进行RALOX方案化疗,将同期符合化疗条件但行对症支持治疗的36例中晚期PLC非化疗患者纳入对照组。每2个周期评价客观缓解率(OR)、疾病控制率(DCR)、中位生存时间(mOS)、中位无进展生存期(mPFS)、1年存活率(SR)及毒副反应。结果:观察组的OR、DCR、mOS及mPFS均明显优于对照组(P<0.05);化疗毒副反应多为轻中度消化道反应、肾毒性、肝毒性、骨髓抑制、周围神经毒性,经积极处理以上毒副反应均可缓解。结论:RALOX方案对中晚期PLC安全有效,具有良好的病情控制和生存获益,毒副反应可耐受,值得临床推广应用。
原发性肝癌; 奥沙利铂; 雷替曲塞; 化疗
原发性肝癌(PLC)是常见的恶性肿瘤之一,在我国恶性肿瘤发病率中居第4位[1],占全球肝癌死亡病例数的51%[2-3],患者总体5年生存率不到5%[4]。手术切除及介入治疗是治疗肝癌最有效手段,但多数肝癌患者就诊时已处于中晚期,失去手术及介入治疗的最佳时机。以索拉菲尼为代表的分子靶向药物为中晚期肝癌的一线治疗药物,但其客观疗效依然较低,延长生存期也只有2个多月[5-6],且价格昂贵。化疗逐渐成为主要的治疗手段,但目前尚无标准的化疗方案。本研究将雷替曲塞联合奥沙利铂(RALOX方案)应用于中晚期PLC患者,与同期符合化疗条件但行对症支持治疗者比较,现报告如下。
1 资料与方法
1.1 一般资料
选取2013年7月至2015年7月广西医科大学附属柳铁中心医院、贵阳中医学院第三附属医院、广西科技大学第二附属医院、广西中医药大学第三附属医院和广西柳州市融水县人民医院等6个肿瘤中心34例接受RALOX方案化疗的中晚期PLC患者为观察组,将同期符合化疗条件但不同意化疗、要求行对症支持治疗的36例中晚期PLC患者纳入对照组。纳入标准:①临床、甲胎蛋白水平(AFP)、影像学或病理学证实为中晚期PLC,既往未接受全身化疗者;②具有可测量病灶(CT诊断≥2 cm),可测量病灶影象诊断时间<15 d;③年龄15~70岁;④Karnofsky评分≥60;⑤预计生存期≥3个月;⑥有随访可能;⑦心脏功能、肝肾功能及血象基本正常;⑧患者签署知情同意书。排除标准:①患者伴有其他恶性肿瘤;②伴有严重的活动性感染或严重的心肝肾和造血系统疾病;③患者无可测量或可评价的病灶;④依从性差;⑤患者要求终止治疗,尚不能评价疗效和不良反应者;⑥临床资料不全者。两组一般资料差异无统计学意义(P>0.05),具有可比性。
1.2 方法
观察组行RALOX方案化疗,具体用法为:雷替曲塞(南京正大天晴制药有限公司生产)3 mg/m2,静脉滴注15 min,d1;奥沙利铂(齐鲁制药有限公司生产)130 mg/m2,静脉滴注3 h,d1,21 d为1个周期,至少完成2周期。对照组行对症支持治疗。
1.3 疗效评价
治疗前进行基线评价,包括CT、磁共振成像(MRI)、AFP等。疗效评价在治疗后每42 d进行(RALOX方案2周期,FOLFOX4方案3周期),采用实体肿瘤评价标准RECIST 1.1进行评价。按WHO标准分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。毒性反应评价按NCI标准分为0~IV级。评价目标包括客观缓解率(OR)、疾病控制率(DCR)、中位生存时间(mOS)、中位无进展生存期(mPFS)、1年存活率(SR)及毒副反应。OR=CR+PR,DCR=CR+PR+SD。每2个治疗周期前入院行影像学、AFP复查,电话随访间隔为半月,总随访时间为12个月。
1.4 统计学分析
采用SPSS 18.0软件进行统计分析。OR、DCR、1年SR采用χ2检验,mOS和PFS采用Log-rank检验并绘制Kaplan-Mweier生存曲线,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般情况比较
两组患者平均年龄、性别、肝功能分级等一般资料见表1。

表1 两组患者一般资料比较
2.2 两组患者疗效比较
Child-PughA组患者完成化疗29例,其中PR6例,SD11例,PD12例,OR6例(20.7%),DCR为17例(58.6%),mOS为7.6个月, mPFS为3.7个月,1年SR为8例(27.6%);Child-Pugh B组患者完成化疗31例,其中PR4例,SD9例,PD18例,OR为4例(12.9%),DCR为13例(41.9%),mOS为6.7个月, mPFS为3.1个月,1年SR为5例(16.1%)。两组均无取得CR的患者。两组患者疗效比较,差异无统计学意义(P>0.05)。两组OS、PFS生存曲线见图1-2。

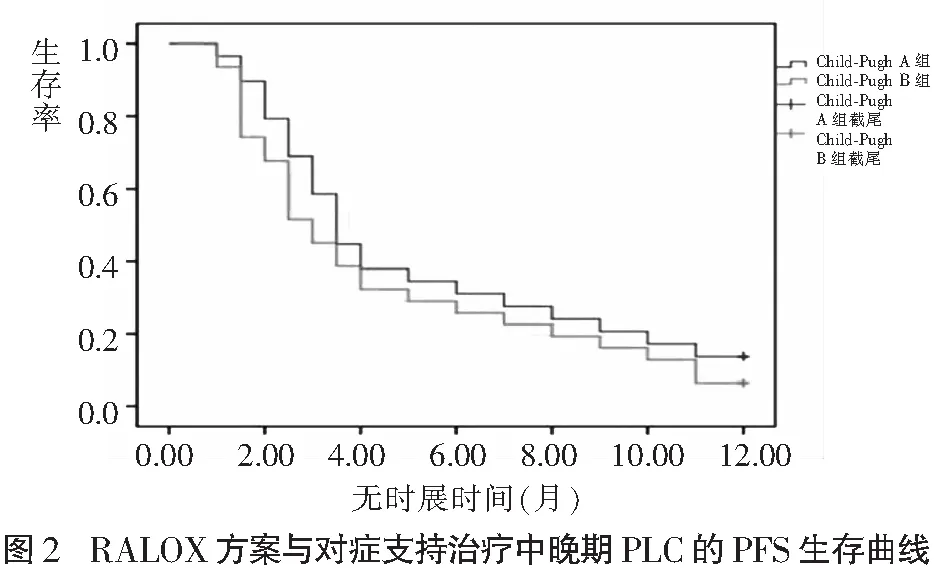
2.3 化疗毒副反应
比较Child-Pugh A组与B组各种不良反应发生率分别为:消化道反应(38.7%vs.72.4%)、肾毒性(12.9%vs.10.3%)、肝毒性(32.3%vs.62.1%)、骨髓抑制(45.2%vs.48.3%)、心脏毒性(6.5%vs.27.6%)、周围神经毒性(29.0%vs.51.7%)及手足综合症(9.7%vs.48.3%),上述不良反应中Child-Pugh A组的消化道反应明显低于B组(P<0.05)。两组严重的(Ⅲ-Ⅳ度)不良反应发生率分别为:消化道反应9(.7%vs.24.1%)、肾毒性(0vs.0)、肝毒性(6.5%vs.20.7%)、骨髓抑制(12.9%vs.10.1%)、心脏毒性(0vs.10.3%)、周围神经毒性(6.5%vs.6.9%)及手足综合症0vs. 10.3%。经积极处理,以上不良反应均可缓解。
3 讨论
长期以来,中晚期肝癌化疗疗效不佳且不良反应较大,很多患者拒绝化疗,医务人员对这部分患者也并不积极推荐化疗。肝癌细胞对化疗药物具有普遍耐药性,传统化疗方案疗效较差,是由于晚期肝癌患者具有较大的肿瘤负荷,此时肝癌的大多数细胞,不处在增殖周期,对化疗不敏感;大多数肝癌细胞表达有较高的多药耐药基因,使肝癌对化疗存在固有的耐药性。同时原发性肝癌患者本身有基础肝脏疾病(肝炎、肝硬化等),肝功能已有损害,而化疗药物多经肝脏代谢,故不良反应较大,一定程度上限制了化疗药物的剂量强度,从而限制了化疗作用[7-8]。
Child-Pugh肝功能分级系统在临床上广泛用于评估肝硬化患者肝功能储备,肝癌患者肝功能储备评估也常采用。本研究采用联合化疗治疗中晚期PLC患者72例,无法耐受化疗不良反应而退出12例(16.7%)。其中Child-Pugh A组退出化疗2例(6.5%),Child-Pugh B组退出化疗10例(24.4%),两组比较,差异有统计学意义(P<0.05)。Child-Pugh A组共完成211周期化疗,平均每例患者完成7.3周期;Child-Pugh B组共完成217周期化疗,平均每例患者完成7.0周期。提示肝功能储备为Child-PughB组的中晚期PLC患者对联合化疗的耐受性比Child-PughA组患者要差。在疗效上,两组患者均能从化疗中获得较好的疾病控制率及临床获益,但Child-Pugh B组患者比Child-Pugh A组有下降趋势,未能得出统计学差异,可能与入组病例数太少有关。在不良反应方面,两组多为轻、中度,经积极处理可缓解,Child-Pugh B组患者消化道反应、肝毒性、心脏毒性、周围神经毒性、手足综合症的发生率和与严重程度均比A组重,肾毒性、骨髓抑制两组相当。较重的不良反应,如严重心脏毒性、手足综合征等,大多数发生在Child-Pugh B组。提示肝功能较差可能导致较明显的化疗不良反应,而疗效下降也可能与患者因不良反应而无法耐受更多的化疗周期有关。RALOX方案与FOLFOX4方案近年来被广泛应用于食管癌[9]、胃癌[10]、结直肠癌[11-12],其不良反应轻于两方案对晚期PLC的治疗,可能与肝癌患者肝功能不良、腹水、对药物生物转化能力下降有关[13]。
综上所述,Child-Pugh A和B的中晚期PLC患者均能从化疗中获得较好的疾病控制率及临床效果,但Child-Pugh B的患者比Child-Pugh A的患者化疗耐受性差,疗效有下降趋势,不良反应也较重。提示联合化疗可能不是治疗Child-Pugh B 中晚期PLC患者的最佳选择,对这类患者的单药化疗或许是我们下一步的研究方向。当然,本研究是局部地区,样本较小、参加的肿瘤中心较少的多中心临床研究,其结论尚待大样本的多中心临床研究进一步证实。
[1] Chen W,Zheng R,Baade PD,etal.Cancer statistics in China,2015[J].CA Cancer J Clin,2016,66(2):115-132.
[2] 吕桂帅,陈磊,王红阳.我国肝癌研究的现状与前景[J].生命科学,2015,27(3):237-248.
[3] Wallace MC,Preen D,Jeffrey GP,etal.The evolving epidemiology of hepatocellular carcinoma:a global perspective[J].Expert Rev Gastroenterol Hepatol,2015,9(6):765-779.
[4] 杨柳青,秦叔逵,华海清,等.XELOX方案治疗中晚期原发性肝癌的临床观察[J].临床肿瘤学杂志,2013,18(8):704-708.
[5] Di Marco V,De Vita F,Koskinas J,etal.Sorafenib:from literature to clinical practice[J].Ann Oncol,2013,24(Suppl 2):ii30-ii37.
[6] Liu Y,Wu W,Hong W,etal.Raltitrexed-based chemotherapy for advanced colorectal cancer[J].Clin Res Hepatol Gastroenterol,2014,38(2):219-225.
[7] Qin S,Bai Y,Lim HY,etal.Randomized,multicenter,open-label study of oxaliplatin plus fluorouracil/leucovorin versus doxorubicin as palliative chemotherapy in patients with advanced hepatocellular carcinoma from Asia[J].J Clin Oncol,2013,31(28):3501-3508.
[8] Meydan N,Kundak I,Yavuzsen T,etal.Cardiotoxicity of de Gramont's regimen:incidence,clinical characteristics and long-term follow-up[J].Jpn J Clin Oncol,2005,35(5):265-270.
[9] Jensen SA,Baeksgaard L,Petersen LN,etal.Cardiotoxicity induced by 5-fluorouracil or capecitabine[J].Ugeskr Laeg,2010,172(1):48-51.
[10]王晓元,李曙光,赵轶锋,等.雷替曲塞或氟尿嘧啶联合奥沙利铂治疗晚期结直肠癌疗效的Meta分析[J].实用癌症杂志,2015,30(9):1354-1356.
[11]Chen PJ,Furuse J,Han KH,etal.Issues and controversies of clinical trials in Asia: experts’ opinion[J].Liver Int,2010,30(10):1427-1438.
[12]刘文稚,李孟考,陈祥明.雷替曲塞联合奥沙利铂治疗结直肠癌肝转移的临床研究[J].中华临床医师杂志(电子版),2015,9(1):146-148.
[13]Avallone A,Di Gennaro E,Silvestro L,etal.Budillon A Targeting thymidylate synthase in colorectal cancer:critical re-evaluation and emerging therapeutic role of raltitrexed[J].Expert Opin Drug Saf,2014,13(1):113-129.
(学术编辑:赵妍丽)
本刊网址:http://www.nsmc.edu.cn
作者投稿系统:http://noth.cbpt.cnki.net
邮箱:xuebao@nsmc.edu.cn
本刊网址:http://www.nsmc.edu.cn
作者投稿系统:http://noth.cbpt.cnki.net
邮箱:xuebao@nsmc.edu.cn
Clinical study of raltitrexed combined with oxaliplatin in the treatment of middle and advanced primary liver cancer
SHEN Yong-qi1,HUANG Jun2,CHEN Chao-ting3,SI Tao4,WANG Zhi-xiang5,XIE Hua-dong6,KONG Xiang-ying2,LIU Jin-e1,HAN Chao-wen1
(1.DepartmentofOncology,LiutieCentralHospitalAffiliatedtoGuangxiMedicalUniversity,Liuzhou545007,Guangxi;2.DepartmentofOncology,TheThirdAffiliatedHospitalofGuiyangCollegeofTraditionalChineseMedicine,Duyun558004,Guizhou;3.No.2DepartmentofChemotherapy,TheSecondAffiliatedHospitalofGuangxiUniversityofScienceandTechnology,Liuzhou545006,Guangxi;4.No.2DepartmentofOncology,TheThirdAffiliatedHospitalofGuangxiUniversityofTraditionalChineseMedicine,Liuzhou545001,Guangxi;5.No.1DepartmentofOncology,TheThirdAffiliatedHospitalofGuangxiUniversityofTraditionalChineseMedicine,Liuzhou545001,Guangxi;6.DepartmentofOncology,People’sHospitalofRongshuiCounty,Liuzhou545300,Guangxi,China)
Objective:To explore the clinical efficacy and drug-toxic reactions of raltitrexed combined with oxaliplatin (RALOX) in the treatment of middle and advanced primary liver cancer (PLC).Methods:A total of 34 patients with middle and advanced PLC were selected as the observation group and treated with RALOX protocol,and another 36 patients with middle and advanced PLC in corresponding period and treated with symptomatic support treatment were took as the control group.Objective remission rate (OR),disease-control rate (DCR),median survival rate (mOS),median progression-free survival (mPFS),1-year survival rate (SR) as well as toxic and adverse reactions were evaluated every 2 cycle.Results:The observation group was notably better than the control group in OR,DCR,mOS and mPFS (P<0.05).The chemotherapy-induced toxic and adverse reactions were mainly mild and moderate gastrointestinal reactions,renal toxicity,liver toxicity,myelosuppression and peripheral nervous toxicity,which were relieved after positive treatment.Conclusions:RALOX protocol is safe and effective in the treatment of middle and advanced PLC,has excellent disease control and survival benefits,and is tolerable in toxic and adverse reactions,thus deserving to be widely applied in clinic.
Primary liver cancer;Oxaliplatin;Raltitrexed;Chemotherapy
10.3969/j.issn.1005-3697.2017.01.016
广西卫计委科研项目(Z2014408);柳州市科技攻关项目(2014J030424)
2016-11-20
沈永奇(1974-),男,副主任医师。E-mail: gxnnsyq@163.com
沈永奇,E-mail:gxnnsyq@163.com
时间:2017-3-6 21∶07
http://kns.cnki.net/kcms/detail/51.1254.R.20170306.2107.032.html
1005-3697(2017)01-0057-03
R735.1
A
