国家“重大新药创制”专项药品市场准入情况研究
2017-04-06刘永军胡琼
刘永军++胡琼


[摘要] 本文通过数量及时间两个指标,分析了2008~2016年国家“重大新药创制”专项药品在注册审评、招标采购、医保三方面的市场准入情况,提出应通过优化专项药品特殊审评制度以加快审评进度,规范并缩短药品实际采购周期,建立医保药品目录动态调整制度,完善新药集中采购及医保药品支付价格形成机制,最终达到完善专项系统性政策安排的目标。
[关键词] 重大新药创制;注册审评;招标采购;医保准入
[中图分类号] R95 [文献标识码] A [文章编号] 1673-7210(2017)02(c)-0142-04
国家“重大新药创制”重大科技专项(以下简称“专项”)自2008年启动以来,提升了我国医药行业自主创新技术与能力,取得了丰硕成果[1]。其中,创新药物研发成果是我国新药研发能力的直接体现,也是专项的工作重点[2]。根据国家食品药品监督管理总局药品审评中心(以下简称“CDE”)统计数据显示,专项启动后,已有90个品种获得新药证书,135个品种取得临床批件[3]。专项资助的新药中,一类新药占56.8%,二类新药占23.9%,三类新药占11.1%[4]。受专项资助研发的创新药物,在资金支持、税收优惠、人才引进等方面,均享受着得天独厚的政策优待[5]。
然而,对于企业和患者来说,新药的研发成功只是第一步,其成功上市销售并为患者所用,才能保障人民的用药需求,同时提高企业的创新积极性。因此,专项的影响范围不应仅局限于对研发的支持,更应该扶持新药的市场化环节。鉴于此,本文将从注册审批、招标采购及医保三方面入手,考察各项政策对国家“重大新药创制”专项药品(以下简称“专项药品”)的支持力度及准入情况,分析存在的问题及其原因,并提出相应的政策建议,以完善我国重大新药创制专项的系统性政策安排,达到“科技惠及民生”的根本目标。
1 市场准入现状与问题
1.1 注册审评
近年来,我国提出建设创新型国家战略,药品申报数量显著提高。CDE年报[6]显示,2013年新药临床试验申请进入CDE的等待时间为6个月,新药生产申请的等待时间为14个月,审评的总时间约为42个月。
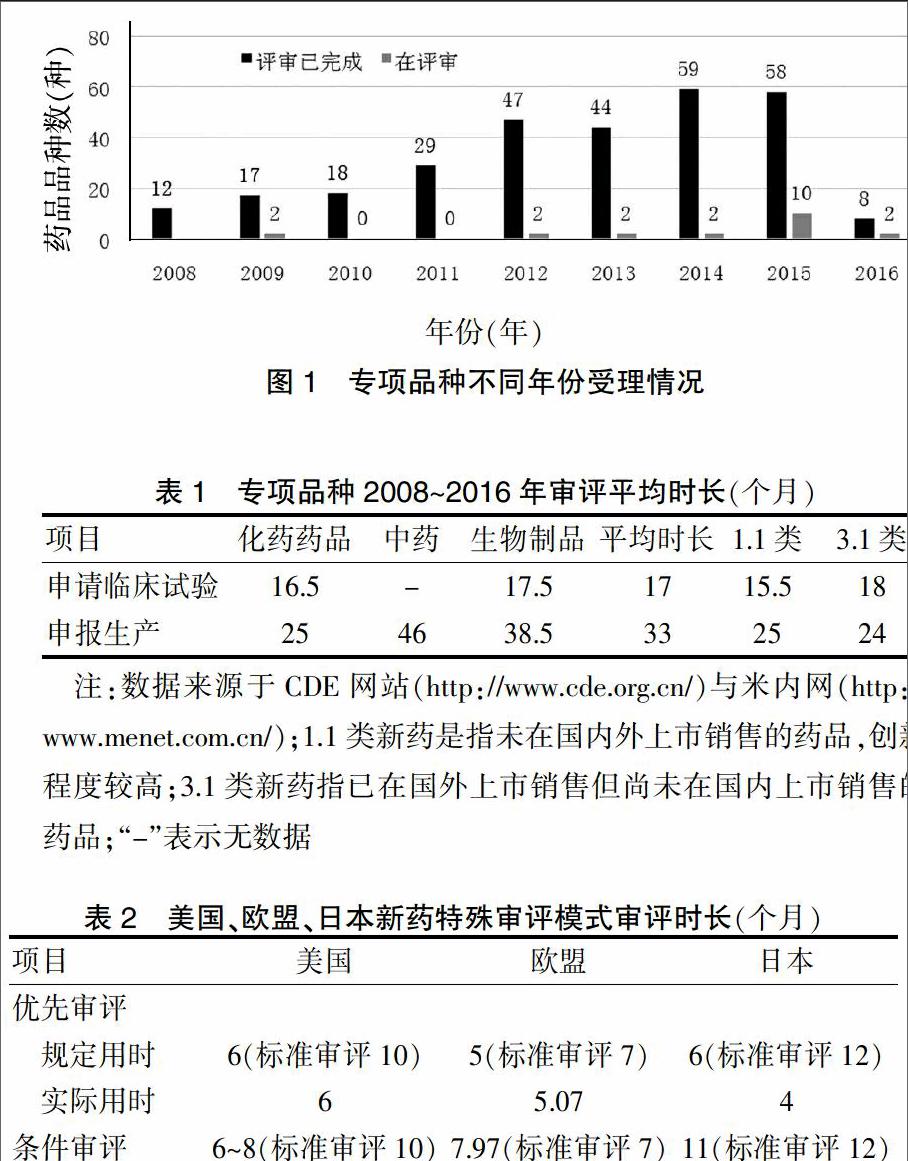
为加快专项资助项目的成果转化效率,重大新药创制专项实施办公室与CDE从2009年开始探索建立专项药品快速审评机制。从审评情况来看,2008~2016年12月,进入CDE的专项药品共计312个(以受理号计,下同),仅20个品种处于“在审评”状态。各年具体情况如图1和表1所示。需要说明的是,表1中的审评平均时长是指2008~2016年专项药品从提交(临床试验或生产)申请至收到审评结果之间的时间,包括药品注册的受理、审评及审批3个环节。
从图1可知,2008年以来,CDE对专项品种的审评速度及效率呈上升趋势。结合表1来看,专项药品申请临床试验和申报生产的平均时长分别为17个月和和33个月,其中专项1.1类申请临床试验和申报生产的平均审评时长分别为15.5个月和25个月,专项3.1类分别为18个月和24个月,分别快于我国1.1类新药总体审评时长(临床14个月,生产27个月),及3.1类新药总体审评时长(临床27个月,生产34个月[7])。
即便如此,我国重大新药创制专项药品的审评时长仍然远高于国外。美国、日本、欧盟等发达国家对新药设置了特殊审评模式,如优先审评(基础性特殊审评模式)、加速审批(针对临床用药空缺、基于替代终点的新药)、快速通道法(治疗严重疾病且目前临床用药空缺的新药)、突破性疗法(针对现有疗法有明显改善的新药)[8]等,这些模式侧重点不同,相互补充,缩短了审评时间。从表2[9]可见,美、日、欧盟等新药特殊审评程序的药品审评周期用时均未超过12个月,优先审评模式下的审评实际用时不超过6个月,是我国专项药品审评时长的1/4。
1.2 招标采购
我国药品进入医院临床需通过集中招标采购制度,该制度直接影响药品的销售情况。对此,本文统计了2008~2016年专项1类新药,筛选出公布招标信息的15种新药,通过米内网查询其在各省的中标信息,见表3。需要说明的是,首次中标间隔时间指该药从获准上市到首次中标之间的时间间隔,平均中标间隔时间指该药从获准上市到不同省份首次中标之间的平均时间间隔。
通过表3可知,不同药品招标进度、中标情况不尽相同。以上15种专项1类新药平均首次中标间隔时间为382 d(约1年),平均中标省份6个,平均中标间隔时间为742 d(约2年)。从批准上市到进入省级集中采购并中标,最快的是鹽酸埃克替尼片,历时166 d(约5.5个月),首先于2011年在广西省中标,目前已在11个省中标,整个招标进度远超其他新药。总体上专项药品进入各省招标目录并中标的间隔时间较长,中标省份数量也不容乐观。有文章指出,算上后续医院进药与进入医保的时间,我国药品获得市场准入比其他国家晚4~8年[10]。
导致专项1类新药招标进度慢、中标省份少的原因在于药品招标周期的不规范与新药采购通道的不完善。我国从2000年实行由政府主导的药品招标采购制度以来,多次对招标范围、方式等进行规定和改革,但对招标周期却一直没有出台明确的规定,各省的招标时间、周期也不同[11]。原则上药品招标采购应为一年进行一次,但事实上各省普遍存在招标周期长和招标时间随意的问题。不在招标周期内上市的新药无法通过招标进入医院临床使用,难以形成规模销售,导致我国有近1/3的新药在上市两年后仍不能进入任何省份的招标采购目录[12]。国家投入巨大财力、人力的重大新药创制专项药品也难逃此运。
1.3 医保准入
目前,我国医疗保障体系覆盖率超过95%,全民医保体系已经形成,基本医疗保险成为药品最大的付费方,因此能否进入医保报销范围在很大程度上决定着药品的市场份额。
我国国家医保药品目录最近一次调整是2009年,而专项药品上市时间都在此之后,因此均未被纳入到国家医保药品目录。除了国家目录外,各省可根据本地区用药需求、医保基金容量等实际情况对国家乙类目录进行调整,形成本地区的医保乙类药品目录。本文通过米内网、各省市人社部与卫计委网站查询了2008~2016年专项1类新药进入各省医保药品报销范围(包括城镇职工与城镇居民医保、新农合及大病保险)的数量及等待时间(表4),其中,等待时间是指该药获准上市到纳入医保报销范围的时间间隔。
从数量来看,2008~2016年共有8个专项1类新药进入医保报销范围,占专项1类新药总数的44.4%,进入报销范围的新药也多是只进入了一、两个省份的医保,总体来说,进入医保报销范围的药品数量及进入省份数目不容乐观。值得一提的是盐酸埃克替尼,在国家层面首批药品谈判之前,只有浙江、湖南、内蒙古、青岛市4个地区将其纳入医保报销范围,谈判成功之后,在国家层面的推动下,17个省份将其纳入医保合规费用范围。由此可见,国家层面的扶持对于新药快速进入各省医保报销范围起着重要的作用,在医保目录更新缓慢的情况下,国家药品谈判是多方共赢的推动方式。
再从等待时间来看,8个进入各省医保范围的专项1类新药,等待时间最短的为康柏西普眼用注射剂(297 d,约1年),最长的艾瑞昔布平均用时1877 d(约5年)。进入医保目录的专项1类新药的平均等待时间为983 d,若算上尚未进入医保的其他药品,等待时间将大大延长。这与美国新药从上市到获得报销许可平均6个月,日本平均3个月[13],德国、英国平均1个月[12]的等待时间形成鲜明对比。同样以盐酸埃克替尼为例,其上市后,在2013~2015年间进入了浙江等4省市的医保报销范围,平均等待时间超过3年。但在国家首批药品谈判成功之后,仅历时6个月就进入其他17省的医保报销范围,等待时间大大缩短。
造成我国专项1类新药进入医保范围数量少、等待时间长的重要原因是我国医保目录更新周期长,国家层面政策扶持少。在此情况下,由于缺乏国家层面的政策扶持,省级层面难以取得谈判价格优势,缺乏谈判增补动力,导致新药在省级增补中也举步维艰。
2 讨论与政策建议
国家重大新药创制专项的新药代表了我国药品创新研发的最高水平。作为国家层面的制度安排更需要产业链相关政策的扶持与促进,避免将产业条块割裂开,应当形成科技、产业、市场的全面协调[10],使创新性的研究成果能够快速应用于临床。
2.1 完善并优化专项药品特殊审评制度,加快审评进度
首先,逐步探索建立适合我國国情的多模式新药特殊评审制度。鉴于新药在创新程度、可替代程度、疾病严重程度、临床需求等方面的侧重点不同,将所有药品纳入同一种特殊审评模式制度难免捉襟见肘。因此,一方面可以借鉴美国优先评审、快速通道法、突破性疗法及加速批准[14]四种模式相互补充,强化激励效应的多通道特殊审评制度。另一方面可从加速临床试验的角度,借鉴英国“早期获得药物计划(EAMS)”,建立早期收获评审机制,允许患有危及生命疾病的患者使用尚未进行审评但临床急需药品,进行临床试用,加速审评进程[15]。
其次,加强注册审评各环节与各部门间的沟通与协调,减少重复审核与转换带来的时间消耗。另外,设定明确的目标审评时限与审评节点用时,使评审工作更加可控。目前我国并未出台有关加快审评品种的具体审评时限规定[16],在一定程度上制约了优先审评制度执行效果的可预期性。在此基础上,可以通过既定审评绩效考核与评估审评工作,配置与审评任务相匹配的审评资源,进一步提高审评效率及质量。
2.2 规范并缩短药品实际采购周期,完善新药集中采购机制
应强化对各省招标采购工作执行的监督,缩短实际采购周期,确保各省按照要求一年一次开展招标采购工作。同时,为鼓励技术创新和技术进步,促使新技术、新产品尽快应用于临床,对采购周期内新批准上市的药品可进行备案采购,重大创新产品开辟绿色通道。
药品政府定价取消以后,药品价格主要依靠集中采购、医保支付价格制度形成。各省对于医保支付价格制定的探索中也主要参考招标或中标价,招标或中标价关系到支付标准制定的合理性[17]。因此,应将完善药品集中采购与医保支付价格制度同步推进,实行带量采购,逐步扩大直接挂网采购、谈判采购品种范围,实现精准招标,规范药品采购行为,提高药品采购透明度,
2.3 建立医保药品目录动态调整制度,完善新药医保支付价格形成机制
缩短目录定时调整周期,以药物经济学评价为基础,结合专家意见,遴选更加安全有效的药品,提高目录中收载药品的经济性及有效性。对于成本效果比不高的药品,建立目录药品退出机制,提高医保基金的使用效率。其次,设计科学的医保药品目录动态调整机制,采用差异化调整的理念,为创新程度较高的专项药品开通进入医保目录的“绿色通道”[18],即在药品目录调整周期内,若有重大创新意义的、可弥补治疗领域空白的新药上市,可根据企业申请,每6个月或3个月为满足要求的新药开启“绿色通道”,通过药物经济学评价的药物便可及时纳入医保报销范围。如此,不仅可以使新药更快惠及更多患者、节省医保费用和个人支出,而且据测算这些创新药年销售可达500~600亿元,可拉动GDP增长近0.1个百分点[19]。
另外,完善创新药品的医保支付价格形成机制,合理确定创新药品价格。鉴于新药市场竞争不充分、价格水平较高的特点,其价格一般采用谈判方式形成[20]。综合考虑企业利润、医保基金承受能力、临床需求程度、预期销售量、国际价格水平等各方因素,通过政府与医药企业之间谈判,合理确定创新药品医保支付价。同时,完善国家层面药品谈判机制,充分发挥国家统一谈判的优势,一方面以国家的市场大份额换取更合理的价格,一方面借助国家层面的推动力量,更快进入各省公立医院采购目录及医保药品报销范围。在此基础上,有条件的省份可根据本省具体情况,将其他临床需要的新药通过谈判纳入医保报销范围,最大程度惠及患者、企业及医保三方。
[参考文献]
[1] 叶仙蓉.对“重大新药创制”科技重大专项的认识和体会[J].中国新药杂志,2013,22(6):632-635.
[2] 孙宇,米献淼,李鹏燕等.“重大新药创制”重大专项:我国药物创新体系建设与发展的新引擎[J].中国新药杂志,2013,22(8):868-872.
[3] 顾金辉.重大新药创制专项将推动新药上市后灵活定价[N].医药经济报,2016-11-28(3).
[4] 肖坤全,虞忠,吕勇均.浅析“重大新药创制”重大专项实施的政策保障及效果[J].现代经济信息,2011,12(23):358-358.
[5] 于嘉轩,任翔,杨东升,等.“重大新药创制”冷思考[N].医药经济报,2016-01-11(3).
[6] 国家食品药品监督管理总局药品审评中心.2013年度药品审评报告[EB/OL].(2014-03-06).http://www.cde.org.cn/news.do?method=largeInfo&id=313280.
[7] 丁香园.药品审评时间知多少[EB/OL].(2014-11-20).http://yao.dxy.cn/article/92630.
[8] FDA.Fast Track,Breakthrough Therapy,Accelerated Approval,Priority Review[EB/OL].(2015-06-12).http://www.fda.gov/forpatients/approvals/fast /default.htm.
[9] 姚雪芳,丁錦希,李鹏辉,等.国外新药特殊审评模式比较与借鉴[J].中国药学杂志,2016,51(19):1714-1720.
[10] 刘正午.1.1类新药集采“门缝”仍小[N].医药经济报,2013-07-24(A04).
[11] 满春霞,管晓东,邹武捷,等.我国各省药品集中招标采购政策分析和思考[J].中国卫生政策研究,2016,9(7):53-59.
[12] 冯君.药品招标周期不可忽视的“痛”[J].中国招标,2015, 21(26):32-32.
[13] 孙燕,孙利华.新药价格管理对医药技术创新的影响[J].中国医药工业杂志,2011,42(3):236-240.
[14] 陶秀梅,江德元,郭卫东,等.美国“突破性治疗”药品的特征分析和启示[J].中国医药工业杂志,2016,47(11):1477-1482.
[15] 北京生物医药产业发展报告编辑委员会.启航2014北京生物医药产业发展报告[M].北京:科学出版社,2014: 12.
[16] 袁林,邵明立.美国FDA加快新药审评策略以及对我国的启示[J].中国新药杂志,2015,24(21):2401-2404.
[17] 常峰,罗修英,路云.药品支付价格制定方法的国际经验及其启示[J].价格理论与实践,2015,24(9):49-51.
[18] 徐伟,白婕.我国创新药物国家医保目录准入情况研究[J].中国药房,2016,27(33):4609-4612.
[19] 石光,刘芳瑜.我国生物医药产业发展的现状与对策[J].中国卫生政策研究,2016,9(3):16-19.
[20] 常峰,罗修英,崔鹏磊.典型国家基于价值的新药定价机制及对我国的启示[J].中国新药杂志,2015,24(18):2047-2051.
(收稿日期:2016-11-03 本文编辑:程 铭)
