微通道内离子液体/乙醇混合溶液吸收CO2的传质特性
2017-02-28张璠玢朱春英付涛涛姜山杜威张沁丹马友光
张璠玢,朱春英,付涛涛,姜山,杜威,张沁丹,马友光
(化学工程联合国家重点实验室,天津大学化工学院,天津化学化工协同创新中心,天津 300072)
微通道内离子液体/乙醇混合溶液吸收CO2的传质特性
张璠玢,朱春英,付涛涛,姜山,杜威,张沁丹,马友光
(化学工程联合国家重点实验室,天津大学化工学院,天津化学化工协同创新中心,天津 300072)
采用高速摄像仪对微通道内离子液体/乙醇混合溶液吸收CO2的传质行为进行了实验研究。考察了弹状流型下气液两相流量比和离子液体浓度对液侧体积传质系数kLa和液侧传质系数kL的影响。当离子液体浓度不变时,kLa、kL均随气液流量比的升高而增大并逐渐趋于恒定。当液相流量不变时,对于不同浓度的离子液体溶液,液侧体积传质系数kLa和液侧传质系数kL随气液流量比的变化曲线出现了交叉点。在交叉点之前,kLa和kL均随着离子液体浓度的增大而减小;在交叉点之后,kLa和kL均随着离子液体浓度的增大而增大。提出了用于预测液侧体积传质系数kLa的新的量纲1经验关联式,预测效果良好。
微通道;离子液体;吸收;二氧化碳;传质
引 言
近年来,CO2作为主要的温室气体,其过量排放造成了日益严重的全球温室效应,因此,CO2的捕集和封存对于抑制温室效应至关重要[1]。同时,由于CO2本身是一种安全、无毒、易得的碳资源,对其进行资源化利用也具有重要意义。目前,工业上广泛采用醇胺类物质吸收CO2,如单乙醇胺(MEA)、二乙醇胺(DEA)及甲基二乙醇胺(MDEA)等。醇胺吸收法吸收速率较快,但液体胺存在腐蚀设备、易挥发、吸收成本高和再生能耗大等问题[2]。
离子液体(ionic liquid,IL)是一种在室温或接近室温条件下呈液态、完全由离子组成的盐。与传统有机溶剂相比,离子液体具有低饱和蒸气压、不易挥发、热稳定性好且选择性好等优点,是一种新型的绿色溶剂。研究表明,CO2气体在离子液体中具有较高的溶解度[3-5]。相比于H2、O2、CH4、N2等气体,离子液体对CO2的吸收选择性更好[6-9]。这也为烟道气、天然气等混合气中CO2的吸收脱除提供了新的选择。同时,离子液体吸收CO2的过程完全可逆,溶剂再生过程较容易实现。但是,离子液体黏度大、价格高,这也限制了其在工业生产中的广泛应用。为此,研究者开始将离子液体与其他纯溶剂进行复配来解决上述问题[5,10-15]。乙醇作为一种常用的有机溶剂,具有黏度低、安全无毒、廉价易得等特点,能够与离子液体互溶并有效降低混合溶液的黏度。因此,离子液体/乙醇混合溶液结合了两者各自的优点,有望成为一种新型的CO2吸收剂。
传统工业中,CO2的吸收过程通常在吸收塔等大型设备中进行,成本高且吸收效率低。相比之下,微反应器能够提供高比表面积,进而提高传质效率,提高能量利用率,减小反应系统体积[16-20],为实现CO2的高效吸收提供了可能。文献中已有一些学者针对微通道内CO2气体的吸收过程进行了研究。Ganapathy等[21]以CO2/N2混合气体为分散相,DEA水溶液为连续相,得到的液侧体积传质系数比传统吸收设备高出2~4个数量级,研究了不同通道当量直径和不同气液相浓度组成对压降、吸收率、传质系数、Sherwood数等的影响,并建立了Sherwood数的经验关联式。Cubaud等[22]针对蛇形长通道内水吸收CO2的过程进行了研究,考察了气泡初始长度与初始液相分率之间的关系,并对气体溶解规律以及通道内的流型转变规律进行了研究。Lokhat等[23]采用降膜微反应器研究了乙二醇溶液吸收CO2的传质过程,考察了微反应器放置角度以及气相流量对传质系数的影响,结果表明,在相同气速下,液测传质系数随着微反应器倾斜角度的增大而增大,而在微反应器倾斜角度较小时,气速的增大能显著提高传质效果。Yue等[24]分别采用水、NaHCO3/Na2CO3缓冲液以及NaOH溶液吸收CO2,研究了水力直径为667 μm的微通道内的物理吸收和化学吸收过程,计算得到的体积传质系数kLa为0.3~21 s-1,比传统气液反应器的传质系数高1~2个数量级。Yao等[25]对微通道内乙醇水溶液吸收CO2过程进行了研究,得到了吸收过程中气泡长度的变化规律,确定了传质系数与乙醇水溶液浓度之间的关系。Zhu等[26]对微通道内CO2的MEA溶液化学吸收过程进行了研究,分别考察了气液流量和MEA溶液浓度对传质系数的影响,并建立了体积传质系数的预测模型。然而,迄今鲜有关于微通道内离子液体/无水溶剂混合溶液吸收CO2的文献报道。
本文利用高速摄像仪对T型微通道内弹状流条件下IL/无水乙醇混合溶液吸收CO2的传质过程进行了观测记录,采用可视化在线分析法考察了气、液两相流量以及混合溶液中IL浓度对气泡长度、液侧体积传质系数和液侧传质系数的影响。考虑操作条件和离子液体浓度对传质效果的影响,提出了新的液侧体积传质系数预测式。
1 实 验
实验装置如图1所示。分别用两个微量注射泵(Harvard Apparatus, PHD2000, USA, 误差为1%)驱动气相和液相进入水平放置的微通道,气液两相流经微通道后进入收集瓶。微通道进口压力由压差传感器(Honeywell ST3000, USA)进行测量,出口压力为大气压,压降测量误差为0.8%。实验过程中固定液相流量不变,改变气相流量。每次改变流量后,待流型及压力稳定后,采用高速摄像仪(Motion Pro Y-5, USA)对通道内气液两相流动及传质过程进行实时观测并记录,拍摄频率设定为1000帧/秒。
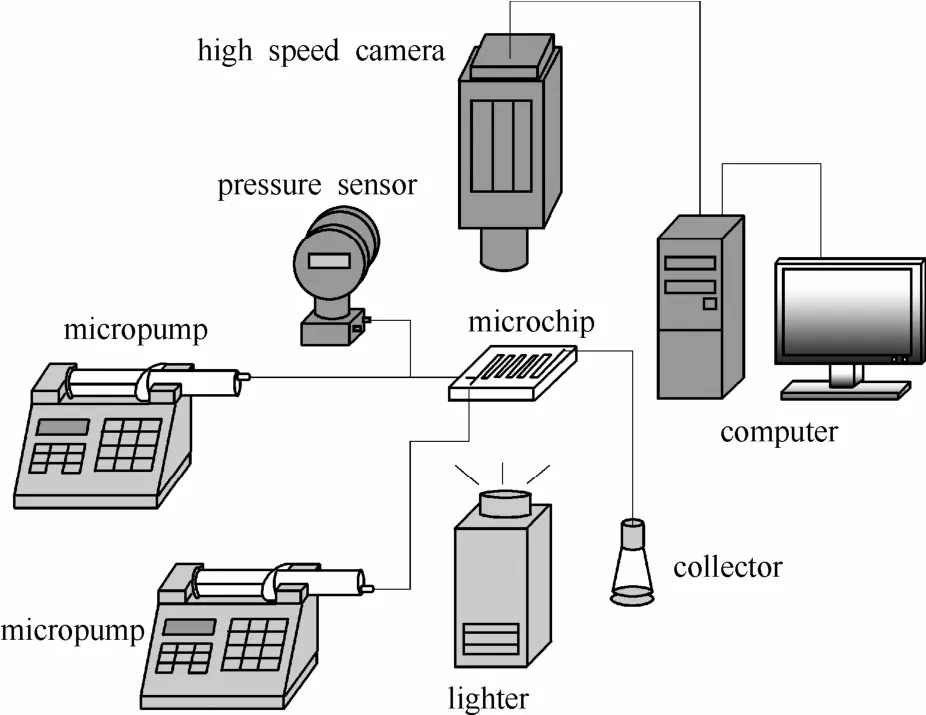
图1 实验装置Fig. 1 Schematic diagram of experimental setup
气相采用CO2气体(质量分数≥99%,天津市六方高科技气体供应站),液相采用不同浓度的1-丁基-3-甲基咪唑四氟硼酸盐[bmim][BF4](纯度≥99%,河南利华制药公司)和无水乙醇(质量分数≥99.7%,天津科密欧化学试剂公司)混合溶液。实验中,液相IL的质量分数wIL分别为5%、15%、25%。实验在弹状流条件下进行,液相体积流量QL分别为20、30、40、50 ml·h-1,气液两相流量比QG/QL的范围是3~11。实验所用液体密度通过密度仪(Anton Paar, Austria)测量,液体黏度通过全自动乌氏毛细管黏度仪(iVisc, LAUDA, Germany)测量,表面张力通过表面张力仪(OCAH200, Data Physics instruments GmbH, Germany)测量。实验在298.15 K和常压下进行。
微通道采用PMMA(聚甲基丙烯酸甲酯)材质的蛇形长通道,采用T型错流进样方式,主通道长度为130 mm,如图2所示。微通道截面是400 μm×400 μm的正方形,气液两相进口段长度均为10 mm。
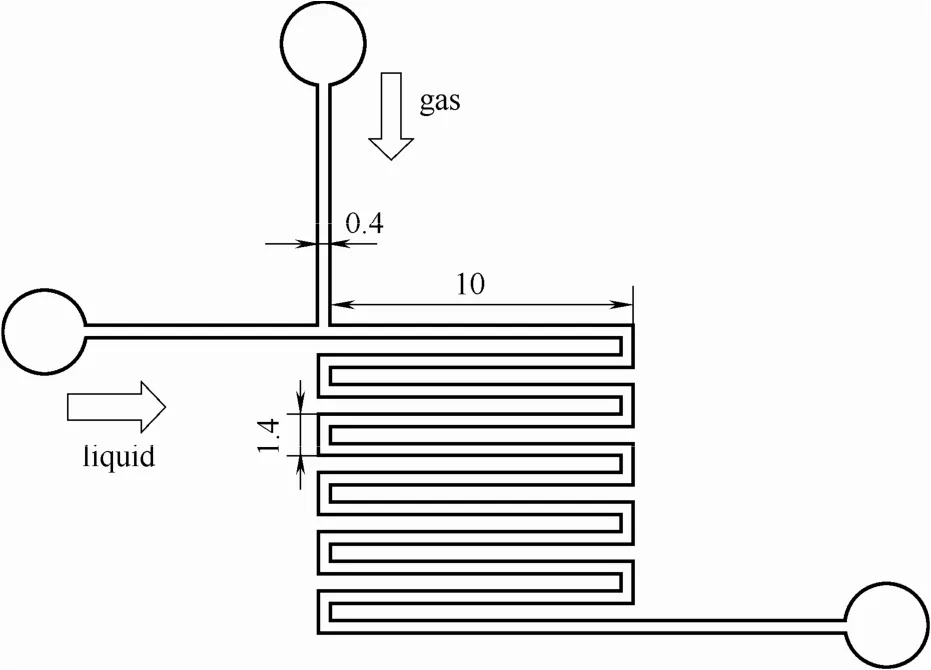
图2 微通道结构Fig. 2 Schematic diagram of microchannel structure
2 结果与讨论
实验中观测到的流型有弹状-泡状流、弹状流、弹状-环状流,如图3所示。与其他流型相比,弹状流具有良好的流动可控性和稳定性,易于确定气液界面和气泡体积。因此,本文主要考察了弹状流型下混合溶液吸收CO2的传质过程。
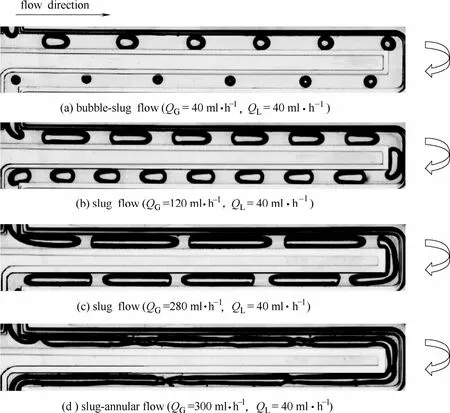
图3 第一、二段通道内的气液两相流型Fig. 3 Flow regimes of gas-liquid two-phase flow in the first and the second sections of microchannel (wIL=5%)
2.1 气泡长度变化
通过对高速摄像仪拍摄的图像进行处理,可以得到气泡头部和气泡尾部的坐标,分别为xF和xR,如图4所示。分别由LB=xF-xR和x=(xF+xR)/2计算得到气泡长度LB和气泡位置x,进而得到流动过程中单个气泡长度的变化曲线,如图5所示。
在微通道入口处,气相在液相剪切力的作用下产生稳定的弹状气泡。在气泡脱离气相主体后,气液两相间存在的传质推动力使得CO2被迅速吸收,气泡长度显著减小。随着气泡在微通道内流动,吸收过程持续进行,液相中CO2浓度逐渐增大,传质推动力减小,吸收速率降低,气泡长度趋于常数。固定液相流速不变,随着气速的增大,气泡长度明显增大,在流动初始阶段气泡减小的速率降低,传质过程经历的时间更长。图6表示了IL浓度对气泡长度变化的影响。在相同的气液流量下,随着混合溶液中IL浓度的增大,气泡生成阶段CO2的吸收量增大,得到的初始气泡长度随之减小。

图4 微通道内气液两相流动Fig. 4 Illustration of gas-liquid two-phase flow in microchannel

图5 气相流量对气泡长度变化的影响Fig. 5 Influence of gas flow rate on bubble length (wIL=5%,QL=20 ml·h-1)

图6 IL浓度对气泡长度变化的影响Fig. 6 Influence of IL mass fraction on bubble length (QG=100 ml·h-1,QL=20 ml·h-1)
2.2 传质系数计算及误差分析
在每个实验条件下,追踪单个气泡在整个过程中的变化情况。当微通道内气泡长度变化小于等于1个像素点(0.01 mm)时,认为此时吸收过程结束,气液两相达到传质平衡,并计算从气液两相开始接触到吸收达到平衡这一过程的平均传质系数。每个实验条件下,对采集的多组图片进行分析,并取平均值。
对于弹状气泡,气泡长度LB大于通道宽度w,可将气泡视为由头部、尾部和主体3部分组成。实验条件下,气泡整体呈子弹状,其头部和尾部呈不对称的椭球形。本文在处理气泡形状时,分别将气泡头部和尾部作为半球形。由于实际气泡的头部和尾部均呈椭球形,且头部要略小于尾部,分别取5个气泡按实际椭球形计算头部和尾部的体积和表面积,气泡体积和表面积的计算误差均小于3.4%,因此可以将气泡头部和尾部视为两个对称的半球体进行简化计算。气泡主体与通道壁面接触的部分为直线,而在通道角落处为圆弧,气泡主体的截面如图7所示[27-28]。气泡主体部分截面面积约占通道截面面积的90%[29]。假设气泡主体截面在通道角落处呈90°圆弧,圆弧半径为r,则气泡体积和表面积由式(1)~式(3)计算得到。
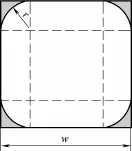
图7 气泡主体部分截面Fig. 7 Schematic diagram of cross section of main body

比表面积a由同一时刻传质段内所有气泡的表面积之和As与传质段通道体积VM之比计算得到

式中,ABi为微通道内第i个气泡的表面积;LM表示传质段的长度。
对于CO2在IL/无水乙醇混合溶液中的传质过程,传质阻力主要存在于液相侧。根据质量平衡方程,得到

式中,ce是CO2在IL/无水乙醇溶液中的平衡浓度;c表示CO2在液相中的浓度。因此
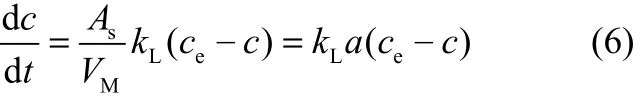
对式(6)进行积分,得到
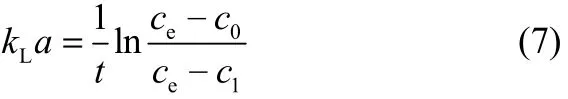
式中,t为从气液两相开始接触到两相达到吸收平衡所用的时间,可根据高速摄像仪记录的图像得到;c0为气液两相开始接触时溶液中CO2浓度,本文中c0=0;c1为传质过程结束时CO2在溶液中的浓度。在实验温度下,乙醇的饱和蒸气压为7.8 kPa[30],离子液体则几乎不挥发,蒸气压通常低于10-9kPa[31-32],考虑实验过程中气泡在微通道内的流动时间很短,仅为0.17~1.45 s,因此本文假定吸收过程中乙醇的挥发可以忽略不计,气相为纯CO2。因此,可根据气泡体积变化得到CO2吸收量,进而计算得到出口浓度c1
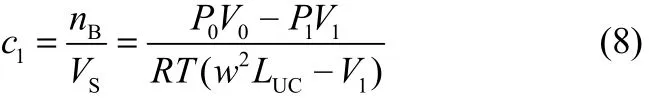
式中,P0为微通道进口处的压力;P1为传质过程结束时的压力;V0为气液间无传质时气泡的初始体积,由气相流量除以气泡生成频率计算得到;V1为传质过程结束时的气泡体积;VS为传质过程结束时与气泡相邻的液弹的体积;LUC为流动单元的长度,如图4所示。
CO2在IL/无水乙醇溶液中的平衡浓度ce可由亨利定律计算得到

式中,H为亨利常数。在CO2吸收过程中,通道内压力逐渐减小,因此式 (9) 中PCO2取平均压力进行计算。
根据CO2分别在IL、无水乙醇两种纯溶剂中的亨利常数[33-34],由Krichevsky[35]提出的公式,计算得到CO2在二元理想混合溶液中的亨利常数

式中,HIL、Hethanol分别表示CO2在IL和无水乙醇中的亨利常数;xIL表示混合溶液中IL的摩尔分数。
为了验证式(10) 的准确性,采用反应釜测定了实验采用的最大离子液体浓度(wIL=25%)混合溶液在298.15 K和低压下吸收CO2的亨利系数:① 将装有混合溶液的密闭反应釜抽真空,然后充入CO2气体至初始压力Pini=0.2 MPa,静置8 h后系统压力趋于恒定值Peq,因此认为吸收已达到平衡;② 利用反应釜容积V和压差计算得到CO2吸收量Δngas=(Pini-Peq)V/RT,溶液中CO2的浓度为xCO2=Δngas/(ngas+nliquid),并根据H=Peq/xCO2(Peq为平衡压力)求得亨利系数。在低压条件下,亨利系数受压力的影响可以忽略不计,仅为温度的函数。在实验温度下,测定值与式(10) 计算得到的亨利系数的相对误差为7.2%。由于离子液体浓度越低,混合溶液越接近于理想溶液,因此可通过Krichevsky提出的方法计算混合溶液的亨利系数。
根据误差传递公式以及传质系数的计算公式,得到液侧体积传质系数kLa和液测传质系数kL的误差计算公式

实验中采用的装置主要有高速摄像机、压力传感器和微量注射泵。实验过程中高速摄像机的拍摄频率为1000帧/秒。在图片处理过程中,传质过程所经历时间的误差为0.74%。实验中压力传感器给压降测量带来的误差是0.8%。实验所使用的微量注射泵的仪器误差为1%。相关参数的测量误差如表1所示。采用表1列出的各参数的实验测量误差,由式(11)、式(12)计算得到液侧体积传质系数kLa和液测传质系数kL的误差分别为7.34%、7.82%。

表1 相关参数的实验误差Table 1 Experimental errors in parameters
2.3 气液两相流量对传质系数的影响
在弹状流条件下,液侧体积传质系数kLa随气液两相流量比QG/QL的变化如图8所示。由图8可以看出,微通道内液侧体积传质系数随两相气液流量比的增大而增大,并逐渐趋于恒定,这与文献中的结果一致[25-26,36-37]。固定液相流量不变,当气液流量比较小时,两相流量比的升高使得比表面积显著增大,同时加速了气泡与液弹的内部循环,促进了液膜的更新,强化了微通道内两相间的传质,液侧体积传质系数kLa随之增大。当气液流量比增大到一定值时,微通道内气液两相流型开始向弹状-环状流发展,两相接触面积趋于恒定,kLa值逐渐趋于常数。当保持气液流量比不变,若液相流量增大时,气相流量也将随之增大,气相对液相的扰动程度增加。同时,根据表面更新理论,液相流量的增加也使得表面更新速率加快,导致kLa增大。实验中发现,当液相流量由40 ml·h-1增大到50 ml·h-1时,传质系数kLa仅有小幅度增大。此时,液相流量对kLa的影响已不显著。
气液两相流量比对液侧传质系数kL的影响如图9所示。随着气液两相流量的升高,传质系数kL逐渐增大并趋于恒定。这与体积传质系数kLa的变化趋势一致。固定液相流量不变,随着气相流量的不断增大,气液两相流型开始向弹状-环状流发展,传质系数kL随之达到最大并趋于恒定。固定两相流量比,当液相流量增大时,液膜表面更新速率加快。同时,气相流量随液相流量的增大而增大,使得微通道内气相对液相的扰动增强,促进了液弹内部循环以及液膜的更新,使得传质效率得到强化。

图8 气液两相流量比对kLa的影响Fig. 8 Influence of gas and liquid two phases flow rate ratio onkLa
2.4 混合溶液中IL浓度对传质系数的影响
图10示出了在固定液速条件下,IL浓度对体积传质系数kLa的影响。一方面,随着IL浓度的增大,混合溶液对于CO2的吸收能力增强,传质通量增大,体积传质系数kLa随之增大;另一方面,IL浓度的增大也使得气泡长度迅速减小,比表面积随之减小,同时气泡运动速率降低,使得气泡在通道内的停留时间更长,体积传质系数有所下降[26]。这两方面因素共同影响着kLa的变化趋势。因此,不同IL浓度溶液吸收CO2过程的体积传质系数随气液流量比的增大出现了交叉。交叉点之前的气液流量比较低,生成气泡的初始长度较小,使得比表面积的下降成为主导因素。此时,体积传质系数kLa随着IL浓度的增大而降低。在交叉点之后,气液流量比相对较大,流型开始向过渡流发展,比表面积趋于常数,IL浓度对比表面积的影响不再显著,混合溶液对于CO2的吸收强化成为主导因素,此时,高浓度混合溶液吸收过程的体积传质系数kLa更高。值得注意的是,在实验范围内的不同液速条件下,交叉点处对应的气液流量比约为QG/QL=8。如图11所示,微通道内IL/无水乙醇混合溶液吸收CO2过程的传质系数kL随IL浓度的变化趋势与kLa大体相同。在固定液速条件下,不同IL浓度吸收CO2过程的传质系数kL随气液流量比的变化也出现了交叉点。在交叉点之前,高浓度IL吸收过程的传质系数更低;在交叉点之后,高浓度IL吸收过程的传质系数更高。
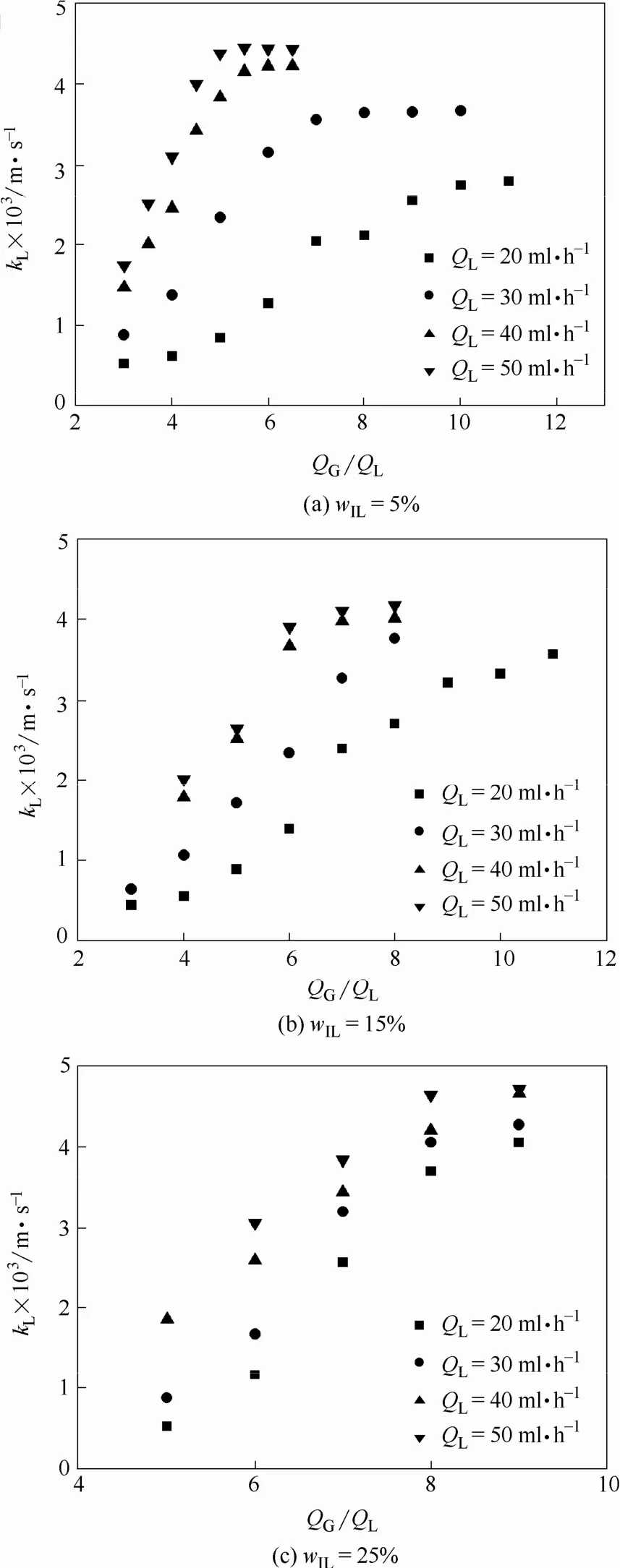
图9 气液两相流量比对kL的影响Fig. 9 Influence of gas and liquid two phases flow rate ratio onkL
本文中得到的体积传质系数kLa的范围是0.81~32.18 s-1,而在微通道内采用纯乙醇作为溶剂的吸收过程中,液侧体积传质系数的范围是0.4~5 s-1[38]。这也说明了离子液体的加入对于吸收效果有显著的提升。本文中得到的传质系数kL的范围是(0.25×10-3~4.67×10-3) m·s-1,与Yue等[24]采用化学吸收法得到的kL具有相同的数量级。
2.5 体积传质系数的预测
目前,已有许多学者对微通道内气液两相传质过程进行了研究,并基于实验数据提出了多种传质系数的预测式。van Baten等[39]在Higbie渗透理论的基础上,将气泡分为主体部分、头部和尾部,并认为微通道内体积传质系数由这3部分组成。Vandu等[40]考察了微反应器内CO2-水物系的物理吸收过程,认为气泡主体部分对传质起主要作用,并基于流动单元长度不变的假设,得到简化后的传质系数预测式。值得注意的是,本文实验中气泡长度随着吸收过程的进行明显减小,而液弹长度可认为保持不变,因此流动单元长度不变的假设在这里不能成立。
Yue等[24]根据能量耗散模型,对微通道内物理吸收过程中液侧体积传质系数kLa进行了预测,发现采用式(16)能够得到更为准确的预测模型

为了提高传质系数预测模型的普适性,Yue等[24]还将量纲1常数Sherwood数Sh、Schmidt数Sc、Reynolds数Re与传质系数进行关联,得到了弹状流条件下的关联式
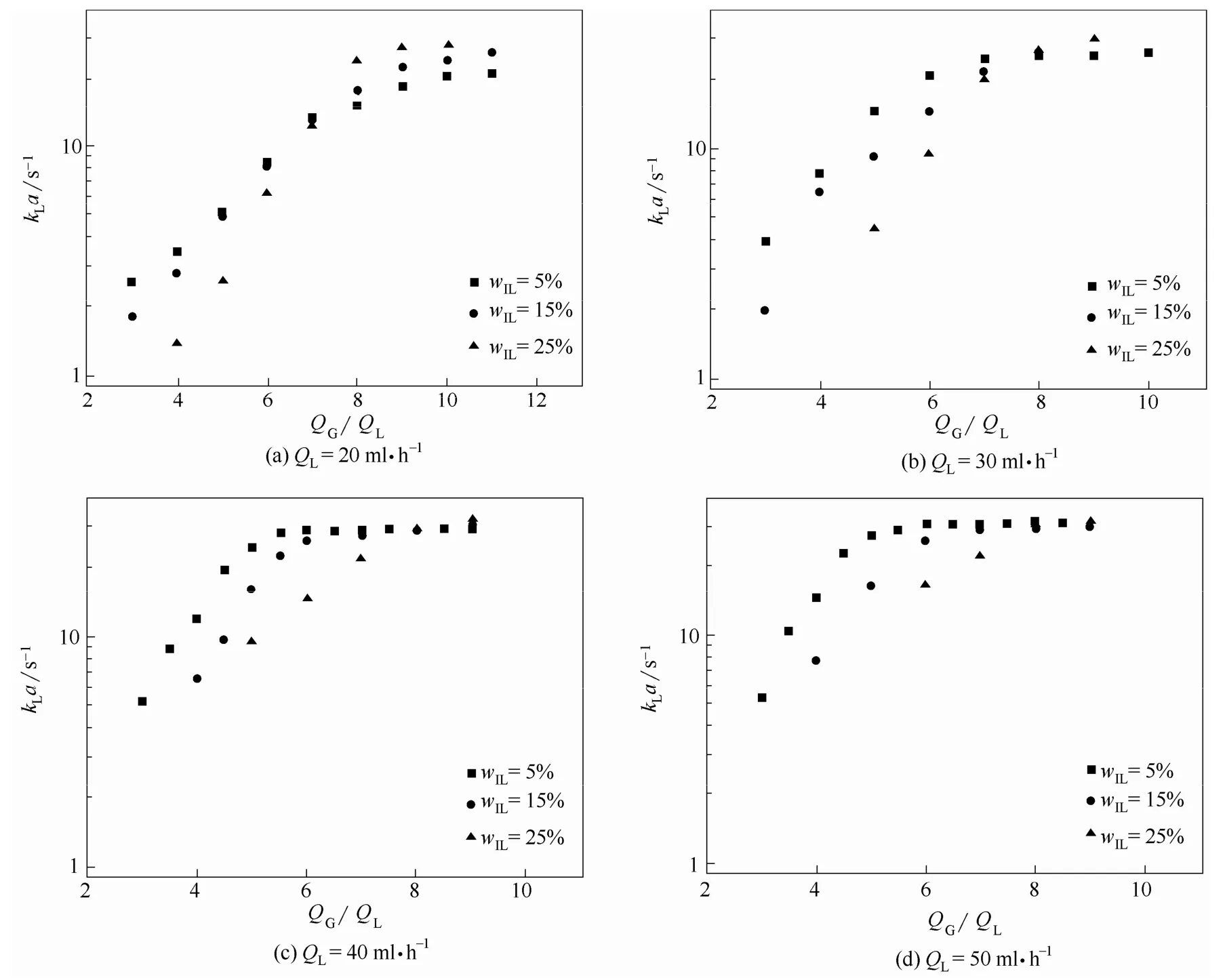
图10 IL浓度对kLa的影响Fig. 10 Influence of IL concentration onkLa

图11 IL浓度对kL的影响Fig. 11 Influence of IL concentration onkL
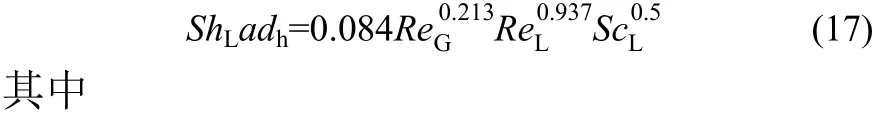

Li等[36]同样采用量纲1关联式预测MEA溶液吸收CO2过程的传质性能,基于实验结果提出了液侧体积传质系数的量纲1关联式
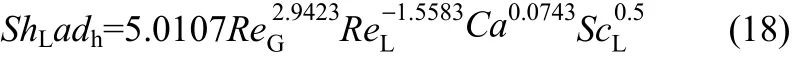
根据不同预测模型计算得到的体积传质系数预测值与实验值的对比如图12所示。从图中可以看出,预测值与实验值偏差较大。考虑到混合溶液中操作条件和IL浓度对液测体积传质系数的影响,本文利用IL摩尔比XIL、液相Reynolds数ReL、气液两相流量比QG/QL、液相毛细数CaL、液相Sherwood数ShL对液侧体积传质系数kLa进行预测。根据kLa变化曲线中交叉点处对应的特征气液流量比QG/QL,采用Matlab对实验数据进行分段拟合,得到如下关联式。


图12 液侧体积传质系数预测值与实验值的比较Fig. 12 Comparison between predicted values and experimental data of volumetric mass transfer coefficient
式(19) 和式(20) 得到的体积传质系数预测值与实验值相比,平均偏差分别为14.91%、10.52%,预测效果良好。
3 结 论
采用可视化在线分析法对400 μm×400 μm正方形截面微通道内IL/乙醇混合溶液吸收CO2的传质过程进行了研究。通过对高速摄像仪拍摄的图像进行处理,得到了气泡长度在流动过程中的变化规律。固定液相流量不变,随着气相流量的升高,初始气泡长度增大,传质过程经历的时间变长。当气液两相流量固定不变时,初始气泡长度随着IL浓度的增大而减小。基于传质过程中气泡的体积变化以及微通道进出口压力,计算得到了传质段的液侧体积传质系数kLa和液侧传质系数kL,并考察了气液两相流量以及IL浓度对传质系数的影响。结果表明,对于相同的IL溶液和液相流量,液侧体积传质系数kLa和液侧传质系数kL均随气液两相流量比的增大而增大,并逐渐趋于恒定。当固定液相流量不变时,对于不同浓度的IL溶液,传质系数随两相流量比的变化曲线出现了交叉。在交叉点之前,比表面积的下降是主导因素,低浓度IL溶液吸收CO2过程的传质系数更高;在交叉点之后,IL溶液对于CO2的吸收强化成为主导因素,高浓度IL溶液吸收CO2过程的传质性能更好。根据实验结果,考虑操作条件和IL浓度对传质的影响,提出了新的液侧体积传质系数预测式,预测效果良好。
符 号 说 明
A——气泡表面积,m2
As——气液相界面积,m2
a——比表面积,m2·m-3
Ca——毛细数
c——浓度,mol·m-3
ce——CO2在液相中的平衡浓度,mol·m-3
DAB——扩散系数,m2·s-1
d——微通道深度,m
dh——微通道当量直径,m
H——亨利系数,mol·m-3·Pa-1
L——长度,m
ka——体积传质系数,s-1
n——物质的量,mol
Δngas——溶液吸收的CO2的物质的量,mol
nliquid——溶液的物质的量,mol
P——压力,Pa
ΔP——微通道内压力降,Pa
Peq——反应釜内的平衡压力,Pa
Pini——反应釜内的初始压力,Pa
Q——流量,m3·s-1
r——气泡主体截面的圆弧半径,m
T——温度,K
t——传质过程经历的时间,s
u——表观流速,m·s-1
V——体积,m3
w——微通道宽度,m
wIL——混合溶液中离子液体的质量分数,%
XIL——混合溶液中离子液体的摩尔比
x——微通道内气泡的坐标,m
xCO2——溶液中CO2的摩尔分数
μ——黏度,Pa·s-1
ρ——密度,kg·m-3
σ——表面张力,N·m-1
下角标
B——气泡
C——微通道
exp——实验值
F——气泡头部
G——气相
L——液相
M——传质段
pre——预测值
R——气泡尾部
S——液弹
UC——流动单元
[1] METZ B, DAVIDSON O, DE CONINCK H, et al.Carbon Dioxide Capture and Storage[M]. New York: Cambridge University Press, 2005
[2] AARON D, TSOURIS C. Separation of CO2from flue gas: a review[J]. Separation Science and Technology, 2005, 40(1/2/3): 321-348.
[3] BLANCHARD L A, HANCU D, BECKMAN E J, et al.Green processing using ionic liquids and CO2[J]. Nature, 1999, 399(6731): 28-29.
[4] HASIB-UR-RAHMAN M, SIAJ M, LARACHI F. Ionic liquids for CO2capture-development and progress[J]. Chemical Engineering and Processing: Process Intensification, 2010, 49(4): 313-322.
[5] ZHAO Z J, DONG H F, ZHANG X P. The research progress of CO2capture with ionic liquids[J]. Chinese Journal of Chemical Engineering, 2012, 20(1): 120-129.
[6] AFZAL W, LIU X Y, PRAUSNITZ J M. Solubilities of some gases in four immidazolium-based ionic liquids[J]. The Journal of Chemical Thermodynamics, 2013, 63: 88-94.
[7] JACQUEMIN J, GOMES M F C, HUSSON P, et al.Solubility of carbon dioxide, ethane, methane, oxygen, nitrogen, hydrogen, argon, and carbon monoxide in 1-butyl-3-methylimidazolium tetrafluoroborate between temperatures 283K and 343K and at pressures close to atmospheric[J]. The Journal of Chemical Thermodynamics, 2006, 38(4): 490-502.
[8] JACQUEMIN J, HUSSON P, MAJER V, et al.Low-pressure solubilities and thermodynamics of solvation of eight gases in 1-butyl-3-methylimidazolium hexafluorophosphate[J]. Fluid Phase Equilibria, 2006, 240(1): 87-95.
[9] RAMDIN M, AMPLIANITIS A, DE LOOS T W, et al.Solubility of CO2/CH4gas mixtures in ionic liquids[J]. Fluid Phase Equilibria, 2014, 375: 134-142.
[10] CAMPER D, BARA J E, GIN D L, et al.Room-temperature ionic liquid-amine solutions: tunable solvents for efficient and reversible capture of CO2[J]. Industrial & Engineering Chemistry Research, 2008, 47(21): 8496-8498.
[11] YANG J, YU X H, YAN J Y, et al.CO2capture using amine solution mixed with ionic liquid[J]. Industrial & Engineering Chemistry Research, 2014, 53(7): 2790-2799.
[12] GAO J B, CAO L D, DONG H F, et al.Ionic liquids tailored amine aqueous solution for pre-combustion CO2capture: role of imidazolium-based ionic liquids[J]. Applied Energy, 2015, 154: 771-780.
[13] LEI Z G, QI X X, ZHU J Q, et al.Solubility of CO2in acetone, 1-butyl-3-methylimidazolium tetrafluoroborate, and their mixtures[J]. Journal of Chemical & Engineering Data, 2012, 57(12): 3458-3466.
[14] BOGEL-ŁUKASIK R, MATKOWSKA D, BOGEL-ŁUKASIK E, et al.Isothermal vapour-liquid equilibria in the binary and ternary systems consisting of an ionic liquid, 1-propanol and CO2[J]. Fluid Phase Equilibria, 2010, 293(2): 168-174.
[15] 王渊涛, 方诚刚, 张锋, 等. 氨基酸离子液体-MDEA混合水溶液的CO2吸收性能[J]. 化工学报, 2009, 60(11): 2781-2786. WANG Y T, FANG C G, ZHANG F,et al.Performance of CO2absorption in mixed aqueous solution of MDEA and amino acid ionic liquids[J]. CIESC Journal, 2009, 60(11): 2781-2786.
[16] LAM K F, SORENSEN E, GAVRIILIDIS A. Review on gas-liquid separations in microchannel devices[J]. Chemical Engineering Research and Design, 2013, 91(10): 1941-1953.
[17] JAHNISCH K, HESSEL V, LOWE H, et al.Chemistry in microstructured reactors[J]. Angewandte Chemie International Edition, 2004, 43(4): 406-446.
[18] CHUNBO Y, GUANGWEN C, QUAN Y. Process characteristics of CO2absorption by aqueous monoethanolamine in a microchannel reactor[J]. Chinese Journal of Chemical Engineering, 2012, 20(1): 111-119.
[19] 张沁丹, 付涛涛, 朱春英, 等. 十字聚焦型微通道内弹状液滴在黏弹性流体中的生成与尺寸预测[J]. 化工学报, 2015, 67(2): 504-511. ZHANG Q D, FU T T, ZHU C Y,et al.Formation and size prediction of slug droplet in viscoelastic fluid in flow-focusing microchannel[J]. CIESC Journal, 2015, 67(2):504-511.
[20] 骆广生, 王凯, 徐建鸿, 等. 微化工系统内多相流动及其传递反应性能研究进展[J]. 化工学报, 2010,61(7):1621-1626. LUO G S, WANG K, XU J H,et al .Multiphase flow, transport and reaction in micro-structured chemical systems[J]. CIESC Journal, 2010, 61(7): 1621-1626.
[21] GANAPATHY H, SHOOSHTARI A, DESSIATOUN S,et al. Hydrodynamics and mass transfer performance of a microreactor for enhanced gas separation processes[J]. Chemical Engineering Journal, 2015, 266: 258-270.
[22] CUBAUD T, SAUZADE M, SUN R. CO2dissolution in water using long serpentine microchannels[J]. Biomicrofluidics, 2012, 6(2): 022002.
[23] LOKHAT D, DOMAH A K, PADAYACHEE K,et al. Gas-liquid mass transfer in a falling film microreactor: effect of reactor orientation on liquid-side mass transfer coefficient[J]. Chemical Engineering Science, 2016, 155: 38-44.
[24] YUE J, CHEN G W, YUAN Q, et al.Hydrodynamics and mass transfer characteristics in gas-liquid flow through a rectangular microchannel[J]. Chemical Engineering Science, 2007, 62(7): 2096-2108.
[25] YAO C Q, DONG Z Y, ZHAO Y C, et al.An online method to measure mass transfer of slug flow in a microchannel[J]. Chemical Engineering Science, 2014, 112: 15-24.
[26] ZHU C Y, LI C F, GAO X Q, et al.Taylor flow and mass transfer of CO2chemical absorption into MEA aqueous solutions in a T-junction microchannel[J]. International Journal of Heat and Mass Transfer, 2014, 73: 492-499.
[27] YAO C Q, ZHAO Y C, YE C B, et al.Characteristics of slug flow with inertial effects in a rectangular microchannel[J]. Chemical Engineering Science, 2013, 95: 246-256.
[28] YUE J, LUO L S, GONTHIER Y, et al.An experimental study of air-water Taylor flow and mass transfer inside square microchannels[J]. Chemical Engineering Science, 2009, 64(16): 3697-3708.
[29] WU Y N, FU T T, ZHU C Y, et al.Asymmetrical breakup of bubbles at a microfluidic T-junction divergence: feedback effect of bubble collision[J]. Microfluidics and Nanofluidics, 2012, 13(5): 723-733.
[30] SMITH V C, ROBINSON R L. Vapor-liquid equilibriums at 25℃ in the binary mixtures formed by hexane, benzene, and ethanol[J]. Journal of Chemical & Engineering Data, 1970, 15(3): 391-395.
[31] REBELO L P, CANONGIA LOPES J N, ESPERANÇA J M,et al.On the critical temperature, normal boiling point, and vapor pressure of ionic liquids[J]. The Journal of Physical Chemistry B, 2005, 109(13): 6040-6043.
[32] ASCHENBRENNER O, SUPASITMONGKOL S, TAYLOR M,et al, Measurement of vapour pressures of ionic liquids and other low vapour pressure solvents[J]. Green Chemistry, 2009, 11(8): 1217-1221.
[33] HUANG J H, R THOMAS. Why are ionic liquids attractive for CO2absorption? - An overview[J]. Australian Journal of Chemistry, 2009, 62(4): 298-308.
[34] DALMOLIN I, SKOVROINSKI E, BIASI A, et al.Solubility of carbon dioxide in binary and ternary mixtures with ethanol and water[J]. Fluid Phase Equilibria, 2006, 245(2): 193-200.
[35] KRICHEVSKY I. Thermodynamics of an infinitely dilute solution in mixed solvents(Ⅰ): The Henry's coefficient in a mixed solvent behaving as an ideal solvent[J]. Zhournal Fizicheskoi Khimii, 1937, 9: 41-47.
[36] LI C F, ZHU C Y, MA Y G, et al.Experimental study on volumetric mass transfer coefficient of CO2absorption into MEA aqueous solution in a rectangular microchannel reactor[J]. International Journal of Heat and Mass Transfer, 2014, 78: 1055-1059.
[37] ROUDET M, LOUBIERE K, GOURDON C, et al.Hydrodynamic and mass transfer in inertial gas-liquid flow regimes through straight and meandering millimetric square channels[J]. Chemical Engineering Science, 2011, 66(13): 2974-2990.
[38] 季喜燕. 微通道内气液两相流动及传质过程研究[D]. 天津: 天津大学, 2011. JI X Y. Study on gas-liquid two-phase flow and mass transfer in microchannels[D]. Tianjin: Tianjin University, 2011.
[39] VAN BATEN J M, KRISHNA R. CFD simulations of mass transfer from Taylor bubbles rising in circular capillaries[J]. Chemical Engineering Science, 2004, 59(12): 2535-2545.
[40] VANDU C O, LIU H, KRISHNA R. Mass transfer from Taylor bubbles rising in single capillaries[J]. Chemical Engineering Science, 2005, 60(22): 6430-6437.
Mass transfer performance of CO2absorption into ionic liquid/ethanol mixture in microchannel
ZHANG Fanbin, ZHU Chunying, FU Taotao, JIANG Shan, DU Wei, ZHANG Qindan, MA Youguang
(State Key Laboratory of Chemical Engineering,Collaborative Innovation Center of Chemical Science and Engineering(Tianjin),School of Chemical Engineering and Technology,Tianjin University,Tianjin300072,China)
The mass transfer behavior of CO2absorption into ionic liquid/ethanol mixture in microchannel was investigated experimentally using a high speed camera. The influences of the ratio of gas to liquid phase flow rates, the concentration of ionic liquid on the liquid side volumetric mass transfer coefficient (kLa) and liquid side mass transfer coefficient (kL) for slug flow were studied. For a given concentration of ionic liquid, bothkLaandkLincrease gradually with increasing the ratio of gas to liquid phase flow rates and then level off. For different concentrations of ionic liquid at a given liquid phase flow rate, there is a transition point in the curve ofkLa(kL) as a function of the flow rate ratio of gas to liquid phase. Before this point,kLa(kL) decreases with increasing the concentration of ionic liquid, while reverse tendency is found after the point. A new dimensionless empirical correlation for predictingkLawas proposed, and the predicted values coincide well with the experimental data.
microchannel; ionic liquid; absorption; carbon dioxide; mass transfer
Prof. MA Youguang, ygma@tju.edu.cn
10.11949/j.issn.0438-1157.20161224
TQ 021.4
:A
:0438—1157(2017)02—0601—11
2016-09-02收到初稿,2016-11-11收到修改稿。
联系人:马友光。
:张璠玢(1992—),女,硕士研究生。
国家自然科学基金项目(21576186,21276175,91434204,21106093)。
Received date: 2016-09-02.
Foundation item: supported by the National Natural Science Foundation of China (21576186, 21276175, 91434204, 21106093).
