N-对甲苯磺酰-5-氨基间苯二甲酸构筑的一维配位聚合物的合成、晶体结构和荧光性质
2017-02-16黄妙龄吴文士陈婉贞
黄妙龄吴文士陈婉贞
N-对甲苯磺酰-5-氨基间苯二甲酸构筑的一维配位聚合物的合成、晶体结构和荧光性质
黄妙龄1,2吴文士*,1陈婉贞2
(1华侨大学材料科学与工程学院,厦门361000)
(2泉州师范学院化工与材料学院,泉州362000)
采用普通溶液法和水热法分别合成了2个金属-有机配位聚合物:{[Cu(Ts-5-AIPA)(phen)(H2O)]·H2O}n(1)和[Cd(Ts-5-AIPA) (phen)]n(2)(Ts-5-AIPA=N-对甲苯磺酰-5-氨基间苯二甲酸根,phen=菲咯啉),并用红外光谱、热重和X射线单晶衍射对配合物的结构进行了表征。结果表明:2个配合物均为单斜晶系,配合物1为P21/c空间群,配合物2为C2/c空间群;2个配合物均为一维链状结构,再通过氢键和π-π堆积作用形成三维超分子结构。另外,还研究了2个配位聚合物的荧光性质。
配位聚合物;N-对甲苯磺酰-5-氨基间苯二甲酸;晶体结构;荧光
0 引言
配位聚合物是有机配体和金属离子之间通过配位键形成的具有高度规整的无限网络结构的配合物[1],它结合了复合高分子和配位化合物两者的特点,不仅具有多样化的结构和新颖的拓扑,更表现出其独特的性质,在非线性光学材料、磁性材料、生物活性、催化、分子储存及发光材料等诸多方面都有广阔的应用前景,使其在过去的几十年里一直被广泛的研究[2-14]。
研究配位聚合物的发光性能是因为其比纯有机配体有更高的稳定性。荧光配位聚合物的典型特征是其具有有机发色团的配位体。芳香羧酸具有丰富的发色基团,是一类多功能的配位剂,能够与金属离子形成多种多样的结构,其芳环和羧基可以形成π-π堆积和氢键作用,在自组装过程中,可通过这些分子间弱的作用力将低维簇拓展为高维网络结构。另外,菲咯啉和2,2′-联吡啶是一类常见的有机配体,很容易和金属离子配位形成螯合物,也容易形成π-π堆积作用,在构筑金属-有机配位化合物中起到重要的作用。基于以上分析,本文设计合成了N-对甲苯磺酰-5-氨基间苯二甲酸,并以此为主配体,菲咯啉作为辅助配体,分别与铜、镉的硝酸盐反应,得到2个一维链状结构的配位聚合物。通过X射线单晶衍射、元素分析、红外光谱、热重分析等对配合物进行结构测定和性质表征,并研究了它们的荧光性质。
1 实验部分
1.1 试剂与仪器
N-对甲苯磺酰-5-氨基间苯二甲酸为自制药品,其它所有试剂均为分析纯,使用时未进行纯化。德国Vario EL元素分析仪,德国布鲁克AVANCEⅢ 500M核磁共振波谱仪,美国Nicolet iS10型FT-IR红外光谱仪(KBr压片),光谱范围4000~400cm-1;德国NETZSCH STA 409PC型综合热分析仪(在He气氛中,升温速率10℃·min-1);德国Bruker SMART APEXⅡCCD单晶衍射仪;日立F-7000荧光分光光度仪。
1.2 配体N-对甲苯磺酰5-氨基间苯二甲酸(Ts-5-H2AIPA)的合成
对甲苯磺酰氯与5-氨基间苯二甲酸按1∶1的物质的量之比混合,置于500mL的烧杯中,加入适量的蒸馏水,用NaOH调节至pH=10,在冰水浴中反应1d,过滤。滤液用浓HCl调至pH=2,产生白色沉淀,抽滤,得乳白色固体,甲醇重结晶,放入烘箱干燥后,研磨至粉末备用[15]。熔点:306℃。元素分析按C15H13NO6S计算值(%):C 53.73,H 3.91,N 4.18;实验值(%):C 53.78,H 3.87,N 4.23。IR主要吸收峰(KBr压片,cm-1):3265s、2607m、1700vs、1603s、1504m、1425s、1342s、1280s、1157vs、1117w、1089m、1020m、991w、866m、806m、757m、671m、592w、568m、535m、447w。1H NMR(DMSO-d6,500MHz):δ 10.72(s,1H,COOH),8.10~7.91(m,2H,Ph),7.65~7.37(m,2H,Ph),3.38(1H,s,NH),2.51~2.32(m,2H,CH3)。反应式如Scheme 1所示。
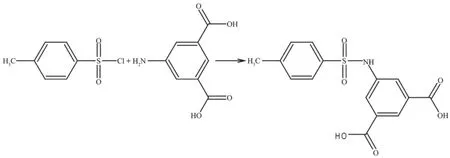
Scheme 1
1.3 配合物1和2的合成
1.3.1 配合物{[Cu(Ts-5-AIPA)(phen)(H2O)]·H2O}n(1)
准确称取0.5mmol的N-对甲苯磺酰-5-氨基间苯二甲酸,加热使之溶于7mL DMF(N,N-二甲基甲酰胺)。称取1.0mmol菲咯啉溶于5mL无水乙醇,1.0mmol硝酸铜溶于6mL水。在磁力搅拌器下,边搅拌边用滴管将硝酸铜溶液逐滴溶于对甲苯磺酰-5-氨基间苯二甲酸溶液。70℃左右回流12h,最后冷却至室温,过滤。滤液放置自然挥发,一周析出蓝色晶体。产率:52%。元素分析按C27H23N3O8SCu计算值(%):C 52.89,H 3.78,N 6.85;实验值(%):C 52.85,H3.73,N6.93。IR主要吸收峰(KBr压片,cm-1):3547s、3073m、1615w、1565vs、1520w、1427m、1342s、1236w、1158vs、1087m、1009m、991w、874w、853m、781s、723s、663m、540m、445w。
1.3.2 配合物[Cd(Ts-5-AIPA)(phen)]n(2)
分别准确称取1.0mmol的N-对甲苯磺酰-5-氨基间苯二甲酸,1.0mmol菲咯啉,1.0mmol硝酸镉,置于25mL的反应釜中,加9mL DMF和5mL水,于烘箱中120℃下反应3d,冷却,无色透明晶体析出。产率:58%。元素分析按C27H19N3O6SCd计算值(%):C 51.81,H 3.06,N 6.71;实验值(%):C 51.83,H 3.10,N6.65。IR主要吸收峰(KBr压片,cm-1):3470m、3296m、3059m、1616s、1581vs、1548vs、1516s、1494m、1404vs、1370vs、1307s、1263w、1235w、1189w、1164vs、1090s、1008s、987m、865s、847s、782s、725vs、661s、567s、544s、420m。
1.4 配合物1和2晶体的X射线衍射
选取配合物1(0.12mm×0.16mm×0.20mm)和2(0.20mm×0.22mm×0.32mm)大小单晶体,置于Bruker SMART APEXⅡCCD衍射仪上,用石墨单色化的Mo靶Kα射线(λ=0.071073nm)以φ-ω扫描方式分别收集衍射数据。数据通过经验吸收校正,晶体结构用SHELXS-97程序[16]通过直接法解析,用SHELXL-97程序[17]基于F2对全部非氢原子坐标及其各向异性热参数进行全矩阵最小二乘法精修。配合物1和2的晶体学数据和结构精修参数列于列于表1,主要键长和键角列于表2。

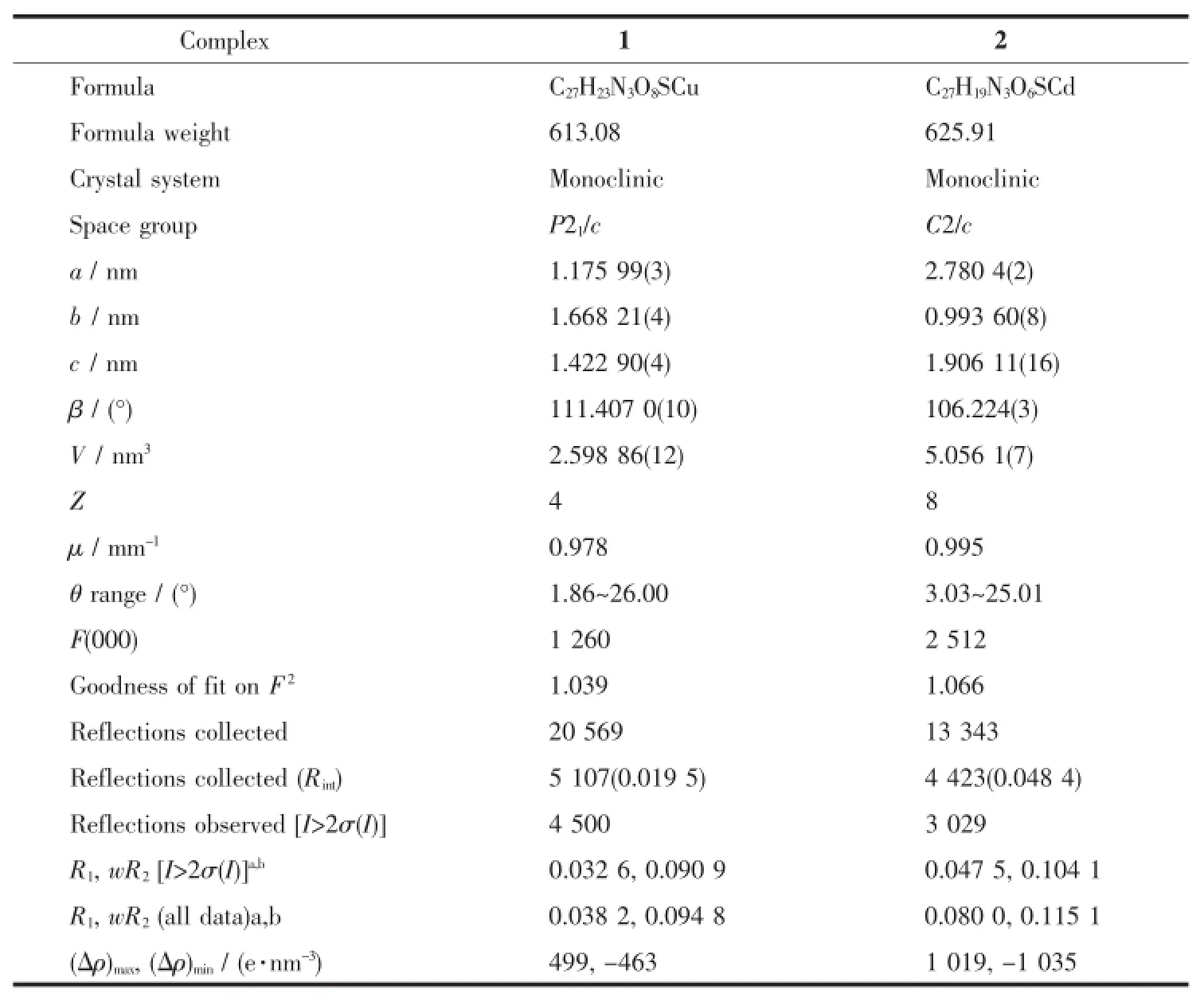
表1 配合物1和2的晶体学数据和结构精修参数Table 1Crystal data and structure parameters of complexes 1and 2

表2 配合物1和2的键长(nm)和键角(°)Table 2Selected bond lengths(nm)and bond angles(°)for complexes 1and 2

续表2
2 结果与讨论
2.1 配合物的晶体结构
2.1.1 配合物{[Cu(Ts-5-AIPA)(phen)(H2O)]·H2O}n(1)的晶体结构

图1 配合物1的结构图:(a)部分分子结构图;(b)一维链结构图;(c)氢键及π-π堆积图;(d)三维超分子结构图Fig.1Structure of complex 1:(a)Part of the molecular structure;(b)1D chain structure;(c)View of hydrogen bonds and π-π stacking;(d)View of 3D supramolecular structure
相邻链间,菲咯啉的吡啶环与配体Ts-5-AIPA2-离子的苯环部分重叠,存在π-π堆积(图1c)[18]:π平面(C7,C8,C9,C10,N2,C11,Symmetry codes:1-x,2-y,1-z;质心Cg1(0.47782,1.05798,0.29566))与相邻π平面(C21,C22,C23,C24,C25,C26,Symmetry codes:x,y,-1+z;质心Cg2(0.19620,0.96670,0.10270))的二面角为14.663°,质心间距离为0.37667(1)nm,此π-π堆积作用使相邻两条链结合更牢固。另外,分子中存在着丰富的氢键O1W-H1WA…O3(2.669(3) nm,157.00°),O1W-H1WB…O6(2.866(3)nm,136.00°),N3-H3…O2(2.820(3)nm,154.00°)。配体芳环之间的π-π堆积和氢键作用将配合物拓展为三维网状超分子结构(图1d)。
2.1.2 配合物[Cd(Ts-5-AIPA)(phen)]n(2)的晶体结构
晶体结构解析表明,配合物2也是一个一维链状结构分子,但分子结构与配合物1不同(图2a)。其基本单元由1个Cd离子、1个对甲苯磺酰-5-氨基间苯二甲酸根离子和1个菲咯啉分子组成。每个Cd离子都和2个双齿桥联的羧基氧(O1、O2)、1个双齿螯合的羧基氧(O3、O4)及菲咯啉的2个氮原子(N1、N2)配位,形成一个变形的八面体几何配位结构。其中O1、O3、O4和N2处于八面体赤道上,∠O1-Cd1-O3=84.58(17)°,∠O3-Cd1-O4=53.51(15)°,∠O4-Cd1-N2=91.44(15)°,∠N2-Cd1-O1=126.61(18)°,4个角总和为356.14°,接近360°,扭转角为∠O3-O1-N2-O4=7.16°;另外,N1、O2在八面体的两极,∠N1-Cd1-O2=158.96(17)°。每个配体Ts-5-AIPA2-的配位方式均相同,其中一个羧基为双齿螯合,另一个羧基双齿桥联。双齿桥联的羧基氧把相邻的2个Cd离子联接起来,Cd-Cd距离为0.39603(6)nm,且2个Cd离子的配位方式呈现中心对称;另外一个螯合的羧基氧则与另外一个Cd离子配位。相邻的5-氨基间苯甲酸上的苯环几乎共面,与另外2个相邻的苯环面夹角为57.676(79)°,整个分子形成宽的锯齿型链状结构,菲咯啉像花朵一样在分子链的上下两侧(图2b)。
相邻2条分子链上菲咯啉的吡啶环部分重叠:π平面(C22,C23,C24,C25,N1,C26,Symmetry codes:-1+x,y,z;质心Cg3(-0.47805,0.01350,0.09967))与相邻π平面(C22,C23,C24,C25,N1,C26,Symmetry codes:-x,-y,-z;质心(-0.52195,-0.01350,-0.09968))的二面角为0.855°,质心间距离为0.36615(3)nm,说明分子间产生π-π堆积效应(图2c)[18]。相邻配体Ts-5-AIPA2-上的对甲苯磺酰基上的苯环相互平行,且大部分重叠,也存在π-π堆积(图2d):π平面(C1,C2,C3,C4,C5,C6,Symmetry codes:1-x,1-y,-z;质心Cg5(0.71362,0.77993,0.40257))与相邻π平面(C1,C2,C3,C4,C5,C6,Symmetry codes:0.5+x,0.5+ y,1+z;质心(0.78638,0.72007,0.58743))的二面角为0.000°,质心间距离为0.37476(3)nm,这些π-π堆积将相邻的分子链相连接,把配合物扩展为3D网络超分子结构(图3d)。
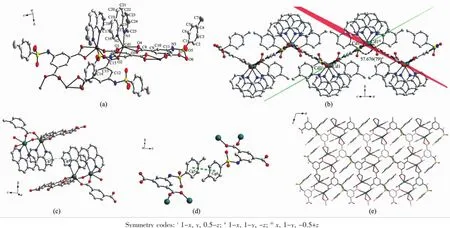
图2 配合物2的结构图:(a)部分分子结构图;(b)一维链结构图;(c),(d)π-π堆积图;(e)三维超分子结构图Fig.2Structure of complex 2:(a)Part of the molecular structure;(b)1D chain structure;(c),(d):π-π stacking; (e)View of 3D supramolecular structure
3.4 红外光谱分析
采用KBr压片法在4000~400cm-1范围内测定了配体和配合物的红外光谱,表3列出各物质的主要特征红外光谱数据。红外光谱分析表明:配体Ts-5-H2AIPA在1700和1425cm-1处有强吸收,归属于羧基的不对称伸缩振动和对称伸缩振动;形成配合物后,这两个吸收峰均有不同程度的红移,配合物1移至1565和1427cm-1,配合物2移至1581和1404cm-1,说明配体Ts-5-H2AIPA的羧酸基团均脱去质子且与金属进行了配位。配体菲咯啉在1597、853和738cm-1分别为C=N的伸缩振动峰,为C-H面外弯曲振动。形成配合物以后,配合物1分别移至1565(此峰与羧基的不对称伸缩振动吸收峰重合)、853和723cm-1;配合物2分别移至1548、847和725cm-1;其中菲咯啉的C=N伸缩振动峰位移较大,说明菲咯啉的2个氮原子均与中心离子进行了配位。
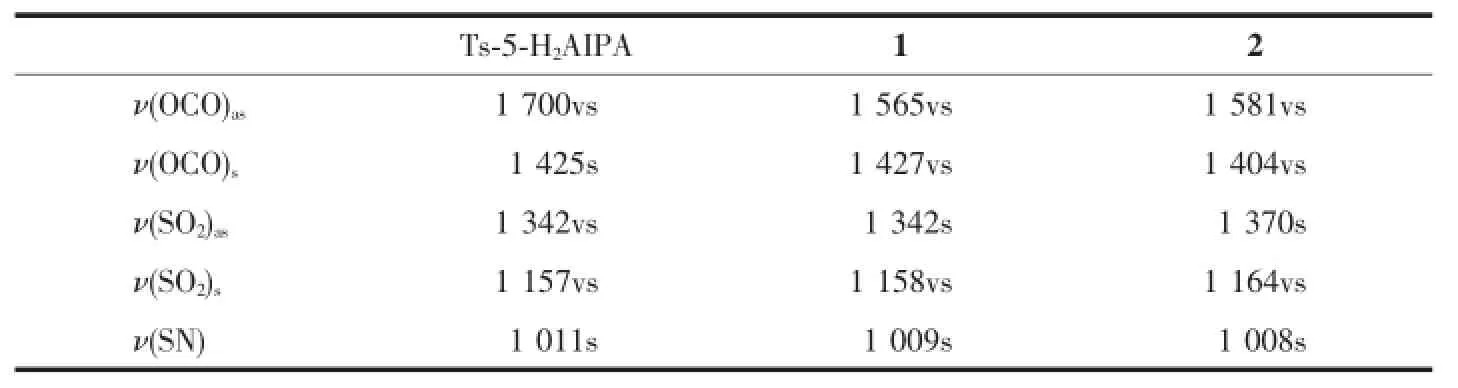
表3 配体及配合物的主要红外光谱吸收峰Table 3Selected infrared bands(cm-1)for complexes 1and 2and ligand
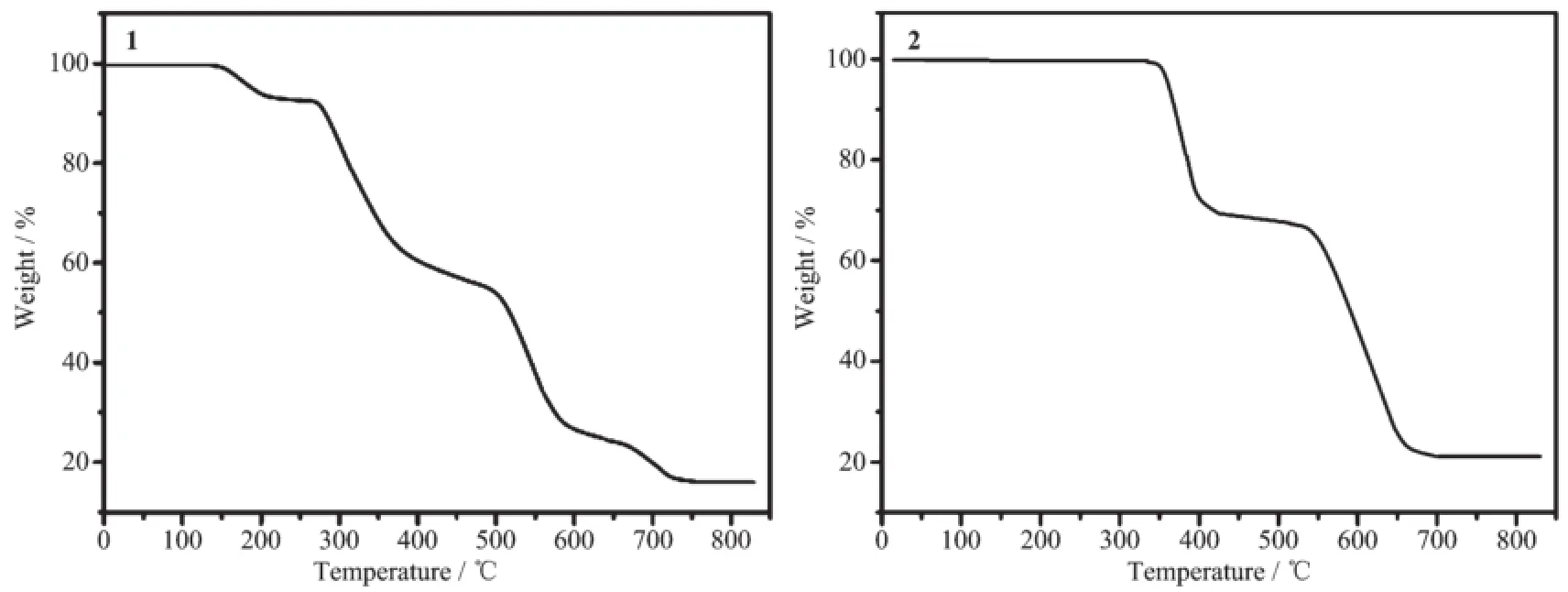
3.5 热重分析
分析配合物的TG曲线可知。2个配合物均是分步分解的。配合物1第一阶段失重出现在178~286℃,失重6.04%,约为1个结晶水分子和1个配位水分子(理论值5.87%);第二阶段286℃开始失重,到724℃趋于恒重,残重13.28%,估计剩余产物为CuO(理论值13.05%)。配合物2第一阶段从335℃开始迅速失重,到422℃稍微平稳,535℃后又开始迅速失重,700℃后趋于稳定,残重21.1%,估计残余物为氧化镉(理论值20.5%)。
3.6 荧光性质
以二甲亚砜为溶剂,配体和配合物浓度均为1× 10-6mol·L-1,在日立F-7000荧光分光光度仪上测定了室温下配体和配合物1和2在300~600nm的发射光谱(图4)。
由图可见,在369nm波长的光激发下,自由配体Ts-5-H2AIPA在429nm处出现较强的荧光发射峰。以364nm波长的光激发,配合物1在429nm处也出现了荧光发射峰,但强度比配体要弱得多,这可能是由于二价铜离子是3d9的电子构型,具有顺磁性,可能产生可逆性的电荷转移作用而导致发生荧光猝灭。而配合物2的最大激发峰出现在350nm,在423nm处出现了较强的荧光发射峰,且比自由配体Ts-5-H2AIPA的荧光有很明显的增强。这是因为二价镉离子(4d10)外层电子全充满,为抗磁性离子,与配体形成配合物后,使得原来配体的单线最低电子激发态S1为n,π*能层转变为π,π*能层,且形成一维配位聚合物后分子结构的共轭性和刚性均增强,减少了配体内部电荷转移带来的能量损失,使配合物的荧光比配体的强。2个配合物的发射峰形和发射波长均与配体相似,表明这2个配合物均由配体吸光和发光,属于L*→L发光[19]。
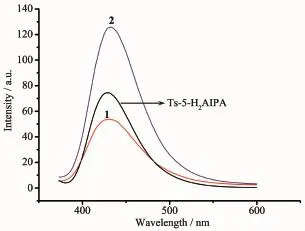
图4 配体和配合物1和2的发射光谱图Fig.4Fluorescence emission spectra of the ligand, complexes 1and 2
3 结论
通过磺酰化5-氨基间苯二甲酸、菲咯啉与2种金属硝酸盐合成了2个配位聚合物:{[Cu(Ts-5-AIPA)(phen)(H2O)]·H2O}n(1)和[Cd(Ts-5-AIPA)(phen)]n(2)。2个配合物均为一维链状结构,再通过氢键和π-π堆积作用形成三维超分子结构。因为配合物所含的金属离子不同,导致它们的荧光性质强弱与自由配体相比发生了变化,配合物1的荧光强度比自由配体弱,配合物2的荧光强度则比配体强很多。
[1]Batten S R,Robson R.Angew.Chem.Int.Ed.,1998,37:1460-1949
[2]Coe B J,Harries J L,Heliwell M,et al.J.Am.Chem.Soc., 2006,128:12192-12204
[3]Coe B J,Fielden J,Foxon S P,et al.Inorg.Chem.,2010,49: 10718-10726
[4]Coe B J,Harris J A,Brunschwig B S,et al.J.Am.Chem. Soc.,2005,127:13399-13410
[5]Shaikh M M,Veenu M,Dhirendra K R,et al.Dalton Trans., 2015,44:1933-1941
[6]Dinca A S,Catalin M,Cojocaru B,et al.Inorg.Chim.Acta, 2016,440:148-153
[7]Zhang X M,Hao Z M,Zhang W X,et al.Angew.Chem.Int. Ed.,2007,46(19):3456-3459
[8]Liang F P,Huang M L,Jiang C F,et al.J.Coord.Chem., 2007,60(21):2343-2350
[9]Yadav R,Trivedi M,Chauhan R,et al.Inorg.Chim.Acta, 2016,450:57-68
[10]Krap C P,Newby R,Dhakshinamoorthy A,et al.Inorg.Chem., 2016,55(3):1076-1088
[11]Hasegawa S,Horike S,Matsuda R,et al.J.Am.Chem.Soc., 2007,129(9):2607-2614
[12]Fang Q R,Zhu G S,Zhao J,et al.Angew.Chem.Int.Ed., 2007,46(35):6638-6642
[13]Cheng M,Ding Y S,Zhang Z C,et al.Inorg.Chim.Acta, 2016,450:1-7
[14]CHEN Man-Sheng(陈满生),DENG Yi-Fang(邓奕芳),CUI Ying(崔莺),et al.Chinese J.Inorg.Chem.(无机化学学报), 2015,31(5):2032-2042
[15]HUANG Miao-Ling(黄妙龄),WENG Wen-Ting(翁文婷), CHEN Qiang(陈强),Chinese J.Inorg.Chem.(无机化学学报),2014,30(9):1041-1048
[16]Sheldrick G M.SHELXS-97,Program for X-ray Crystal Structure Solution,University of Göttingen,1997.
[17]Sheldrick G M.SHELXL-97,Program for X-ray Crystal Structure Refinement,University of Göttingen,1997.
[18]Ikai M,Ishikawa F,Aratani N,et al.Adv.Funct.Mater., 2006,16:515-519
[19]XUJin-Gou(许金钩),WANGZun-Ben(王尊本).Fluorescence Analysis.3rd Ed(荧光分析法.3版).Beijing:Science Press, 2006:21-22
Syntheses,Crystal Structures and Fluorescent Properties of One-Dimensional Coordination Polymers with N-p-Tolylsulfonyl-5-aminoisophthalic Acid
HUANG Miao-Ling1,2WU Wen-Shi*,1CHEN Wan-Zhen2
(1College of Materials Science and Engineering,Huaqiao University,Xiamen,Fujian 361000,China)
(2College of Chemical Engineering and Materials,Quanzhou Normal University,Quanzhou,Fujian 362000,China)
Two metal-organic coordination polymers,{[Cu(Ts-5-AIPA)(phen)(H2O)]·H2O}n(1)and[Cd(Ts-5-AIPA) (phen)]n(2)(Ts-5-AIPA=N-p-tolylsulfonyl-5-aminoisophthalic acid radical,phen=phenanthroline),were synthesized using common solution method and hydrothermally method,respectively.Their crystal structures were determined by IR,TG and single-crystal X-ray diffraction.Two complexes crystalize in monoclinic system,space group P21/c for complex 1and C2/c for complex 2.They are one-dimensional chain structure,and further extended into a three-dimensional supramolecular structure through hydrogen bonds and π-π interactions.In addition,fluorescent properties of two complexes were investigated.CCDC:839135,1;1472441,2.
coordination polymer;N-p-tolylsulfonyl-5-aminoisophthalic acid;crystal structure;fluorescent
O614.121;O614.24+2
A
1001-4861(2017)01-0066-07
10.11862/CJIC.2017.005
2016-07-08。收修改稿日期:2016-11-02。
福建省教育厅基金(No.JA14261)和国家大学生创新创业训练(No.201610399007)资助项目。*
。E-mail:wws@hqu.edu.cn;会员登记号:S06N1116M1111。
