羟乙基淀粉40氯化钠注射液过敏实验研究
2017-02-16宗卫峰汪玉馨张微峰陆益红
宗卫峰,汪玉馨,刘 洋,王 瑶,张微峰,陆益红
(江苏省食品药品监督检验研究院,南京 210008)
羟乙基淀粉40氯化钠注射液过敏实验研究
宗卫峰,汪玉馨,刘 洋,王 瑶,张微峰,陆益红*
(江苏省食品药品监督检验研究院,南京 210008)
目的 评价羟乙基淀粉40氯化钠注射液过敏安全性。方法 进行了主动全身过敏反应试验、体内过敏指标测定与筛查及被动皮肤过敏反应试验的方法,考察样品的过敏安全性。结果 我们对3个企业45批羟乙基淀粉40氯化钠注射液进行了豚鼠全身过敏反应和被动皮肤过敏试验,均未发生过敏反应。通过对血浆中过敏性指标,组胺(HIS)、IgG、IgM和IgE进行测定和比较,发现IgM和IgE在各组间均无明显变化;组胺及IgG阳性组与阴性组及样品组间均有差异。结论 建议羟乙基淀粉40氯化钠注射液安全性评价应包括过敏反应,还可在羟乙基淀粉临床应用时进行组胺及IgG这两项过敏指标的监测。
羟乙基淀粉40氯化钠注射液;过敏反应;组胺;IgG
羟乙基淀粉为羟乙基化支链淀粉的水解产物,其制剂是一种良好的血浆代用品,具有降低血液黏度、改善血流动力学、扩充血容量、提高组织供氧、进而改变微循环、抑制炎症等作用[1]。羟乙基淀粉40氯化钠注射液作为血容量补充药,有抑制血管内红细胞聚集作用,用于改善微循环障碍,临床用于低血容量性休克,如失血性、烧伤性及手术中休克等;少数患者使用本品可出现过敏现象,表现为眼睑水肿、荨麻疹及哮喘等。为进一步弄清羟乙基淀粉40氯化钠注射液过敏反应情况,我们进行了主动全身过敏和被动皮肤过敏试验研究,以期进一步明确羟乙基淀粉40氯化钠注射液不良反应的真正原因,为确保安全用药提供依据。同时,优选过敏方法指标,为羟乙基淀粉40氯化钠注射液安全性研究提出合理化建议。
1 材料和方法
1.1 实验动物
普通级豚鼠,体重280~310 g,来源于无锡市惠山江南实验动物场[SCXK(苏)2015-0004]。实验环境室温度20~24 ℃,相对湿度为45%~60%,实验于江苏省食品药品监督检验研究院设施内进行[SYXK(苏)2012-0043]。并按实验动物使用的3R原则给予人道的关怀。
1.2 试剂与仪器
41批羟乙基淀粉40氯化钠注射液(企业A、B)、4批高渗氯化钠羟乙基淀粉40注射液(企业C)、2批羟乙基淀粉130/0.5氯化钠注射液(企业D)。氯化钠注射液(江苏四环生物制药有限公司,批号:15070410,规格:100 mL:0.9 g);新生牛血清(浙江天杭生物科技有限公司, 批号:141011)。
豚鼠组胺ELISA 试剂盒(96T 批号:BPE40015);豚鼠IgE ELISA 试剂盒(96T 批号:BPE40020);豚鼠IgG ELISA 试剂盒(96T 批号:BPE40003);豚鼠IgM 试剂盒(96T 批号BPE40022),均购自朗顿生物公司。
L-550离心机(长沙湘仪离心机仪器有限公司);全自动酶标仪(Synergy H1,BIOTEK公司)。
1.3 实验方法
1.3.1 豚鼠全身主动过敏试验
将豚鼠按体重随机分组(每组6只),分别为:氯化钠注射液组、10%小牛血清组、羟乙基淀粉40注射液组、羟乙基淀粉130注射液组。取豚鼠6只,隔日给药一次,给予每只动物0.5 mL相应的供试药液,连续3次,然后分别于末次给药后的14 d和21 d,给予每只动物前肢静脉注射各组1.0 mL相应的供试药液激发注射。观察各组动物在激发注射后15 min内是否出现过敏反应(有无竖毛、发抖、干呕、连续喷嚏3 声、连咳3 声、紫癜、呼吸困难、二便失禁、步态不稳或倒地、抽搐、休克、死亡等过敏反应症状)。21 d给药后15 min 取血浆检测组胺、总IgE、IgG、IgM 水平[2]。
1.3.2 被动皮肤过敏试验[3]
1.3.2.1 剂量组别
设阴性、阳性对照组、受试药组。阴性对照组用氯化钠注射液,阳性对照组用新生牛血清10倍稀释液。
1.3.2.2 每组动物数
普通级豚鼠,雌雄各半。致敏每组 6只,激发每组 6只 , 均为雌雄各半。
1.3.2.3 致敏方法及抗血清的制备
取上述豚鼠,随机分组,每组6只,雌雄各半,分别为受试药组、小牛血清组和氯化钠注射液组,按无菌操作方法,隔日腹腔注射上述三种药品致敏,0.5 mL/只,共计注射3次,然后于最后一次致敏注射后第10日,股动脉采血,分离血清, 将各组6只豚鼠的血清分别混合, -20℃保存,2周内备用。
1.3.2.4 PCA反应的激发
取上述各组抗血清用生理盐水稀释成1∶2、1∶8、1∶32。然后取上述豚鼠,随机分组,每组6只,雌雄各半,在豚鼠两侧背部预先剪毛,再取受试物组、新生牛血清组和氯化钠注射液组的稀释抗血清,于剪毛处皮内注射各0.1 mL。经48 h后,各组静脉注射与致敏剂量相同的激发抗原加等量的1%依文思兰染料溶液,1 mL/只。30 min后麻醉处死各组动物,剪取背部皮肤,测量皮肤内层的斑点大小,直径大于5 mm者判定为阳性。
1.4 统计学方法
采用SPSS13.0统计软件处理组间差异,实验数据以均数±标准差(±s)表示,用双侧t检验进行统计学计算,P< 0.05 表示有统计学意义。
2 结果
2.1 豚鼠全身主动过敏试验
取3个企业45批羟乙基淀粉40氯化钠注射液原液,致敏并激发豚鼠,结果均未发生豚鼠主动全身过敏反应。 羟乙基淀粉130/0.5氯化钠注射液(企业D)1412042批号的其中一只豚鼠出现连续咳嗽现象,小牛血清组攻击3 min后即出现步态不稳,咳嗽,抽搐,倒伏等强阳性反应。
通过对血浆中过敏性指标组胺(HIS)、IgG、IgM和IgE进行测定和比较发现IgM和IgE在各组间均无明显变化,而组胺及IgG在小牛血清阳性组内有比较明显的升高,见图1、2及表1。用双侧t检验进行统计学计算发现,阳性组与阴性组及样品组间均有差异,阳性结果成立。组胺及IgG在羟乙基淀粉40各组间无显著差异,与阴性对照组无显著区别。
2.2 豚鼠被动皮肤过敏试验
我们对3个企业45批羟乙基淀粉40氯化钠注射液,取原液,致敏并攻击豚鼠,考察豚鼠被动皮肤过敏反应,结果均未发生豚鼠被动皮肤过敏反应。
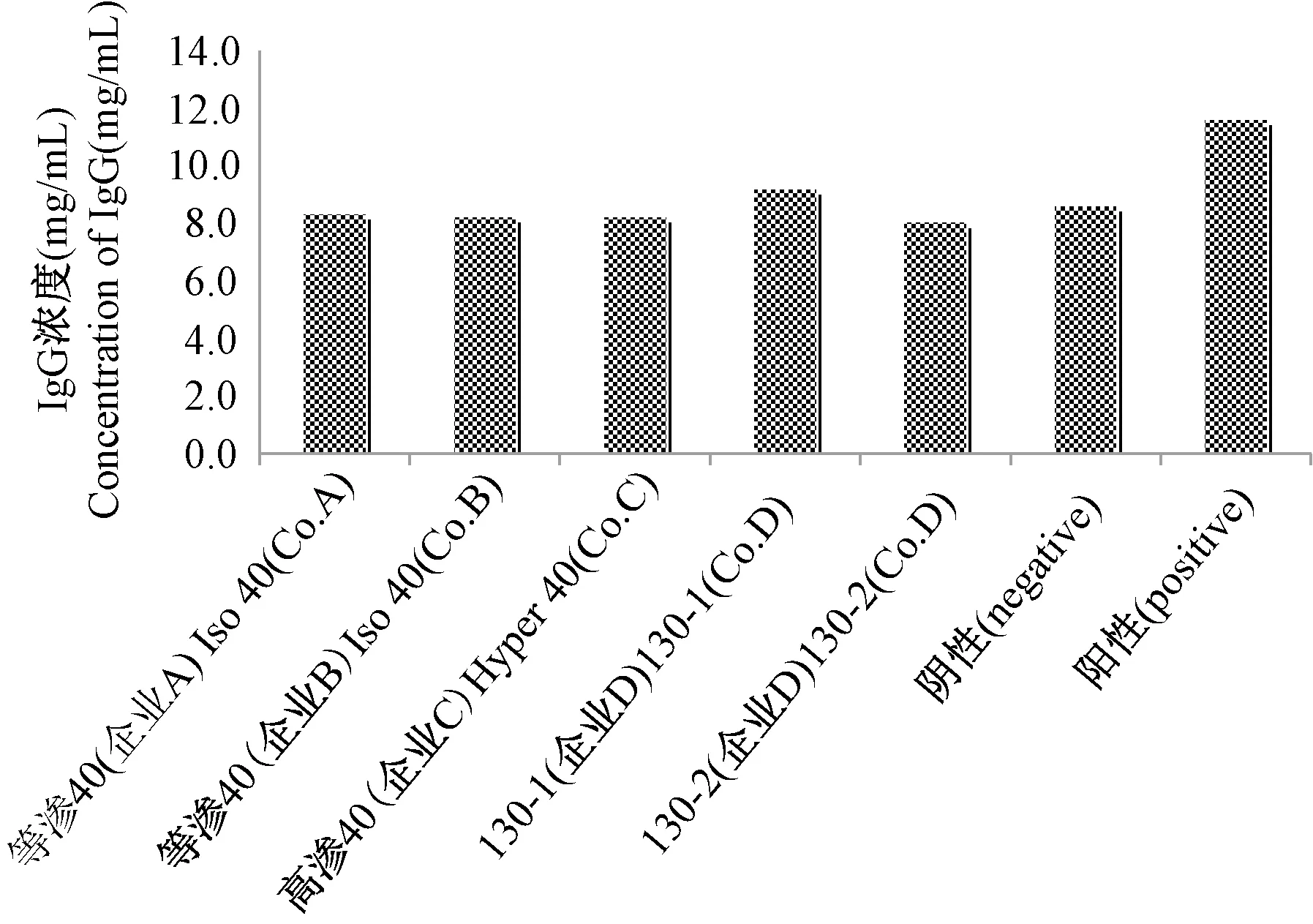
图1 各组间IgG均值比较Fig.1 Comparison on average of IgG in each group.
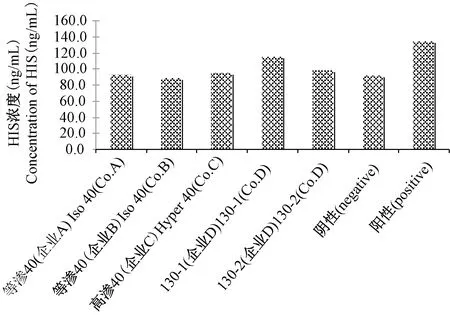
图2 各组间HIS均值比较Fig.2 Comparison on average of HIS in each group.
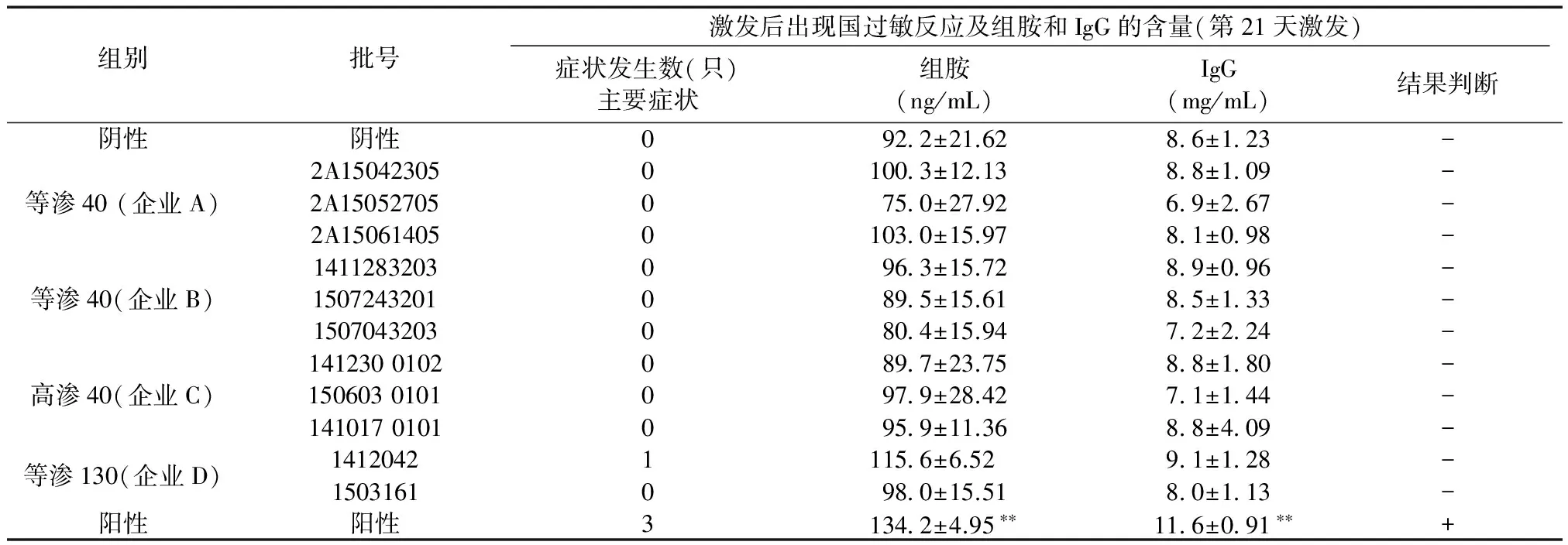
组别批号激发后出现国过敏反应及组胺和IgG的含量(第21天激发)症状发生数(只)主要症状组胺(ng/mL)IgG(mg/mL)结果判断阴性阴性0922±21.6286±123-2A1504230501003±12.1388±109-等渗40(企业A)2A150527050750±27.9269±267-2A1506140501030±15.9781±098-14112832030963±15.7289±096-等渗40(企业B)15072432010895±15.6185±133-15070432030804±15.9472±224-14123001020897±23.7588±180-高渗40(企业C)15060301010979±28.4271±144-14101701010959±11.3688±409-等渗130(企业D)141204211156±6.5291±128-15031610980±15.5180±113-阳性阳性31342±4.95∗∗116±091∗∗+
注:与阴性相比较,**P< 0.05。
Note.Compared with the negative control ,**P< 0.05.
3 讨论
本研究对企业A和B的41批羟乙基淀粉40氯化钠注射液、企业C的4批高渗羟乙基淀粉氯化钠注射液、企业D的羟乙基淀粉130/0.5氯化钠注射液,用豚鼠进行了全身主动过敏和被动皮肤过敏实验,结果显示,羟乙基淀粉40氯化钠注射液等渗和高渗溶液均无明显过敏反应。目前羟乙基淀粉40氯化钠注射液质量标准中未制定过敏反应检查项,但因药物在临床不良反应中有过敏反应现象,故建议企业增加过敏反应发生的质量监控。另外因《中国药典》中过敏反应检查是用豚鼠全身主动过敏检查法,仅是对动物行为学指标进行观察,也受试验者主观因素影响,存在误差。而在临床上出现的一些超过敏反应症状在此检查法中也不能体现出,故可对过敏实验敏感动物模型方面作进一步研究。
本次研究中羟乙基淀粉130组中有1只豚鼠出现咳嗽症状,该组组胺及IgG水平比阴性及羟乙基淀粉40组也略有升高,虽统计学分析无显著性差异,但结合前期不良反应检索结果提示我们分子量大小与过敏反应存在一定的正相关,中、高分子量的羟乙基淀粉存在过敏反应的风险,其作为代血浆使用时,为急救用药且用量大,所以安全性尤为重要。故有必要对羟乙基淀粉130、羟乙基淀粉200进行进一步过敏研究,同时在其临床应用时收集组胺及IgG这两项过敏指标与不良反应相关性的数据,对易过敏病人提高警惕,以减少不良反应的发生,保障用药的安全。
[1] 陈燕,骆喜宝,潘云. 羟乙基淀粉的药理作用和临床应用研究进展[J]. 医学综述,2012,18(4):593-595.
[2] 张美玉,李贻奎,张嘉,等.鱼腥草注射液过敏及类过敏实验研究[J].中国现代应用药学杂志,2009,26(8):610-614.
[3] 国家食品药品监督管理总局.药物刺激性、过敏性和溶血性研究技术指导原则(2014年版)[OL].http://www.sfda.gov.cn/WS01/CL1616/101018.html
Experimental Study on Anaphylactoid Reactions of Hydroxyethyl Starch 40 Sodium Chloride Injection
ZONG Wei-feng,WANG Yu-xin,LIU Yang,WANG Yao,ZHANG Wei-feng,LU Yi-hong*
(Jiangsu Institute for Food and Drug Control,Nanjing 210008,china)
Objective To evaluate the sensitizations of Hydroxyethyl Starch 40 Sodium Chloride Injection. Methods Active systemic anaphylaxis(ASA) test, internal sensitive index’s determination and screening and Passive Cutaneous Anaphylaxis(PCA) test are carried out. Observe the allergy safety of the samples. Results We use guinea pigs to carry on ASA test and PCA test with Hydroxyethyl Starch 40 Sodium Chloride Injection from 45 batches of 3 companies and no changes have occurred. Measuring and comparing the sensitive index of HIS,IgG, IgM and IgE in plasma, IgM and IgE are not obvious variation; HIS and IgG positive group and negative group and sample groups are different.Conclusions It is suggestion that Hydroxyethyl Starch 40 Sodium Chloride Injection safety evaluation should include allergic reactions, HIS and IgG sensitive index monitoring in clinical application of hydroxyethyl starch.
Hydroxyethyl starch 40 sodium chloride injection;Anaphylactoid reactions; HIS; IgG
宗卫峰(1978-),男,副主任药师,研究方向:药品药理毒理研究、实验动物检测。E-mail:wfzong@sina.com
陆益红,主任药师,研究方向:药品药理毒理研究、实验动物检测。E-mail:yihonglu@163.com
研究报告
R-332
A
1671-7856(2017) 01-0064-03
10.3969.j.issn.1671-7856.2017.01.013
2016-06-14
