活性炭负载镍催化二苯并呋喃加氢的研究
2017-01-12王广兴蔡洪涛王守凯
李 强,王广兴,蔡洪涛,藏 娜,刘 佳,王守凯
(1. 中钢集团鞍山热能研究院有限公司,辽宁 鞍山 114044;
2. 中唯炼焦技术国家工程研究中心有限责任公司,辽宁 鞍山 114044)
活性炭负载镍催化二苯并呋喃加氢的研究
李 强1,2,王广兴1,蔡洪涛1,2,藏 娜1,2,刘 佳1,2,王守凯1,2
(1. 中钢集团鞍山热能研究院有限公司,辽宁 鞍山 114044;
2. 中唯炼焦技术国家工程研究中心有限责任公司,辽宁 鞍山 114044)
以活性炭负载镍为催化剂,对二苯并呋喃催化加氢工艺进行了研究,通过GC/MS分析加氢产品的组成,对加氢组份含量变化趋势进行分析,并提出了加氢反应路线。同时对二苯并呋喃加氢制备2-环己基环己醇的反应进行了研究,考察反应温度、反应压力和反应时间对产品收率的影响。实验结果表明:在甲苯溶剂中,反应温度150℃,反应压力0.5 MPa,反应时间为12 h,产品收率为63.3%,纯度>98%(GC)。产品结构经IR和1H-NMR表征
二苯并呋喃;活性炭负载镍;催化加氢;2-环己基环己醇
二苯并呋喃(DBF)具有两个苯环和一个呋喃结构,是高温煤焦油深加工产品之一。在煤焦油中的含量约为0.5%~1%,大部分集中在洗油馏分中,在洗油中的含量约为10%[1]。近年,国外以贵金属为催化剂,对含氧和含氮化合物进行选择性加氢得到相应的醇的衍生物和脱氧产物的文献报道很多[2-4]。有研究者以硫化Ni(Co)-Mo为催化剂,对二苯并呋喃加氢反应机理进行了研究,并提出了一系列加氢反应路线[5-7]。从反应路线来看,二苯并呋喃先发生环氢化,然后通过C-O键加氢反应脱氧。Hall等人以负载钼催化剂,在10 MPa压力下,反应温度为300~450℃对二苯并呋喃进行加氢。反应路线检测到苯环加氢的产物,即2-环己基苯酚,并在超过450℃以上的高温条件下,得到了联苯和2-苯基苯酚[8]。
目前,加氢研究多使用Pt和Pd等贵金属催化剂,并且反应条件苛刻,研究焦点主要集中深度加氢脱氧,造成了二苯并呋喃资源的浪费。笔者以廉价的活性炭负载镍为催化剂,对二苯并呋喃进行加氢,可以有效的控制加氢程度,得到半加氢化合物,特别对2-环己基环己醇表现出较好的选择性。
1 实验
1.1 试剂和仪器
试剂:二苯并呋喃(98%、鞍山鞍钢实业三块石化工厂),高纯氢(99.999%,北京公司),活性炭负载Ni(营口太秦科技公司),二甲苯(AR,国药集团化学试剂有限公司)。
仪器:FYxD0.3射350型机械搅拌高压反应釜(大连第四仪表厂),GC/MS-QP2010气相色谱-质谱联用仪(日本Shimaszu公司),Avance 500 MHZ核磁共振波谱仪(瑞士Bruker),Magana傅里叶红外光谱仪(美国Nicolet)。
1.2 合成方法
实验开始时先将23.3 g(0.138 mol)二苯并呋喃(DBF),150 mL二甲苯和2.5 g活性炭负载镍加入反应釜,经密封抽真空后通入约0.3 MPa氢气,升高反应釜温度并恒定到设定的反应温度,向反应釜中通氢气至目标压力,开始搅拌。此时釜内二苯并呋喃在催化剂作用下发生加氢反应,记录加氢组份随时间的变化情况。反应结束后的产物通过GC/Ms进行定性、定量分析。
2 结果与讨论
2.1 DBF加氢GC/MS分析和加氢路线
2.1.1 DBF加氢GC/MS分析
以活性炭负载镍为催化剂,在100℃下,氢压在0.5 MPa进行二苯并呋喃加氢。经GC/MS检测产物组成包括十二氢二苯并呋喃(DHDBF)、六氢二苯并呋喃(HHDBF)和四氢二苯并呋喃(THDBF)。除此以外,加氢过程中还检测到C-O键断裂产生化合物,其中包括二氢化2-羟基联苯、2-苯基环己醇(PCHOH)、2-环己基苯酚(CHPOH)和2-环己基环己醇(CHCHOH)。还有一些脱氧产物被检测到,例如环己基苯(CHB)和对环己基环己烷(BCH)。还发现2-异丁烯基环己酮(CHIB),这说明在加氢过程中发生了裂解。
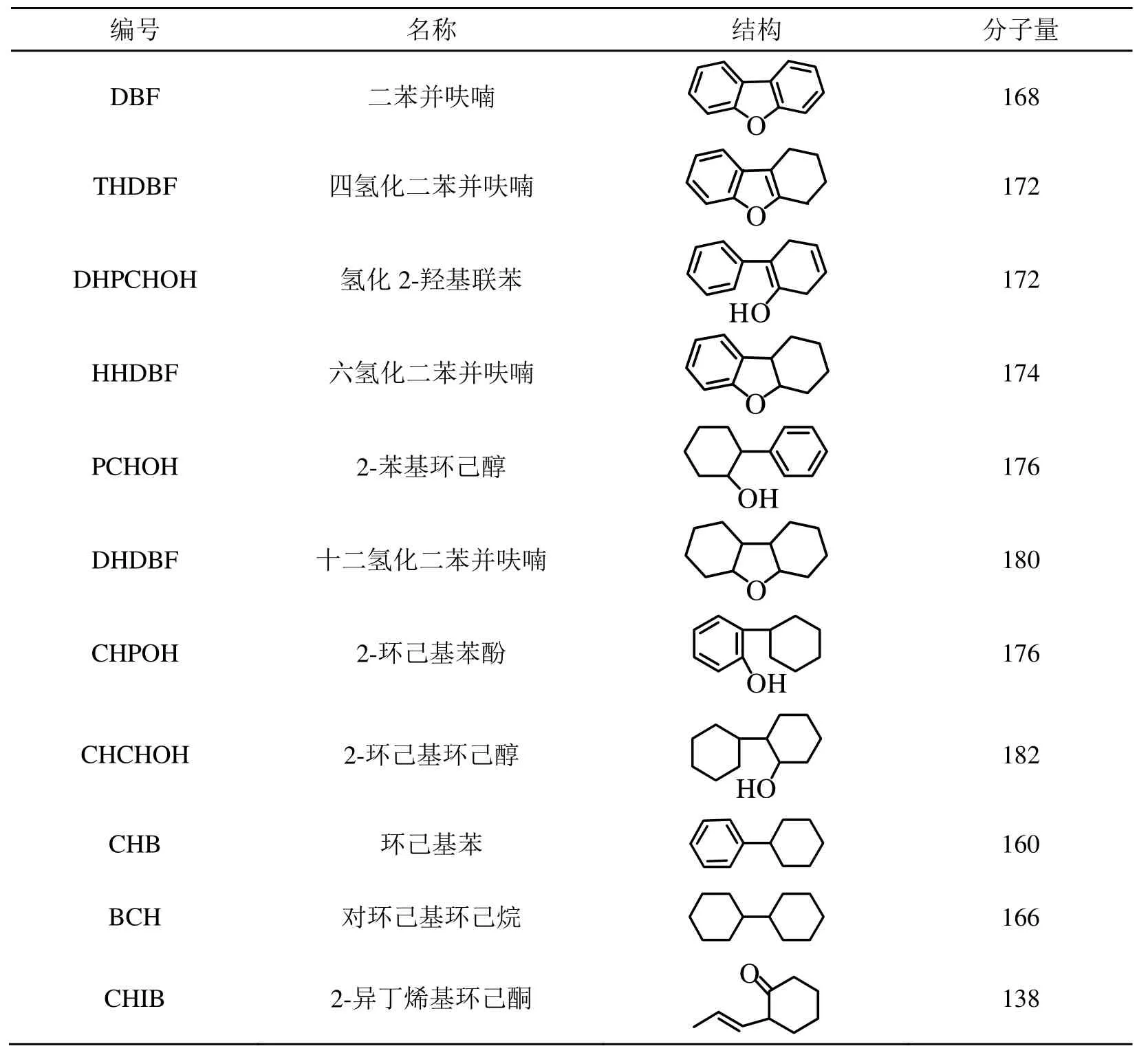
表1 二苯并呋喃加氢GC/MS分析结果
2.1.2 DBF加氢组份变化趋势
以活性炭负载镍催化二苯并呋喃加氢,加氢产物组份变化趋势如图1所示。

图1 二苯并呋喃加氢产品含量
由图1表明, CHCHOH的含量随着反应进行而不断增加,是加氢的主要产物;HHDBF的含量先随反应进行而增加,当DBF的量下降的一定水平后,HHDBF被继续加氢,含量开始下降;产物中THDBF含量初期增加较快,DHPCHOH增加缓慢,且含量很低,这说明在反应的初始阶段,DBF的C-O键断裂较难,主要以苯环加氢为主;随反应时间的延长,PCHOH的和CHPOH的开始增加,THDBF开始减少,苯环加氢破坏了共轭体系,反应向C-O键断裂方向进行,由于HHDBF中一个苯环和氧原子的p-π共轭作用,使另一边与环烷基相邻的C-O键更容易断裂,因此PCHOH的含量较CHPOH低;DHDBF和BCH作为全加氢产物,其含量一直在较低水平波动;CHB为加氢脱氧产物,在反应后期含量有一定增加。通过产物结构的分析说明,在该催化条件下,可以有效控制加氢程度,得到全加氢和半加氢产物。
2.1.3 DBF加氢路线
根据加氢组份变化趋势得到加氢反应路线:DBF先进行苯环加氢得到HHDBF,随着加氢进行C-O键断裂转化为CHPOH。再进一步进行苯环加氢得到CHCHOH,其中一部分CHPOH再进一部分加氢脱氧得到CHB。
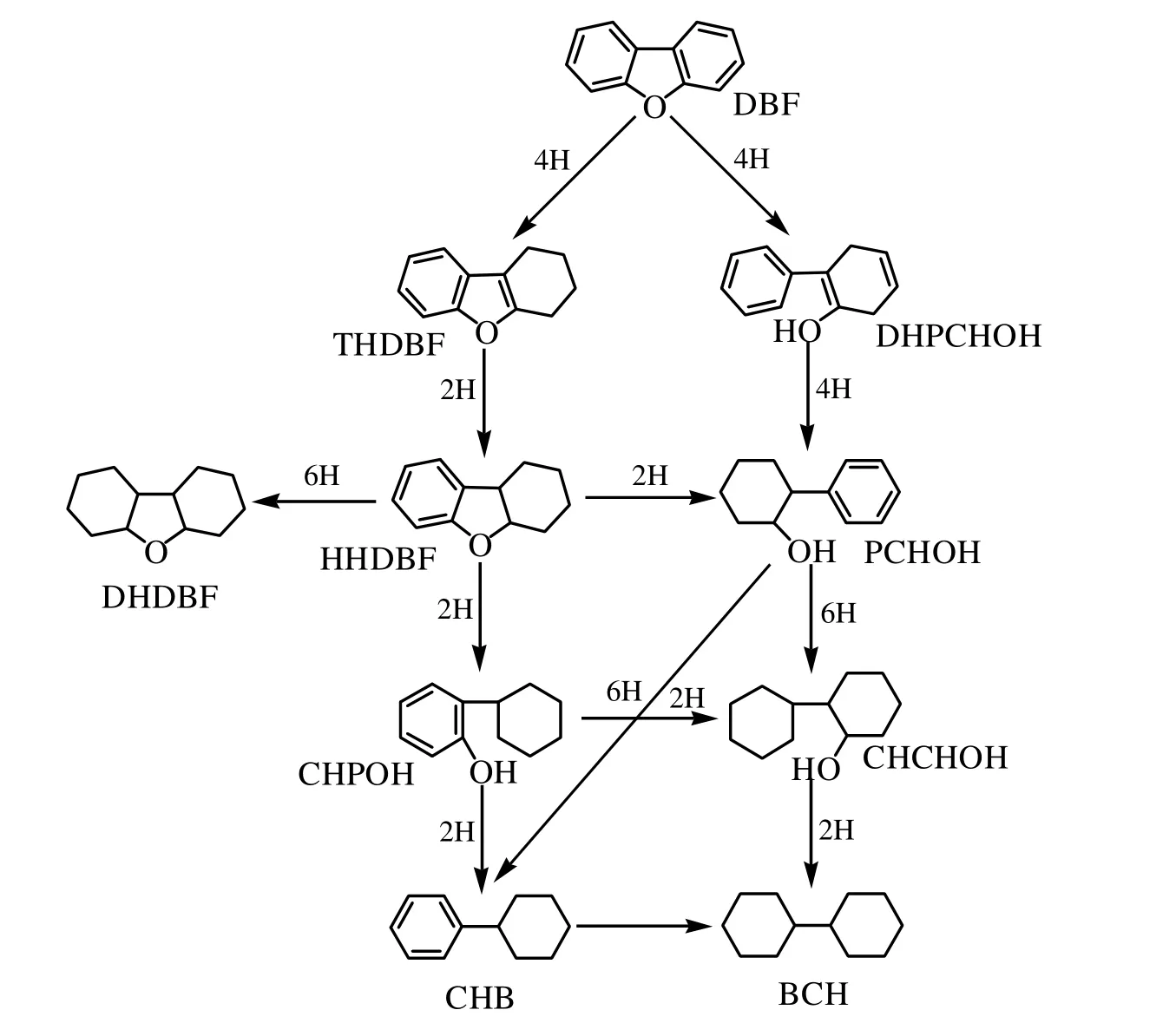
图2 二苯并呋喃加氢路线图
2.2 目标化合物合成条件
2.1.2 反应温度对产率收率的影响
称取DBF 23.3 g(0.138 mol),2.33 g活性炭负载镍为催化剂,150 mL二甲苯为溶剂,通入0.5 MPa氢气,反应时间为16 h,改变反应温度,考察反应温度对产品收率的影响,实验结果如表2所示。
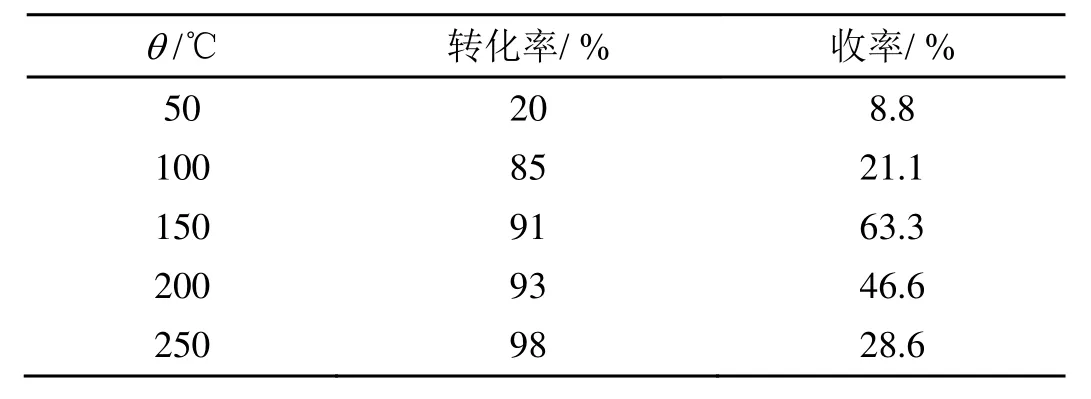
表2 反应温度对收率的影响
从表2结果可知,当反应温度在50℃时,加氢反应进行不完全,DBF转化率太低。当反应温度在100℃时,产品收率提高,但产品选择性降低,产品收率反而降低。而当反应温度在150℃时,产品收率达到最高。随着温度继续增加时,DBF转化率也随着升高,但产品也进一步氢化导致产品收率降低。
2.1.3 反应压力对产物收率的影响
称取DBF 23.3 g(0.138 mol),2.33 g活性炭负载镍为催化剂,150 mL二甲苯为溶剂,反应温度为150℃,反应时间为16 h,改变反应压力,实验结果如表3所示。

表3 反应压力对收率的影响
从表3结果可知,随着反应压力升高,DBF的转化率逐渐增加。但由于选择性随温度升高而降低,收率反而逐渐降低。当反应压力为0.5 MPa时,DBF转化率最低,但产品收率最高
2.1.3 反应时间对产物收率的影响
称取DBF 23.3 g(0.138 mol),2.33 g活性炭负载镍为催化剂,150 mL二甲苯为溶剂,通入0.5 MPa氢气,反应温度为150℃,改变反应时间,实验结果如表4所示。
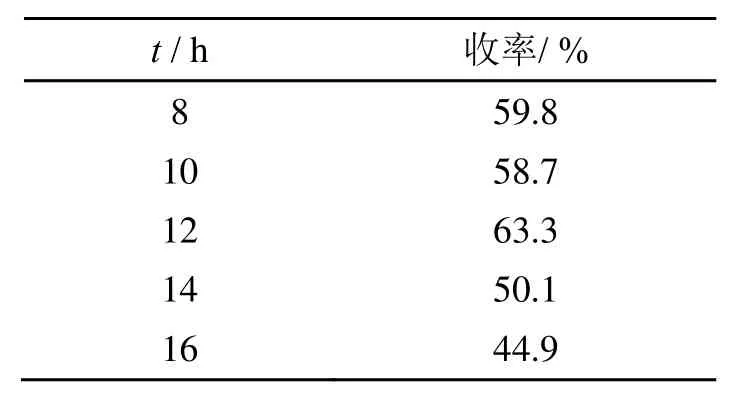
表4 反应时间对收率的影响
从表4结果可知,反应时间为12h收率最高,为63.3%。时间太短,反应不完全,收率偏低;延长反应时间,CHCHOH继续加氢反应,收率开始降低。
3 结论
1)活性炭负载镍催化二苯并呋喃加氢工艺,表现出对加氢程度良好的控制性,为合成半加氢产物提供了新思路。通过GC/MS分析二苯并呋喃加氢组份,研究各组份随反应进行的变化趋势,并提出了加氢路线:先经历苯环加氢,再加氢使C-O键断裂,最后再进行苯环加氢,期间部分会发生脱氧反应。
2)以二苯并呋喃加氢制备2-环己基环己醇的最佳的工艺条件为:在甲苯溶剂中,活性炭负载镍为催化剂,反应温度为150℃,反应压力为0.5 MPa,反应时间为12 h。收率63.3%,产品纯度98%(GC)。
[1] 汪镭, 张明明, 张淼, 等. 二苯并呋喃在负载型钯催化剂上加氢脱氧反应性能研究[C]. 中国会议, 2013: 376-378.
[2] Jiang Y J, Buchel R, Huang J, et al. Efficient solvent-free hydrogenation of ketones over flameprepared bimetallic Pt-Pd/ZrO2catalysts[J]. Chem Sus Chem, 2012, 5(7): 1190-1194.
[3] Lee C R, Yoon J S, Suh Y W, et al . Catalytic roles of metals and supports on hydrodeoxygenation of lignin monomer guaiacol[J]. Catal Commun, 2012, 17: 54-58.
[4] Huang J, Jiang Y, Hunger M, et al. Tuning the support acidity of flame-made Pd/SiO2-Al2O3catalysts for chemoselectivehydrogenation[J]. J Catal, 2011, 281(2): 352-360.
[5] Girgis M J, Gates B C. Catalytic hydroprocessing of simulated heavy coal liquids. 1. Reactivities of aromatic hydrocarbons and sulfur and oxygen heterocyclic compounds[J]. Ind Eng Chem Res. 1995, 36(1): 1098-1106.
[6] Krishnamurthy S, Panvelker S, Shah Y T. Hydrodeoxygenation of dibenzofuran and related-compounds[J]. AlChE J, 1981, 27(6): 994-1001.
[7] Furimsky E. Catalytic hydrodeoxygenation[J]. Appl Catal Agen, 2000, 199(2): 147-190.
[8] Hall C C, Cawley C M. A review of some of the reactions involved in the hydrogenation- cracking of tar[J]. J Soc Chem Ind, 1934, 53: 806-811.
Study on the Hydrogenation of Dibenzofuran by Activated Carbon Supported Nickel
Li Qiang1,2, WANG Wang-xing1, CAI Hong-tao1,2, ZHANG Na1,2, LIU Jia1,2, WANG Shou-kai1,2
(1. Sinosteel Group Anshan Research Institute of Thermo-energy, Anshan 114044, China; 2. National Engineering Research Center for Coking Technology, Anshan 114044, China)
The hydrogenation of dibenzofuran was studied by using activated carbon supported nickel as the catalyst. The composition of the hydrogenation products was analysized by GC/MS, the trend of component content had been conducted, and hydrogenation route had been proposed. The synthesis of 2-cyclohexyl cyclohexanol was studied by hydrogenation of dibenzofurans. The optimal reaction conditions, such as the reaction temperature, reaction pressure and reaction time were found. The experimental results showed that the yield of product was 63.3% and the purity was greater than 98% (GC), when the reaction was carried out for 12h at 150℃ at 0.5 MPa of H2pressure using toluene as solvent. The chemical structure of the product was characterized by IR and1H-NMR.
dibenzofuran; activated carbon supported nickel; catalytic hydrogenation; 2-cyclohexyl cyclohexanol
TQ251.1
A
1009-220X(2016)06-0018-06
10.16560/j.cnki.gzhx.20160616
2016-08-25
李 强(1983~),男,辽宁鞍山人,硕士,工程师;主要从事精细化工中间体合成的研究。
* 通讯作者:王守凯(1965~),男,辽宁鞍山人,教授级高工;主要从事煤焦油基功能材料的研究。wsk5840863@126.com
