低频超声透皮给药过程流场影响分析*
2017-01-09彭瀚旻喻伯平朱攀丞陈致钧
彭瀚旻, 喻伯平, 毛 婷, 朱攀丞, 陈致钧
(南京航空航天大学机械结构力学及控制国家重点实验室 南京,210016)
低频超声透皮给药过程流场影响分析*
彭瀚旻, 喻伯平, 毛 婷, 朱攀丞, 陈致钧
(南京航空航天大学机械结构力学及控制国家重点实验室 南京,210016)
针对低频超声透皮给药过程中声场和流场的促渗机理问题,基于压电方程、声压方程以及湍流k-ε模型,利用COMSOL有限元软件建立了其声-压电-流耦合仿真计算模型。通过理论分析和Franz体外透皮实验分别获得了给药系统中的声场与流场的大小及分布,以及体外实验的超声促渗后的渗透量。仿真计算与实验结果表明:离体皮肤在超声作用下渗透量更大,皮肤上产生更多褶皱与空化穴,这说明存在空化效应与交变载荷,而后者可能是流场流动或涡流引起的;药液中流场沿超声换能器的辐射面下方流动到辐射面侧面,形成搅拌作用,且辐射面正下方的流速最大,当输入电功率为5.5 W时,可达0.55 m/s,皮肤上方伴有较强涡流;流场在超声促渗中起搅拌与扩张皮肤通道的作用,对促渗起辅助作用。
低频超声; 透皮给药; 超声换能器; 流场; 有限元
引 言
近20年来,人们已经发现低频超声[1]对透皮给药具有促渗的效果,国内外专家学者已经对其进行了多方面的研究,其内容涵盖超声波促渗机理[2]、超声设备设计[3]、理论建模方法[4]、药物作用机理[5]以及临床安全[6]等。20世纪90年代初,文献[7-8]发现低频超声(20~100 kHz)可以暂时破坏皮肤角质层从而形成新的渗透通道,使药物得以在皮肤无创的前提下渗入人体的新陈代谢系统当中,实现安全可靠的透皮给药操作。Mitragotri等[9]验证了胰岛素、γ-干扰素等蛋白质的低频超声透皮给药方法。Tezel等[10]发现超声透皮给药具有提高免疫效果的作用。Park等[11]发现超声造影剂可与超声联合加强促渗作用。Han等[12]提出了低频超声与微针相结合可以导入分子量大于500 Da的牛血清白蛋白。Cobo等[5]使用低频超声成功从鱼鳃给鱼注入疫苗,使低频超声透皮给药技术从哺乳动物扩展到非哺乳动物。
国内方面,Zhang等[13]研究低频超声与局部麻醉之间的关系。Liu等[14]研究了低频超声和月桂基磺酸钠联合作用下环孢霉素A透皮给药效果。吕川等[15]发现低频超声给药可显著提高皮瓣毛细血管密度,增加皮瓣的成活率。由此可见,低频超声技术不但能够实现透皮给药,同时还具有活化细胞、加速新陈代谢及提高免疫能力的功能。
虽然低频超声透皮给药技术发展了很多年,但是由于其中的多场耦合作用,具体机理尚不完全清楚。目前,低频超声给药系统促渗的原理主要有两个作用因素:a.超声波对角质层进行超声辐照,药液中产生空化效应,空化气泡爆炸产生冲击波破坏皮肤角质层结构,形成新的药液渗透通道;b.皮肤上层的声场与流场会造成皮肤的收缩与膨胀,加速渗透通道的形成。其中,在超声与液体耦合问题研究领域,Trujillo等[16]应用COMSOL Multiphysics有限元软件对声化学反应器中的声学流进行了建模,获得了反应器中的流速分布。梁松等[17]利用换能器压电耦合和声场模型进行了分析计算,获得了液体中的声压分布。笔者建立了低频超声透皮给药过程中压电-声-热多物理场耦合的计算数学模型[18],获得了给药系统的温度分布及温升规律。但是目前低频超声透皮给药过程中的声场与流场的具体运动规律还不清楚,哪种因素对渗透率影响更大,仍然是值得关注的科学问题。笔者拟通过建立低频超声给药系统中的声-压电-流多场耦合计算方法,获得声场与流场的大小及分布,分析其在促渗过程中的不同作用,结合体外透皮给药渗透的实验结果研究低频超声透皮给药过程中的机制。
1 低频超声给药系统
本研究所采用的低频超声给药系统主要包括两部分:a.21 kHz超声换能器(苏州工业园区海纳科技有限公司);b.Franz扩散池透皮体外实验系统(天津正通公司TT-8透皮仪系统),如图1所示。前者在21 kHz的驱动电压下可由变幅杆向药液及皮肤辐射一定功率的低频超声波,本研究采用40 V(零峰值电压)为计算与实验的输入电压。后者是一种在恒温水域系统中(37℃)模拟皮肤表面药物渗透过程的系统,单个Franz扩散池结构单元主要包括供给体、垫圈(聚四氟乙烯压盖)、皮肤(本研究采用大鼠离体皮肤)及接受体等部件。其中,供给体内存放药液,而接受体内则接收皮肤渗透后的药液。为方便检测药液浓度与给药渗透率,笔者采用一种荧光剂钙黄绿素(Calcein)模拟药液有效成分,使用紫外可见光光度分光计检测接受体中钙黄绿素的吸光度。其浓度与吸光度成线性关系,吸光度越大表明钙黄绿素浓度越高,因此可以用吸光度大小来表示药液渗透量的大小,从而验证超声对皮肤渗透量的影响规律。
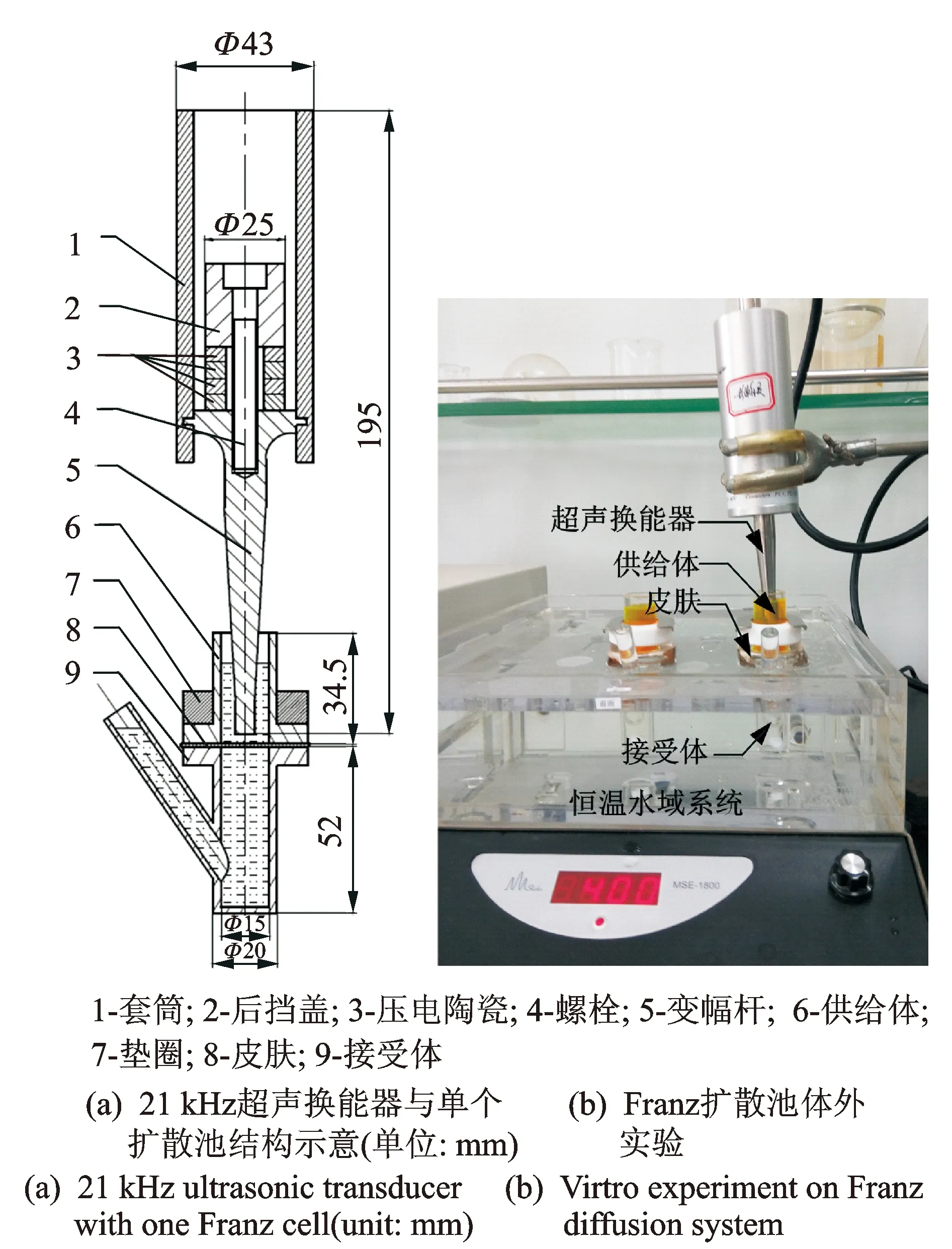
图1 低频超声给药系统Fig.1 Low-frequency sonophoresis system
2 流场计算有限元模型
2.1 理论模型
低频超声透皮给药过程包含多个物理场,本研究主要分析电能通过压电陶瓷的逆压电效应转化为药液中声场与流场的物理关系,从而获得超声促渗的物理规律。笔者以人体温度37℃为基本温度,不考虑温度场变化对声场及流场的影响,即满足给药温度始终小于安全阀值42℃,理论模型采用COMSOL Multiphysics 多物理场仿真软件对上述过程进行声场与流场的建模,主要分为两个步骤:a.对系统进行声压电耦合的分析计算获得超声换能器辐射面振幅、声场及声强;b.基于上述结果进行流场分析计算从而获得药液的流速与压强分布。
声压电耦合的计算首先建立在压电平衡方程的基础上,从而获得电场与力场之间的耦合关系,详见文献[19]。
超声透皮给药过程中的声场主要作用在供给体、接收体和皮肤中,声场中声压的平衡方程满足
(1)
其中:pt为总声压;ρc为复密度;keq为水声学中考虑声衰减系数后的等效波数。
结合电场、固体力学、声场的初始条件与边界条件,式(1)与压电平衡方程可联立求解得到总声压pt的分布。其中,复密度ρc也涵盖了等效声衰减系数的信息,详见文献[18]。
由超声透皮给药过程可知,声能衰减产生的声学流主要作用在供给体内液体中,因而笔者主要考虑供给体中的流场运动规律。由于超声功率必须超过声空化阀值从而产生空化起泡,此时液体中的流场适用湍流k-ε模型[16],满足如下Navier-Srokes方程
ρ(u)u=[-pI+(μ+μT)(u+(u)T)-(
(2)
其中:ρ为流场的液体密度;u为流体速度场矢量矩阵;p为压强,I为单位矢量矩阵;μ为流体的动力黏度;μT为湍流的涡流黏度;k为湍流动能;F为流体内部的体积力。
同时,湍流k-ε模型中关于湍流动能k与湍流耗散速率ε的平衡方程满足
(3)
(4)
μT=ρCμk2/ε
(5)
Pk=μT[u:(u+((u)2]-u
(6)
其中:Cμ,Cε1,Cε2,σε和σk为湍流k-ε模型常数。
因此,结合系统的初始条件与边界条件就可以通过上述平衡方程求得低频超声给药系统的流场速度及压强分布。
2.2 仿真计算
笔者通过COMSOL有限元软件对低频超声透皮给药系统分别进行声压电与流场的分析和计算。由于声压主要作用于液体和皮肤之上,而声流则主要作用于供给体的药液中,为简化计算量,声压电仿真计算模块选取二维轴对称模型,而流场则选择二维模型,并且只考虑供给体中的流场。模型主要假设如下:
1) 忽略扩散池接受体中支管对声场的影响;
2) 皮肤的复杂结构简化为具有一定声衰减系数的液体;
3) 计算时扩散池中的液体(皮肤除外)都简化为水,除特别说明外,都采用水的物理性质与参数。
2.2.1 声压电模块的仿真计算
笔者采用COMSOL的声压电耦合模块对低频超声给药系统中的声场进行仿真计算,其主要零部件的尺寸参数见图1和表1。系统的初始条件包括环境温度为26℃,压电陶瓷施加电压为40 V(零-峰值),药液起始与工作温度都设为37℃。边界条件为超声换能器的铝合金外壁设为固定边界,溶液、皮肤与玻璃内壁接触部分简化为硬声场边界,与空气接触部分简化为软声场边界。此外,压电陶瓷、螺栓、铝合金与钛合金的结构阻尼损耗因子分别设为1.1×10-2,1.1×10-3,1.1×10-3和1.1×10-5。超声空化作用会对声波传递产生反射、散色、介质黏滞及热传导等因素,造成声能的衰减。为简化计算,供给体内药液的平均声衰减系数取为29.4 NP/m,接受体为2.9 NP/m,声速取1 450 m/s。通过以上初始条件,结合式(1),可以计算出低频超声给药系统中的声场分布,包括声压大小、声压分布以及声强分布,并为下一步流场计算奠定基础。
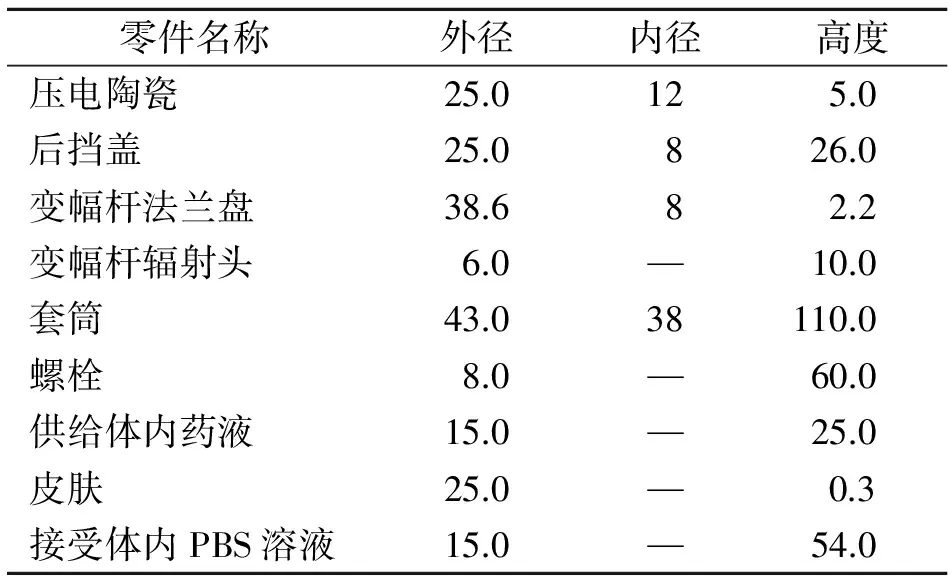
表1 零部件主要结构参数尺寸
2.2.2 流场模块的仿真计算
由于低频超声给药系统中供给体的药液为轴对称结构,为降低计算量,流场采用2D湍流k-ε模型。其中模型常数Cμ,Cε1,Cε2,σε和σk如表2所示,而流场计算网格及边界条件设定如图 2所示。其中,超声换能器辐射面设为流场入口,侧面设为出口(压强为0)。

表2 k-ε模型湍流参数值

图2 流场计算网格及边界条件Fig.2 Computing grid and boundary conditions of flow field
流场入口的边界条件包含速度场u0(下标0表示z=0处的变量值,下同),湍流强度IT0与湍流长度LT0,其中湍流长度LT0可由超声换能器的声空化流场中经验公式表示为
(7)
其中:rH为超声辐射面半径。
湍流强度IT0满足
(8)
其中:u0为流场入口处流体的流速幅值;k0为入口处的湍流动能。
由式(5)可求得
(9)
ε0满足
(10)
超声换能器的声空化流场中辐射面上的涡流黏度μT0[16]可以用经验公式表示为
(11)
K0为入口处流体的运动学动量[16],它与超声换能器辐射面的声功率W0密切相关,满足
(12)
其中:ρ0为超声辐射面处的液体密度;c为液体中声速。
此外,基于声波平面波假设,W0可以表示为
W0=A0I0
(13)
其中:A0为超声辐射面面积;I0为辐射面处液体的平均声强。
联立式(7)~式(13),可得入口边界条件湍流强度IT0的表达式
(14)
此外,流场入口的初始条件为速度场u0,它满足如下高斯分布[16]
(15)
将式(12)~式(13)代入式(16),可得
(16)
最后将式(16)代入式(14)即可获得入口边界条件湍流强度IT0与射流宽度S与声强分布I0之间的关系,前者主要来源于实验值[16],后者可由声压电耦合模块计算得出,其余参数为常量,从而计算获得了流场入口处的全部边界条件。
3 计算与实验结果讨论与分析
根据以上的理论和算法,可获得低频超声透皮给药系统中的声场分布,其中声压与声强的大小与分布如图3所示。图中声压最大值约为2×105Pa, 分布在超声换能器辐射面的正下方, 并主要集中在皮肤与换能器之间的区域。声强则主要集中在超声换能器辐射面附近,这说明在辐射面附近的液体振动速度最大。从图3中可以看出,声压与流场造成的促渗作用主要发生在Franz扩散池的供给体内药液中。
针对流场计算, 根据式(16)首先需要获得超声辐射面处的声强I0的2D 分布曲线, 它可由上述声场计算获得,如图4所示。同时根据式(14)~式(16)可求得流场入口边界条件,即等效入口速度u0和湍流强度IT0的分布,其中S[16]取0.015,如图5所示,其最大值出现在超声辐射面中心处。
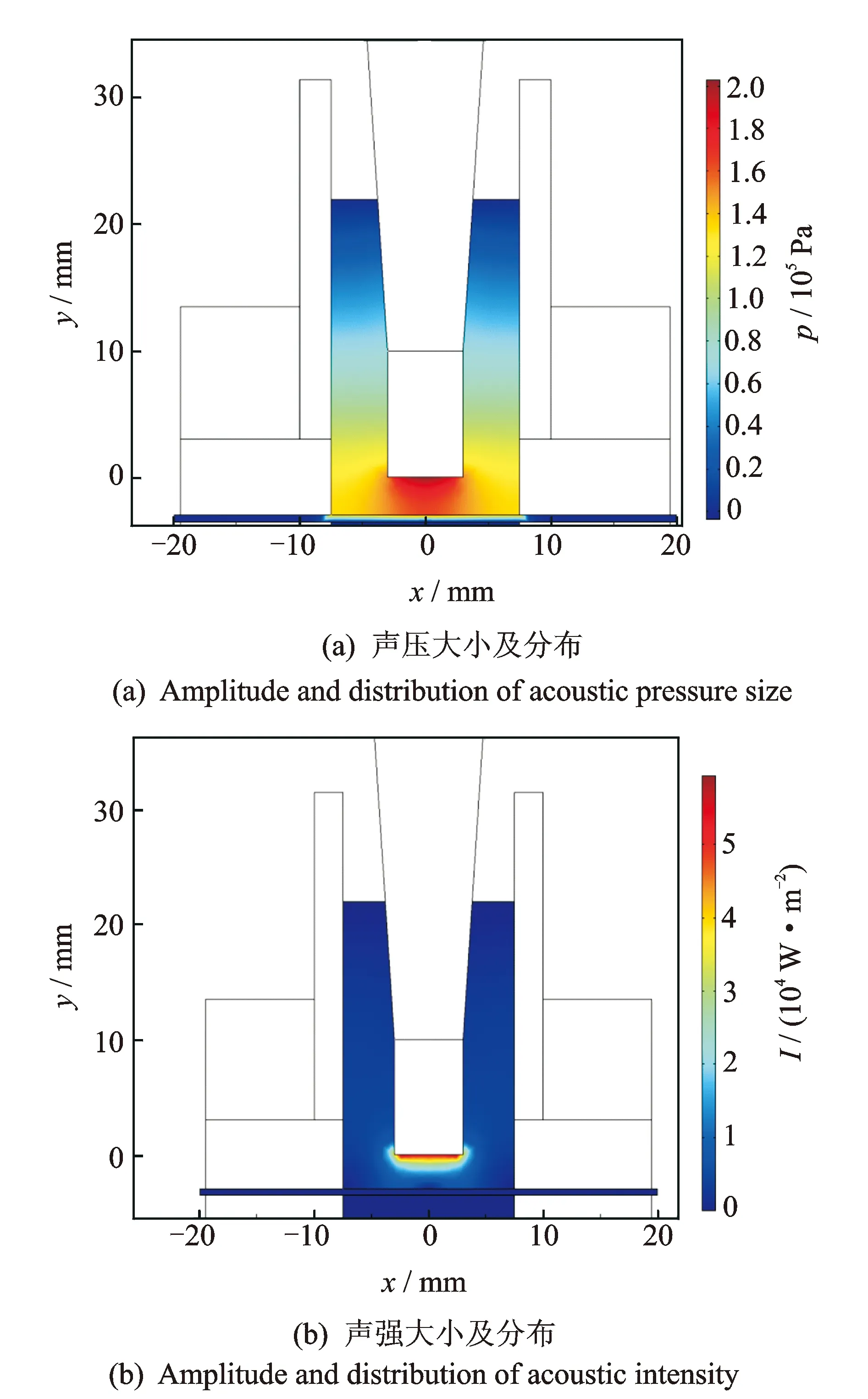
图3 低频超声透皮给药声场计算结果Fig.3 Calculated results of acoustic fields in low-frequency sonophoresis
根据图4和图5的初始条件与2.2.2节中的边界条件,以及2.2.1节中的计算方法,可以获得低频超声透皮给药系统中的流场分布,如图6所示。从图6(a)中可以看出, 供给体内药液的最大流速主要集中在超声换能器的正下方,可达0.55 m/s;在低频超声作用下,流体沿辐射面中心位置向外扩散,在供给体的药液内循环流动形成一种声流作用的搅拌现象。图6(b)显示在超声换能器的辐射面会形成一些涡流,涡流强度最大值可达479 1/s,而皮肤上表面涡流强度可以产生较大的搅拌作用。因此,低频超声透皮给药系统中的声学流主要可以起到药液搅拌和促进扩散作用,有利于药液渗透。

图4 超声辐射面处的声强均值I0分布曲线Fig.4 Distribution curve of acoustic intensity I0 on ultrasonic radiation face
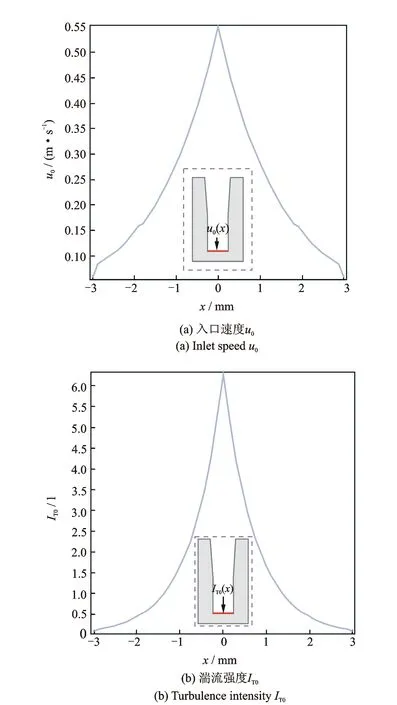
图5 超声辐射面处的初始条件Fig.5 Initial condition on ultrasonic radiation face
在低频超声透皮给药系统中,压强对渗透有促进作用,尤其是皮肤上表面的压强,可以对皮肤渗透通道产生升压作用。在供给体中压强的来源主要是超声产生的声压与流场流动产生的压力,压强的大小及分布如图7所示。从图7可以看出,声场的压强最大值仍然在超声辐射面的正下方,可达1.64×105Pa;而流场压强最大却只有70 Pa,中间位置也只有50 Pa, 远远小于声压。

图6 工作时供给体内的流场分布Fig.6 Flow field distribution in the donor at working state
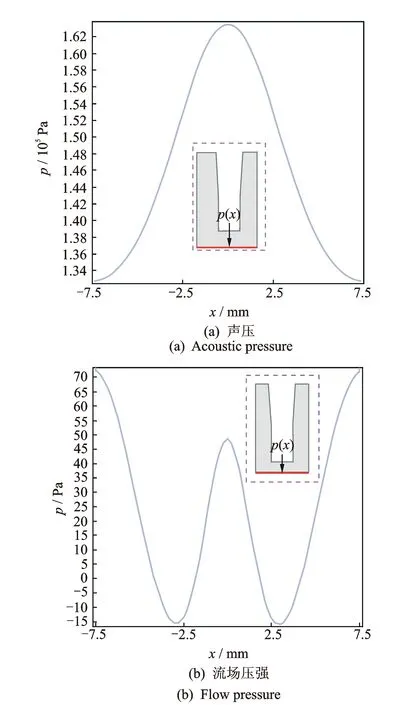
图7 表皮上的压强分布Fig.7 Pressure distribution on the epidermis
图8为5.5 W输入功率下21 kHz低频超声与自然渗透下的接受体中钙黄绿素渗透率(低浓度的Calcain溶液的吸光度与浓度关系为线性正比关系)对比图(都添加了月桂基硫酸钠,即SLS促渗剂)。其中,取3~5片大鼠离体皮肤作为体外实验样本。从图8可以看出,低频超声作用下渗透率显著高于自然渗透下的透皮给药过程。从图9可以看出,低频超声作用后的皮肤表面,比自然渗透后的表面更加粗糙,且伴有空化气泡腐蚀后的痕迹。这说明在低频超声给药过程中,存在空化效应以及声学流,空化效应可以使得皮肤表面产生空蚀现象,而声学流可以使皮肤产生更多的褶皱,加速渗透通道的形成,最终提高渗透率。

图8 低频超声与自然渗透的渗透率对比图Fig.8 Permeability contrast figure between low-frequency ultrasonic and natural permeation

图9 低频超声与自然渗透90 min后的皮肤显微镜图片Fig.9 Microscope skin images after low-frequency ultrasonic and natural permeation in 90 min
4 结束语
通过以上分析计算与实验结果,笔者获得了低频超声透皮给药过程中的声-压电-流体的耦合计算方法,并且模拟出药液内部的流场大小及分布。计算与实验结果表明,超声换能器的辐射面正下方的流速最大,当输入电功率为5.5 W时,可达0.55 m/s且产生涡流,从而实现搅拌的功能。从实验与计算结果可以看出,声压与空化效应的联合作用可使药液有效成分注入皮肤并形成新的渗透通道,而流场主要起搅拌作用,把药液有效成分迅速带到皮肤上方,使药液浓度保持均匀。
[1] Park D, Park H, Seo J, et al. Sonophoresis in transdermal drug deliverys[J]. Ultrasonics, 2014,54(1):56-65.
[2] Polat B E, Deen W M, Langer R, et al. A physical mechanism to explain the delivery of chemical penetration enhancers into skin during transdermal sonophoresis-insight into the observed synergism[J]. Journal of Controlled Release, 2012,158(2):250-260.
[3] Zhang H Y, Yeo S H. Single flexible ultrasound transducer for enhancement of permeability of silicone membrane[J]. Sensors and Actuators, A: Physical, 2005,120(1):37-43.
[4] Tezel A, Sens A, Mitragotri S. Investigations of the role of cavitation in low-frequency sonophoresis using acoustic spectroscopy[J]. Journal of Pharmaceutical Science, 2002,91(2):444-453.
[5] Cobo C, Makosch K, Jung R, et al. Enhanced Aeromonas salmonicida bacterin uptake and side effects caused by low frequency sonophoresis in rainbow trout (oncorhynchus mykiss)[J]. Fish Shellfish Immunol, 2014,36(2):444-452.
[6] Ahmadi F, Mcloughlin I V, Chauhan S, et al. Bio-effects and safety of low-intensity, low-frequency ultrasonic exposure[J]. Progress in Biophysics and Molecular Biology, 2012,108(3):119-138.
[7] Tachibana K, Tachibana S. Transdermal delivery of insulin by ultrasonic vibration[J]. Journal of Pharmaceutical Pharmacdogy, 1991,43(4):270-271.
[8] Mitragotri S, Edwards D, Blankschtein D, et al. A mechanistic study of ultrasonically-enhanced transdermal drug delivery[J]. Journal of Pharmaceutical Science, 1995,84(6):697-706.
[9] Mitragotri S, Blankschrein D, Langer R. Ultrasound-mediated transdermal protein delivery[J]. Science. 1995, 269(5225):850.
[10]Tezel A, Paliwal S, Shen Z, et al. Low-frequency ultrasound as a transcutaneous immunization adjuvant[J]. Vaccine, 2005,23(29):3800-3807.
[11]Park D, Ryu H, Kim H S, et al. Sonophoresis using ultrasound contrast agents for transdermal drug delivery: an in vivo experimental study[J]. Ultrasound in Medicine and Biology, 2012,38(4):642-650.
[12]Han T, Das D B. Permeability enhancement for transdermal delivery of large molecule using low-frequency sonophoresis combined with microneedles[J]. Journal of Pharmaceutical Science, 2013,102(10): 3614-3622.
[13]Zhang Guoliang, Lu Rongjun, Chen Xin. Application of low frequency ultrasound to promote topical eutectic mixture of local anesthetics induced analgesia:a randomized controlled study[J]. Chinese Journal of Clinical Rehabilitation, 2004,8(17):3364-3365.
[14]Liu H, Li S, Pan W, et al. Investigation into the potential of low-frequency ultrasound facilitated topical delivery of Cyclosporin A[J]. International Journal of Pharmaceutical, 2006,326(1-2):32-38.
[15]吕川.VEGF、FGF-2低频超声透皮给药系统对猪超长筋膜瓣应用的初步研究[D].上海:第二军医大学,2009.
[16]Trujillo F J, Knoerzer K. A computational modeling approach of the jet-like acoustic streaming and heat generation induced by low frequency high power ultrasonic horn reactors[J]. Ultrasonics Sonochemistry, 2011,18(6):1263-1273.
[17]梁松,张义民.超声清洗换能器设计及性能分析[J].振动、测试与诊断,2013(S2):87-90.
Liang Song, Zhang Yimin. Ultrasonic cleaning transducer design and vibration performance research[J]. Journal of Vibration, Measurement & Diagnosis, 2013,33(S2):87-90. (in Chinese)
[18]彭瀚旻,陈致钧,卢鹏辉,等.低频超声透皮给药系统压电-声-热计算模型[J].振动、测试与诊断,2015,35(6):1037-1043.
Peng Hanmin, Chen Zhijun, Lu Penghui, et al. Piezoelectric-acoustic-thermal calculation model of low-frequency sonophoresis transdermal drug delivery system[J]. Journal of Vibration, Measurement & Diagnosis, 2015,35(6):1037-1043. (in Chinese)
[19]赵淳生.超声电机技术与应用[M].北京:科学出版社,2007:130-136.

10.16450/j.cnki.issn.1004-6801.2016.06.012
*国家自然科学基金青年基金资助项目(51405224);江苏省科技计划青年基金资助项目(BK20140818);中央高校基本科研业务费专项资金资助项目(NJ20160003);江苏省大学生创新创业训练计划资助项目(201510287010Y)
2016-03-22;
2016-05-11
TH113.1; TB552; Q819
彭瀚旻,男,1984年4月生,讲师。主要研究方向为压电换能器理论分析、设计及应用。曾发表《Model study of IPMC beam response based on root deformation》(《Journal of Wuhan University of Technology-Mater》2013,Vol.28,No.1)等论文。 E-mail:penghm@nuaa.edu.cn
