纳米铝/氧化铜复合材料的制备及热性能
2016-12-29董小虎汪营磊舒远杰吴敏杰
董小虎,胡 岚,汪营磊,舒远杰,严 蕊,吴敏杰
(1.氟氮化工资源高效开发与利用国家重点实验室,陕西 西安 710065;2.西安近代化学研究所,陕西 西安 710065)
纳米铝/氧化铜复合材料的制备及热性能
董小虎1,2,胡 岚1,2,汪营磊1,2,舒远杰1,2,严 蕊1,2,吴敏杰1,2
(1.氟氮化工资源高效开发与利用国家重点实验室,陕西 西安 710065;2.西安近代化学研究所,陕西 西安 710065)
以聚乙二醇(PEG)为模板制备了纳米氧化铜。以一种高分子材料为包覆材料自组装制备了纳米铝/氧化铜(Al/CuO)复合材料。采用扫描电子显微镜(SEM)、透射电子显微镜(TEM)、能谱仪(EDS)、X射线衍射(XRD)等对材料的结构形貌进行了表征。利用热重分析法(TG)和差示扫描量热法(DSC)对比研究了自组装法(含包覆材料)与超声共混法(不含包覆材料)制得样品的热性能。研究了不同Al与CuO摩尔比下Al/CuO复合材料的放热量。结果表明,纳米铝与CuO发生铝热反应的放热峰约为576.4℃,放热量达1093J/g。含有包覆材料的复合材料比不含包覆材料的复合材料具有更大的放热量。在纳米铝与CuO摩尔比为1.0∶1.2时铝热反应放热量最大,可达1093J/g。
纳米铝热剂;纳米铝/氧化铜;热性能;聚乙二醇;超声共混法
引 言
由纳米级铝粉和金属/非金属氧化物组成的纳米级金属基反应体系被称为纳米铝热剂,也叫亚稳态分子间复合材料(Metastable Intermolecular Composites,MIC)。当其被引发时,能够发生氧化还原反应,并放出大量的热(反应温度超过3000K)[1-5]。与传统铝热剂相比,MIC材料尺寸显著降低,比表面积增大,组分间传质速度增快,反应释能速度成倍增长。研究表明[6-7],MIC材料可以明显影响火炸药的起爆、点火、燃速、比冲等性能,并可以通过改变材料的粒径、比例对相关性能进行调节。
Granier等[8]将纳米Al粉与纳米MoO3混合制备了纳米铝热剂,并测试了点火时间和燃烧速度,研究表明,减小铝粉直径有助于提高燃速,降低点火延迟时间。美国Lawrence Livermore国家实验室[9-10]采用溶胶-凝胶法制备Al/ Fe2O3纳米复合材料,比表面积达300~390m2/g,成功用于点火剂和传爆药。Kim和Zachariah[11]将A1和Fe2O3通过带电气溶胶粒子分别带有正负电荷,利用静电力进行自组装制备了复合材料,结果表明,通过静电自组装制备的材料比普通混合得到的材料组分间的界面接触明显增大,放热量也更高。Rajesh Shende等[12]将纳米Al与CuO纳米棒制备成复合材料,通过合适的化学计量配比,其燃速最高可达2400m/s。Rossi等[13]以互补的单链DNA分别包覆纳米Al和CuO,通过DNA杂交自组装制备了Al/CuO复合材料,放热量最高可达1800J/g。
在MIC材料中,Fe2O3、CuO、MnO2等金属氧化物均可用作体系的氧化剂[14-17],其中,Al/CuO体系具有更高的单位体积反应热且反应产物的相变温度更低,因此是最受关注的纳米铝热剂[18]。本研究以纳米Al/CuO为体系,分别通过自组装及超声共混的方式制备了MIC材料,采用SEM、TEM、XRD等手段对材料的结构形貌进行了全面表征,并研究了材料的热性能,对比了不同组分摩尔比下材料的热性能差异。
1 实 验
1.1 试剂与仪器
水合氯化铜(CuCl2·H2O)、异丙醇、氢氧化钠(NaOH)、乙醇,均为分析纯,天津科密欧化学试剂有限公司;聚乙二醇400(PEG400),分析纯,Alfa Aesar化学有限公司;高分子包覆材料,自制;纳米铝,平均粒径120nm(采用氧化还原滴定法[19]测得活性铝质量分数83.1%),阿拉丁试剂有限公司。
TGL-16GB型台式离心机,上海安亭科学仪器厂; KQ-250DE型超声波清洗机,昆山舒美超声仪器有限公司; Quanta400场发射环境扫描电子显微镜,美国FEI公司,测试时设定高压为30kV,电流为4A,工作距离为7.6mm; INCAIE350能谱仪,英国牛津公司; HITACHI H-7650B型透射电子显微镜,日本日立公司,操作电压为80kV,分辨率0.2nm (晶格像); D/MAX-3C型粉晶衍射仪,日本理学公司,X-射线源采用Cu Kα,波长0.15406nm,测角仪精度±0.02°,重现性±0.03°(2θ),强度综合稳定度±0.5%; 449C型TG-DSC 同步热分析仪,德国Netzsch 公司,载气为氩气, 流量为75mL/min, 升温速率为10K/min。
1.2 复合材料的制备
1.2.1 纳米CuO的制备
将10.09 g CuCl2·H2O、6g NaOH、12mL PEG400在研钵中充分混合研磨1h,产物加入1L去离子水,超声并搅拌2h,离心分离后加入1L乙醇超声2h,随后继续用去离子水及乙醇洗涤、离心数次,产物在100℃下干燥4h,充分研磨后在450℃下煅烧4h,得到黑色粉末。
1.2.2 包覆纳米CuO的制备
将1g纳米CuO在1L含0.1%(质量分数)包覆材料的异丙醇溶液中超声4h,离心分离,所得固体继续用异丙醇超声洗涤4~5次,产物在100℃下干燥2h。
1.2.3 纳米Al/CuO复合材料的制备
将400mg 纳米CuO与一定量的纳米Al在10mL异丙醇中超声3h,加入90mL异丙醇稀释后继续超声30min,离心分离,室温真空干燥5h。采用包覆纳米CuO制备的复合材料(Al与CuO摩尔比分别为1.0∶1.2、1.0∶1.5、1.0∶1.8)记为MIC-1、MIC-2、MIC-3,;采用未经包覆的纳米CuO制备的复合材料(Al/CuO摩尔比分别为1.0∶1.2、1.0∶1.5、1.0∶1.8)记为MIC-4、MIC-5、MIC-6。
2 结果与讨论
2.1 XRD表征
图1为纳米CuO及复合材料的XRD图谱。

图1 纳米CuO和纳米Al/CuO复合材料的XRD图谱Fig.1 XRD patterns of nano-CuO and nano Al/CuO composite
由图1可以看出,2θ为35.56°、38.69°、48.92°、53.49°、58.28°、61.67°、66.37°、67.97°处的衍射峰对应于标准卡片库中的单晶黑铜矿,并且几乎没有杂质,说明由铜盐经过水解、煅烧后所制备样品的化学组分为CuO。加入包覆材料及纳米Al制备成复合材料后,经XRD表征,除含有CuO的特征衍射峰之外,在2θ为38.51°、44.76°、65.13°、78.26°处出现Al的衍射峰(Al在38.51°处衍射峰与CuO在38.69°处衍射峰重叠),说明制备的材料为纳米Al及CuO的复合物。
2.2 SEM和TEM表征
图2和图3分别为纳米CuO和纳米Al/CuO复合材料(MIC-1)的SEM及TEM图。由图2可以看出,纳米CuO为球形颗粒,粒径约为40~50nm,说明制备过程中PEG400可以有效地控制纳米颗粒的生长粒径。纳米颗粒存在一定程度的团聚,通过材料包覆改性后,分散性有所提高。采用BET法测试其比表面积为20.53m2/g,计算平均粒径为45nm,与电镜所测得的粒径结果吻合。

图2 纳米CuO的SEM和TEM图Fig.2 SEM and TEM images of nano-CuO

图3 纳米Al/CuO复合材料的TEM图Fig.3 TEM images of nano Al/CuO composite
由图3可以看出,在TEM图中能够分辨出纳米Al/CuO复合材料中的两种组分。其中,纳米Al颗粒更大,呈规则的圆形,边缘清晰,比CuO衬度低;CuO粒径更小,存在一定程度的团聚并附着在纳米Al表面。
利用EDS能谱对自组装法和超声共混法制备的复合材料(MIC-1和MIC-4)进行表征,随机选取3个不同区域测定材料的元素组成。图4为MIC-1在扫描电镜下的EDS能谱图,元素含量分析结果见表1。从表1可以看出,自组装制备的纳米Al/CuO(MIC-1),3个区域的Al/Cu元素摩尔比接近,而超声共混法制备的MIC-4不同区域的Al/Cu元素摩尔比有较大差异。这说明自组装制备的复合材料中,由于包覆材料的配位作用,纳米Al与CuO在纳米尺度的复合更为均匀。

图4 纳米Al/CuO复合材料(MIC-1)的SEM和EDS图Fig.4 SEM and EDS images of nano Al/CuO composite (MIC-1)
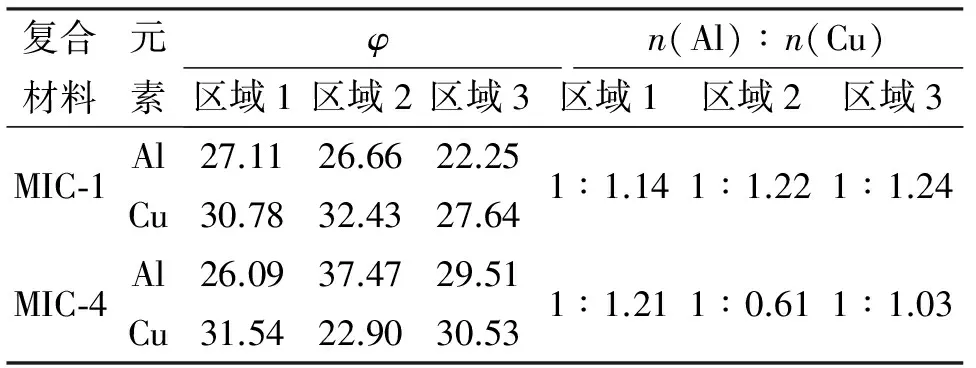
复合材料元素φn(Al)∶n(Cu)区域1区域2区域3区域1区域2区域3MIC⁃1Al27.1126.6622.251∶1.141∶1.221∶1.24Cu30.7832.4327.64MIC⁃4Al26.0937.4729.511∶1.211∶0.611∶1.03Cu31.5422.9030.53
注:φ为原子百分比。
2.3 纳米Al/CuO的热性能
在材料的制备过程中,纳米CuO在含有包覆材料的异丙醇溶液中进行超声包覆,为了表征CuO表面的包覆量,对材料进行热重分析,结果见图5。从图5可以看出,样品在320℃左右开始发生明显的失重,整个过程失重约4.65%,说明在包覆改性后的CuO中,包覆材料质量分数为4.65%。
图6为两种方法制备的纳米Al/CuO复合材料的DSC数据。由图6可以看出,MIC-1复合材料在323.6℃存在一个较小的放热峰,此为包覆材料的分解; 576.4℃左右发生铝热反应,出现较大的放热峰; 660.2℃有一个较小的吸热峰,此处为单质铝的熔化所引起的吸热,这说明前一步铝热反应并不彻底,仍有少量铝粉未发生反应; 1090.1℃的吸热峰与单质铜的熔点吻合,进一步证明了铝热反应的发生。

图5 包覆纳米CuO的热重分析曲线Fig.5 TGA curves of coated nano-CuO
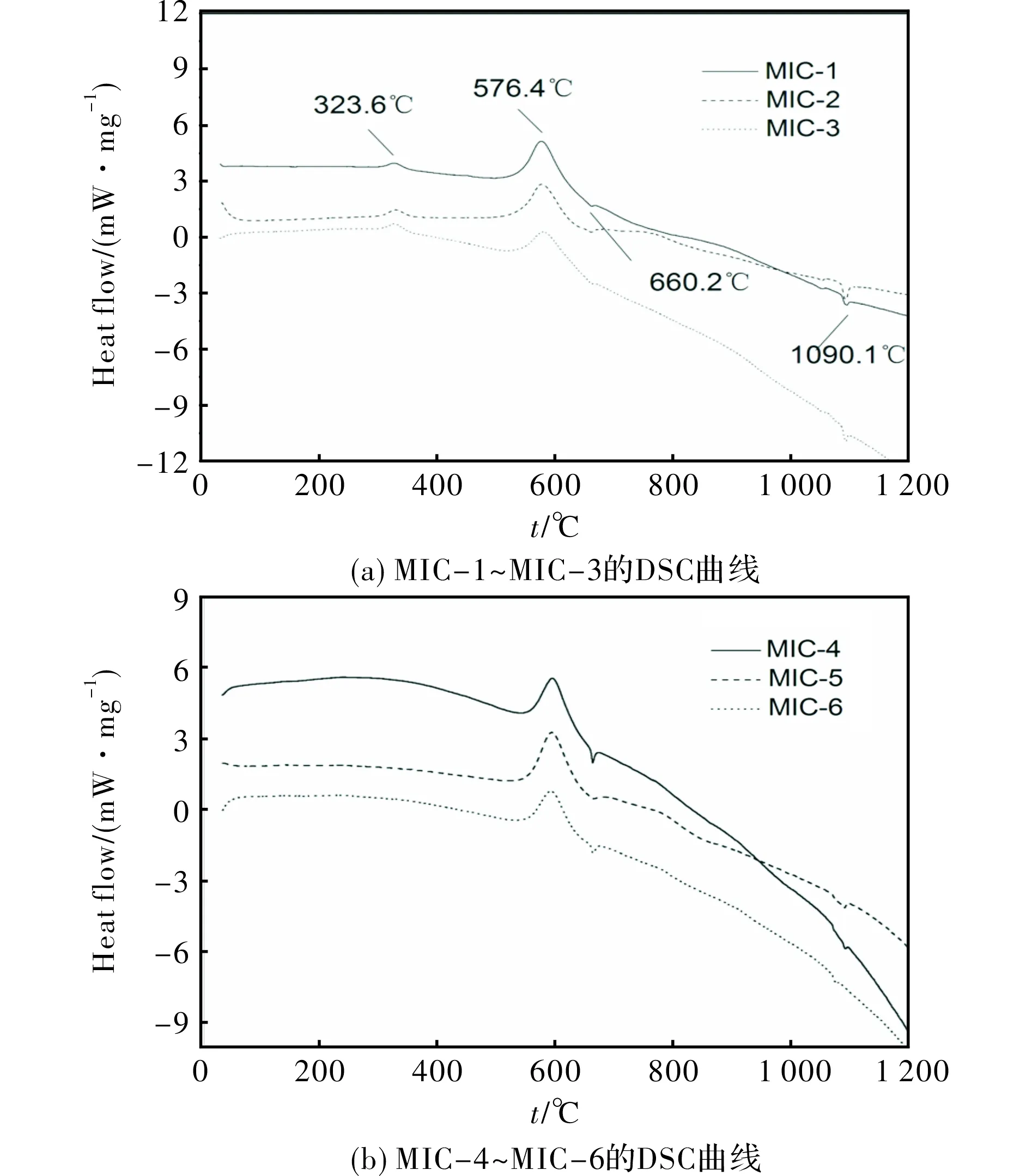
图6 纳米Al/CuO复合材料的DSC曲线Fig.6 DSC curves of nano Al/CuO composite
对比Al/CuO含量不同的样品,单位质量放热量随着CuO含量增加逐渐降低。Al与CuO发生铝热反应的化学计量比为1.0∶1.5,因此,当CuO过量时,多余的CuO不参与反应,降低体系的放热量。但从实际测试数据中,Al/CuO摩尔比为1.0∶1.2时放热量最大,而非满足化学计量比1.0∶1.5的条件。由于测试氛围为氩气,Al只能与CuO发生铝热反应而无法自身氧化放热,因此推测可能的原因是,在Al/CuO摩尔比为1.0∶1.5的条件下,虽然理论上与化学计量比吻合,但实际无法完全发生反应。在复合材料中,CuO的含量较大,过量的CuO势必会降低材料的单位质量放热量,而在Al/CuO摩尔比为1.0∶1.2时,铝粉适当过量,CuO反应更加完全,有助于提高材料的放热量。
图7为含包覆材料Al/CuO的热重分析曲线。
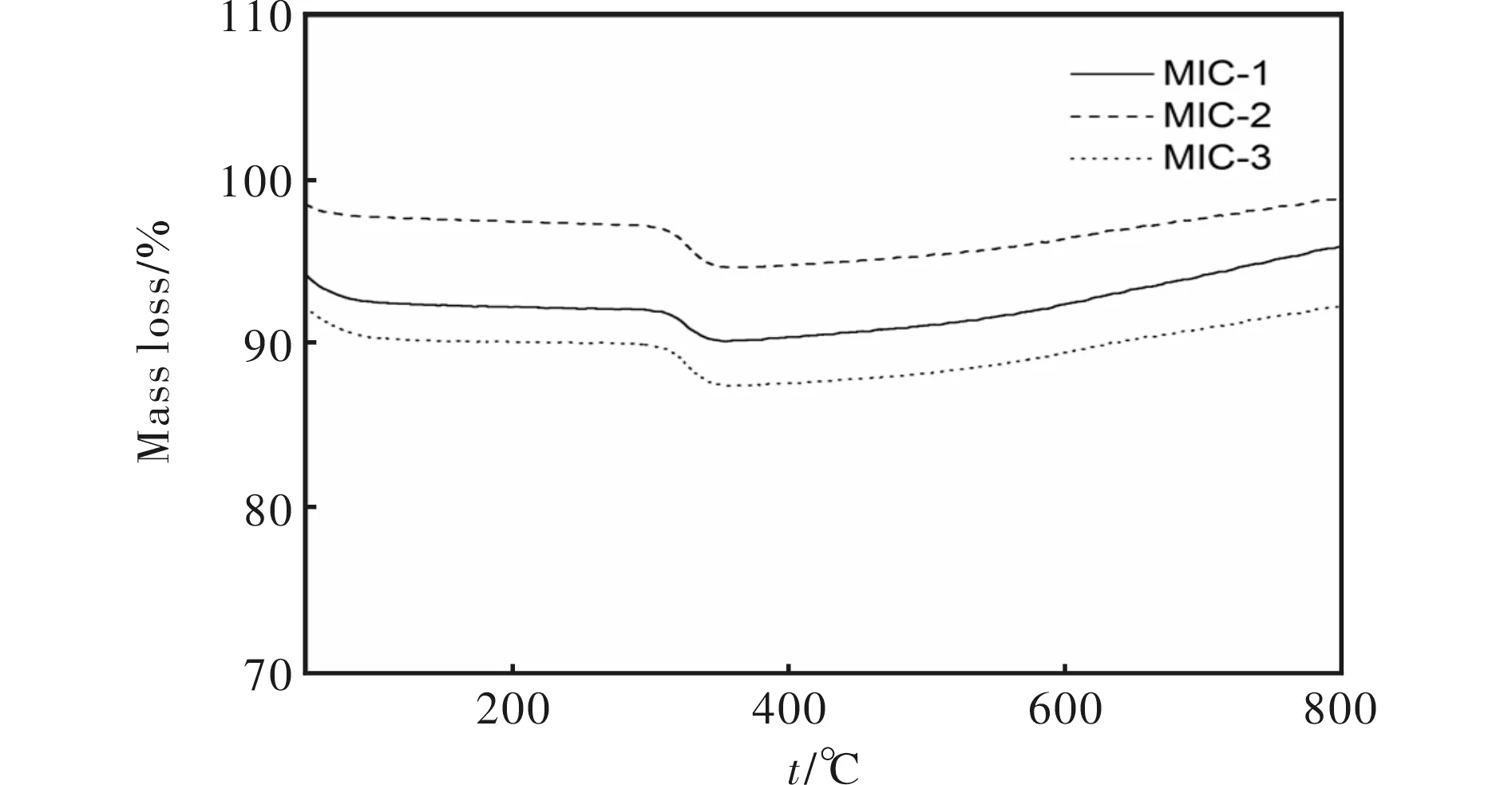
图7 包覆Al/CuO复合材料的热重分析曲线Fig.7 TGA curves of coated Al/CuO composite
从图7可以看出,复合材料在320℃左右发生失重,此处对应DSC曲线在323.6℃的放热峰,代表包覆材料的分解,通过失重数据可以计算出包覆材料在复合材料中的质量分数约为2%~3%。根据包覆材料在CuO中质量分数为4.65%进行计算,在Al/CuO摩尔比为1.0∶1.5时,复合材料中包覆材料的理论质量分数为2.7%,这说明在复合材料的制备过程中,包覆材料几乎没有损失,也间接证明了包覆材料具有较强的配位能力,适用于纳米粒子的包覆及自组装。
表2为两种方法制备的纳米Al/CuO复合材料的热性能数据。
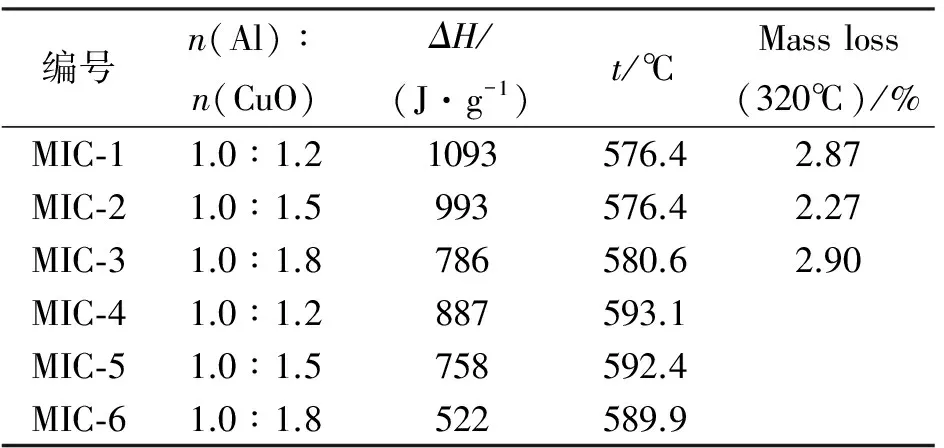
表2 纳米Al/CuO复合材料的热性能数据
从表2可以看出,在Al/CuO摩尔比相同的条件下,经过包覆进行自组装合成的复合材料(MIC-1~MIC-3)比直接超声复合的材料(MIC-4~MIC-6)具有更高的单位质量放热量,放热温度低10~15℃,这说明通过包覆材料自组装制备的复合材料,纳米Al与CuO的复合程度更高,组分在纳米尺度上具有更好的均匀性,更有利于铝热反应的传质和传热,降低反应温度,提高放热量。
3 结 论
(1) 以聚乙二醇为模板制备了纳米CuO,通过高分子包覆材料自组装制备了纳米Al/CuO复合材料。所制备的纳米CuO粒径小于50nm,经TEM及EDS表征,Al与CuO在纳米尺度上具有较好的复合,分布较为均匀。
(2) 在同样的制备条件下,含有包覆材料的纳米Al/CuO比不含包覆材料的Al/CuO具有更大的放热量,放热温度低10~15℃,这说明通过包覆材料的配位作用,可以提高Al与CuO在纳米尺度的复合程度,有利于铝热反应的传质传热。
(3) 复合材料中Al/CuO摩尔比为1.0∶1.2时放热量最大,可达1093J/g,表明在Al含量略大于化学反应计量比时更有助于提高铝热反应的完全程度。
[1] Valliappan S, Swiatkiewicz J, Puszynski J A. Reactivity of aluminum nanopowders with metal oxides [J]. Powder Technology, 2005, 156 (2/3):164-169.
[2] Dreizin E L.Metal-based reactive nanomaterials [J]. Progress in Energy and Combustion Science, 2009, 35 (2):141-167.
[3] Siegert B, Comet M, Muller O, et al. Reduced-sensitivity nanothermites containing manganese oxide filled carbon nanofibers [J]. Journal of Physical Chemistry, 2010, 114 (46): 19562-19568.
[4] 安亭, 赵凤起, 肖立柏.高反应活性纳米含能材料的研究进展[J].火炸药学报, 2010, 33 (3): 55-62. AN Ting, ZHAO Feng-qi, XIAO Li-bai. Progress of study on high activity nano-energetic materials [J]. Chinese Journal of Explosives & Propellants (Huozhayao Xuebao), 2010, 33(3): 55-62.
[5] 周超, 李国平, 罗运军. 纳米铝热剂的研究进展[J]. 化工新型材料, 2010,38(4): 4-7. ZHOU Chao, LI Guo-ping, LUO Yun-jun. Research progress on nano-thermite [J]. New Chemical Materials, 2010, 38(4): 4-7.
[6] Pantoya M L, Granier J J. Combustion behavior of highly energetic thermites: nano versus micron composites [J]. Propellants, Explosives, Pyrotechnics, 2005, 30(1): 53-62.
[7] Bhattaeharya S, Gao Y, Apperson S, et al. A novel on-chip diagnostic method to measure burn rates of energetic materials [J]. Journal of Energetic Materials, 2006, 24(1): 1-15.
[8] Granier J J, Pantoya M L. Laser ignition of nano composite thermites [J].Combustion and Flame, 2004, 138(4):37-383.
[9] Hrubesh L W. A shared award in aerogel process technology[J]. LLNL Science and Technology Review, 1995, 22-25.
[10] Parker A. Nanoscale chemistry yields better explosives [J]. LLNL Science and Technology Review, 2000(10): 19-21.
[11] Kim S H, Zachariah M R. Enhancing the rate of energy release from nanoenergetic materials by electrostatically enhanced assembly [J]. Advance Materials, 2004, 16(20): 1821-1825.
[12] Shende R, Subramanian S, Hasan S, et al. Nanoenergetic composites of CuO nanorods, nanowires, and Al-nanoparticles [J]. Propellants, Explosives, Pyrotechnics, 2008, 33(2): 122-130.
[13] Severac F, Alphonse P, Esteve A, et al. High-energy Al/CuO nanocomposites obtained by DNA-directed assembly[J]. Advanced Functional Materials, 2012, 22 (2): 323-329.
[14] 安亭,赵凤起,马海霞,等. 氧化锰纳米管及其超级铝热剂:制备及对环三亚甲基三硝胺热分解的影响[J]. 无机化学学报,2015,31(1): 97-102. AN Ting, ZHAO Feng-qi, MA Hai-xia, et al. MnO2Nanotube and its super thermite: preparation and their effect on thermal decomposition of cyclotrimethylene trinitramine [J]. Chinese Journal of Inorganic Chemistry, 2015, 31(1): 97-102.
[15] 赵宁宁,贺翠翠,刘健冰,等. 超级铝热剂Al/MNO2的制备、表征及其与推进剂组分的相容性[J]. 火炸药学报, 2012, 35 (6): 32-36. ZHAO Ning-ning, HE Cui-cui, LIU Jian-bing, et al. Preparation and characterization of superthermite Al/MnO2and its compatibilities with the propellant componets [J]. Chinese Journal of Explosives and Propellants (Huozhayao Xuebao), 2012, 35 (6): 32-36.
[16] Li Rui, Xu Hong-mei, Hu Hai-long, et al. Microstructured Al/Fe2O3/nitrocellulose energetic fibers realized by electrospinning [J]. Journal of Energetic Materials, 2014, 32(1): 50-59.
[17] Yang Y, Zhang Z C, Wang P P, et al. Hierarchical MnO2/SnO2heterostructures for a novel free-standing ternary thermite membrane [J]. Inorganic Chemistry, 2013, 52 (16): 9449-9455.
[18] Rossi C, Zhang K, Estève D, et al. Nanoenergetic materials for MEMS: a review [J]. Journal of Microelectromechanical Systems, 2007, 16(4):919-931.
[19] Fedotova T D, Glotov O G, Zarko V E. Application of cerimetric methods for determining the metallic aluminum content in ultrafine aluminum powders [J]. Propellants, Explosives, Pyrotechnics, 2007, 32(2): 160-164.
Preparation and Thermal Properties of Nano-Al/CuO Composite
DONG Xiao-hu1,2, HU Lan1,2, WANG Ying-lei1,2, SHU Yuan-jie1,2, YAN Rui1,2, WU Min-jie1,2
(1.State Key Laboratory of Fluorine & Nitrogen Chemicals, Xi′an 710065, China; 2.Xi′an Modern Chemistry Research Institute, Xi′an 710065, China)
Nano-CuO was prepared using polyethylene glycol (PEG) as template. Nano-Al/CuO composite was prepared by self-assembling using a kind of polymer as coating material. The structure and morphology of the composite were characterized by scanning electron microscopy (SEM), transmission electron microscopy (TEM), energy dispersive spectrometer (EDS), X-ray diffraction (XRD), etc. The thermal properties of samples prepared by self-assembling method (with coating materials) and ultrasonic blending method (without coating materials) were studied and compared by thermogravimetry (TG) and differential scanning calorimetry (DSC). Exothermic quantity of the composite with different Al-CuO molar ratio was investigated. Results show that the exothermic peak occurring the thermite reaction of nano-Al and CuO is at about 576.4℃ and the exothermic quantity is 1093J/g. The composite with coating material has a higher exothermic quantity than that without coating material. The exothermic quantity of the thermite reaction is a maximum, reaching 1093 J/g when the molar ratio of Al and CuO is 1.0∶1.2.
nano thermite; nano-Al/CuO; thermal properties; polyethylene glycol (PEG); ultrasonic blending method
10.14077/j.issn.1007-7812.2016.06.007
2016-04-06;
2016-06-20
总装备部高能毁伤科研专项(No.004010201-1)
董小虎(1986-),男,博士,高级工程师,从事火炸药理化性能研究。E-mail:bobo_hu1986@163.com
胡岚(1968-),女,硕士,研究员,从事火炸药理化性能研究。E-mail:hulan204@126.com
TJ55;O614
A
1007-7812(2016)06-0044-05
