玉米芯发酵乙醇残余物中木素酸化分离过程的研究
2016-12-28王高升夏蕊蕊
王 霞,王高升,肖 林,夏蕊蕊
(1. 天津市制浆造纸重点实验室,天津科技大学造纸学院,天津 300457;2. 山东省秸秆生物炼制技术重点实验室,山东龙力生物科技股份有限公司,德州 251200)
玉米芯发酵乙醇残余物中木素酸化分离过程的研究
王 霞1,王高升1,肖 林2,夏蕊蕊2
(1. 天津市制浆造纸重点实验室,天津科技大学造纸学院,天津 300457;2. 山东省秸秆生物炼制技术重点实验室,山东龙力生物科技股份有限公司,德州 251200)
为了提高纤维素乙醇生产的经济效益,最大限度地利用发酵残余物,木素的分离利用是十分重要的.以玉米芯发酵乙醇残余物为原料,采用碱溶-酸沉淀的方法分离木素,讨论酸沉淀过程pH、温度对木素得率的影响,并且对木素酸化过程中Zeta电位、粒径大小及分布、聚集体形态进行分析.从木素得率和分离操作性综合考虑,pH为3左右,酸化温度65,℃时,从玉米芯发酵乙醇残余物中分离木素将会取得较好的效果.
玉米芯;发酵乙醇残余物;木素;分离;酸化
近年来,随着经济的快速发展,世界能源需求量大幅增加,面对煤炭、石油等矿物资源日益枯竭以及环境污染日渐严重等问题,绿色替代能源的开发成为国内外亟待解决的问题之一,以燃料乙醇为代表的生物燃料能源以其环保、可再生的特点引起人们的广泛关注,得到迅速发展.虽然,以甘蔗、玉米为原料的第一代燃料乙醇产业已形成规模,但是存在“与人争粮、与粮争地”的问题.同时,由于国家出台相关政策不再批准新建粮食乙醇项目,鼓励积极发展以纤维素生物质为原料的生物液体燃料技术,因而纤维素乙醇越来越引人注目,成为业界研发的一个重要方向[1].
纤维素乙醇生产工艺主要包括预处理、酶解和发酵等关键步骤[2].以玉米芯纤维素乙醇生产为例,玉米芯原料研磨后首先进入预处理反应器,经稀酸预水解后,绝大部分半纤维素转化为木糖、低聚木糖等,木糖渣再经碱预处理后进入同步糖化发酵塔,产生粗乙醇,同时,从塔底得到发酵乙醇残余物.最后,粗乙醇经蒸馏脱水得到燃料级乙醇.
在玉米芯纤维素乙醇生产过程中面临两方面的困难:一是纤维素酶成本较高,二是约占原料30%,的发酵残余物的处理与利用问题[3].通常,发酵残余物被当作废料堆积或直接烧掉,造成了资源的大量浪费,且污染环境.有相关研究数据显示,发酵残余物中含有大量的未酶解的纤维素、木素、半纤维素及其他物质[4].因此可以充分分离、利用发酵残余物中木素、纤维素组分,从而实现乙醇-高附加值产品联产,这样不仅为企业解决了大量残余物浪费的问题,而且增加了纤维素乙醇生产的经济效益.对此,国内外学者对发酵乙醇残余物中的木素与纤维素的分离、利用进行了一些探究.Oksman等[5]从发酵乙醇残余物中分离纤维素制备纳米纤维素晶须,Song等[6]研究了纳纤化纤维素(NFC)和葡萄糖的联产技术,刘晓玲等[7]以玉米秸秆制备纤维素乙醇的残余物为原料,采用碱性水溶液萃取法和有机溶剂萃取法从中分离得到木质素,并对其结构进行了研究,结果表明所得木素分子质量较小,木素分子上各种活性基团得到较好地保留.甦程贤等[8]研究发现采用上述两种方法分离出的木素可溶解于1,4-丁二醇、苯酚和碱性水溶液,但不溶于水,红外光谱与磨木木质素相似,具有较高的化学活性,能够直接与醛、环氧氯丙烷或异氰酸酯等反应,形成木素的改性衍生物.Cotana等[9]研究了自发酵残余物中分离的木素应用于热塑性高分子材料的潜力.
本文采用碱溶和酸沉淀结合的方法,对玉米芯发酵乙醇残余物中的木素进行分离.该方法操作简便、成本低、作用条件温和,同时不损伤残余物中的纤维物质,便于进一步开发利用,如制备纳米纤维素等.本文主要研究酸化过程中pH和温度对木素沉淀的影响,同时研究了酸化过程中Zeta电位、粒径及粒径分布的变化,并对木素在水溶液中聚集状态进行了探讨,以期为木素进一步开发利用提供依据.
1 材料与方法
1.1 材料
玉米芯发酵乙醇残余物由山东龙力生物科技股份有限公司提供,干度约45%,,自然风干,粉碎后待用.实验中所使用的氢氧化钠、硫酸等均为分析纯化学试剂.
1.2 木素的分离方法
实验所采用的木素分离工艺技术路线如图1所示.称取玉米芯发酵乙醇残余物100,g(绝干),放入三口烧瓶中,固液比1∶6(g:mL),氢氧化钠用量8%,(相对绝干原料),在温度80,℃下反应1.5,h,然后离心分离,转速3,500,r/min,时间10,min,收集上层离心液备用,固体部分洗涤至中性.取100,mL碱溶出液放入250,mL烧杯中,边搅拌边加入2,mol/L的硫酸溶液,在规定温度下轻轻搅拌5,min,之后用定性滤纸抽滤,用蒸馏水洗涤至中性,在(55±5)℃下真空干燥.

图1 木素分离工艺流程Fig. 1Separation flowsheet of lignin from the residues of corncob bioethanol production
1.3 分析方法
1.3.1 原料成分分析
玉米芯发酵乙醇残余物中纤维素、聚戊糖、木素、灰分的分析参见文献[10],蛋白质含量测定采用凯式定氮法.
1.3.2 碱溶出液中木素浓度的测定
碱溶出液中木素浓度采用紫外吸收光谱法测定,吸收波长为225,nm,具体方法参见文献[11].
1.3.3 Zeta电位分析
Zeta电位采用美国布鲁克海文(Brokhaven)公司的Zeta 90,Plus Zeta型电位及粒度分析仪,在常温下进行测量.
1.3.4 粒径及粒径分布分析
采用美国贝克曼库尔特有限公司的LS13320型激光衍射粒度分析仪测量木素在酸化过程中平均粒径及粒径分布,激光衍射粒度分析仪的检测范围是0.4~2,000,µm.测量之前将溶液摇匀,按照仪器要求加入所需量的样品(要求颗粒散射光百分比为8%,~12%,),平行测量2次,取平均值,粒径以体积平均粒径D(4,3)表示.
1.3.5 木素形态分析
采用日本奥林巴斯(OLYMPUS)CX41型光学显微镜对木素聚集形态进行观察并拍摄记录.
1.4 木素得率与耗酸量的计算
木素得率与耗酸量的数值分别按照式(1)、式(2)进行计算.


式中:X1为木素得率;m1为酸沉淀分离后木素质量,g;m为碱溶出液中木素质量,g;X2为耗酸量;m2为质量分数98%,的硫酸用量,g.
2 结果与讨论
2.1 玉米芯发酵乙醇残余物的化学成分
玉米芯是一种富含半纤维素的农业废弃物,是当前生产木糖、木糖醇和糠醛等产品的主要原材料,玉米芯的主要化学成分及含量分别是:纤维素32%,~36%,、半纤维素35%,~40%,、木素17%,~20%,、灰分1.2%,~1.8%,[12].本文所用的原料是玉米芯联产功能糖和燃料乙醇后的残余物,玉米芯中的半纤维素先经过稀酸水解生产低聚木糖、木糖和木糖醇等功能糖,产生的木糖渣中纤维素含量可高达50%,~60%,,经过预处理、糖化发酵等过程生产燃料乙醇[13],最终残余物的主要化学组成见表1.
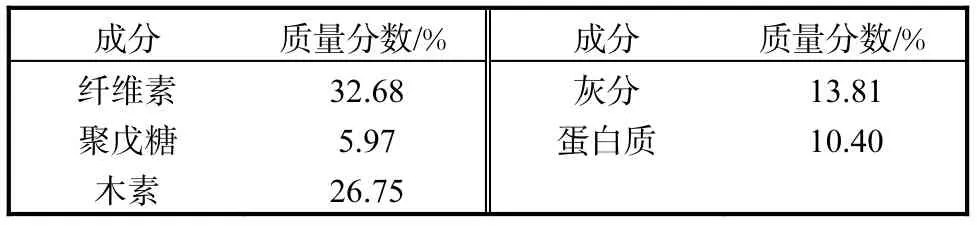
表1 玉米芯发酵乙醇残余物主要化学成分Tab. 1 Chemical composition of the bio-residue from corncob bioethanol production
与玉米芯原料比较,半纤维素(以聚戊糖为代表)的含量大大降低,木素含量增加,而纤维素含量变化不大.由于在前面的加工过程中,添加了酸、碱等化学物质,以及酶、酵母,导致了灰分和蛋白质含量的增加.当然,由于酸、碱、酶和微生物等作用,残留的纤维素、木素等物质的物理和化学结构及性质也发生了变化.
为了将玉米芯发酵乙醇残余物中的木素分离,在碱性条件下将其中的木素溶解,成为碱木素,利用其不溶于酸性溶液的特性,用硫酸将木素沉淀分离.
2.2 酸化时的pH对木素分离的影响
对玉米芯发酵乙醇残余物进行碱处理后,得到以碱木素为主的液体部分和以纤维素为主的固体部分.液体部分的初始pH在11.21左右,木素质量分数为4.23%,.用硫酸调节溶出液的pH,在酸化温度为65,℃时,pH对木素得率的影响如图2所示.
总体来看,随着pH降低,木素得率升高.当pH在8附近时,开始有木素沉淀产生,当pH接近6时,木素得率大幅度增加.当pH为6.27时,木素得率为4.67%,,而当pH进一步降为5.28,木素得率快速升到75.02%,,此后随着pH降低,木素得率缓慢升高,当pH为3时,木素得率达到85.02%,.

图2 pH对木素得率和耗酸量的影响Fig. 2Effect of pH values on the yield of lignin and consumption of sulfuric acid
随着pH降低,消耗的硫酸量逐渐增加,当pH大于8时,虽然硫酸消耗量在增加,但几乎没有木素沉淀,当pH从6.27降到5.28,虽然硫酸消耗量变化不大,但木素得率大幅度提高,pH低于3后继续降低pH,硫酸消耗量快速增加,但木素得率变化不大,此时经济性差.因此,pH为3左右作为酸沉淀终点是较好的选择.
2.3 酸化温度对木素分离的影响
在酸化过程中,温度对分离木素的得率有较大的影响.不同酸化温度下木素得率变化情况如图3所示.可以发现,在所研究的25~70,℃范围内,随着酸化温度升高,木素得率呈现先上升后下降的趋势,在50,℃时达到最大值,此后缓慢下降.
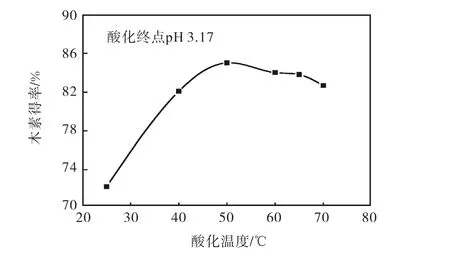
图3 不同酸化温度下木素的得率Fig. 3 Yield of lignin at different acidification temperature
从木素生产的操作性来讲,是否容易脱水分离是一个关键因素.在酸化温度较低时(如50,℃),木素的得率虽然较高,但是难以脱水过滤,并且不易干燥;而酸化温度60,℃以上时,得到的木素易过滤和干燥.这是因为随着pH降低,碱木素首先以胶体形式分散在溶液中,只有当体系含有过多的胶粒而无法稳定后,木素才沉淀出来.当温度较低时,该胶体体系稳定性较高,易于生成凝胶,故木素得率升高,但滤水困难;当温度提高以后,分子热运动加剧,粒子之间碰撞几率增加,不利于凝胶结构的形成,而容易发生聚沉,因此加热酸化有利于沉淀絮聚,易于澄清过滤.当温度为65,℃时,木素容易聚沉析出并出现明显分层,虽然得率稍低于50,℃时的得率,但得到的木素易过滤和干燥,因此选用65,℃作为酸化温度较为合适.
2.4 在酸化过程中木素Zeta电位的变化
为探求木素在酸化过程中的稳定性与所带电荷的关系,研究在酸化过程中,随着pH的降低,溶出物中木素聚集体Zeta电位的变化,结果如图4所示.

图4 不同pH下木素聚集体Zeta电位的变化Fig. 4 Changes of Zeta potential of lignin aggregates at different pH value
由图4可见,碱处理后的溶出物木素聚集体带负电,Zeta电位大小为-64.54,mV,这是因为木素与NaOH反应过程中,木素分子含有的—COOH、—OH等基团电离生成—COO-、—O-,使得木素粒子带负电荷[13].在pH由11.21减少到8.18的过程中,Zeta电位变化较小,从-64.54,mV升到-61.58,mV,此时,木素分子上的—OH、—COOH离子化程度高,表面分布着密集的负电荷,彼此之间存在较强的静电斥力,因此,木素及其聚集体在溶液中能够相对稳定的存在[14-15].继续加入硫酸,木素胶粒的Zeta电位开始缓慢升高,表面负电荷缓慢减少,静电斥力减弱,导致体系中木素有聚沉析出的趋势.当pH低于6时,Zeta电位开始急剧升高,表明体系中胶粒带电量剧烈下降.从斯特恩扩散双电层模型可知:反离子H+的加入,压缩扩散层使其变薄,更多的H+挤进滑动面以内,与—COO-、—O-等阴离子电中和,造成滑动面与溶液本体之间的电势差减小,表现为Zeta电位数值减小,此时,木素脱稳且逐步聚集.在pH为4左右出现等电点,此时Zeta电位趋近于0,继续增加酸用量,Zeta电位没有明显的变化.在等电点附近时,由于木素之间斥力几乎消失,体系产生大量絮体沉淀,此时木素得率最高.
2.5 在酸化过程中粒径及粒径分布的变化
从2.4节的分析可知,在酸化过程中,木素聚集体的Zeta电位发生明显的变化,随着pH的降低,Zeta电位逐渐升高,最后趋近于0,Zeta电位对胶体体系的稳定性有很大的影响.本节研究在酸化过程中木素在水溶液中的粒径及其分布的变化,结果如图5、6所示.

图5 木素在不同酸化温度下平均粒径随pH的变化Fig. 5Size of lignin aggregates with various pH values at different acidification temperature
由图5可知:酸化温度无论是25,℃还是65,℃,沉淀木素的平均粒径大小随着pH变化趋势相似,在pH低于6后,随着pH的降低,木素粒径快速增长,由几微米上升到几十微米;而pH高于6时,木素粒径相对来说变化不大,只是65,℃时的粒径稍高于25,℃时的粒径.与图4对比可以发现,木素粒径随着pH的变化趋势和木素Zeta电位随着pH的变化趋势非常相似,说明木素的聚沉和木素颗粒表面的Zeta电位关系密切.随着硫酸的加入,木素分子上的—O-、—COO-等阴离子逐渐被中和,木素颗粒表面电荷逐渐降低,粒子之间的静电斥力减小,使木素不断聚集变大.
图6是在酸化温度分别为25,℃和65,℃时,不同pH下木素聚集体的粒径分布.当pH在10附近时,粒径分布出现2个或3个峰值,说明开始加入硫酸,木素溶出物体系就有颗粒形成,粒径分布范围从最低检测值到几微米.继续加入硫酸,在pH为8左右时,粒径分布范围继续增宽,从最低检测值到几十微米,说明此时木素在不断的聚集,由小变大.当pH在5左右时,小于1,µm的木素颗粒几乎消失,最大粒径也超过了100,µm,平均粒径在35,µm左右;pH继续降低到3左右时,木素颗粒继续增大,平均粒径超过了50,µm.这说明在酸化过程中,木素由溶解状态不断聚集,先形成小颗粒,随着pH下降,小颗粒不断聚集变大,在一定条件下沉淀析出.
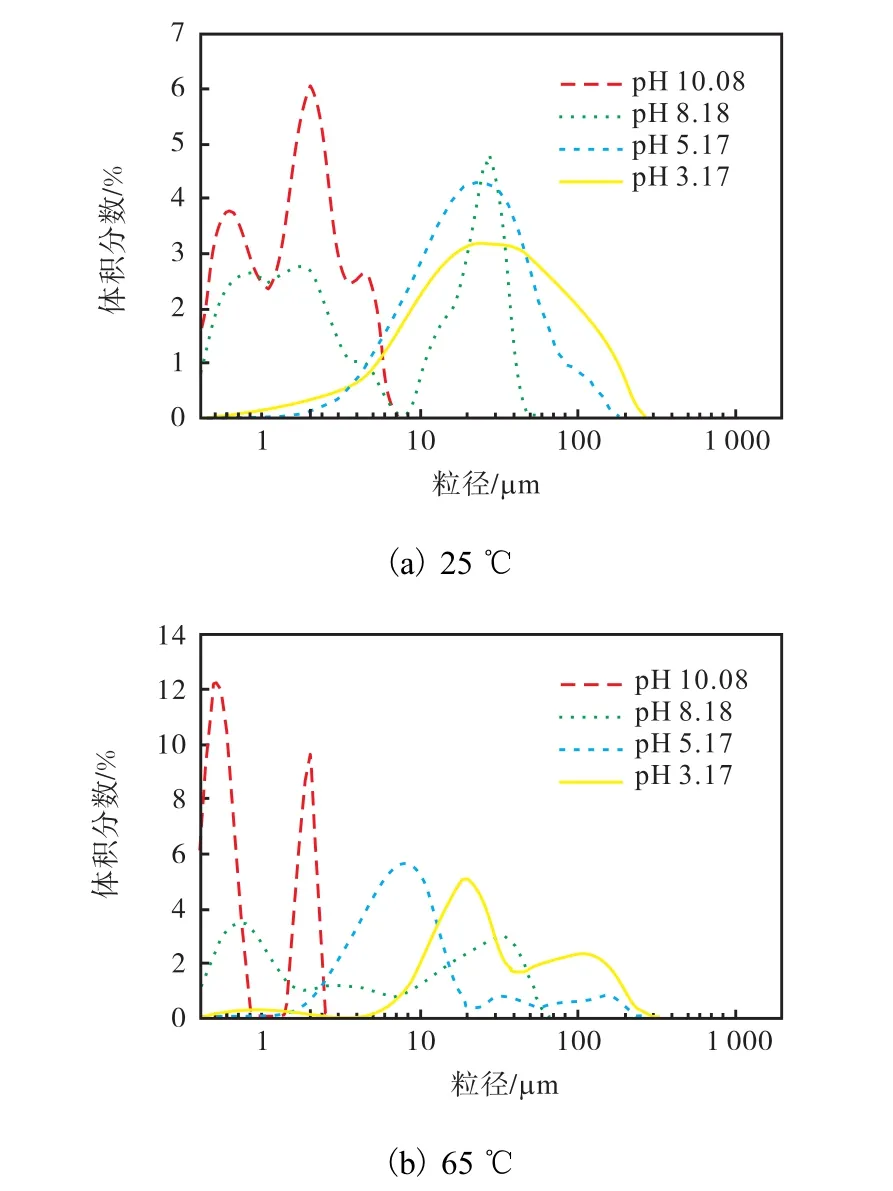
图6 木素在不同酸化温度下粒径分布随pH的变化Fig. 6 Size distribution of lignin aggregates with various pH values at different acidification temperature
2.6 酸化温度对木素聚集体形态的影响
为了进一步了解在酸化过程中木素的形态,利用光学显微镜观察了不同pH和温度下木素聚集体的形态,结果如图7所示.可以发现:相同放大倍数下,在酸化温度为25,℃、pH为8.18时,大的木素聚集体呈花瓣状,周围散布着粒状小聚集体,当pH降为5.17和3.17时,木素聚集体主要呈棒状,且不同聚集体相互连接.而当酸化温度为65,℃时,木素聚集体形态发生变化,呈不规则的块状,并且随着pH降低,大的颗粒数目不断增加.
对pH为11.21的木素溶出液进行观察时,视野中看不到聚集体存在,这或许是因为此时木素以溶解的大分子的形式存在于溶液中[16].硫酸的加入引起木素胶体粒子的形成,在低温下,以胶体分散状态析出的粒子既不沉降,也不能自由行动,而是形成棒状结构,以此为骨架,在整个溶液中连接成连续的网状结构,形成凝胶.以范德华力形成的凝胶骨架,其结构稳定性差,在外力作用下容易被破坏,但放置后又可以恢复,表现出触变特性.随着温度的升高,分子热运动加剧,不利于形成网络结构,而倾向于无序聚集,形成块状颗粒,从分散介质中沉降下来.在酸化温度较低时,由于木素凝胶的形成,使得木素聚集体脱水困难,当温度大于60,℃时,木素聚集体形态发生改变,不容易形成凝胶结构,易于聚沉析出、脱水干燥.

图7 不同酸化温度和pH下木素聚集体形态Fig. 7Optical microscopy images of lignin aggregates with different pH values at different acidification temperature
3 结 论
对于玉米芯发酵乙醇残余物,通过碱溶解和硫酸沉淀相结合的方法能够实现木素的分离,其中酸化时的pH和温度是影响木素分离的重要因素.在酸化过程中,随着pH降低,木素得率、粒径和Zeta电位均随之增加,当pH小于6时,木素得率迅速上升、粒径也大幅增长、Zeta电位趋向于零,在pH为4左右出现等电点,此后,木素得率变化变缓,但粒径继续增大.温度对酸化时木素聚集体的形态有显著影响,当酸化温度低时(如25,℃),木素聚集体成花瓣状或棒状,易形成凝胶,导致后续脱水和干燥困难;当酸化温度高时(如65,℃),木素聚集体成不规则块状,此时脱水和干燥容易.从木素得率和分离操作性综合考虑,pH为3左右,酸化温度65,℃时,由玉米芯发酵乙醇残余物分离木素将会取得较好的效果.
[1] 国家能源局. 可再生能源发展“十二五”规划[R]. 北京:国家能源局,2012.
[2] Poursorkhabi V,Misra M,Mohanty A K. Extraction of lignin from a coproduct of the cellulosic ethanol industry and its thermal characterization[J]. BioResources,2013,8(4):5083-5101.
[3] Guo G,Li S,Wang L,et al. Separation and characterization of lignin from bio-ethanol production residue[J]. Bioresource Technology,2013,135:738-741.
[4] 王闻,庄新姝,袁振宏,等. 纤维素燃料乙醇产业发展现状与展望[J]. 林产化学与工业,2014,22(4):144-150.
[5] Oksman K,Etang J A,Mathew A P,et al. Cellulose nanowhiskers separated from a bio-residue from wood bioethanol production[J]. Biomass and Bioenergy,2011,35(1):146-152.
[6] Song Q,Winter W T,Bujanovic B M,et al. Nanofibrillated cellulose(NFC):A high-value co-product that improves the economics of cellulosic ethanol production [J]. Energies,2014,7(2):607-618.
[7] 刘晓玲,甦程贤. 酶解木质素的分离与结构研究[J].纤维素科学与技术,2007,15(3):41-46.
[8] 甦程贤,刘晓玲. 玉米秸秆发酵残渣中木质素的分离与性质研究[J]. 现代化工,2006,26(增刊2):99-100.
[9] Cotana F,Cavalaglio G,Nicolini A,et al. Lignin as coproduct of second generation bioethanol production from ligno-cellulosic biomass[J]. Energy Procedia,2014,45:52-60.
[10] 李洲,王高升,王霞,等. 亚硫酸氢盐在SPORL法预处理稻草中的作用[J]. 中国造纸学报,2014,29(4):1-6.
[11] Lee R A,Bédard C,Berberi V,et al. UV-Vis as quantification tool for solubilized lignin following a single-shot steam process[J]. Bioresource Technology,2013,144:658-663.
[12] 赵建,曲音波. 木质纤维素资源生物精炼技术研究进展[J]. 生命科学,2014,26(5):489-496.
[13] 罗才典,陈祖恬,陈仁悦. 麦草硫酸盐法制浆黑液中木素酸化沉降机理初探[J]. 中国造纸学报,1990,5(1):33-42.
[14] Jiang C,He H,Jiang H,et al. Nano-lignin filled natural rubber composites:Preparation and characterization[J]. Express Polymer Letters,2013,7(5):480-493.
[15] Moreva Y L,Alekseeva N S,Chernoberezhskii Y M. Histograms of the size distribution of kraft lignin particles in aqueous solutions at various pH values[J]. Russian Journal of Applied Chemistry,2010,83(7):1281-1283.
[16] Norgren M,Edlund H,Wagberg L. Aggregation of lignin derivatives under alkaline conditions. Kinetics and aggregate structure[J]. Langmuir,2002,18(7):2859-2865.
责任编辑:周建军
Lignin Separation from Residues of Corncob Bioethanol Production
WANG Xia1,WANG Gaosheng1,XIAO Lin2,XIA Ruirui2
(1.Tianjin Key Laboratory of Pulp and Paper,College of Papermaking Science and Technology,Tianjin University of Science & Technology,Tianjin 300457,China;2.Shandong Key Laboratory of Straw Biorefinement Technologies,Shandong Longlive Bio-technology Co.,Ltd.,Dezhou 251200,China)
To improve the economic viability of the cellulosic ethanol production,it is of great importance to add value to residues of bioethanol production.In this research,lignin was separated from the fermentation residues of the corncob ethanol production with a solid-liquid extraction method using alkali solution and then precipitated by sulfuric acid.The yields of lignin and zeta potential change through the acidification process were reported,and the morphology and size distribution of lignin aggregates were investigated.While taking the lignin yield and practicability into consideration,pH about 3.0 and temperature 65,℃ are the most suitable acidification conditions for lignin separation.
corncob;fermentation residues of bioethanol production;lignin;separation;acidification
O636.2
A
1672-6510(2016)06-0044-06
10.13364/j.issn.1672-6510.20150201
2015-11-11;
2016-02-22
国家高技术研究发展计划(863计划)资助项目(2014AA021903);天津市高等学校科技发展基金资助项目(20080522)
王 霞(1990—),女,山东日照人,硕士研究生;
王高升,教授,gswang@tust.edu.cn.
