反相高效液相色谱法测定大鼠血浆中奥沙利铂的质量浓度
2016-12-26张志清杨秀岭
刘 剑,张志清,杨秀岭
(河北医科大学第二医院,河北 石家庄 050000)
反相高效液相色谱法测定大鼠血浆中奥沙利铂的质量浓度
刘 剑,张志清,杨秀岭
(河北医科大学第二医院,河北 石家庄 050000)
目的 建立测定大鼠血浆中奥沙利铂质量浓度的反相高效液相色谱(RP-HPLC)法。方法 色谱柱为DiamonsilTMC18柱(250 mm× 4.6 mm,5 m),流动相为乙腈-水(7∶93),检测波长为210 nm,流速为0.8m L/min,柱温为30℃,进样量为20 L。结果 奥沙利铂保留时间为8.51min,标准曲线方程为 Y=8 035.7X-11 791(r=0.999 5),线性范围为2.0~160.0 g/mL。低、中、高3个质量浓度奥沙利铂血浆样品的方法回收率分别为(112.7±3.61)%,(102.8±3.33)%,(101.6±4.60)%,RSD分别为3.20%,3.24%,4.53%;低、中、高3个质量浓度奥沙利铂血浆样品的提取回收率分别为(79.84±2.01)%,(82.29±3.28)%,(84.89±3.35)%,RSD分别为2.51%,3.98%,3.95%。血浆样品在-40℃反复冻融3次后性质稳定,对测定无影响。测定10只大鼠血浆样品中奥沙利铂的平均质量浓度为(67.4±10.45) g/m L。结论 该方法准确、简便、灵敏度高、重复性好,可为大鼠血浆中奥沙利铂的质量浓度测定提供方法学参考。
反相高效液相色谱法;大鼠;血浆;奥沙利铂;血药浓度
奥沙利铂(L-OHP)为第3代铂类抗癌药物,毒性较低,安全性良好,是大肠癌的有效抗肿瘤药物,美国食品药物管理局(FDA)于2004年1月批准了奥沙利铂联合方案作为晚期结直肠癌的一线方案[1]。此外,奥沙利铂对卵巢癌、非小细胞肺癌、淋巴瘤、头颈部肿瘤等也有客观疗效[2]。关于奥沙利铂主药含量测定及杂质和其他成分测定已有相关报道[3-7],新剂型脂质体中含量测定也有部分研究[8-9],但未见大鼠体内奥沙利铂质量浓度测定方法的研究。为此,本研究中采用反相高效液相色谱-紫外检测法(RP-HPLC-UV)测定大鼠血浆样品中奥沙利铂的药物浓度,并探索和改进方法,为今后研究提供方法学参考。
1 仪器、试药与动物
Waters高效液相色谱仪,包括Waters-515型高压泵、7725i型进样阀(Rhedyne)、Waters-486型紫外检测器、Empower Application型操作平台(美国 Waters公司);CPA2250型电子天平(Sartorius);MDF-U2086S型低温冰箱(日本三洋);XW-80A型涡旋混合器(上海精科实业有限公司);D37520型高速离心机(美国雅培);AP-01P型抽滤泵(天津市协同仪器有限公司);KQ-300B型超声波清洗器(昆山市超声仪器有限公司)。注射用奥沙利铂(江苏恒瑞医药股份有限公司,批号为13011311);奥沙利铂对照品(江苏恒瑞医药股份有限公司,批号为619111204,纯度99.8%);帕洛诺司琼(欧赛,齐鲁制药<海南>有限公司,批号为B1G1206005);乙腈为色谱纯,高氯酸溶液为分析纯,蒸馏水。健康W istar大鼠,清洁级,雄性,体重(170±10)g,均由河北省实验动物中心提供,许可证号为SCXK(冀)2008-1-003。
2 方法与结果
2.1 色谱条件
色谱柱:DiamonsilTMC18柱(250 mm×4.6 mm,5μm);流动相:乙腈-水(7∶93);检测波长:210 nm;流速:0.8mL/min;柱温:30℃;进样量:20μL。
2.2 溶液制备
精密称取奥沙利铂对照品200.0mg,置100m L容量瓶中,加水至刻度并摇匀,得质量浓度为2 000.0μg/mL的奥沙利铂贮备液;分别精密量取奥沙利铂贮备液适量,制成质量浓度为 1 600.0,1 000.0,800.0,500.0,200.0,100.0,50.0,20.0μg/mL的系列对照品溶液。
2.3 血浆样品处理
空白血浆制备:大鼠眼眶取血,将所取空白血置涂有肝素的离心管中,离心2 min(10 000 r/min),吸取上清液,即得空白血浆,立即贮存于-40℃的冰箱,备用。
血浆样品处理:取血浆200μL,置2 m L塑料离心管中,加入6%高氯酸溶液160μL,涡旋振荡0.5 min,离心2 min(10 000 r/min),吸取上清液20μL进样,并采用高效液相色谱(HPLC)法分析。
2.4 方法学考察
专属性试验:将奥沙利铂对照品溶液直接进样;另取空白血浆、空白血浆+奥沙利铂对照品及血浆样品按拟订方法处理并测定,记录色谱图,见图1。结果表明,血浆中内源性物质不干扰奥沙利铂的测定,色谱峰分离良好,奥沙利铂的保留时间为8.51min。

图1 高效液相色谱图
标准曲线制备:精密量取2.2项下不同质量浓度的对照品溶液20μL,置2m L塑料离心管中,加入空白血浆180μL,制成质量浓度分别为160.0,100.0,80.0,50.0,20.0,10.0,5.0,2.0μg/m L的模拟血浆样品,按拟订方法处理并测定。以奥沙利铂峰面积(Y)对血浆药物质量浓度(X)进行线性回归,得标准曲线回归方程Y=8 035.7X-11 791,r=0.999 5(n=8)。结果表明,奥沙利铂检测质量浓度在2.0~160.0μg/mL范围内与峰面积线性关系良好。定量下限为2μg/m L。
精密度试验:精密量取质量浓度为50,200,1000μg/m L的奥沙利铂对照品溶液20μL各5份,加入180μL空白血浆,制成5.0,20.0,100.0μg/m L3种质量浓度的奥沙利铂模拟血浆样品,按拟订方法处理并测定,于同日内测定5次,计算日内 RSD;另每日测定1次,连续测定5 d,计算日间RSD。结果见表1。
表1 精密度试验结果(s,n=5)
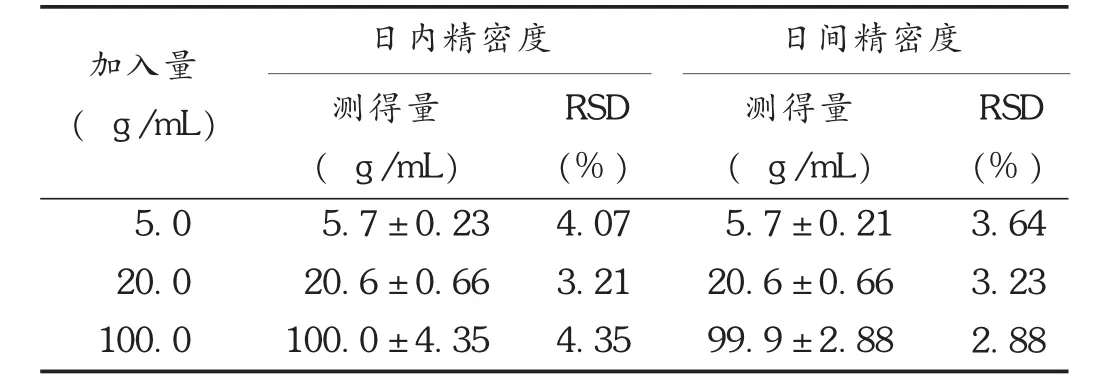
表1 精密度试验结果(s,n=5)
日内精密度 日间精密度加入量( g/m L)5.0 20.0 100.0测得量( g/mL)5.7±0.23 20.6±0.66 100.0±4.35 RSD(%)4.07 3.21 4.35测得量( g/m L)5.7±0.21 20.6±0.66 99.9±2.88 RSD(%)3.64 3.23 2.88
稳定性试验:精密量取质量浓度为200.0μg/mL的奥沙利铂对照品溶液20μL,加入180μL空白血浆,制成质量浓度为20.0μg/m L的奥沙利铂模拟血浆样品,按拟订方法处理,处理时间分别为即刻处理和反复冻融3次后处理,结果的 RSD为1.67%。另外,同上操作配制质量浓度为20.0μg/mL的奥沙利铂模拟血浆样品即刻处理后,分别在室温和0℃放置0,0.5,1,2,3,4 h后测定并计算,结果的 RSD分别为41.85%和7.15%,表明奥沙利铂在室温放置环境下不稳定,在其他考察条件下性质稳定。
回收率试验:精密量取质量浓度为50.0,200.0,1 000.0μg/mL的奥沙利铂对照品溶液20μL各5份,加入180μL空白血浆,制成5.0,20.0,100.0μg/m L 3种质量浓度的奥沙利铂模拟血浆样品各5份,按拟订方法处理并测定,测得峰面积(A)并代入标准曲线方程,求得奥沙利铂实际质量浓度(B),并与配制质量浓度(C)做比较,计算方法回收率(B/C)。精密量取质量浓度为50.0,200.0,1 000.0μg/mL的奥沙利铂对照品溶液20μL各5份,加入180μL蒸馏水,制成5.0,20.0,100.0μg/m L 3种质量浓度的奥沙利铂样品各5份,按拟订方法处理并测定,测得峰面积(D),然后计算提取回收率(A/D)。结果见表2。
表2 奥沙利铂回收试验结果(s,%,n=5)
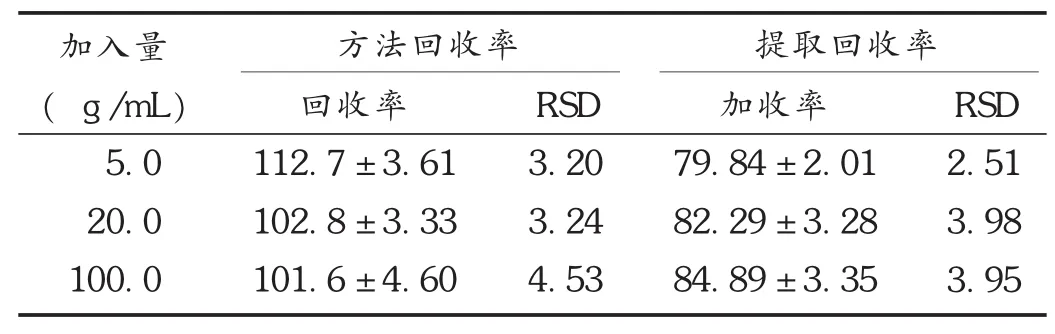
表2 奥沙利铂回收试验结果(s,%,n=5)
方法回收率加入量 提取回收率( g/m L)5.0 20.0 100.0回收率112.7±3.61 102.8±3.33 101.6±4.60 RSD 3.20 3.24 4.53加收率79.84±2.01 82.29±3.28 84.89±3.35 RSD 2.51 3.98 3.95
2.5 血浆样品测定
精密称取注射用奥沙利铂50.0mg,溶于7m L蒸馏水中,制备相应质量浓度的奥沙利铂溶液。取大鼠10只,根据文献[10]推算大鼠给药量,奥沙利铂为23.1mg/kg,用1mL注射器尾静脉给药,且均在给药后即刻由眼底静脉丛取血 0.5 m L,置涂有肝素的离心管中,离心2 min(10 000 r/min),吸取上清液即刻按拟订方法处理,分别进行测定。结果10只大鼠血浆样品中奥沙利铂的质量浓度分别为65.2,62.2,71.5,58.6,77.6,59.7,47.6,77.6,78.6,75.8μg/mL,平均质量浓度为(67.4±10.45)μg/mL。
3 讨论
3.1 流动相的选择
比较了甲醇-水和乙腈-水,结果表明,选用甲醇-水作流动相时,血浆杂质峰较多,不能与奥沙利铂色谱峰较好地分离;而选用乙腈-水作流动相时,可得到峰形良好的单峰,且与血浆内源性物质分离完全,保留时间适中,有利于试验顺利进行。故选用乙腈-水(7∶93)为流动相。
3.2 血浆样品的处理
因流动相中含有乙腈,故拟订使用乙腈沉淀蛋白,经试验发现,用乙腈沉淀蛋白处理血浆样品时奥沙利铂测得质量浓度很小,不利于样品的测定。郑仁娟等[11]的研究结果显示,奥沙利铂最稳定的pH为4.2,偏酸或偏碱均会加速其水解。赵雁等[12]的研究结果显示,改用6%高氯酸溶液沉淀蛋白效果良好,奥沙利铂的质量浓度有明显改善,有利于样品的测定。
3.3 方法学考察
考虑到药物在大鼠全血中会降解[12-13],以及经处理后在室温放置下性质不稳定,为避免样品测定受到影响,所有血浆样品应即刻处理即时测定。
[1]任 鹏,孙坚彤,沈云玉,等.反相高效液相色谱法测定奥沙利铂的含量[J].抗感染药学,2005,2(1):24-26.
[2]宋晓坤,杜春双,巴 一,等.两种剂量下血浆中不同形式奥沙利铂的药动学[J].中国医院药学杂志,2009,29(12):980-983.
[3]牛 冲,李 军,李 涛,等 .HPLC法测定奥沙利铂杂质B的研究[J].中国药品标准,2012,13(4):255-258.
[4]黄毅岚,张 丹.HPLC法测定奥沙利铂中有关物质的含量[J].中国药房,2008,19(1):50-51.
[5]费瑞娟,陈祥峰,任 风.奥沙利铂原料药3种含量测定方法比较[J].中国当代医药,2010,17(34):57-58.
[6]张建华,黄毅岚,张 丹.HPLC法测定奥沙利铂中的左旋异构体[J].华西药学杂志,2009,24(6):651-652.
[7]葛 滨,时贞平.奥沙利铂左旋异构体测定方法研究[J].海峡药学,2009,21(10):73-74.
[8]赵 静,赵 华,蒋心惠.HPLC法测定奥沙利铂脂质体中奥沙利铂的含量[J].中国药房,2010,21(32):3 058-3 060.
[9]刘小平,耿丹清,石炳光,等.奥沙利铂脂质体中奥沙利铂的含量测定[J].中国医药导报,2007,4(25):101-102.
[10]黄继汉,黄晓辉,陈志扬,等.药理试验中动物间和动物与人体间的等效剂量换算[J].中国临床药理学与治疗学,2004,9(9):1 069-1 072.
[11]郑仁娟,张文成,梅兴国,等.奥沙利铂水解动力学初步研究[J].中国药学杂志,2011,46(10):781-784.
[12]赵 雁,贺 宁,陶 涛.奥沙利铂聚乙二醇修饰脂质体的制备及其大鼠体内的药动学[J].中国医药工业杂志,2012,43(11):913-916.
[13]Luo FR,Wyrick SD,Chaney SG.Biotransformations of oxaliplatin in ratblood in vitro[J].JBiochem Mol Toxicol,1999,13(3-4):159-161.
M ass Concentration Determ ination of Oxalip latin in Plasm a of Rats by RP-HPLC
Liu Jian,Zhang Zhiqing,Yang Xiuling
(The Second Hospital of Hebei Medical University,Shijiazhuang,Hebei,China 050000)
Objective To establish a RP-HPLC method for determining the mass concentration of oxaliplatin in plasma of rats.M ethods The DiamonsilTMC18column(250 mm×4.6 mm,5μm)was used with mobile phase consisted of acetonitrile-water(7∶93)at the flow rate of 0.8 mL/min,the detection wavelength was set at 210 nm and column temperature was 30℃,and the injection volume was 20μL.Resu lts The retention time of oxaliplatin was 8.51 min.the standard curve was Y=8 035.7 X-11 791(r=0.999 5)with a linearity range of 2.0-160.0 μg/mL.The recovery rate of method of low,midd le and high concentration were(112.7± 3.61)%,(102.8±3.33)%,(101.6±4.60)%,RSD were 3.20%,3.24% and 4.53%,respectively;the recovery rate of extraction of low,middle and high concentration were(79.84±2.01)%,(82.29±3.28)%,(84.89±3.35)%,RSD were 2.51%,3.98% and 3.95%,respectively.The plasma samples were stable when stored at-40℃ for freeze-thaw for thrice and the processed samples were stable,but were unstable at room temperature.The average of plasma concentration in 10 rats were(67.4±10.45)μg/mL.Conclusion The method is accurate,simple and has high sensitivity and reproducibility.It can provide methodology reference for the determination of oxaliplatin concentration in plasma of rats.
RP-HPLC;rats;plasma;Oxaliplatin;plasma concentration
R965;R979.1
A
1006-4931(2016)04-0054-03
刘剑(1979-),硕士研究生,主管药师,研究方向为药动学和药物体内相互作用,(电话)0311-66003452(电子信箱)ljhaiyang@aliyun.com。
2015-07-05)
