应用 PLFA 技术分析氮沉降对三江平原小叶章湿地土壤微生物群落结构的影响
2016-12-21张荣涛杨立宾李梦莎刘赢男柴春荣王继丰付晓玲钟海秀倪红伟
隋 心,张荣涛 ,杨立宾 ,李梦莎 ,许 楠 ,刘赢男 ,柴春荣 ,王继丰,付晓玲,钟海秀,倪红伟
(1.东北林业大学 林学院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 自然与生态研究所湿地与生态保育国家地方联合工程实验室,黑龙江 哈尔滨 150040)
应用 PLFA 技术分析氮沉降对三江平原小叶章湿地土壤微生物群落结构的影响
隋 心1,2,张荣涛2,杨立宾2,李梦莎2,许 楠2,刘赢男2,柴春荣2,王继丰2,付晓玲2,钟海秀2,倪红伟2
(1.东北林业大学 林学院,黑龙江 哈尔滨 150040;2.黑龙江省科学院 自然与生态研究所湿地与生态保育国家地方联合工程实验室,黑龙江 哈尔滨 150040)
为了研究氮沉降对三江湿地土壤微生物群落结构的影响,利用磷脂脂肪酸技术(PLFA)对三江平原小叶章湿地土壤微生物多样性进行了分析。2010年5月,在黑龙江省科学院自然与生态研究所三江平原湿地生态定位研究站内的小叶章湿地中建立模拟氮沉降试验平台,设置3个氮沉降浓度梯度:N1(0 g N·m-2a-1)、N2(4 g N·m-2a-1)、N3(8 g N·m-2a-1),于2014年6月用土钻进行土壤样品采集。结果表明:本研究共检测到 PLFAs 75种,其中特征脂肪酸 29 种。不同氮沉降处理下,真菌群落的生物量较高,土壤微生物生物量的总量介于30~33 nmol·g-1。氮沉降增加对真菌群落数量的影响比较显著(P<0.05),但是对细菌和放线菌影响并不显著。低氮时土壤微生物的数量最多,对照最低;高氮时土壤微生物群落的多样性值和丰度值最高。根据典型性相关分析,得出铵态氮和硝态氮对土壤中真菌含量影响较为显著。通过本研究可以得出,施氮增加了土壤微生物总量。铵态氮和硝态氮是影响土壤微生物数量的主要因子,低氮增加了土壤微生物多样性,高氮则产生抑制作用。
氮沉降;磷脂脂肪酸;小叶章湿地;微生物多样性
近半个世纪以来,随着大量化石燃料的燃烧所导致的大气氮沉降已经成为全球变化重要的现象之一,大气氮沉降的增加给整个陆地生态系统的结构、功能以及生物地球化学循环都产生了重要的影响[1]。我国由于工业发展的需要以及农业氮肥的过量使用,使得氮沉降增加非常迅速,已经成为世界第三大氮沉降区,而且氮沉降逐渐从东南向西北开始蔓延,这给我国整个生态系统造成了严重的影响[2-3]。三江平原湿地位于我国东北地区,是我国面积最大、分布最为集中的淡水湿地[4],对维持该地区的气候具有重要的作用,同时该地区也是氮沉降比较敏感的地区之一,由于农业上大量氮肥的使用,造成了湿地氮沉降量的显著增加,给湿地生态系统的结构和功能都产生了一定的影响[5-6]。
土壤微生物是地下生态系统的最为重要组成部分[7],在凋落物的分解、营养元素的循环过程中具有重要的作用[8-9],同时也对维持生态系统功能和稳定上发挥着重要的作用[10]。目前关于大气氮沉降对三江平原湿地生态系统的影响已经做了大量的研究,如植物生物量的变化[11]、植物生理生态[12]和营养物质循环等方面[13],而有关氮沉降对三江平原小叶章Deyeuxia angustifolia湿地土壤微生物群落结构的研究还缺乏深入研究。
近年来,随着生物学技术的快速发展,越来越多的新方法、新技术运用到微生物学的研究领域,使得我们可以很好的对土壤微生物进行深入的研究。例如末端限制性片段长度多样性技术(T-RFLP)、磷脂脂肪酸技术(Phospholipid fatty acid,PLFA)、 宏 基 因 组 技 术 (Microbial Environmental Genome)等。磷脂脂肪酸是微生物细胞膜的一种主要成分,存在与所有的活体微生物之中,并且随着细胞的死亡而迅速分解,所以不同样品中土壤微生物中的磷脂脂肪酸的组成和含量是不同的[14]。所以,利用磷脂脂肪酸技术可以非常准确、定量的检测出微生物群落结构组成和多样性变化。因此,本研究利用黑龙江省科学院自然与生态研究所三江平原湿地生态定位研究站内的模拟氮沉降研究平台,利用磷脂脂肪酸技术研究模拟氮沉降条件下,研究三江平原小叶章湿地土壤微生物多样性的变化,为三江平原湿地生态系统在氮沉降背景下的变化提供科学依据,并为三江平原湿地的管理与保护提供理论参考。
1 材料与方法
1.1 研究区域概况
研究样点设置在黑龙江省科学院自然与生态研究所三江平原湿地生态定位研究站-洪河国家级自然保护区内(图1)。研究区域海拔55~65 m,多年平均气温1.9℃,≥10℃有效积温2 165~2 624 ℃。年平均降水量为550~600 mm,50%~70%集中在6~9月份,无霜期125 d左右。主要植被类型为草甸和沼泽,优势植物有小叶章、狭叶甜茅Glyceriaspiculosa、毛果苔草Carexlasiocapa、漂筏苔草Carexpseudocuraica等[15]。
1.2 样品采集
2010 年5 月在小叶章沼泽化草甸湿地设置9块20 m×20 m的样地,进行3种处理:对照组:N1(0 g N·m-2a-1)、低氮组:N2 (4 g N·m-2a-1) 和高氮组:N3 (8 g N·m-2a-1),每种处理重复3次。每年5月份进行施氮处理,将NH4NO3溶于水,用花洒均匀喷施。于2014年6月采样土壤样品,土壤样品为混合土样,用直径为4 cm的土钻按混合采样法采集0~20 cm 土层,每个土样由5~10 个采集点的土壤混合,用四分法取适量于土袋中,迅速带回实验室。去除土样中的植物和动物残体等杂质,混合均匀后一部分保存在-80 ℃冰箱,用于分析土壤微生物群落结构。另一部分风干、磨细过100目筛,用于测定土壤理化性质。
1.3 土壤理化性质检测
土壤pH测定的水土比为2.5∶1;土壤含水率采用烘干法测定;土壤有机碳利用碳氮分析仪测定(耶拿-2100S,德国);土壤中全氮采用半微量凯氏定氮法测定;硝态氮采用酚二磺酸比色法测定;铵态氮采用氯化钾浸提-靛酚蓝比色法测定。
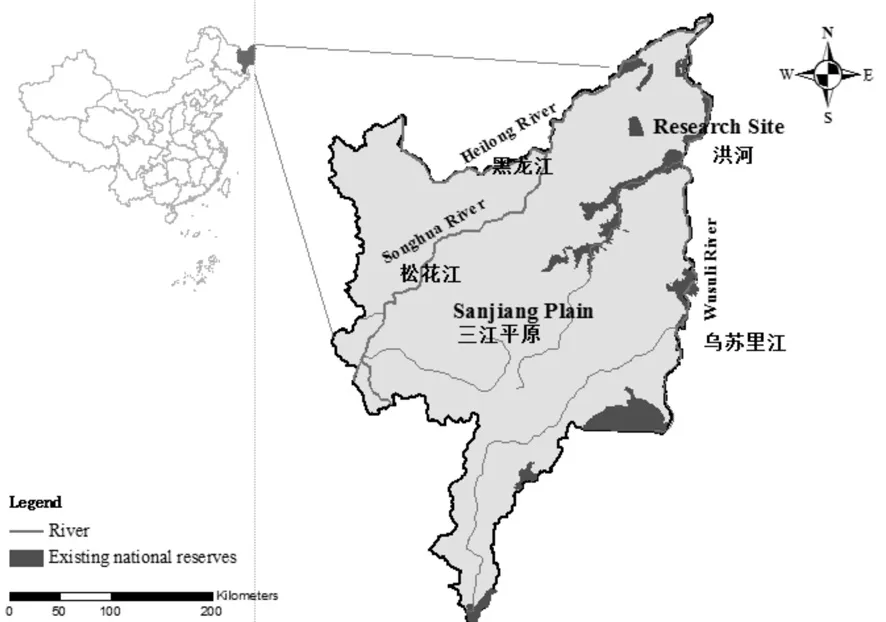
图1 实验区位置-洪河国家级自然保护区Fig. 1 Location of sampling sites in the Sanjiang plain-Honghe national nature reserve
1.4 磷脂脂肪酸检测
磷脂脂肪酸的检测采用氢氧化钾-甲醇溶液甲酯化法来完成[16],以十九烷酸为内标,在Agilent 6850 气象色谱中检测,采用Sherlock MIS 4.5 系统分析土壤样品中的PLFA图谱中磷脂脂肪酸的成分。每种脂肪酸的浓度基于碳内标19:0 的浓度来计算,脂肪酸浓度用nmol·g-1干土表示。
1.5 数据分析
土壤真菌量细菌量和革兰氏阳性菌含量、革兰氏阴性菌含量、放线菌含量和原生动物含量等特征脂肪酸参照已发表文献[17-19]。然后后对样品中PLFAs 含量按照下列公式进行计算[20]:

式(1)中:N代表为脂肪酸含量 (nmol·g-1),Response为生物标记的响应值,19∶0为内标物c19∶0 ( ng·μL-1),FAME为脂肪酸甲酯的摩尔质量(g·mol-1),溶样体积单位μL,样品干质量单位g。
使用SPSS17.0计算单因素方差分析,显著性为α=0.05,Shannon-Wiener多样性指数 (H)、Simpson多样性指数(D)、丰度(S)、均匀度(J)采用excel进行计算,绘图采用SigmaPlot软件。
2 结果与分析
2.1 模拟氮沉降条件下土壤理化性质的变化特征
模拟氮沉降样地的土壤理化性质分析结果见表2,样地的土壤类型主要为草甸土,且不同样地的pH值存显著性差异(P<0.05),其中高氮样地的pH均值最低。不同样地土壤的有机碳、全氮、硝态氮、铵态氮存在显著的差异(P<0.05)。有机碳、全氮、硝态氮、铵态氮呈现出随着氮沉降的增加而升高的趋势。

表2 模拟氮沉降条件下的土壤理化性质的比较†Table 2 The physical and chemical properties under different nitrogen concentration conditions
2.2 各处理对土壤微生物总生物量的影响
土壤微生物群落的生物量和结构可以利用土壤中磷脂脂肪酸的组成来表示,并且脂肪酸含量的高低可以反应出土壤微生物生物量的多少[21-22]。本研究中一共检测出磷脂脂肪酸75种,其中特征微生物29种,C链长度11~24,包括了不同脂肪谱类型的特征微生物(表3)。
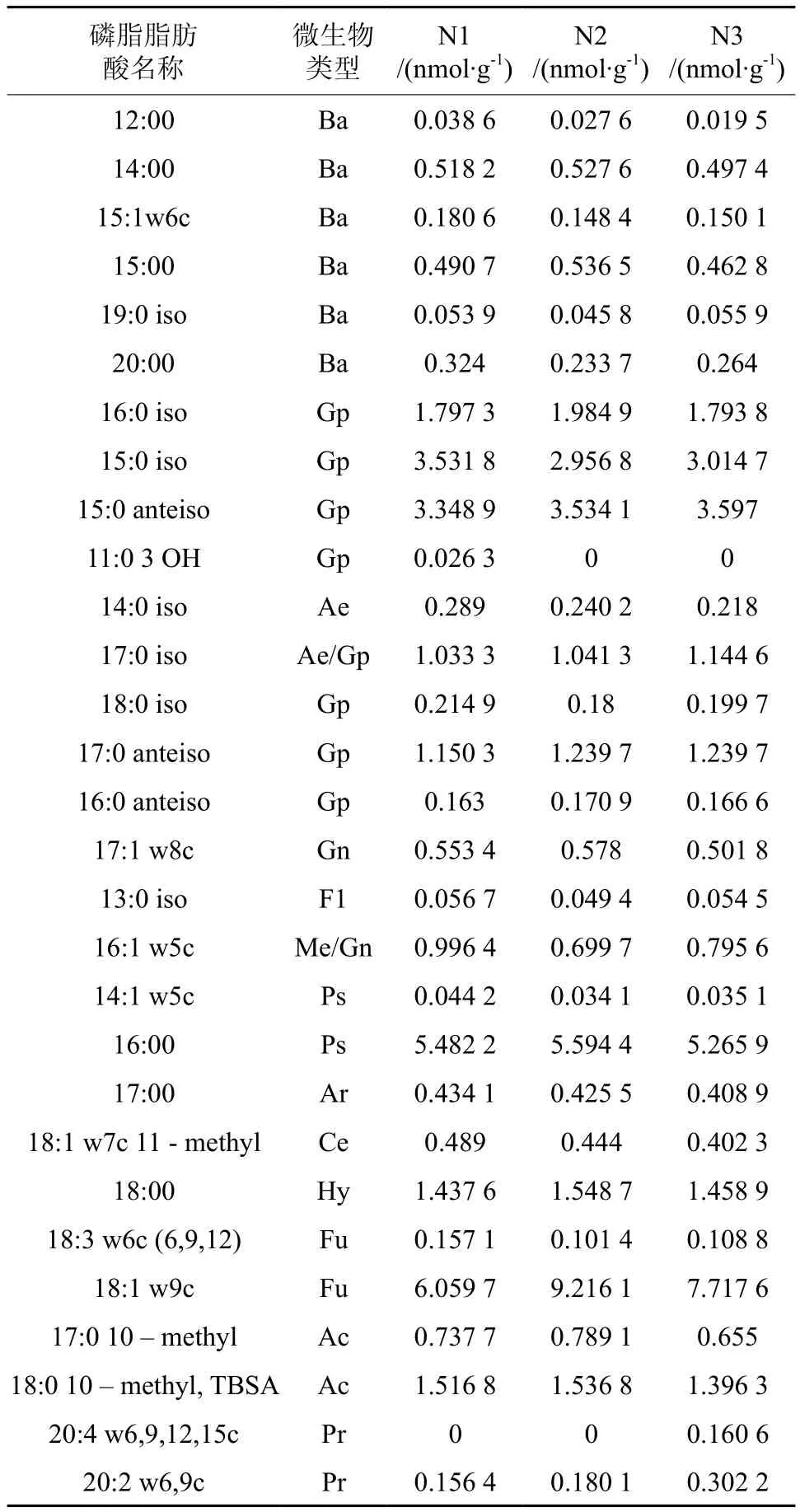
表3 不同氮沉降下土壤微生物特征磷脂脂肪酸标记分析†Table 3 Analysis of PLFA biomarkers in soil of different nitrogen deposition treatments
通过对3个氮沉降处理的PLFA分析可以看出,不同氮处理处理条件下,土壤微生物生物量的范围为30~33 nmol·g-1(图2)。氮沉降增加后,土壤中PLFA总量显著升高,随着氮沉降量的增加呈现出先升高后降低的趋势,在低氮处理达到最大值,高于对照处理8.89%。不同氮沉降浓度下革兰氏阴性菌与PLFA总量变化趋势相同,但革兰氏阳性菌与PLFA总量变化趋势不同,但变化幅度均略小。
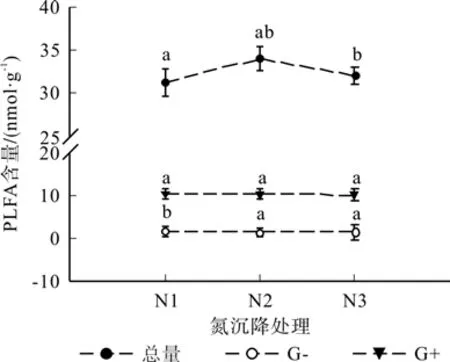
图2 不同氮沉降处理土壤微生物总的PLFA含量Fig.2 PLFA contents in different nitrogen deposition treatments
2.3 不同氮沉降条件下土壤细菌、真菌和放线菌含量变化
不同氮沉降条件下土壤细菌、真菌、放线菌的含量变化是不同的(图3)。由图2a可见,不同氮沉降浓度条件下土壤细菌含量差异不显著。其中,低氮处理和高氮处理均低于对照样地。随着施氮量的增加,其变化趋势为逐渐降低,在对照时达到最大值,高氮处理时最低,低氮处理比对照小5.71%,高氮处理比对照小10.05%。图2b表明,不同氮沉降浓度见土壤真菌含量差异显著。其中,各处理均高于对照样地。随着氮沉降的增加呈现出先升高后降低的趋势,在低氮处理时达到最大值,高于对照处理50.66%。图2c表明,不同氮沉降条件下土壤中放线菌含量呈现出先升高后降低的趋势,但差异不显著。在低氮时达到最大值,高于对照3.43%,在高氮处理时达到最小值,低于对照8.93%。
2.4 不同处理对土壤微生物群落结构的影响
通过对PLFA的特征脂肪酸进行分析,可以得出不同氮沉降处理间的多样性指数并不相同(表4)。低氮处理时,土壤微生物群落多样性指数最高(Shannon指数和Simpson分别为2.325 9和0.480 8),微生物群落的丰富度为90,均匀度为0.988 2。所以,低氮处理时更利于微生物的生长,微生物多样性较高,而高氮处理时,多样性指数最低。
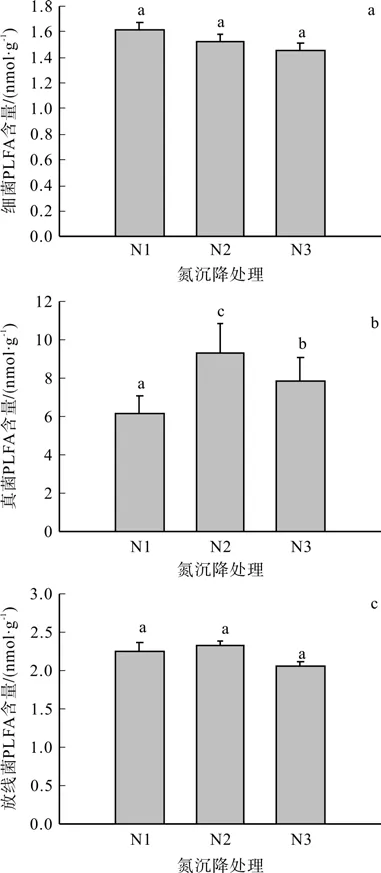
图3 不同氮处理土壤中细菌(a)、真菌(b)和放线菌(c)的PLFA含量Fig.3 The PLFA content of bacteria (a), fungi (b) and actinomyces (c) in soil of different nitrogen treatments
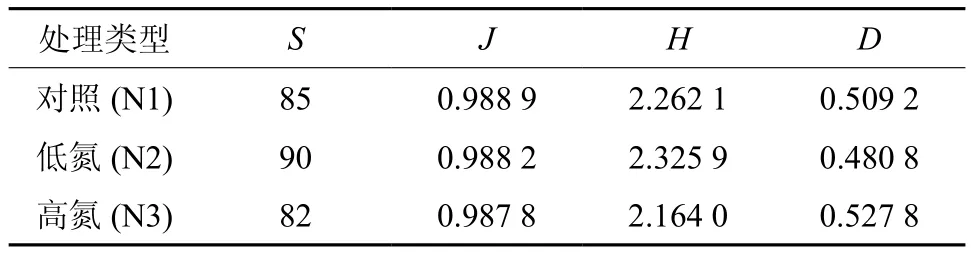
表4 不同氮沉降处理下土壤微生物PLFA多样性指数Table 4 Diversity indices of PLFA in soil of different nitrogen deposition
典型性相关分析可以很好的用来解释环境因子对微生物群落结构的影响,U代表环境变量的标准化变量,V代表群落结构生物量的标准化变量。如表5所示,将U和V进行Bartlett的χ2检验,从获得的4组相关系数来看,在α= 0.05时,第1组和第2组相关系数均小于0.05,第1组小于0.01,所以可以看出,前2组的典型相关系数是极显著和显著的。
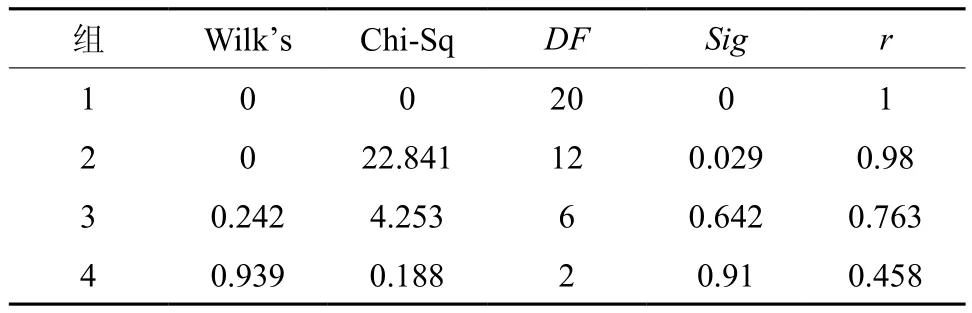
表5 典型变量相关系数和显著性检验Table 5 Canonical correlation coefficient and significant test
由表6 可知环境变量的典型变量相关系数。U1=0.148×pH值-0.357×有机碳含量+0.207总氮含量-1.183×铵态氮含量+2.397×硝态氮含量,由此可知,影响U1的主要因子为铵态氮和硝态氮。U2=0.461×pH值-2.091×有机碳含量-0.684总氮含量-4.396×铵态氮含量+7.004×硝态氮含量,从上述方程可知U2的主要影响因子也为铵态氮和硝态氮。表7为微生物群落结构因子的典型变量,V1=-0.224×微生物总量-0.538×细菌含量+0.878×真菌含量-0.377×放线菌含量,V1的主要代表因子为真菌;V2=0.887×微生物总量+0.378×细菌含量-1.534×真菌含量+0.198×放线菌含量,即V2的主要因子为真菌。
所以,根据U和V的典型相关关系分析得出,土壤铵态氮含量和硝态氮含量对微生物群落中真菌含量影响比较显著。N沉降对土壤微生物群落中真菌的影响最大,细菌次之,放线菌最小。
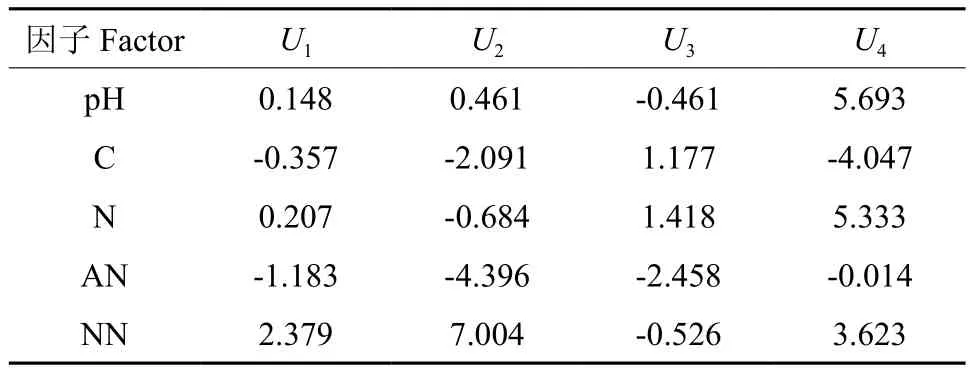
表6 典型变量U与原始标准化变量X的相关系数Table 6 Canonical correlation coefficient and significant test
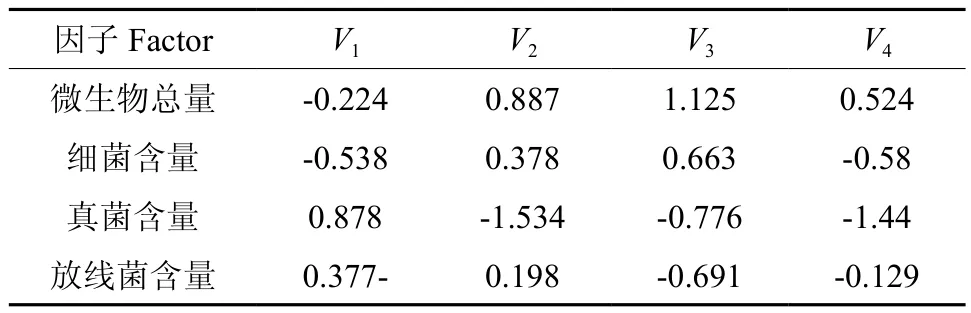
表7 典型变量V与原始标准化变量Y的相关系数Table 7 Canonical correlation coefficient and significant test
3 讨 论
氮沉降增加会改变土壤微生物生物量和微生物群落结构。本研究表明,PLFAs表征的细菌生物量和放线菌生物量随着氮沉降的增加并无显著变化,但是对于真菌来看,施氮显著增加了真菌生物量。施氮对微生物PLFAs总量影响比较显著,但是对革兰氏阴性菌和阳性菌的影响并不显著。许多研究表明:在不同的生态系统中,施氮对土壤微生物的影响是不同的。例如,施瑶等[23]对内蒙古草原土壤微生物的研究发现,氮添加会土壤微生物总量和细菌数量、放线菌数量,但是真菌却增加并不显著;薛璟花等[24]在热带森林生态系统中研究发现,氮沉降增加会增加细菌和放线菌生物量,但是会对真菌生物量产生明显的抑制作用。但是也有研究表明氮沉降的增加会抑制细菌的生长[25]。而本研究的结果先发现,氮增加显著增加了土壤真菌的含量,但是对细菌和放线菌的影响并不显著。这可能是因为在三江湿地生态系统中,土壤真菌属于异养型微生物,利用土壤有机碳作为碳源,当对小叶章湿地进行施氮后,土壤有机碳增加,pH值下降,土壤真菌分泌物含量增加,从而引起真菌生物量增加或者群落发生改变,这与Smolander的研究结果是一致的[26]。但是对于不同生态系统和生境中,微生物生物量对氮沉降的响应是不同的和复杂的,这可能与土壤性质、温湿度、气候条件、地上植被组成以及凋落物性质等紧密相关,但是对其具体的影响机理和规律仍需要进一步的研究。
多样性指数由物种丰富度和均与度两部分组成,多样性指数的高低表示土壤微生物群落多样性的高低,是一种分析土壤微生物群落结构十分有效的方法[27-28]。本研究结果表明,不同氮沉降条件下土壤微生物的群落结构发生了显著的变化,Shannon指数呈现出N2>N3>N1的趋势(表2),可见,氮沉降会改变土壤微生物的多样性,低氮较高,高氮略有下降,说明氮沉降增加微生物多样性具有阈值限制性,即氮浓度增加到一定阈值时,微生物多样性则由升高转变为下降。这可能是由于氮沉降增加了土壤中的营养物质,为微生物的生长提供了丰富的营养来源,因此,一定浓度的氮素会促进细菌的生长,这和刘彩霞等[29]的研究结果是一致的。但是在高氮水平下,氮增加改变了土壤中营养物质的有效性,这导致了某些微生物种群(如偏于利用植物残体的种群)的生长,但是同时又抑制了其他种群,致使群落多样性指数的下降。总的来说,氮沉降会对土壤微生物的群落结构具有一定促进作用。由此可以推断,长期的高氮沉降必势会对三江平原湿地土壤微生物群落产生深远影响。
湿地由于其生态环境的特殊性,越来越受到科学家的重视。近年来,有关氮沉降对三江平原湿地生态系统的影响也做了大量而且深入的研究。例如模拟大气氮沉降条件下,小叶章生物量及分配的变化[30],氮素循环以及分配[31]、不同形式氮的季节性变化特征等[32]。而本研究更加深入的揭示了氮沉降条件下三江平原湿地土壤微生物数量、结构组成以及多样性的变化规律,这更进一步丰富了大气氮沉降条件下三江平原湿地土壤微生物生态学领域的研究。此外,本研究虽然利用PFLA技术对模拟氮沉降条件下土壤微生物数量和多样性进行了研究,但是这种方法也存在着一些不足之处:(1)目前还不能确定所有特征脂肪酸和特定微生物或微生物群落的对应关系。(2)PLFA不能在种属水平上进行鉴定。所以为了克服该方法的缺点,更加准确地获取微生物结构功能方面的信息,未来需要采用多种技术相结合的方法,如利用高通量测序技术,biolog技术与PLFA技术想结合,从种属水平,微生物活性水平和微生物量水平多角度进行分析,这样就可以比较清楚的了解氮沉降对三江平原小叶章湿地土壤微生物群落结构、功能、数量的影响。
4 结 论
(1)研究表明,在3个氮沉降处理中单不饱和脂肪酸和支链脂肪酸含量较低,多不饱和脂肪酸为优势脂肪酸类群,即各处理土壤中微生物群落结构中真核微生物为主要类群,真菌为其群落结构中的优势菌群,原核微生物所占比例较小。
(2)不同氮浓度条件下,土壤中PLFA 总的脂肪酸含量均高于对照样地,但是,革兰氏阳性菌、革兰氏阴性菌脂肪酸含量与对照样地差异不大。细菌随着施氮量的增加呈现下降趋势,真菌和放线菌呈现出先升高后降低的趋势,低氮时最高,而原生动物随着施氮量的增加而逐渐增加。根据典型性相关分析可知,土壤铵态氮含量和硝态氮含量对微生物群落中真菌含量影响比较显著。
[1]Galloway J N, Dentener F J, Capone D G,et al.Nitrogen cycles:past, present, and future[J]. Biogeochemistry, 2004,70(2):153-226.
[2]孙崇基. 酸雨[M].. 北京: 中国环境科学出版社, 2001.
[3]Dentener F, Drevet J, Lamarque J F,et al. Nitrogen and sulfur deposition on regional and global scales: a multimodel evaluation[J]. Glob. Biogeochem. Cycle, 2006, 20(4):16615-16615.
[4]隋 心, 张荣涛, 钟海秀, 等. 利用高通量测序对三江平原小叶章湿地土壤细菌多样性的研究 [J].土壤,2015,47(5):919-925.
[5]刘兴土, 马学慧. 人类大面积开荒对三江平原环境影响及区域性生态环境保护[J]. 地理科学, 2000, 20(1): 14-19.
[6]张继舟, 倪红伟, 王建波, 等. 模拟氮沉降和 CO2浓度增加对三江平原小叶章群落土壤总有机碳和氮素含量的影响[J]. 地球与环境, 2013, 41(3): 216-225.
[7]丁思一, 佘济云, 杨庆朋,等. 间伐和修枝对杉木人工林土壤微生物量碳和酶活性的影响[J]. 中南林业科技大学学报,2015, 35(6):75-79.
[8]Kazda M. Indications of unbalanced nitrogen nutrition of Norway spruce stands. Plant Soil, 1990, 128(1):97-101.
[9]Lovett G M, Reiners W A, Olson R K. Cloud droplet deposition in subalpine balsam fi r forests: hydrological and chemical inputs.Science, 1982, 218(4579):1303-1304.
[10]Parker G G. Throughfall and Stemflow in the Forest Nutrient Cycle. Adv. Ecol. Res., 1983, 13(4):57-133.
[11]邢军会, 倪红伟, 王建波. 二氧化碳浓度升高与氮沉降对三江平原小叶章群落生物量累积及其分配格局的影响[J]. 中国农学通报, 2011, 27(13):49-54.
[12]窦晶鑫,刘景双,王 洋,等. 小叶章对氮沉降的生理生态响应[J]. 湿地科学, 2009(1):40-46.
[13]张继舟, 倪红伟, 王建波,等. 模拟氮沉降和CO2浓度增加对三江平原小叶章群落土壤总有机碳和氮素含量的影响[J].地球与环境, 2013, 41(3) :216-225.
[14]陈晓芬, 李忠佩, 刘 明, 等. 长期施肥处理对红壤水稻土微生物群落结构和功能多样性的影响[J]. 生态学杂志, 2015,34(7): 1815-1822.
[15]倪红伟,李 君.洪河自然保护区生物多样性[M].哈尔滨:黑龙江科技出版社,1999.
[16]Drenovsky R E, Elliott G N, Graham K J,et al.Comparison of phospholipid fatty acid(PLFA)andtotal soil fatty acid methyl esters(TSFAME)for characterizing soil microbial communities.Soil Biol Biochem, 2004, 36(11):1793-1800.
[17]Jain D K, Stroes-Gascoyne S, Providenti M,et al. Characterization of microbial communities in deep groundwater from granitic rock. Can J Microbial, 1997, 43(3):272-283.
[18]Joergensen R G, Potthoff M. Microbial react ion in activity,biomass, and community structure after long term continuous mixing of a grassland soil. Soil BiolBiochem, 2005, 37(7):1249-1258.
[19]Sakamoto K,IijimaT,Higuchi R. 2004. Use of specific phospholipid fatty acids for identifying and quantifying the external hyphae of the arbuscularmycorrhizal fungus Gigasporarosea. Soil BiolBiochem, 36(11):1827-1834.
[20]文 倩, 林启美, 赵小蓉, 等. 北方农牧交错带林地, 耕地和草地土壤微生物群落结构特征的 PLFA 分析[J]. 土壤学报,2008, 45(2): 321-327.
[21]Bardgett R D,Hobbs P J,Frostegrd. Changes in soil fungal bacterial ratios following reductions in the intensity of management of up land grassland. Biol. Fertil. Soils,1996,22(3):261-264.
[22]于 树, 汪景宽, 李双异. 应用 PLFA 方法分析长期不同施肥处理对玉米地土壤微生物群落结构的影响[J]. 生态学报,2008, 28(9): 4221-4227.
[23]施 瑶, 王忠强, 张心昱, 等. 氮磷添加对内蒙古温带典型草原土壤微生物群落结构的影响[J]. 生态学报, 2014, 34(17):4943-4949.
[24]薛璟花, 莫江明, 李 炯,等. 土壤微生物数量对模拟氮沉降增加的早期响应. 广西植物. 2007, 27(2):174-9.
[25]Paul J W, Beauchamp E G. SHORT COMMUNICATION: Soil microbial biomass C, N mineralization, and N uptake by corn in dairy cattle slurry-and urea-amended soils [J].Can. J. Soil Sci.,1996, 76(4): 469-472.
[26]Smolander Aino, VeikkoKitunen. Soil microbial activities and characteristics of dissolved organic C and N in relation to tree species[J]. Soil BiolBiochem, 2002, 34(5): 651-660.
[27]Harch, B D, Meech W, Pankhurst C E, Correll R L. Using the Gini coef fi cient with BIOLOG substrate utilization data to provide an alternative quantitative measure for comparing bacterial soil communities[J]. J Microbiol Meth, 1997,30(1):91-101.
[29]Staddon W J, Duchesne L C, Trevors J T. Microbial diversity and community srutcture of postdisturbance forest soil as determined by soil-carbon source utilization patterns [J]. Microbial Ecol,1997, 34(2): 125-130.
[30]刘彩霞, 焦如珍, 董玉红, 等. 应用 PLFA 方法分析氮沉降对土壤微生物群落结构的影响[J]. 林业科学, 2015, 51(6): 155-162.
[31]赵光影, 窦晶鑫, 郝冬梅. 模拟氮沉降对三江平原湿地小叶章生物量及分配的影响[J]. 地理与地理信息科学, 2012,28(4):103-106.
[32]孙志高, 刘景双, 王金达. 三江平原典型湿地系统大气湿沉降中氮素动态及其生态效应[J]. 水科学进展,2007,18(2):182-192.
[33]孙志高, 刘景双, 牟晓杰. 三江平原小叶章湿地土壤中硝态氮和铵态氮含量的季节变化特征[J]. 农业系统科学与综合研究,2010, 26(3): 277-282.
Study on microbial diversity of Deyeuxiaangustifolia wetland under the simulation nitrogen depositions with the PLFA method in Sanjiang plain
SUI Xin1,2, ZHANG Rong-tao2, YANG Li-bin2, LI Meng-sha2, XU Nan2, LIU Ying-nan2, CHAI Chun-rong2,
WANG Ji-feng2, FU Xiao-ling2, ZHONG Hai-xiu2, NI Hong-wei2
(1. College of Forestry, Northeast Forestry University, Harbin 150040, Heilongjiang, China; 2. National and Provincial Joint Engineering Laboratory of Wetlands and Ecological Conservation Institute of Nature & Ecology, Heilongjiang Academy of Sciences, Harbin 150040,Heilongjiang, China)
In order to understand the effects of nitrogen deposition on soil microbial community, this study analyzed the microbial diversity in Sanjiang Plain wetland by using the phospholipids fatty acids (PLFA) biomarkers. In May 2010, nitrogen deposition plat was established in the Sanjiang Plain fi eld experiment station of the institute of Nature & ecology, Heilongjiang Academy of Sciences.Nitrogen loadings were designed at 3 levels such as N1, N2, N3 at the doses of 0,4 and 8 g N·m-2a-1, respectively. After four years treatment, soil samples were collected with a soil drill. The result showed that a total of 75 PLFAs were detected,and among them the characteristic fatty acids were 29 kinds.The analysis on type and content of the characteristic fatty acids indicated that eucaryon microorganism was the predominant group in the plot soil treated with all nitrogen treatments.In different nitrogen treatment plots, the range of soil microbial biomass with characteristics of total PLFAs content was 30 ~ 33 nmol·g-1. The amount of fungus were signi fi cant different (P<0.05) and the amount of bacteria were not (P>0.05) in different nitrogen deposition treatments. In the low nitrogen deposition treatment, the PLFAs of soil microorganisms had the highest quantity and diversity, but in the high nitrogen deposition treatment the PLFAs of soil microorganisms had the lowest quantity and diversity. According to the Canonical Correlations, ammonium nitrogen and nitrate nitrogen in soil were positively correlated with the fungus. In conclusion, adding nitrogen will promote the growth of microorganisms, lowest nitrogen treatment is highest and control is the lowest. Ammonium nitrogen and nitrate nitrogen were main factors in fl uence the amount of soil microorganism, which low nitrogen would promote soil microbial diversity and high nitrogen would restrain the soil microbial diversity.
nitrogen deposition; phospholipid fatty acids;Deyeuxiaangustifoliawetland; microbial diversity
S718.52+1.3
A
1673-923X(2016)12-0091-07
10.14067/j.cnki.1673-923x.2016.12.016
http: //qks.csuft.edu.cn
2016-02-21
国家自然科学基金项目(31470019,31400429,31500410);十三五国家重点研发计划(2016YFC0500405);黑龙江省科学院项目(STJB16-01,STJB16-04,2015YZ01,2014ST05);黑龙江省博士后基金(LBH-Z14184);黑龙江省科研机构创新能力提升专项计划(GY2014KC0039);黑龙江省科学院青年创新基金资助
隋 心,副研究员,博士
倪红伟,研究员,博士;E-mail:nihongwei2000@163.com
隋 心,张荣涛,杨立宾,等.应用PLFA 技术分析氮沉降对三江平原小叶章湿地土壤微生物群落结构的影响[J].中南林业科技大学学报,2016, 36(12): 91-97.
[本文编校:文凤鸣]
